利福昔明治疗乙型肝炎肝硬化腹水疗效观察
2021-10-14王会敏韩际奥徐于平马英杰刘璨宇
王会敏,韩际奥,,徐于平,马英杰,,刘璨宇
(1.新乡医学院研究生院,河南 新乡 453003;2.郑州人民医院消化内科,河南 郑州 450000)
肝硬化是由一种或多种病因长期或反复作用形成以肝脏弥漫性纤维化、假小叶形成、肝内外血管增殖为特征的慢性进行性肝脏疾病[1]。在我国,肝硬化最常见的病因是病毒性肝炎,其中以乙型病毒性肝炎最为常见。腹水是肝硬化患者常见且较为严重的并发症之一,患者一旦出现腹水,其1 a 病死率为15%,5 a病死率为44%~85%[2]。目前针对肝硬化并发腹水患者的治疗尚无特效药物,主要以限制钠的摄入量、利尿剂以及白蛋白等常规对症治疗为主。有研究发现,约有1/3肝硬化并发腹水的患者存在小肠细菌过度生长(small intestinal bacterial overgrowth,SIBO)[3]。随着对肠道菌群失调与肝硬化关系研究的不断深入,有研究发现,肠道菌群失调、细菌易位与SIBO是肝硬化相关并发症的重要致病诱因[4-5]。近年来,肠道去污治疗已被逐渐用于肝硬化患者。利福昔明作为一种不被肠道吸收的广谱抗生素,去污效果好,成为目前根治SIBO的主要药物。利福昔明可通过降低内毒素、白细胞介素-6(interleukin-6,IL-6)和肿瘤坏死因子的水平来改善机体血流动力学的相关指标,且这些指标与肝硬化腹水患者高动力循环状态的发病机制有关[6]。目前,有关利福昔明治疗乙型肝炎肝硬化腹水患者疗效的研究较少。因此,本研究旨在探讨利福昔明治疗乙型肝炎肝硬化腹水患者的疗效,以期为临床应用提供依据。
1 资料与方法
1.1 一般资料选择2018年9月至2020年1月郑州人民医院消化内科收治的乙型肝炎肝硬化腹水患者70例为研究对象。病例纳入标准:(1)符合“慢性乙型肝炎防治指南(2019年版)”中乙型肝炎肝硬化的诊断标准[7];(2)经超声检查初次诊断有腹水。排除标准:(1)对利福昔明过敏;(2)糖尿病、假性肠梗阻等可能引起胃肠动力不良的肝外疾病;(3)入院前3周内使用过抗生素、抑酸药、导泻灌肠药或其他促胃肠动力的药物;(4)难治性腹水、腹腔感染。根据治疗方式将患者分为对照组和观察组,每组35例。对照组:男22例,女13例;年龄35~68(45.63±5.67)岁,乙型肝炎病程 6~11(9.74±7.05)a,肝硬化病程 2~6(5.82±3.31)a,腹水病程1~4(2.11±2.53)a;肝功能Child分级:B级 13例,C级22例。观察组:男27例,女8例;年龄32~70(44.65±6.48)岁;乙型肝炎病程10~31(20.91±5.85)a,肝硬化病程2~8(6.14±2.46)a,腹水病程1~4(2.65±2.13)a,肝功能Child分级:B级 9例,C级26例。2组患者的性别、年龄、乙型肝炎病程、肝硬化病程、腹水病程及肝功能Child分级比较差异无统计学意义(P>0.05),具有可比性。本研究通过医院医学伦理委员会批准,患者或家属知情同意并签署知情同意书。
1.2 治疗方法对照组患者给予恩替卡韦(中美上海施贵宝制药有限公司,国药准字H20052327)0.5 mg,口服,每日1次,共治疗180 d;异甘草酸镁注射液(江苏正大天晴药业,国药准字H20051942)200 mg,静脉滴注,每日1次,共治疗14 d;呋塞米片(上海朝辉药业,国药准字H31021074)40 mg,口服,每日1次,共治疗14 d;螺内酯片(江苏长江药业,国药准字H20084493)100 mg,口服,每日1次,共治疗14 d。在对照组治疗方案基础上,观察组患者给予利福昔明(意大利阿尔法韦氏曼制药公司,国药准字H20181212),每个疗程连续口服3 d,每日3次,每次400 mg,14 d 为1个疗程,共12个疗程。
1.3 观察指标
1.3.1 临床指标分别于治疗前和治疗6个月后检测所有患者的体质量(晨起排尿、排便后)、腹围(晨起用卷尺绕脐1周)和24 h尿量(留取24 h内排出体外的尿液)。
1.3.2 腹水量分别于治疗前和治疗6个月后采用彩色多普勒超声测定患者腹水量,并根据《肝硬化腹水及相关并发症的诊疗指南》[8]进行腹水量分级,Ⅰ级:只通过超声检查才能发现的腹水,一般无腹胀表现,移动性浊音阴性,腹水位于各个间隙(包括肠间隙、腹膜间隙、膀胱间隙),腹水深度<3 cm;Ⅱ级:常有中度腹胀和对称性腹部隆起,移动性浊音阴性或阳性,腹水深度3~10 cm;Ⅲ级:腹胀明显,移动性浊音阳性,可有腹部膨隆甚至脐疝,超声下腹水占据全腹部,中腹部被腹水填满,腹水深度>10 cm。
1.3.3 SIBO阳性率分别于治疗前和治疗6个月后,采用氢呼气试验检测所有患者的SIBO情况。患者未口服乳果糖前空腹深呼吸后屏住呼吸,缓慢、匀速、充分地将气体呼入氢呼气实验仪,作为氢呼气浓度基础值。然后将乳果糖10 g、温开水50 mL搅匀后口服,每隔15 min呼气1次,至少2次,取平均值作为氢呼气浓度最终值,整个氢呼气试验检查过程至少2 h。参考文献[9]拟定了氢呼气试验阳性的诊断标准:服用乳果糖90~120 min,氢呼气浓度最终值-氢呼气浓度基础值≥20 mg·L-1。氢呼气试验阳性即为SIBO阳性,统计2组患者SIBO阳性例数,并计算SIBO阳性率,SIBO阳性率=SIBO阳性例数/总例数×100%。

2 结果
2.1 2组患者临床指标比较结果见表1。治疗前2组患者的体质量、腹围、24 h 尿量比较差异无统计学意义(P>0.05)。治疗6个月后,2组患者体质量、腹围显著低于治疗前,24 h 尿量显著高于治疗前,差异有统计学意义(P<0.05)。治疗6个月后,观察组患者的体质量、腹围显著低于对照组,24 h 尿量显著高于对照组,差异有统计学意义(P<0.05)。
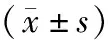
表1 2组患者治疗前后临床指标比较
2.2 2组患者腹水分级比较结果见表2。治疗前2组患者的腹水分级比较差异无统计学意义(Z=-0.721,P>0.05)。2组患者治疗6个月后与治疗前腹水分级比较差异有统计学意义(Z=-2.124、-4.021,P<0.05)。治疗6个月后,观察组与对照组患者的腹水分级比较差异有统计学意义(Z=-2.447,P<0.05)。

表2 2组患者治疗前后腹水分级比较
2.3 2组患者SIBO阳性率比较治疗前,对照组和观察组患者的SIBO阳性率分别为54.29%(19/35)、45.71%(16/35);治疗6个月后对照组和观察组患者的SIBO阳性率分别为22.9%(13/35)、8.6%(4/35)。治疗前2组患者的SIBO阳性率比较差异无统计学意义(χ2= 0.514,P>0.05)。治疗6个月后,2组患者的SIBO阳性率均显著低于治疗前,差异有统计学意义(χ2=-2.236、-3.464,P<0.05)。治疗6个月后,观察组患者的SIBO阳性率显著低于对照组,差异有统计学意义(χ2=11.822,P<0.05)。
3 讨论
肝硬化是临床上常见的慢性进行性肝脏疾病,早期无明显临床症状,晚期常出现一系列并发症,如消化道出血、腹水、肝性脑病、自发性腹膜炎等。据报道,约17%的肝硬化患者会出现顽固性腹水[10]。肝硬化尤其是出现并发症时会引起患者肝脏库普弗细胞吞噬细菌的能力减弱、肠道蠕动减慢、胃肠道淤血、胆汁酸分泌减少等,进而引发SIBO。SIBO可能是引发肠道菌群移位的先决条件,可使患者发生高内毒素血症,肝硬化患者的内毒素血症主要是肠源性内毒素血症,肠源性内毒素诱导的炎症细胞因子水平升高,导致肠系膜血管扩张,继而增加肝硬化腹水的难治性[11]。30%~70%的肝硬化患者可发生SIBO[12]。细菌过度生长可能会增加肠道通透性和细菌移位,同时促进内毒素和促炎细胞因子的水平,这与腹水、肝性脑病、自发性细菌性腹膜炎等并发症的发生相关[11]。GMEZ-HURTADO等[12]研究发现,过度生长的细菌导致的菌群移位在肝硬化及其相关并发症的发生发展过程中发挥着至关重要的作用。肝硬化腹水与内脏高动力循环有关。有研究发现,利福昔明能够通过降低肝硬化患者内毒素、IL-6和肿瘤坏死因子的循环水平来改善血流动力学,进而改善腹水情况[6]。因此,减少SIBO、肠道去污、抑制内毒素血症的发生将为肝硬化并发腹水的治疗提供新思路。
利福昔明是利福霉素衍生物,对革兰阳性和阴性的需氧和厌氧微生物均表现出较高的抑菌活性[13]。利福昔明可通过保护上皮细胞功能(如限制细菌移位)来抑制肠道和全身炎症反应,且能减少结肠黏膜的先天免疫效应细胞水平[14]。利福昔明可作为控制SIBO的重要药物,且其具有较好的去污效果[11,15]。MEYRAT等[16]对经氢呼气检测诊断为SIBO阳性的106例患者进行14 d的利福昔明治疗后,患者的阴转率为84%;一项荟萃分析结果显示,利福昔明治疗SIBO的总根除率为70.8%[17]。本研究结果显示,治疗6个月后2组患者的SIBO阳性率均显著低于治疗前,且观察组患者的SIBO阳性率显著低于对照组,说明在常规治疗的基础上联用利福昔明对肝硬化腹水患者的SIBO根除有一定的疗效。
有研究发现,利福昔明对防治腹水有一定的效果[18]。利福昔明能够下调促炎细胞因子的表达,进而减少肝硬化腹水的发生率[14]。最近一项研究显示,利福昔明可通过调节肠道菌群功能,改善全身炎症状态,从而减轻肝硬化腹水并提高患者的生存率[19]。另一项对600例肝硬化并发腹水患者的前瞻性队列研究发现,利尿剂螺内酯联合利福昔明组患者治疗12周后体质量显著低于治疗前,且显著低于单用利尿剂的对照组患者,这与本研究结果一致[20]。本研究发现,2组患者治疗后腹水分级降低较治疗前有显著改善,且观察组腹水分级降低显著优于对照组。本研究结果还发现,2组患者治疗6个月后的体质量、腹围显著低于治疗前,24 h 尿量显著高于治疗前;治疗6个月后观察组患者的体质量、腹围显著低于对照组,24 h 尿量显著高于对照组。说明利福昔明可促进腹水消退并防止腹水再发生。
综上所述,利福昔明可降低乙型肝炎肝硬化腹水患者的腹水量,并且能够降低SIBO阳性率。但因本研究纳入的病例数较少,仍需大规模多中心随机对照研究进一步证实。
