零价铁类芬顿法处理含低浓度重金属离子有机废水
2021-10-11邹亚辰贾小宁周林成赵泉林叶正芳
邹亚辰,贾小宁,冉 浪,周林成,赵泉林,叶正芳
1.兰州理工大学石油化工学院,甘肃 兰州 730050;2.兰州大学化学化工学院,甘肃 兰州 730000;3.北京大学环境科学与工程学院,北京 100871
随着社会的发展,环境问题得到了越来越多人的关注,其中含重金属离子的工业废水具有较高的毒性,排放后不易被自然降解,能够长时间存在,重金属废水的排放不但会造成资源的浪费,还会严重污染水源,影响饮用水的安全[1]。当重金属离子废水中有络合剂时,不仅增加了重金属离子的稳定性,还造成了有机污染,开展新型含有络合剂重金属离子废水的处理工艺和技术研究显得尤为重要[2]。
常见的含络合态重金属离子废水处理方法有化学沉淀法、氧化法、吸附法和铁置换和还原法等[3]。高级氧化技术(AOPs),由于其具有的强氧化性,在去除络合态金属方面已有很多研究。使用芬顿(Fenton)试剂进行氧化是一种常见的高级氧化技术,可以降解大量有害有机污染物[4]。但是传统的芬顿反应存在药剂使用量大,沉淀生成多,易造成二次污染等缺点[5]。因此,采用成本较低、环境友好、氧化还原电位较低的Fe0作为Fe2+/Fe3+的供体,得到了广泛的关注,其中涉及的反应式见式(1)~式(3),反应机理见图1。

图1 反应机理Fig.1 Reaction mechanism

在酸性条件下,Fe0产生Fe2+。随后,Fe2+与H2O2迅速反应产生羟基自由基(·OH)并导致Fe3+的形成。随后,Fe0表面可以将Fe3+还原为Fe2+。通过芬顿反应,产生的·OH 氧化破络,释放出游离态的金属离子,随即通过化学沉淀去除。
骨胶是从动物体内提取的一种天然物质,可以用作电镀添加剂、施胶剂或者助凝剂[6]。由于骨胶的存在,使得废水中的部分金属离子呈络合态存在。本研究以含骨胶的铜离子、镍离子和铅离子废水为研究对象,通过零价铁类芬顿法氧化破络沉淀,详细地研究了初始pH 值,H2O2投加量,反应时间,铁刨花(Fe0)投加量对重金属离子和有机物的去除效果,并探讨了同时去除有机质和重金属离子的机理。
1 实验部分
1.1 实验材料
铁刨花取自兰州市某机械加工厂,使用前用蒸馏水洗净,以去除表面的污垢;再用质量分数为10%的硫酸浸泡直至产生大量气泡,以去除表面的铁锈;然后置于70 ℃的真空干燥箱中烘干,密封后备用。骨胶为化工厂购买的特级工业骨胶,用70 ℃水浴加热融化后使用。其余化学药剂均为分析纯,按照所需浓度完全溶解后使用。
1.2 实验方法
1.2.1 实验操作
将100 mL 实验用水置于250 mL 锥形瓶中,用稀硫酸调至一定pH 值,加入一定量的铁刨花,将锥形瓶至于160 r/min 摇床上30 min,随后加入一定量双氧水,并继续在160 r/min 摇床上反应一段时间,待反应结束后,用NaOH 调节pH 值至8.0,继续将锥形瓶置于160 r/min 摇床上反应1 h 后取出,静置30 min 后过滤取上层清液进行检测。
1.2.2 模拟废水
实验室配置的模拟废水,将骨胶作为唯一提供化学需氧量(COD)的物质。废水中COD 约为250 mg/L。废水中Cu2+,Pb2+和Ni2+离子的浓度均为5 mg/L。本实验中未进行特别说明,均使用此模拟废水。
1.2.3 实验设计
固定水浴温度为30 ℃,摇床转速为160 r/min,分别考察初始pH 值,H2O2投加量,反应时间,铁刨花投加量对废水COD 和重金属离子去除率,优化工艺条件。
1.2.4 样品表征
采用意大利哈纳公司HI96740微电脑低量程镍浓度测定仪和HI96702 微电脑高量程铜离子浓度测定仪测定镍和铜离子浓度;采用美国哈希公司DR1900 便携式可见分光光度计测定COD;采用日本日立公司的S-48001I 型场发射电子扫描电镜(SEM)对反应前后铁刨花表面和沉淀物进行测定;采用德国布鲁克光谱仪器公司VECTOR-22 型傅里叶变换红外光谱仪(FT-IR)对模拟废水和反应后沉淀进行测定,模拟废水是在室温下干燥后,将其制成废水薄膜后进行测定;采用德国Netzsch 公司的TG-209 型热重分析仪对模拟废水(废水薄膜)和反应后沉淀进行测定;采用尤尼克(上海)仪器有限公司UV−2800A 型紫外可见分光光度计,对反应时铁离子含量使用邻菲罗啉分光光度法进行检测。
2 结果与讨论
2.1 单因素试验
2.1.1 初始pH 值的影响
在H2O2投加量为2 mL/L,反应时间为60 min,铁刨花投加量为30 g/L的条件下,考察初始pH 值对反应的影响,结果如图2 所示。由图可看出,COD的去除率在pH 值为2~6 时,随着pH 值的升高而降低,这是由于在强酸性条件下,铁刨花的表面能短时间产生大量的Fe2+可以催化H2O2产生更多的·OH,有利于Fenton 反应的进行,从而氧化分解有机物,降低COD。随着pH 值的升高,铁刨花表面产生Fe2+的速度变慢,同时过高的pH 值还使得H2O2产生无效分解,不利于Fenton 反应的进行,导致COD 去除率下降。当pH 值在接近7 时COD的去除率又略有提升,这是由于铁刨花产生大量的Fe3+,增强了反应中絮凝沉淀的效果,使得COD的去除率有所升高。由图2 还可以看出,在pH 值为2~5 时,Cu2+的去除率随着pH 值的升高而降低,这是由于pH 值的升高,不利于Fenton 反应的进行。从而导致Cu2+不能被有效地去除。在pH 值为5~7 时Cu2+去除率又升高,这是因为Fe3+与络合物的结合稳定性更高,在反应中Fe3+与络合态金属离子存在置换反应,随着pH 值的升高,溶液中的Fe3+量增多,通过置换反应将溶液中的络合态金属离子解离后,随着调碱生成氢氧化物沉淀而去除,使得去除率升高。Ni2+在pH 值为2 时,去除率最低,这是因为Ni2+的去除主要依靠絮凝沉淀的作用,当反应的初始pH 值小于3 时,溶液中Fe3+的量较少,随着pH 值的升高,Fe3+溶出率升高絮凝沉淀的效果增强使得Ni2+的去除率增高,镍离子除了依靠絮凝沉淀去除,也会与高价铁离子存在置换反应,因此去除率基本维持在98%以上。经过综合考虑,初始pH 值为3 较合适。

图2 初始pH 值对反应的影响Fig.2 Effect to initial pH value on reaction
2.1.2 H2O2投加量的影响
在初始pH 值为3,反应时间为60 min,铁刨花投加量为30 g/L,考察H2O2投加量对反应的影响,结果如图3 所示。由图可知,COD,Cu2+和Ni2+去除率随着H2O2投加量的增加呈现先增加后减少的趋势,H2O2投加量为1.5 mL/L 时去除率最大,分别是59.6%,99.7%和99.6%。这是由于H2O2投加量低于1.5 mL/L 时,反应系统中·OH 不足,其不利于有机物的降解,同时还影响破络的效果,导致COD和金属离子的去除率低。随着H2O2投加量增加,溶液中的污染物去除率明显升高,但当H2O2过量后,由于过量的H2O2会和·OH 反应,使得·OH 减少,H2O2被无效分解,反应如式(4)和式(5)。因此,H2O2投加量为1.5 mL/L 较合适。


图3 H2O2 投加量对反应的影响Fig.3 The influence of H2O2 dosage on the reaction
2.1.3 反应时间的影响
在初始pH 值为3,H2O2投加量为1.5 mL/L,铁刨花投加量为30 g/L,考察反应随时间的变化情况,结果如图4 所示。由图可看出,在60 min 以内,随着反应时间的增加,COD 和金属离子的去除率增加。60 min 时COD 去除率50.8%,Cu2+和Ni2+去除率分别为98.2%和98.22%。当超过60 min 后,反应趋于稳定,COD,Cu2+和Ni2+去除率变化较小。因此,反应时间为60 min 较合适。

图4 反应时间对反应的影响Fig.4 The effect to reaction time on reaction
2.1.4 铁刨花投加量
在初始pH 值为3,H2O2投加量为1.5 ml/L,反应时间为60 min,考察铁刨花投加量对反应的影响,结果如图5 所示。由图可以看出,当铁刨花投加量少于30 g/L 时,随着铁刨花投加量的增加,COD 去除率相应增加,这是因为当铁刨花用量增加时产生Fe2+的量增多,这有利于催化H2O2分解,产生·OH的量增多,从而加快了反应效率。而当铁刨花的量过多时,会导致在很短的时间内产生过量的Fe2+,多余的Fe2+又会与·OH 反应生成Fe3+,反应如式(6),·OH 被消耗不利于反应的进行。综上所述,铁刨花投加量为30 g/L 较合适。

图5 铁刨花投加量对反应的影响Fig.5 The effect of iron dosage on the reaction

2.2 有机物和金属离子的去除机理
铁刨花投加量为30 g/L,加到装有100 mL 蒸馏水的锥形瓶中,在160 r/min 摇床上反应1 h,考察不同pH 值下铁刨花在水溶液中溶出的铁的量,结果见图6。由图可知,铁刨花在强酸性条件下可以溶出大量Fe2+,但随着pH 值的升高Fe2+的溶出量降低,说明在强酸性条件下有利于该Fenton 反应进行。从图6 中还可以发现在酸性条件下,溶液中存在大量Fe3+,这有利于重金属离子在调碱絮凝沉淀过程中被去除。

图6 不同pH 值时溶液中溶出Fe的量Fig.6 Amount of Fe dissolved in solution at different PH values
为考察Fenton 氧化和絮凝沉淀两种作用对废水中COD 和Cu2+去除贡献率的影响,设置3 组实验作对比,设定初始pH 值为3,反应时间为60 min,不同的是第1 组加入1.5 mL/L的H2O2和30 g/L的铁刨花,第2 组只加入30 g/L的铁刨花,第3 组只加入1.5 mL/L的H2O2,反应结果见图7。对比第1 组和第2 组实验结果可知,在第2 组没有添加H2O2的实验中,COD的去除率比第1 组低了11.3%,而Cu2+的去除率仅低了4.2%,说明COD的去除主要有两种方式,Fenton 反应氧化去除和加碱后絮凝沉淀去除,其中氧化去除约占总去除效果的20%,通过絮凝沉淀去除约占总去除效果的80%。以Cu2+为例,对于金属离子的去除,反应中是否投加H2O2没有明显的区别,说明废水中低浓度的重金属离子主要依靠絮凝共沉淀的方式去除。对比第1 组和第3 组实验的结果可知,在只添加H2O2时,对废水几乎没有处理效果,Cu2+的去除率仅有2.8%,并且过量的H2O2还会引起COD的升高,导致COD的去除率为负值。

图7 不同条件对COD 和Cu2+去除率的影响Fig.7 Effect of different conditions on removal efficiency of COD and Cu2+
2.3 扫描电子显微镜分析
图8 为各物质的SEM 图。由图8(a)可知,反应前铁刨花表面形貌较为光滑圆润,存在有大量链状聚集的球形颗粒[7],说明反应前铁刨花表面存在较多的Fe0。由图8(b)可知,反应后铁刨花的表面明显粗糙,产生大量颗粒状和层状结构的物质,出现明显的腐蚀现象,这是由于经过酸的腐蚀表面的Fe0被氧化为Fe2+/Fe3+,提供了足够的Fe2+用于反应。8(c)为反应后沉淀物,可观察到了一些小分子有机物表明反应结束后溶液中的骨胶分子被氧化分解,最终通过沉淀去除。沉淀中还有类似8(b)中的小颗粒或片状结构,判断应该是氢氧化物沉淀,说明溶液中的重金属离子通过氢氧化物沉淀和絮凝沉淀的方式被除去。

图8 各物质的SEM 照片Fig.8 SEM image of each substance
2.4 FT-IR 光谱分析
图9 为各物质的FT-IR 曲线,其中曲线a 对应的物质是骨胶,曲线b 对应的物质是模拟废水,曲线c 对应的物质是Fenton 反应后的沉淀物。由图可知,曲线a 在3426 cm-1[N—H 伸缩或O—H 伸缩(氢键)],1645 cm-1[酰胺Ⅰ带(反对称羧基或基团C=O的伸缩振动)],1 544 cm-1[酰胺Ⅱ带(C—N伸缩振动或N—H 弯曲振动)]出现3 个骨胶的红外特征峰。当骨胶溶解中加入铜、铅、镍等金属离子配置成模拟废水后,骨胶的红外特征峰分别移至3 403,1 654 和1 540 cm-1(见曲线b)。这是由于部分金属离子与骨胶分子中的—NH 和=O 发生了配位反应,并且形成较为稳定的五元环结构[8],而这样的结构导致金属离子的去除变得困难。由图9 所示,曲线c 相较于曲线b 骨胶的3 个红外特征峰无论是峰的强度还是峰的面积都明显的减小。这是由于经过反应后骨胶被降解为小分子有机物,骨胶分子内连接氨基酸的氢键断裂。同时与金属离子发生配位反应的—NH 和=O 也断裂,为去除金属离子提供了条件。

图9 各物质的FT-IR 曲线Fig.9 FT-IR curves of each substance
2.5 热重分析
图10 为Fenton 反应后沉淀和模拟废水的热重分析(TG)曲线。由图可看出,模拟废水的初始热分解温度约为350 ℃,热分解趋于平缓时温度约为490 ℃,而反应后沉淀的初始热分解温度约为220 ℃,热分解趋于平缓时温度约为375 ℃。这是因为沉淀中的有机物是由骨胶氧化分解产生,它的热稳定性不如骨胶,分子中氢键的数量少,分子结构的稳定性不如骨胶分子。这也进一步说明了Fenton 反应能有效地降解骨胶分子。
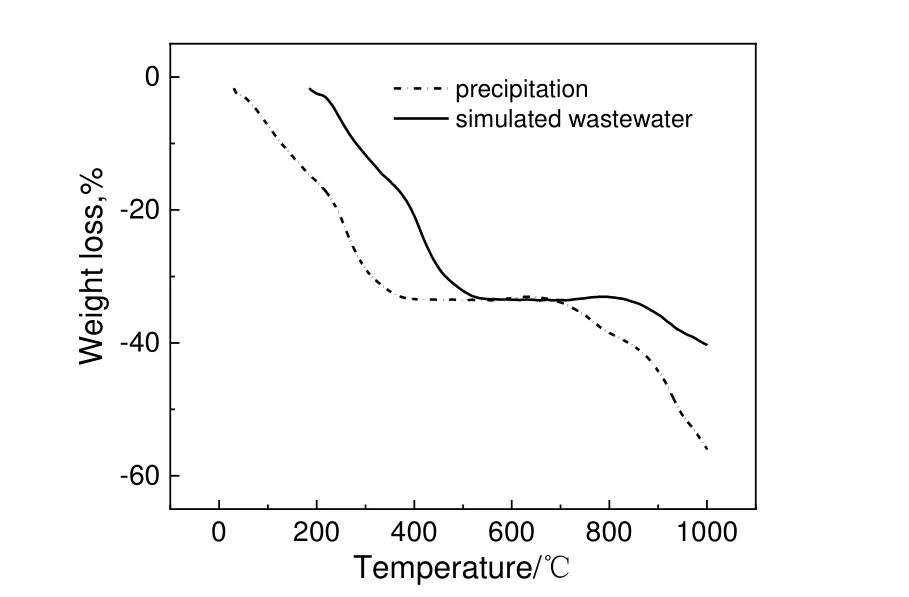
图10 Fenton 反应后沉淀和模拟废水的TG 曲线Fig.10 TG curves of precipitation after reaction and precipitation
2.6 Fe0-类芬顿法与传统芬顿法进行比较
对Fe0-类芬顿法与传统芬顿法处理废水能力进行比较,两组实验均处理100 mL 模拟废水,初始pH 值为3,H2O2投加量为1.5 mL/L。不同的条件为:采用Fe0-类芬顿法组处理的实验需要投加30 g/L的铁刨花;采用传统芬顿法处理废水,当Fe2+与H2O2的物质的量之比为1 时效果最好[9],因此,计算得需投加4.17 g/L的硫酸亚铁。两组对比实验结果如表1 所示。

表1 类芬顿法与传统芬顿法处理效果对比Table 1 Comparison of Fenton-like Method and Traditional Fenton Method
结果表明,Fe0-类芬顿法所使用的铁刨花可以重复使用,但传统芬顿法中的硫酸亚铁无法重复使用,因此传统芬顿法的用药量大。在对废水的处理效果上,传统芬顿法COD 去除率比Fe0-类芬顿法低15%,对3 种金属离子的去除率也均比Fe0-类芬顿法低10%左右。通过产污泥量的对比发现Fe0-类芬顿法的产泥量仅为传统芬顿法的20%,很大程度上减少了运行成本。说明处理该类废水Fe0-类芬顿法明显优于传统芬顿法。
2.7 重复性试验
在初始pH 值为3,H2O2投加量为1.5 mL/L,铁刨花投加量为30 g/L,反应时间为60 min的反应条件下。反应物为配制的模拟废水,将前一次反应后的铁刨花,用蒸馏水清洗表面的沉淀后投入下一次反应中,考察铁刨花重复利用效果,结果见图11。由图可知,COD 和铜离子的去除率随着重复次数的增多都略有降低,经过5 次实验后COD 和金属离子去除率分别在60%和88%以上,仍具有良好的去除效果,并且去除率的下降趋势也明显变缓。将重复反应5 次后的铁刨花冲洗掉表面沉淀并干燥后与反应前铁刨花做对比,反应后铁刨花质量仅减少了0.013 6 g,说明铁刨花作为Fe2+/Fe3+的供体可以多次使用。说明零价铁类芬顿法具有良好的重复性。

图11 重复性实验中COD 和金属离子去除率Fig.11 COD and Metal Ions removal rate in repeated experiments
3 结论
以Fe0-类芬顿法处理含低浓度重金属离子的有机废水,研究了初始pH 值,H2O2投加量,反应时间,铁刨花投加量等因素对实验的影响,结果表明,初始pH 值和H2O2投加量对处理效果影响较大。当初始pH 值为3,H2O2投加量为1.5 mL/L,铁刨花投加量为30 g/L,反应时间为60 min的条件下,处理COD 初始浓度250 mg/L,铜、铅和镍金属离子浓度均为5 mg/L的废水时,COD 去除率为71%,铜、铅和镍离子的去除率分别为99.7%,99.6%和99.6%。与传统芬顿法的比较,发现Fe0-类芬顿法对废水中COD 和金属离子具有去除率更高、产泥量低和所需药品少等优势,有良好的经济效益。铁刨花作为Fe2+/Fe3+的供体参与反应具有良好的重复性。
