腹腔镜肾部分切除术后肾萎缩的影响因素分析
2021-09-28郭园园刘贝贝高五岳李立强岳晓娥杨小淮刘建民
郭园园,刘贝贝,孙 巍,高五岳,李立强,岳晓娥,杨小淮,刘建民
(蚌埠医学院第一附属医院泌尿外科,安徽蚌埠 233004)
肾细胞癌是泌尿系统常见的恶性肿瘤之一,其主要治疗方式根据肿瘤体积大小和位置等不同选择根治性肾切除和肾部分切除术。基于降低手术损伤程度和保留部分肾功能的优点,近年来,腹腔镜肾部分切除术的应用越来越广泛。然而,手术仍不可避免地引起患者急性和慢性肾损伤,尤其术后肾萎缩导致的不可逆性肾单位丧失是术后肾功能恢复的关键因素[1-2]。然而,如何在完全切除肿瘤的前提下最大限度地避免术后肾萎缩仍不明确。因此,本文通过分析临床T1期肾部分切除术患者的临床资料,探讨肾部分切除术后肾萎缩的影响因素,为预防和减少术后肾萎缩的发生提供依据,现报道如下。
1 资料与方法
1.1 一般资料
回顾性分析2016年7月至2019年10月本院泌尿外科行腹腔镜肾部分切除术的120例T1期肾癌患者的临床资料。所有患者均无自身免疫性疾病、高血压、糖尿病及肾病等合并症,术前均通过CT或磁共振成像(MRI)诊断为单侧肾占位,对侧肾正常,且术后病理证实为肾透明细胞癌。
1.2 方法
1.2.1资料收集
收集患者性别、年龄、BMI、肿瘤大小、分期、R.E.N.A.L评分、术前患肾肾小球滤过率(glomerular filtration rate,GFR)、手术时间、热缺血时间及术前、术后3个月、术后6个月双肾CT等资料。根据文献,应用术前和术后3个月的CT计算残余肾实质体积比(percent of preserved normal parenchymal volume,PPV),PPV=术后3个月患肾体积/术前患肾体积×100%[3],根据术后6个月患肾实质厚度小于术前患肾实质厚度,且超过4%则认为存在肾萎缩[4],根据术后肾萎缩情况将患者分为肾萎缩组和无肾萎缩组。
1.2.2手术方式
手术由同一团队主治或主任医师完成,均采用腹膜后途径腹腔镜肾部分切除术。手术过程如下:全身麻醉后取健侧侧卧折刀体位,球囊扩张法制备后腹腔,常规腰背部三操作孔手术,气腹压力调至12 mm Hg。自上方穹窿处向下卷帘样清理腹膜外脂肪,背侧腰大肌前方打开肾周筋膜,于肾周脂肪囊外沿腰大肌表面向内分离,寻找并游离出肾动脉,皮筋穿绕肾动脉,两端钛夹夹闭防止脱出。清理肾周脂肪,充分显露肾肿瘤。血管夹夹闭已游离的肾动脉并计时,在距肿物0.5~1.0 cm处用剪刀将肿物完整切除,使用倒刺线分别缝合深层和浅层,必要时辅助hem-o-lock固定缝线,防止滑脱。去除血管夹恢复血运,观察创面无渗血后取出标本,留置引流管,关闭切口。
1.3 统计学处理
2 结 果
2.1 两组临床资料比较
所有患者均手术成功,术中未损伤重要血管或器官,无中转开放、二次手术或出血行介入手术病例。与无肾萎缩组比较,肾萎缩组R.E.N.A.L评分更高、热缺血时间更长、PPV更小,差异有统计学意义(P<0.05),见表1。

表1 两组临床资料比较
2.2 术后肾萎缩的多因素logistic回归分析
将以上差异有统计学意义的单因素指标纳入多因素logistic回归分析,结果显示PPV(OR=0.010,95%CI:0.001~0.144)为T1期肾部分切除术后肾萎缩的独立影响因素(P<0.05),见表2。

表2 术后肾萎缩的多因素logistic回归分析
2.3 ROC曲线评价PPV对术后肾萎缩的影响
根据诊断效能较高的选择依据,当PPV为83.5%可作为腹腔镜肾部分切除术后肾萎缩的预测值,其灵敏度和特异度分别为74.5%和72.2%,见图1。该结果表明当肾脏损失大于16.5%时,腹腔镜肾部分切除术后可能出现肾萎缩。
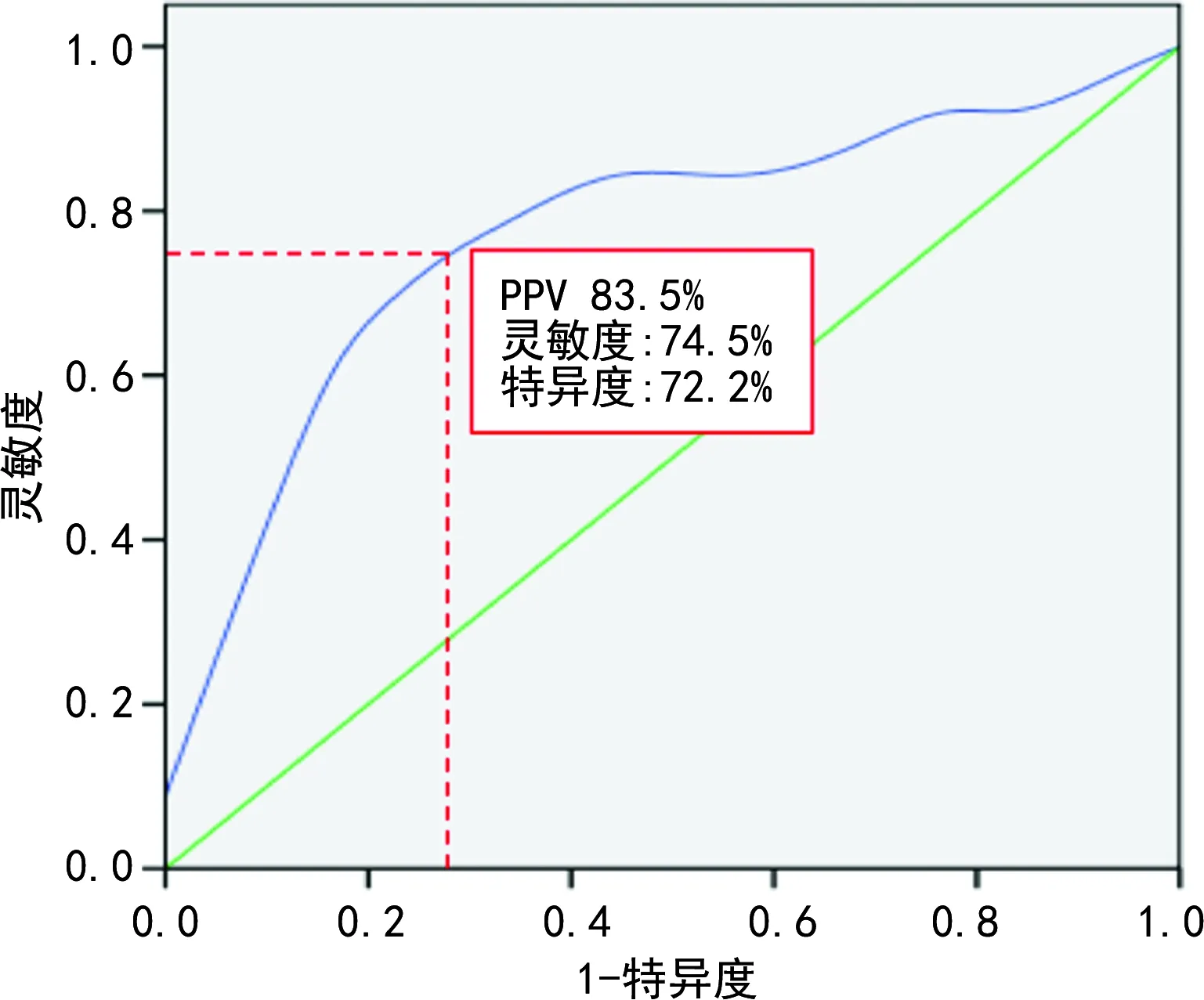
图1 ROC曲线评价PPV对术后肾萎缩的影响
3 讨 论
腹腔镜根治性肾切除术和肾部分切除术已成为标准的肾癌根治性治疗方式。鉴于多项研究结果表明两者在治疗T1期肾癌的生存预后方面无明显差异[5-6],而腹腔镜肾部分切除术可以保留部分肾单位的优势,使其在肾癌治疗中的地位不断升高,且应用范围逐渐扩大至部分T2期肾癌[7]。虽然肾部分切除术避免了患肾的完全切除,但手术仍会损伤肿瘤周围正常肾脏组织,导致术后肾功能不必要的下降。因此,除了改善患者的肿瘤预后,如何最大限度地保留肾单位是肾部分切除术应用中需要解决的另一关键问题。
近年来,腹腔镜手术已基本取代传统的开放手术,尤其机器人辅助腹腔镜肾部分切除术在一定程度上缩短了热缺血时间,减少肾损伤,但仍无法避免部分肾功能的丧失[8-9]。腹腔镜肾部分切除术后主要表现为急性或慢性肾损伤,而后者更易引起不可逆性的肾萎缩,造成肾功能无法恢复。虽然多种因素能够影响肾部分切除术后肾功能恢复,其中肾实质的丢失和重建是术后肾功能下降的主要原因[10-11],而热缺血或低温损伤也是重要的因素[12]。然而,这些因素是否能够导致术后肾萎缩性改变仍存在争议。多项研究发现热缺血时间和术后肾萎缩密切相关,并认为40 min为肾萎缩性改变的临界时间点[4,13]。FUNAHASHI等[14]报道热缺血时间仅超过25 min则出现10%~20%肾实质的减少。与此不同,有研究发现短时热缺血与术后长期的肾功能恢复无明显相关[15]。虽然手术切除造成的肾实质丢失会引起肾功能下降,但目前并未见相关研究表明其与肾萎缩的相关性。
本研究通过分析肾萎缩患者的临床资料,发现R.E.N.A.L评分、热缺血时间与腹腔镜肾部分切除术后肾萎缩相关,R.E.N.A.L评分越高、热缺血时间越长,术后肾萎缩风险越大,该结果与大多数结果基本一致。此外,本研究还发现PPV越小则越容易发生术后肾萎缩,且logistic回归分析结果表明该因素为术后肾萎缩的独立影响因素。为了进一步为临床工作提供可借鉴的依据,本研究绘制了ROC曲线,选取灵敏度和特异度较高的临界点,发现当PPV<83.5%时,腹腔镜肾部分切除术后极可能出现术后肾萎缩,造成肾功能无法恢复。除此之外,因患者高血压、糖尿病等合并症对肾部分切除术后肾功能预后的影响尚存在争论[16-17],故为排除这些因素对结果的影响,本课题组在病例选择中排除存在潜在影响的合并症患者,且选择同一手术团队完成手术的患者,从而增加了结果的可靠性。
以上结果提示腹腔镜肾部分切除术中应在保证完全切除肿瘤的前提下尽量减少正常肾组织的丧失。然而,如何衡量切除边距使其达到最小的安全切除范围仍未达成共识。李园等[18]通过观察和分析T1期肾癌组织和假包膜外癌灶的分布,发现包膜外侵犯和肾癌分级相关,并表明T1a肾癌安全切除边距为0.5 cm以内,而T1b肾癌需扩大至0.5~1.0 cm的肾实质。沈弋桢等[19]检测T1肾癌及不同距离癌旁组织(0.5、1.0、2.0 cm)中上皮膜抗原EMA和肾癌标记物RCC-Ma的表达,表明0.5 cm为早期肾癌腹腔镜肾部分切除术的安全边距。本课题组进一步通过免疫组织化学检测了肾癌周边组织中细胞程序性死亡-配体1(PD-L1)和PD-L1的表达,认为切除癌组织边距1.0 cm可能是较为安全的选择[20]。可见,目前关于肾部分切除术切除边距的研究均聚焦于完全切除肿瘤组织,而忽略了保护残余肾组织的功能。本研究更加关注后者,并提出保护肾脏功能的可参考阈值。因此,联合两方面考虑可能为临床切除边距提供最佳的选择。
综上所述,本研究探讨了腹腔镜肾部分切除术后肾萎缩的影响因素,并证实PPV为术后肾萎缩改变的独立影响因素。在此基础上,检测了PPV对术后肾萎缩的预测效能,发现肾脏损失大于16.5%时,腹腔镜肾部分切除术后可能发生肾萎缩。该研究为预防和减少腹腔镜肾部分切除术后患肾萎缩提供了方向,同时为肾肿瘤的切除范围提供了参考。当然,这一发现仍需要更多的临床数据分析进一步证实。
