燃料电池碳基氧还原催化剂的设计与应用
2021-09-28刘苗苗杨茅茂舒欣欣张进涛
刘苗苗,杨茅茂,舒欣欣,张进涛
胶体与界面化学教育部重点实验室,山东大学化学与化学工程学院,济南250100
1 引言
随着化石能源危机与环境污染问题的日益加重,积极推动和发展新能源技术具有重大战略意义。利用清洁可再生燃料(氢气等)发电的燃料电池因其理论能量转化效率高、环境污染少、噪音小等优势而受到广泛的关注。原理上,燃料电池利用燃料在阳极的氧化和氧气在阴极的还原产生电能。电子通过外电路由阳极运动到阴极,阳极产生的阳离子(或阴极产生的阴离子)通过电解质运动到阴极(或阳极),从而实现体系的物质平衡和电荷平衡(图1)1。氧还原(Oxygen reduction reaction,ORR)反应作为燃料电池阴极的关键反应,在化学能向电能的转换过程中发挥着重要作用,然而其缓慢的动力学过程、过高的反应能垒、较低的选择性很大程度上降低了燃料电池的能量转化效率,因此开发高活性的电催化材料以加快反应速率、提高反应选择性是当前研究的重点。碳载铂催化剂(Pt/C)具有优异的氧还原催化活性,是目前燃料电池最常用的催化剂。但是,贵金属资源有限,价格昂贵,并且Pt在碳载体表面的迁移和团聚限制了稳定性2。因此开发低成本、高催化活性及耐久性的非贵金属催化剂至关重要。
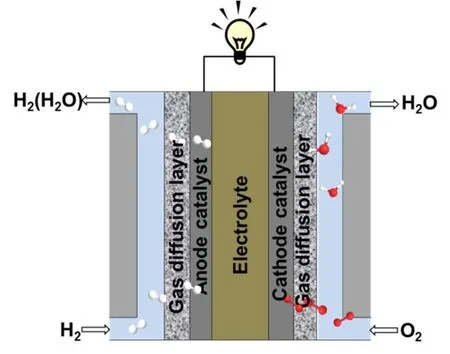
图1 燃料电池工作原理示意图Fig. 1 Schematic diagram of working principle of fuel cells.
碳材料具有结构多样性(包括石墨烯、碳纳米管、碳纳米纤维、碳纳米球等多维结构)、良好的导电性、较高的比表面积以及在电化学环境中的高稳定性等优点,在清洁能源转换和储存领域有着广泛的应用3-6。杂原子掺杂碳基催化剂(氮7,8、磷9,10、硫11,12、硼13,14等)通过改变邻近碳原子的sp2自旋电荷分布,从而影响氧还原中间体的吸附态,促进氧气的还原15-17。过渡金属与杂原子掺杂碳基催化剂能够利用过渡金属与杂原子的相互配位和协同作用,创造更多活性位点,从而提高催化剂的氧还原催化活性18,19。本文将总结杂原子掺杂和过渡金属引入的碳基催化剂的合成思路及其氧还原催化活性的影响规律和燃料电池中的性能优化,并对碳基催化剂在研究中的发展趋势进行展望。
2 非金属杂原子掺杂碳催化剂
自Dai等8提出氮掺杂的碳纳米管作为无金属碳基催化剂,表现出优异的电催化活性及稳定性以来,非金属杂原子掺杂的碳材料(石墨烯8,16,20、碳纳米管14、碳纳米纤维21)引起广泛关注。氮原子掺杂的碳材料中,氮原子与碳原子电负性的差异导致邻近的碳原子周围呈现相对较高的正电荷密度,从而改变催化剂的表面电子构型,为氧气分子及其还原中间体的选择性吸附创造了更多活性位点;同时,氮诱导的电荷离域使得O2分子的吸附态由端键吸附变为桥式吸附,降低O2吸附的能量势垒,进而提高氧还原活性15,16。石墨氮、吡啶氮、吡咯氮、氧化氮以及sp-杂化氮是掺杂氮在碳材料中的主要存在形式(图2),是改变碳材料催化活性和机理的活性位点22,23。Xu等24在950 °C氩气气氛中热解炭黑与尿素混合物得到氮掺杂碳催化剂。结合X射线光电子能谱(XPS)和理论计算结果表明氧还原的催化活性与吡啶氮、吡咯氮的含量呈明显的正相关关系。Nakamura等17通过氩气刻蚀及随后的氨气气氛热解设计得到以吡啶氮为主的高定向热解石墨(HOPG),结合二氧化碳程序升温脱附(CO2-TPD)测试发现氧还原的催化活性主要依赖于邻近吡啶氮的具有路易斯碱特性的碳原子。众多的研究工作以不同的方式方法设计合成氮掺杂的碳材料用于氧还原催化过程25-28。结合以上不同氮掺杂形式催化活性的探讨,通过合理的实验设计揭示氮掺杂碳材料催化活性中心仍然是当前研究和关注的热点问题。

图2 X射线光电子能谱(XPS)表征的氮掺杂碳催化剂中的典型氮物种及其结合能22,23Fig. 2 Typical nitrogen species in N-doped carbon and their binding energies 22,23.
相比于单一的氮原子掺杂,氮和磷9,10,29,30、氮和硼13,31、氮和硫32,33等共掺杂碳材料由于其不对称电子结构的增强,往往表现出优于单一杂原子掺杂的催化活性。磷与氮位于同一主族,具有相似的电子结构与化学性质。理论计算表明,磷的原子半径(0.119 nm)大于氮和碳,掺杂碳材料与周围碳原子形成非平面的四面体结构。同时,电负性的差异使得磷原子与周围原子能够形成极性共价键,可能会破坏碳原子的电中性结构,导致磷原子表面富集正电荷成为潜在的氧气分子吸附位点,改善碳材料的氧还原催化活性34。Zhang等35以植酸为磷源,双氰胺为氮源,聚乙二醇为软模板,制备了氮磷共掺杂的单层石墨碳纳米笼催化剂。电化学测试结果显示其氧气还原的半波电位为0.91 V (vs RHE),比商用Pt/C催化剂高出76 mV;与石墨烯结构相比,类似富勒烯结构表面氮、磷位点具有更大的不对称自旋分布,使得氧还原活性显著提高。Wang等33将硫脲与氮磷掺杂的多孔碳共热制备了三元掺杂的三维多孔碳催化剂。在酸性和碱性电解质中,该催化剂均表现出优异的氧还原活性,且催化性能得到较大的提高。X射线近边吸收谱(XANES)结果显示还原态硫(-C=S-,-C-S-C-)对催化活性的提高起到主要作用,这归因于硫掺杂导致电子自旋密度的变化显著影响氧还原的催化活性位点。因此,杂原子掺杂对碳原子电子结构和自旋状态的影响有助于提高碳基催化剂的氧还原活性。同时,丰富的有机前驱体为共掺杂碳催化剂设计和催化活性调控提供了多种可行方案,但是,掺杂方式和形式的调控以及性能最优化设计仍是当前研究的重点和难点。
燃料电池中,氧还原过程发生在气、液、固三相界面处,故对于催化剂而言一定的孔隙度和多孔结构是很重要的,有利于电解质溶液的渗透和O2的传输。二氧化硅常用作硬模板制备多孔碳催化剂。但是,去除硅模板需要使用腐蚀性的氢氟酸或浓碱溶液,导致该类方法复杂且对环境不利36。无机盐模板(CaCO337、ZnCl238,39、NaCl40,41等)具有简单易得、环境友好等优点,有助于构建多孔结构,降低电子传递阻力,加速氧气和电解质的传输与扩散,为氧气分子的转化提供丰富的活性位点,从而提高电催化活性。例如,Wei等40以氯化钠晶体作为纳米结构模板,利用聚苯胺等原料高温碳化制备具有多级孔结构的氮掺杂碳材料。作为质子交换膜燃料电池阴极催化剂,峰值功率密度可达到600 mW·cm-2。Xiao等37以明胶为碳源,CaCO3为模板、KHCO3为活化剂,高温热解制备三维蜂窝状多孔氮、氧共掺杂碳催化剂,比表面积达3099.6 m2·g-1,表现出优异的氧还原活性。此外,Zhang等10利用苯胺在植酸存在下溶液聚合、无模板直接热解,制备氮磷共掺杂的三维介孔碳泡沫材料,增大的比表面积有助于暴露出大量的活性中心,使得催化剂氧还原活性可与Pt/C相当(图3)。Zhi等42利用同轴纺丝技术合成了氮磷共掺杂的中空碳纳米纤维膜,其多孔结构和较大的比表面积有利于降低离子电阻来改善电解液离子的传输动力学,从而提高本征催化活性。

图3 氮磷共掺杂的三维介孔碳泡沫催化剂合成示意图10Fig. 3 Schematic illustration of the synthesis process for the N and P co-doped mesoporous nanocarbon (NPMC) foams 10.
基于杂原子掺杂的深入研究发现,杂原子掺杂位置导致的碳基催化剂内在缺陷的存在对氧还原活性及稳定性的作用不可忽视43。Chen等44以二氧化锰球作为苯胺聚合的引发剂和自牺牲模板,热解得到氮磷共掺杂的多孔碳球。实验结果表明高孔隙率允许更多的杂原子掺杂边缘位点,暴露更多活性位点,展现出更为优异的氧还原催化活性,首次从实验上揭示了边缘掺杂对催化活性的影响。智林杰等45利用化学氧化策略对多壁碳纳米管逐步剥离,调节氧化程度实现边缘位点的可控暴露。实验结果表明电导率与边缘位点呈现一定程度的依赖性,边缘位点的过度暴露会导致电导率的降低,电子传递受阻。硫脲作为氮源和硫源修饰氧化碳纳米管,边缘位点充当锚定位点以容纳杂原子。边缘调控和杂原子掺杂的协同效应诱导相邻碳原子电荷离域产生额外的活性中心,从而改变O2的化学吸附态,有效削弱O-O键,提高氧还原催化活性。
3 过渡金属与杂原子协同掺杂碳催化剂
过渡金属(铁、钴、镍等)氧化物、氮化物具有原料来源丰富、良好的电催化活性等优点,被认为具有替代贵金属作为氧还原催化剂的可能。然而,其电导性差、易于团聚等问题导致氧还原活性远远低于预期。以高导电性的碳材料为基底,非贵金属与氮原子通过配位作用协同掺杂碳材料,有利于改善催化剂的电催化活性,因此,过渡金属杂原子掺杂碳材料是很有前途的非贵金属催化剂。过渡金属掺杂碳材料通常包括纳米颗粒负载的碳催化剂和单原子掺杂的过渡金属基碳催化剂两种类型。
纳米颗粒负载的碳催化剂的一般合成策略是将金属盐、氮源和碳源混合直接热解碳化。聚苯胺10、聚吡咯46、聚乙烯亚胺11,47等含氮有机聚合物常被用作氮源及碳源。二氧化硅48常作为硬模板有效调控碳催化剂的多孔结构。Atanassov等49以氨基吡啶有机分子为氮源,采用牺牲支撑法聚合制备铁-氮-碳(Fe-N-C)催化剂,表现出优异的氧还原活性。此外,Zhang等50采用锌介导的模板合成策略合成了铁-氮-碳催化剂。其中,锌的还原作用可以有效地避免高温热解过程中Fe3C@C纳米颗粒的形成,而二氧化硅硬模板用于创造介孔碳纳米结构,为氧还原提供大量活性位点。电化学测试结果显示其氧还原性能优于商业Pt/C催化剂。Shu等20以单宁酸作为螯合剂,将钴离子均匀地固定在氧化石墨烯薄片表面,有效避免了钴纳米颗粒团聚。随后,在NH3条件下热处理,原位形成了Co5.47N纳米颗粒嵌入的多孔氮掺杂石墨烯。其氧气还原的半波电位可以达到0.94 V (vs RHE),优于商业Pt/C 21 mV。Ji等51将羧基修饰的碳纳米管、聚丙烯腈、锰盐、镍盐共混后静电纺丝。随后,碳化制备得到具有Ni|MnO异质结构的多孔碳纳米纤维。其中,碳纳米管的羧酸基团作为锚定位点稳定金属离子,避免其自团聚,从而提高催化剂活性位点密度。
金属有机骨架材料(MOFs)是一类由金属离子与多齿有机配体自组装形成的周期性网状骨架的多孔材料,与传统多孔材料相比,具有比表面积大、结构多样、孔径可调等优点52,53。最近,MOFs的碳化反应作为合成金属-氮-碳(M-N-C)催化剂的自牺牲模板法而备受关注。M-N-C催化剂由于FeNx、CoNx等配位结构的存在而表现出优异的四电子还原催化活性。由MOFs衍生的M-N-C催化剂不仅具有丰富均匀的催化活性位点,其多孔结构有利于优化传质过程与电子输运。一般来说,以锌基MOF作为模板,利用Zn在1000 °C左右高温条件下热解蒸发特性,可以合成多孔结构的氮掺杂碳催化剂,增加催化反应活性位点54,55。例如,Xue等56以血红素和ZIF-8 (2-Methylimidazole Zinc Salt)为前驱体,采用一步热解法制备了酸性和碱性介质中具有良好ORR催化活性和稳定性的分级结构多孔碳(Zn/Fe-N-C)催化剂。其中,ZIF-8前驱体中独特的烃类支链及其Zn2+的空间分离有效防止了Fe2+团聚,直接转化为Fe-N-C结构,在保持其原有多面体结构的基础上Zn的蒸发增大了催化剂的孔隙率与表面积。He等57在合成MOF过程中引入表面活性剂,利用表面活性剂的限域效应,制备得到核壳结构的Co-N-C催化剂,从而提高活性位点密度,表现出不错的氧还原性能。
单原子掺杂的过渡金属基碳催化剂具有高效的原子利用率和较高的电催化活性(图4)。Xu等58提出二氧化硅介导的MOF模板策略制备单原子Fe掺杂的屋檐状碳催化剂。二氧化硅包覆MOF产生的吸附力有助于缓解MOF前驱体的各向异性收缩以及热解过程中十二面体平面的坍塌;屋檐状结构在提供更多的拉伸边缘的同时最大限度地暴露具有催化活性的金属位点,从而在酸性和碱性介质中都表现出优异的氧还原性能(图4b)。Deng等59通过调节ZIF前驱体中锌与钴的配比,实现了原子、团簇以及颗粒不同聚集度钴基金属催化剂的可控合成。Zn2+的引入部分取代了MOF中原有的Co2+位点,在原子水平上实现了Co2+的空间分离。与金属颗粒相比,以碳材料作为基底的单原子分布能够充分均匀分散和利用活性的金属原子。Feng等60则采用氯化铵低温后处理方法,选择性地去除石墨烯层包覆的金属纳米颗粒,弥补了酸洗只能去除暴露的金属纳米颗粒的不足。同时,内部颗粒的去除增加了催化剂的比表面积和孔容,降低了金属含量,暴露了更多的活性中心。最终,该催化剂在酸性电解质中展现出氧还原反应的高催化活性和稳定性,为单原子掺杂催化剂的制备提供了一个新的思路(图4a)。

图4 (a)氯化铵处理制备单原子催化剂示意图60,(b)“屋檐状”碳催化剂示意图58Fig. 4 (a) Schematic illustration of the removal of M-NPs from M-N-C ORR catalysts by a low-temperature NH4Cl-treatment process 60; (b) schematic illustration of synthesis process of Fe/OES(Fe/overhang-eave structure) 58.
大量研究表明,金属中心在氮掺杂碳催化剂中并非一个孤立的活性位点,而是与周围杂原子配位来催化氧还原反应61-65。Zitolo等66结合穆斯堡尔谱和X射线吸收近边光谱(XANES)共同揭示,铁-氮-碳催化剂中FeN4C12的卟啉平面结构有助于实现较高的氧还原活性。同时,氨气气氛中热解形成的高碱性氮基团进一步增强了基团的催化性能。Yao等67进一步强调边缘位FeN4结构的重要性。理论计算表明缺陷形成的边缘位FeN4结构导致更为显著的局部电子重分布和带隙收缩,使其对氧还原四电子过程的能量势垒降低(图5)。最近的研究认为吡咯氮配位的FeN4可能是具有优异氧还原活性的来源,吡咯氮不仅可以调控键合铁原子的氧气分子吸附能,而且可以诱导相邻碳原子形成FeN4-C8结构作为活性位点以提高氧还原本征催化活性68,69。Zhang等70在氨气气氛中高温热解聚苯胺前驱体,得到含有高纯吡咯氮配位FeN4结构的催化剂,将其与氩气气氛焙烧得到的样品对比表明,氨气热解辅助去除多余的碳原子,引起FeN4位点周围氮原子的变化,促进吡啶氮构型向吡咯氮和吡咯氮配位FeN4结构转变,结合理论计算结果揭示吡咯型FeN4表现出较高的四电子反应选择性。此外,钴在氧还原催化过程中不会发生芬顿反应,使得钴-氮-碳催化剂作为氧还原催化剂表现出不错的活性57,64,71-74。尽管其应用于燃料电池的功率密度较铁-氮-碳相对较低,但其不错的发展潜力依旧受到广泛关注,对于钴-氮-碳的催化机理研究也在不断展开。Sun等73对钴掺杂石墨烯的CoN4和CoN2配位结构和ORR机制进行了理论研究,表明CoN4表现出更低的反应能垒。Wang等72借助高角度环状暗场成像-扫描透射电子显微镜(HAADF-STEM)图像和电子能量损失谱(EELS),在原子尺度上直接观察到配位的单原子钴位点,结合XANES表明CoN4配位结构的形成。Xiao等64通过控制催化剂结构,合成了具有双核Co2Nx位点的钴-氮-碳催化剂,借助HAADF-STEM直接观察到双核位点,并通过扩展X射线吸收精细结构(EXAFS)结合密度泛函计算确定了构型Co2N5,与CoN4位点相比,表现出更低的ORR能量势垒及催化活性。

图5 (a)中心位FeN4与边缘位FeN4模型的最高占据轨道(HOMO)及最低空轨道(LUMO)电荷分布;(b)氧还原自由能图;(c,d)不同金属添加量的缺陷变化及氧还原活性对比67Fig. 5 (a) The highest-occupied molecular orbital (HOMO) and lowest-unoccupied molecular orbital (LUMO)distributions of the c-ND-Fe (a) and e-ND-Fe models; (b) oxygen reduction reaction (ORR) free-energy diagrams of the c-ND-Fe and e-ND-Fe models; (c, d) the comparison of defect variation and ORR activities 67.
单金属位点的碳催化剂可以通过引入额外的过渡金属或异质原子来形成新的配位结构以改善电催化活性75。Hu等76通过热解多巴胺包覆的MOF,将原子分散的钴-镍位点嵌入到氮掺杂的中空碳纳米立方体中,球差校正扫描透射电子显微镜(AC-STEM)和同步X射线吸收光谱(XAS)技术证明了孤立的单金属位点的存在。同时,理论计算结果表明,与单金属催化剂相比高反应活性的单原子催化位点和双金属配位的Co-Ni-N结构的协同作用有效降低了氧还原的反应势垒,从而加速了反应动力学。Li等77采用吡咯-噻吩共聚物热解的方法将铁单原子锚定于硫、氮共修饰的多孔碳催化剂,XAS和XPS结果揭示,铁与氮形成FeN4配位结构,硫掺杂影响了铁周围配位的氮的电荷密度,促进了中间吸附物种(OH*)的释放,加速了氧还原过程。Yuan等46从理论和实验的角度揭示,氮磷双配位的铁掺杂碳纳米片优异的催化活性得益于磷部分取代氮原子形成Fe-N3P活性位点,导致氧还原反应过程中捕获氧气的能力增强,加快了反应动力学,表现出与Pt/C相当的电催化活性。
4 碳基催化剂阴极在燃料电池中的应用
4.1 质子交换膜燃料电池(PEMFCs)
质子交换膜燃料电池(Proton exchange membrane fuel cells,PEMFCs)是一种具有发展前景的可持续新能源转换技术78,79。基于质子交换膜材料的广泛研究与商业化,开发在酸性介质下具有优异氧还原活性的阴极催化剂尤为重要。在酸性条件下,氧气的连续质子化反应是电催化还原的主要机理80:
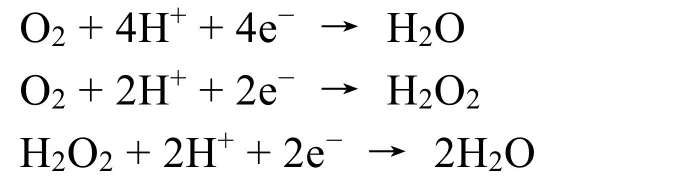
杂原子掺杂碳催化剂作为PEMFCs阴极的研究受到广泛重视81。最近,Xing等82制备得到三维氮磷共掺杂的碳纳米片催化剂,其峰值功率密度可达到579 mW·cm-2,这归因于合成过程中,ZnCl2热解形成的大孔结构以及氮磷共掺杂诱导的极化碳原子的高催化活性。Peng等83采用NaCl/ZnCl2双模板作为膨胀剂,以木质素制备得到三维多级孔碳催化剂,达779 mW·cm-2的功率密度,优于大部分文献报道的杂原子掺杂碳催化剂。无金属碳基催化剂无需考虑金属离子失活以及耐腐蚀的优势,被广泛用作模型电极催化剂研究氧还原的反应机理和催化活性中心84。在燃料电池单电池测试中有待于开发更多类型的具有优异电池性能的无金属碳基催化剂。
过渡金属与杂原子协同掺杂的碳催化剂表现出不错的电池性能。然而对于过渡金属基氮掺杂碳催化剂而言,直接热解得到的金属氮掺杂碳催化剂往往面临金属颗粒团聚的问题,极大地限制了电池效率85,因此增大阴极催化剂的比表面积和孔隙度,提高金属颗粒的分散度,对于改善PEMFC的性能起着重要的作用。表1总结了近期过渡金属基氮掺杂碳催化剂应用于PEMFCs的电池性能。例如,Wang等86用聚苯乙烯球模板压型法制备了有序分级多孔结构的铁-氮-碳催化剂并作为PEMFC的阴极,其催化活性达到420 mW·cm-2@0.57 V。Shui等87将介孔二氧化硅包覆于MOF表面,通过650 °C预热使得二氧化硅刻蚀形成具有表面塌陷的丰富微孔结构的载体,利用静电吸附作用将正电荷的邻二氮杂菲-亚铁配合物吸附于载体上,进一步碳化得到单原子掺杂的铁-氮-碳催化剂,最大程度暴露催化剂内部的Fe-N4位点。该催化剂不仅表现出优异的催化活性、高稳定性以及耐甲醇性能,而且作为PEMFC阴极,其催化活性达到0.022 A·cm-2@0.9 V,超过了美国能源部(DOE) 2018年的目标;在H2-空气的工作环境下,该催化剂仍表现出不错的电池活性;并且在250 kPa的H2-O2工作环境中其峰值功率密度达到1.18 W·cm-2,是目前文献报道的最高值之一(图6)。
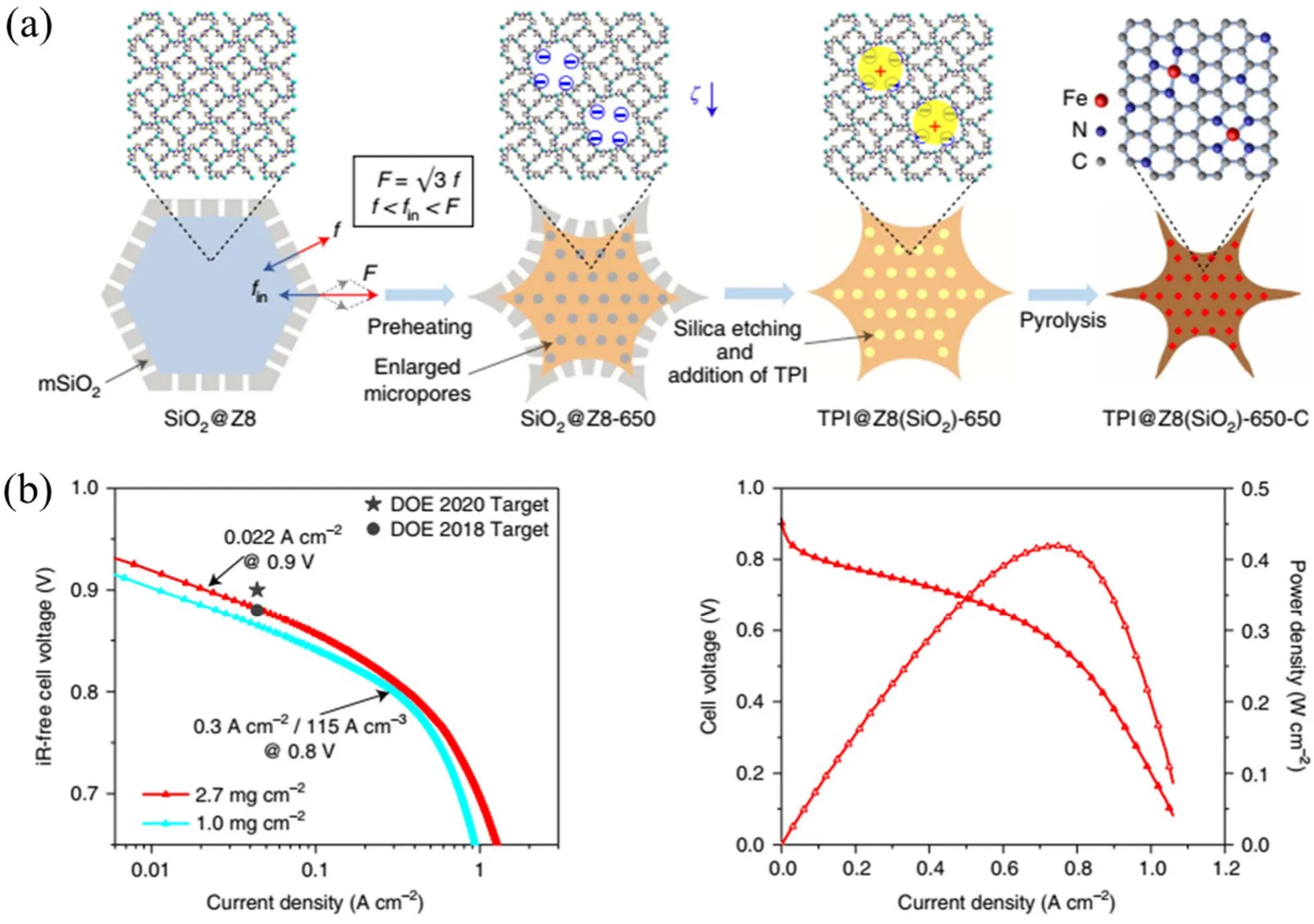
图6 TPI@Z8(SiO2)-650-C催化剂的合成路线及PEMFC性能87Fig. 6 The synthesis and PEMFC activity of TPI@Z8(SiO2)-650-C catalyst 87.

表1 近期发表的阴极催化剂在PEMFCs中的性能比较Table 1 The comparison of PEMFCs activities of cathode catalysts recently published.
过渡金属与杂原子协同掺杂的碳基催化剂的稳定性对于燃料电池的发展有着重要作用。Zhang等93通过在ZIF-8合成过程中引入Fe2+部分取代Zn2+,制备得到铁含量可控的原子分散的铁-氮-碳催化剂,表现出不错的初始电池活性。但是,运行100 h后,电池性能有所下降。同样,Proietti等94合成的铁-氮-碳催化剂在运行100 h后电流密度明显降低。这种情况表明电池运行过程中催化剂的稳定性仍需提高。酸性介质中,催化剂会发生碳腐蚀或金属溶解,碳腐蚀会引起电极表面孔结构的破坏。同时,Fe2+与反应产生的过氧化氢发生芬顿反应,可能毒化活性位点,使得电池性能下降81,95。目前,改善催化剂稳定性的策略主要包括提高碳基质的石墨化程度以及M-Nx活性和稳定性。由于钴、锰对芬顿反应的耐受性,钴-氮-碳72,锰-氮-碳91催化剂作为PEMFCs的阴极催化剂表现出不错的稳定性。Li等91以碳化及酸洗后的掺锰的ZIF-8多孔碳作为宿主,进一步吸附额外的锰源和氮源并对其活化制备高活性位点密度的锰-氮-碳催化剂,不仅在酸性介质中具有很好的催化活性,并且其稳定性与铁-氮-碳催化剂有了明显的提升。同时,Li等91借助拉曼光谱发现,锰不仅可作为活性位点提高催化活性,而且有助于提高所得碳结构的石墨化程度,从而改善碳基体的稳定性。Fu等96以NH4Cl作为造孔剂,利用苯胺在氯化铁的催化作用下聚合得到多孔石墨烯状网状结构,借助拉曼结果表明高孔隙导致的石墨化程度的提高有助于改善碳基体的耐腐蚀效果和保持活性位点。
4.2 阴离子交换膜燃料电池(AEMFCs)
近年来,阴离子交换膜燃料电池(Anion exchange membrane fuel cells,AEMFCs)引起研究者们的极大兴趣97。在碱性环境中,阳极氢气氧化和阴极氧气还原的交换电流密度比酸性电解液中高,表现出较高的反应活性。另外,在碱性介质中,水分子不仅作为溶剂,而且作为反应物,提供质子并与O2反应,释放羟基自由基(OH-)80,98。

采用非贵金属催化剂,对电极材料的耐腐蚀性要求较低,有利于降低催化剂成本99。碳基催化剂被认为是很好的碱性体系中的催化剂97。Thiele等100制备了缺陷丰富的杂原子掺杂的碳纳米管。其中,缺陷密度的增加是通过氧化碳纳米管而形成石墨烯纳米带以及高温分解掺杂的氟原子两种策略来实现的,半电池测试显示该催化剂具有优异的氧还原催化活性。进一步将其与Pt/C阳极以及17 μm厚的六甲基对三苯基聚甲基苯并咪唑(HMT-PMBI)碱性膜组装电池组件,测得电池的开路电压为0.9 V,峰值功率密度为250 mW·cm-2。杂原子掺杂碳材料在碱性介质中表现出更为优异的氧还原催化活性10,44,45。例如,Cai等101以管状高岭土为模板,葡萄糖或糠醛为碳源,尿素为氮源,水热得到氮掺杂的碳催化剂,峰值功率密度可达到703 mW·cm-2。这归因于氮的掺杂改变了碳的表面电荷密度,促进氧还原四电子过程;同时,大的比表面积以及丰富的多级孔结构改善了电荷传输过程。
铁基、钴基氮碳催化剂作为AEMFC阴极催化剂也表现出不错的电池性能及稳定性。Li等102提出一种“二氧化铈辅助”策略,利用静电作用将铈离子和铁离子吸附于聚吡咯纳米线上,高温热解得到原子分散的Fe-N-C催化剂。其中,氧化铈在热解过程中起到对铁原子的空间限域作用,从而增加单原子的相对含量,提高氧还原活性,并作为AEMFC阴极表现出496 mW·cm-2的峰值功率密度102。Peng等103利用氯化钠作为模板,将其与葡萄糖、乙二胺四乙酸(EDTA)热解制备氮掺杂碳-氧化钴杂化物(N-C-CoOx),在阳极催化剂PtRu负载量为0.1 mg·cm-2条件下,其峰值功率密度达720 mW·cm-2。过渡金属与杂原子的协同催化作用使其具有不错的发展前景,后续工作需综合考虑催化剂负载量、催化剂层厚度等因素以优化过渡金属基氮掺杂碳催化剂的燃料电池性能。
目前阴离子交换燃料电池逐渐受到研究者们的青睐,然而相比较质子交换膜燃料电池,阴离子交换膜燃料电池目前报道的峰值功率密度高达1 W·cm-2的阴极材料仍然多以铂基、钯基催化剂为主104,105,故想充分利用非贵金属催化剂的优势还需更加深入的研究工作。
5 结论与展望
高活性、低成本的碳基催化剂应用于燃料电池氧还原反应取得了很大的发展。本文综述了具有优异氧还原催化活性的碳基催化剂的设计思路及其在燃料电池方面的应用。杂原子掺杂碳催化剂利用杂原子与碳原子电负性、原子半径上的差异影响碳原子周围电荷密度分布,从而改变氧气分子的吸附状态,改善氧还原活性;过渡金属与杂原子通过配位作用,为氧还原反应创造大量新的活性位点。单原子掺杂充分利用过渡金属与氮原子间相互作用实现高的原子利用率,显著提高其电催化活性。将碳基催化剂应用于燃料电池提高电池性能,表现出不错的发展潜力。未来碳基催化剂在燃料电池中的发展可能从以下几个方面展开:
(1)目前,高催化活性的燃料电池阴极催化剂设计合成与性能方面取得很大进步,然而其应用于燃料电池的稳定性问题是制约其实际应用的重要因素。因此,精确调控碳基催化剂的形貌、结构及原子配位状态,充分利用碳基催化剂高稳定性优势,提高燃料电池的稳定性。此外,可以开发具有催化剂和扩散层的集成膜电极,利用如静电纺丝技术等发展碳基自支撑电极。
(2)尽管目前大部分材料基于旋转圆盘电极测试技术表现出优异的氧还原活性,但由于燃料电池反应体系的复杂性以及实际应用过程中催化剂的负载量较大等问题,导致很多催化剂应用于燃料电池的实际性能差强人意。将催化剂应用于膜电极组件能够对其燃料电池性能进行更为客观准确的评估。因此,燃料电池整体性能的评估需要综合考虑催化剂、电极结构、燃料电池温度、湿度等条件的影响。未来对氧还原催化剂的性能评价应着重将其应用在实际能源器件,更为准确直接地评估催化剂的可行性。
(3)借助原位技术跟踪研究电极材料在电池运行中的变化过程,深入剖析电极材料微观结构变化对电池性能的影响,为燃料电池催化剂的设计及应用提供理论指导。
猜你喜欢
杂志排行
物理化学学报的其它文章
- 有序金属间化合物电催化剂在燃料电池中的应用进展
- Recent Progress in Proton-Exchange Membrane Fuel Cells Based on Metal-Nitrogen-Carbon Catalysts
- 提升燃料电池铂基催化剂稳定性的原理、策略与方法
- 高温聚合物电解质膜燃料电池膜电极中磷酸分布及调控策略研究进展
- Formic Acid Electro-Oxidation Catalyzed by PdNi/Graphene Aerogel
- Enhanced Performance and Durability of High-Temperature Polymer Electrolyte Membrane Fuel Cell by Incorporating Covalent Organic Framework into Catalyst Layer
