DWI联合MRI动态增强扫描在诊断子宫内膜癌中的价值分析
2021-09-27周永钢张莹坤
周永钢 薛 鹏 张莹坤
1.柘城中医院影像科 (河南 柘城 476200)
2.郑州市人民医院影像科 (河南 郑州 450000)
3.柘城中医院内科 (河南 柘城 476200)
子宫内膜癌是妇科常见恶性肿瘤之一,目前该疾病发病率成稳步上升趋势,且其预后取决于总体分期、宫颈间质、组织学分级等诸多因素[1]。故早期合理的诊断以尽早予以合理的手术方法是延长生存期的关键。因病理组织学检查创伤较大且重复性较差等缺陷而限制其作为诊断该疾病的首选方法,随着影像技术的进一步发展,其因重复性好且创伤小的特点成为当前疾病诊断不可或缺的检查方式[2]。目前临床多采用磁共振弥散加权成像(DWI)和MRI动态增强扫描(DCEMRI),其中DWI是以水分子运动为基础,以提供肌层浸润深度等信息参数[3],但其组织结构分辨率不高。DCE-MRI是通过观察对比剂在血管内分布量、分布时间及清除速度以获取信息参数的方法[4],但动态增强扫描影响因素复杂,易导致结合带显示缺失,以往两种方式单独应用较多,联合应用相对较少,或许将两者联合可取长补短。基于此,本研究将探讨DWI联合DCE-MRI在子宫内膜癌中的诊断价值。
1 资料与方法
1.1 一般资料本研究经医院伦理委员会批准,患者及家属同意,选取2017年1月至2019年12月我院收治的132例子宫内膜病变患者为研究对象,以不规则阴道流血为主要表现,排除其他部位恶性肿瘤,近期服用过甾体类激素药物。其中年龄38~70岁,平均年龄(56.85±5.69)岁;体质量22~24kg/m2,平均体质量(22.48±0.28)kg/m2;病程2~20个月,平均病程(7.28±2.69)个月。
1.2 方法MRI扫描仪(Philips Achieva 1.5T)及配套腹部相控阵表面线圈。检查前1d患者半流质饮食,检查前12h服用缓泻药物,减少检查过程中的伪影,检查前适量饮水确保膀胱充盈。
DWI扫描:单次激发SE-EPI序列TR/TE为1500ms/63.2ms,层厚和层距分别为6、1.5mm;b值为800、1000s/mm2,扫描结束后自动生成ADC图。
DCE-MRI扫描:以3D-THRIVE序列行轴位DCE-MRI,TR/TE:5.32ms/1.85ms;矩阵:134×256;FOV:380mm×380mm;翻转角:15°;NEX1:1mm ;层厚:1mm;层距:1mm。然后静脉注射剂量0.1~0.2mL/kg体质量Gd-DTPA,予以生理盐水15mL冲管,进行5个动态扫描后注入对比剂,获取动态扫描数据发送值工作站,获取图像信息。
图像采集均由2名高年资影像学医师进行,最终图像结果由1名经验高年资主治医师综合判定。
1.3 观察指标以病理结果为“金标准”,比较DWI、DCEMRI及两者联合在子宫内膜癌诊断中的敏感性、特异度、阳性预测值、阴性预测值以及子宫内膜癌术前分期情况。
1.4 统计学方法数据全部录入SPSS 22.0软件中分析,计数资料以%表示,采用χ2检验,与“金标准”一致性采用Kappa值,P<0.05表示差异具有统计学意义。
2 结 果
2.1 病理结果以病理结果作为金标准,132例子宫内膜病变患者中,子宫内膜癌108例,占108/132(81.82%),子宫内膜良性病变24例,占24/132(18.18%)。
2.2 单独检查与联合检查诊断结果对比以病理结果作为“金标准”,108例子宫内膜癌中,DWI扫描:102例阳性,6例阴性;DCE-MRI扫描:101例阳性,7例阴性;DWI联合DCE-MRI:106例阳性,2例阴性。24例子宫内膜良性病变中,DWI扫描:4例阳性,20例阴性;DCE-MRI扫描:3例阳性,21例阴性;DWI联合DCE-MRI:1例阳性,23例阴性。见表1。
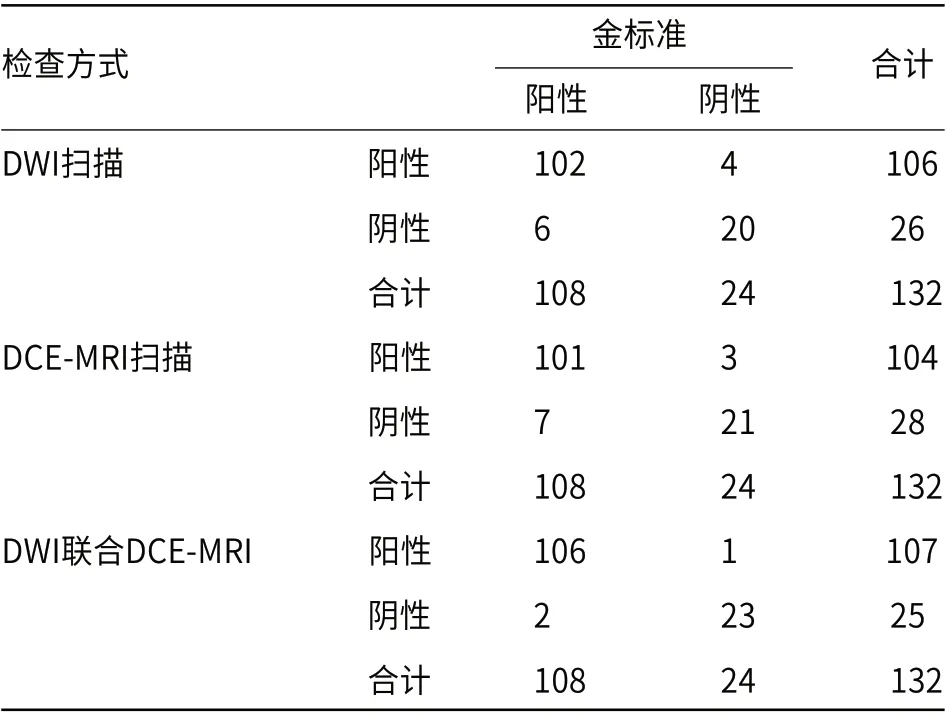
表1 单独检查与联合检查诊断结果对比(例)
2.3 单独与联合检查诊断效能对比DWI联合DCE-MRI敏感性(98.15%)、特异性(95.83%)、阳性预测值(99.07%)及阴性预测值(92.00%)分别较DWI扫描(94.44%、83.33%、96.23%、73.92%)和DCE-MRI扫描(93.52%、87.50%、97.12%、75.00%)高(P<0.05),且与“金标准”的一致性好(Kappa值=0.925,P<0.05),见表2。
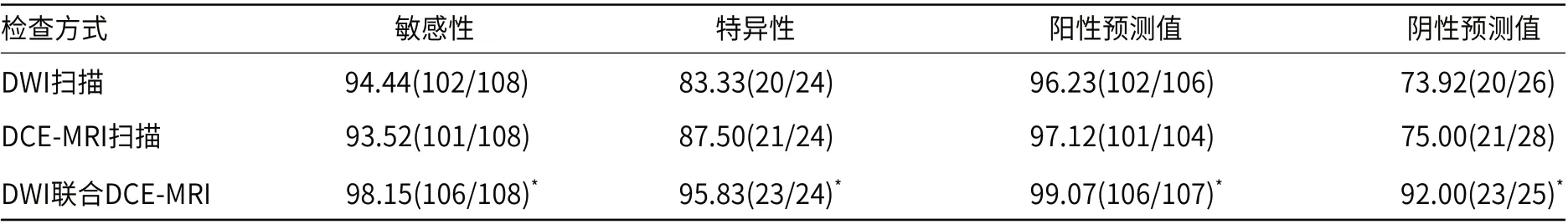
表2 单独与联合检查诊断效能对比[%(n)]
2.4 单独与联合检查对子宫内膜癌术前分期诊断对比DWI联合DCE-MRI对子宫内膜癌术前分期诊断分期符合率较单独检查高(P<0.05),见表3。

表3 单独与联合检查对子宫内膜癌术前分期诊断对比[n(%)]
3 讨 论
目前对于子宫内膜癌发病原因尚未明确,其中主要高危因素包括内源性因素(肥胖、绝经延迟等)和外源性因素(放疗、外源性雌激素应用等)[5]。其早期无明显症状,晚期可转移至腹腔,长期肿瘤消耗可导致全身衰竭表现。手术是治疗该疾病的主要手段,但因患者的治疗方法和预后情况与多种因素有关,除手术治疗之外还需结合病情辅以放化疗等[6]。诊断性刮宫活检虽然可判断病理类型,但其存在盲目性且无法准确判断肿瘤扩散范围、深度等高危因素,故影像学检查在该疾病诊断中具有重要意义。
DCE-MRI是顺磁性对比剂经血管注入后组织T1时间缩短的MRI技术,是以各种组织血液供应和供应来源差异为原理,观察对比剂在不同组织中的分布量、清除速度以及分布时间的差别,定量反映肿瘤血管微循环情况,以评价肿瘤的生物学特性。但由于动态增强扫描影响因素复杂,易导致结合带显示缺失,进而无法准确判断肿瘤是否侵犯肌层等情况,而影响诊断价值。DWI是以活体水分子扩散运动为原理的无创性影像学检查方法,因不同病理状态下,水分子运动受弥散系数影响,其可通过施加扩散敏感梯度场前后组织发生分信号强度变化,精确检测水分子运动微小变化情况,采集清晰图像以定位病灶,能够弥补动态增强扫描时结合带显示缺失而对诊断效能造成的影响。同时DCE-MRI的高组织结构分辨率又可弥补DWI组织结构分辨率相对较差的特点。两者联合取长补短,在准确反映组织微循环血流灌注情况下,又能提供更加可靠的影像学图像,进而提高对子宫内膜癌的诊断价值[7-8]。
本研究中,以病理结果作为“金标准”,132例子宫内膜病变患者中,子宫内膜癌108例,占108/132(81.82%),子宫内膜良性病变24例,占24/132(18.18%);且DWI联合DCE-MRI敏感性(98.15%)、特异性(95.83%)、阳性预测值(99.07%)及阴性预测值(92.00%)均较DWI扫描、DCE-MRI扫描单独检查高(P<0.05),提示与DWI、DCE-MRI单一检测相比,两者联合检测可提高对子宫内膜癌的诊断效能。分析原因:DCE-MRI可通过任意角度断层形成三维重建图像,以准确定位和直接观察肿瘤病灶特点。同时因良恶性病变组织在间隙结构、血管通透性、局部微循环等方面存在明显差异,DCE-MRI可精确判断病灶强化程度以提高其诊断效能。另外,在不同病理状态下,弥散系数、生物膜等因素会对水分子运动造成不同程度的影响,其表现出的图像也存在差异。子宫内膜癌细胞密度高且排列紧密,进而使细胞内外水分子扩散运动受到一定程度的限制,DWI正是以水分子布朗运动为基本原理,利用扩散敏感梯度前后组织之间不同信号强度变化,检测组织中水分子扩散状态,从细胞分子水平上反映微观结构特点和变化情况,获取细胞形态、细胞通透性和不同信号的图像,与DCE-MRI联合不仅从形态上、大小等获取三维重建图像,还可通过细胞中水分子运动状态反映肿瘤细胞内部情况,进而提高对子宫内膜癌的诊断效能。且DWI联合DCE-MRI诊断与“金标准”诊断结果一致性高(Kappa值=0.925,P<0.05),进一步表明联合诊断价值高,这与张梅芳等[9]的研究结果相符。
本研究中,DWI联合DCE-MRI对子宫内膜癌术前分期诊断分期符合率较单独检查高(P<0.05),说明DWI联合DCE-MRI可提高对子宫内膜癌术前分期的诊断。分析原因:恶性肿瘤细胞繁殖速度相对良性肿瘤细胞的繁殖速度快,且单位体积内细胞数量相对较多,进而导致细胞外容积变小,使得水分子弥散运动受到一定程度的限制,进而在DWI图像上表现为高信号,使肿瘤病灶和周围组织形成明显的对比,在广义上的功能呈像可弥补DCE-MRI从形态学上观察子宫内膜分期的不足,但组织结构分辨率相对较差。在动态增强扫描中,因通过观察癌组织和周围肌层存在的血供差异,则在DCE-MRI图像上癌组织和肌层的信号反差较大,其强化程度较周围正常组织低,故延迟其较为明显,进而可清晰显示范围及边缘,以提高组织结构分辨率,两者优势互补,以提高对子宫内膜癌分期的判断,这与张敏等[10]的研究结果相符。
综上所述,DWI联合DCE-MRI可提高对子宫内膜癌的诊断价值,为术前癌症分期提供依据,值得进一步推广。
