慢加急性肝衰竭合并细菌感染患者的临床特征及预后影响因素分析
2021-09-25刘晓燕胡瑾华童晶晶关崇丹彭宇辉严立龙苏海滨
刘晓燕, 胡瑾华, 李 晨, 陈 婧, 童晶晶, 关崇丹, 彭宇辉, 宁 鹏, 严立龙, 苏海滨
解放军总医院第五医学中心 肝病学部, 北京 100039
感染不仅是慢加急性肝衰竭(ACLF)的常见并发症,也是引起患者死亡的主要原因之一[1];严重感染甚至会导致患者失去肝移植机会。有关ACLF合并感染的发生部位及致病菌,不同地区报道不一[2-3],且院内感染是感染相关ACLF发生的独立风险因素。由此可见,感染的及时诊断和治疗有着重要的意义。对既往收治的合并感染的ACLF患者进行了回顾性研究,分析患者临床感染特点及90 d生存率的相关影响因素。
1 资料与方法
1.1 研究对象 选取2014年1月—2015年12月本院收治的ACLF合并细菌感染患者,ACLF诊断符合《肝衰竭诊治指南(2012年版)》[4];原发性腹膜炎、胸腔感染、肝性脑病等并发症诊断符合《肝硬化腹水及相关并发症的诊疗指南》[5];急性肾损伤诊断符合2015年国际腹水俱乐部共识建议:肝硬化患者急性肾损伤的诊断与管理[6];肺炎、泌尿系感染、败血症等诊断标准参考《终末期肝病合并感染诊治专家共识》[7]。排除标准:(1)年龄<18岁;(2)其他脏器严重器质性病变;(3)恶性肿瘤患者;(4)肝、肾移植术后患者;(5)妊娠。
1.2 研究方法 采集ACLF患者基线资料,包括性别、年龄、基础肝病病因;所有患者记录自诊断ACLF至出院时感染发生的相关情况,包括感染发生时间、发生率、感染部位、微生物阳性率及种类等指标;发生感染时血常规、生化、降钙素原、乳酸以及并发症;通过电话随访采集患者自诊断ACLF合并感染后28 d和90 d预后(包括存活、死亡和肝移植)信息。
1.3 伦理学审查 本研究方案经由解放军总医院第五医学中心伦理委员会审批,批号: 2019089D。
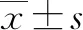
2 结果
2.1 ACLF患者感染发生率及基本情况 共收治ACLF患者1074例,其中合并细菌感染者609例,发生率为56.7%。入组患者中有16例在90 d内行肝移植手术,其余593例均完成了相关数据统计。593例患者中,男女性别比为1∶4.44(109/484),平均年龄(49.83±18.94)岁;525例患者有肝硬化基础;肝衰竭的基础病因包括:HBV感染388例,HCV感染8例,酒精性肝病121例,自身免疫性肝病29例(自身免疫性肝炎16例,原发性胆汁性胆管炎10例,自身免疫性肝炎重叠原发性胆汁性胆管炎综合征3例),药物性肝损伤14例及其他7例(肝窦阻塞综合征、肝豆状核变性各2例,血吸虫、进行性家族型肝内胆汁淤积、非酒精性脂肪性肝炎各1例),不明原因26例。409例为住院48 h内诊断感染,余184例考虑为院内感染。
在合并感染的593例ACLF患者中,感染部位比率由高到低依次为腹腔感染(416例, 70.15%)、肺部感染(244例,41.15%)、败血症(71例,11.97%)、泌尿系统感染(32例,5.40%)、胸腔感染(29例,4.89%),其他部位(口腔、胆道、肛周、胆囊、肠道、皮肤、鼻窦等)或感染部位不明患者51例。64.76%(384例)的患者为单部位感染,29.34%(174例)的患者为2个部位感染,其余合并3、4、5个部位感染的比率分别为5.23%(31例)、0.51%(3例)、0.17%(1例)。
2.2 不同部位细菌培养阳性情况 对怀疑感染的患者均行了血培养,培养阳性患者诊断为败血症。416例原发性腹膜炎患者中有392例行腹水培养,阳性89例,阳性率为22.70%;244例肺部感染患者中有142例行痰培养,阳性75例,阳性率为52.82%;29例胸腔感染患者中有28例行胸水培养,阳性9例,阳性率为35.71%;32例泌尿系统感染患者均行中段尿细菌培养,阳性13例,阳性率为40.63%;此外,有2例为胆道系统感染患者,胆汁引流液培养均为阳性(分别为胶冻罗斯氏菌和大肠埃希菌)。 具体细菌培养阳性结果详见表2。
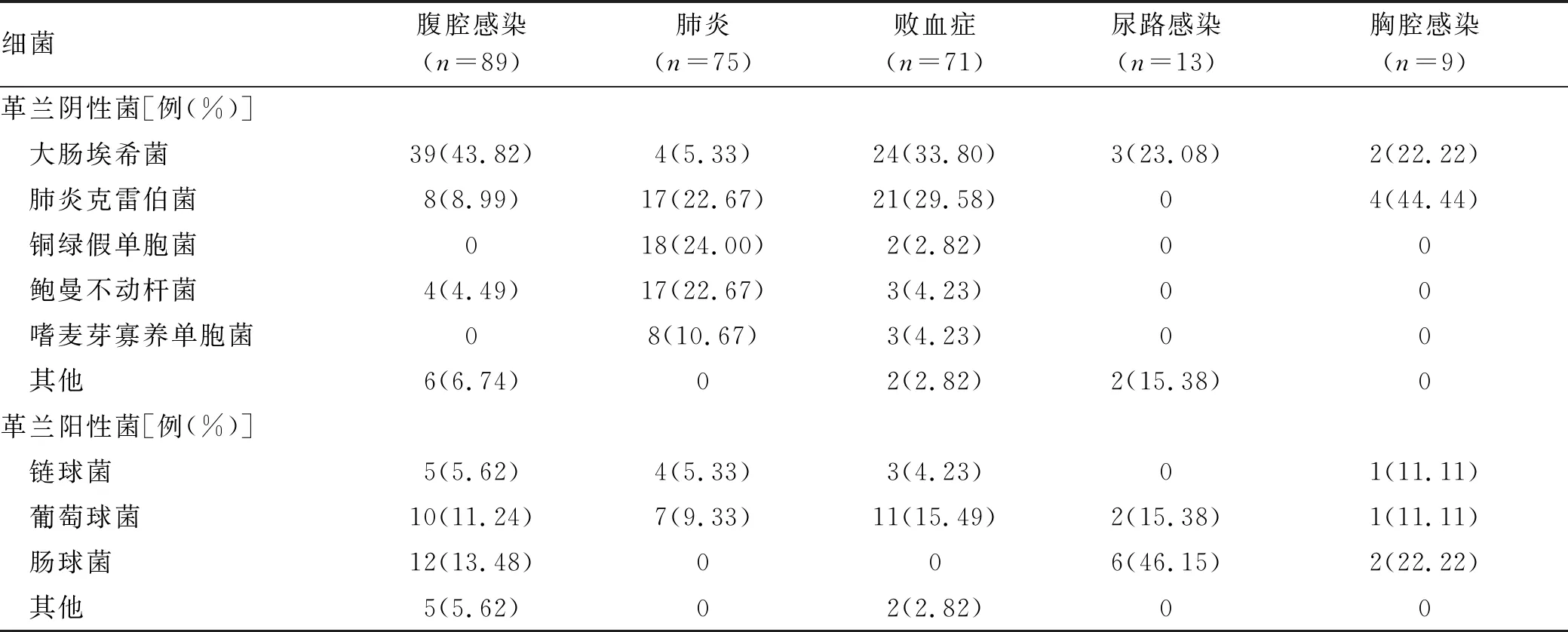
表2 不同部位细菌培养阳性情况
2.3 ACLF合并感染患者的生存分析 593例ACLF患者合并感染后28 d生存率为56.66%(336/593),90 d生存率为38.11%(226/593)。生存曲线见图1。
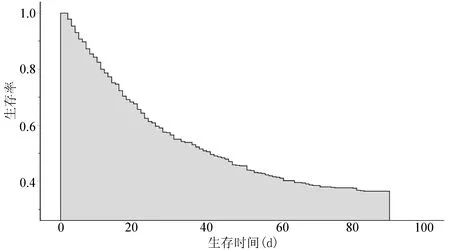
图1 诊断ACLF合并细菌感染后生存曲线
2.4 单因素分析 593例患者诊断ACLF合并感染90 d后,存活226例,死亡367例,两组患者单因素分析结果显示,年龄、病因、感染部位数、肺炎、肝性脑病、上消化道出血、胸腔感染、国际标准化比值、总胆红素、血肌酐、肝衰竭分期、白细胞、中性粒细胞、MELD评分比较,差异均有统计学意义(P值均<0.05)(表3)。
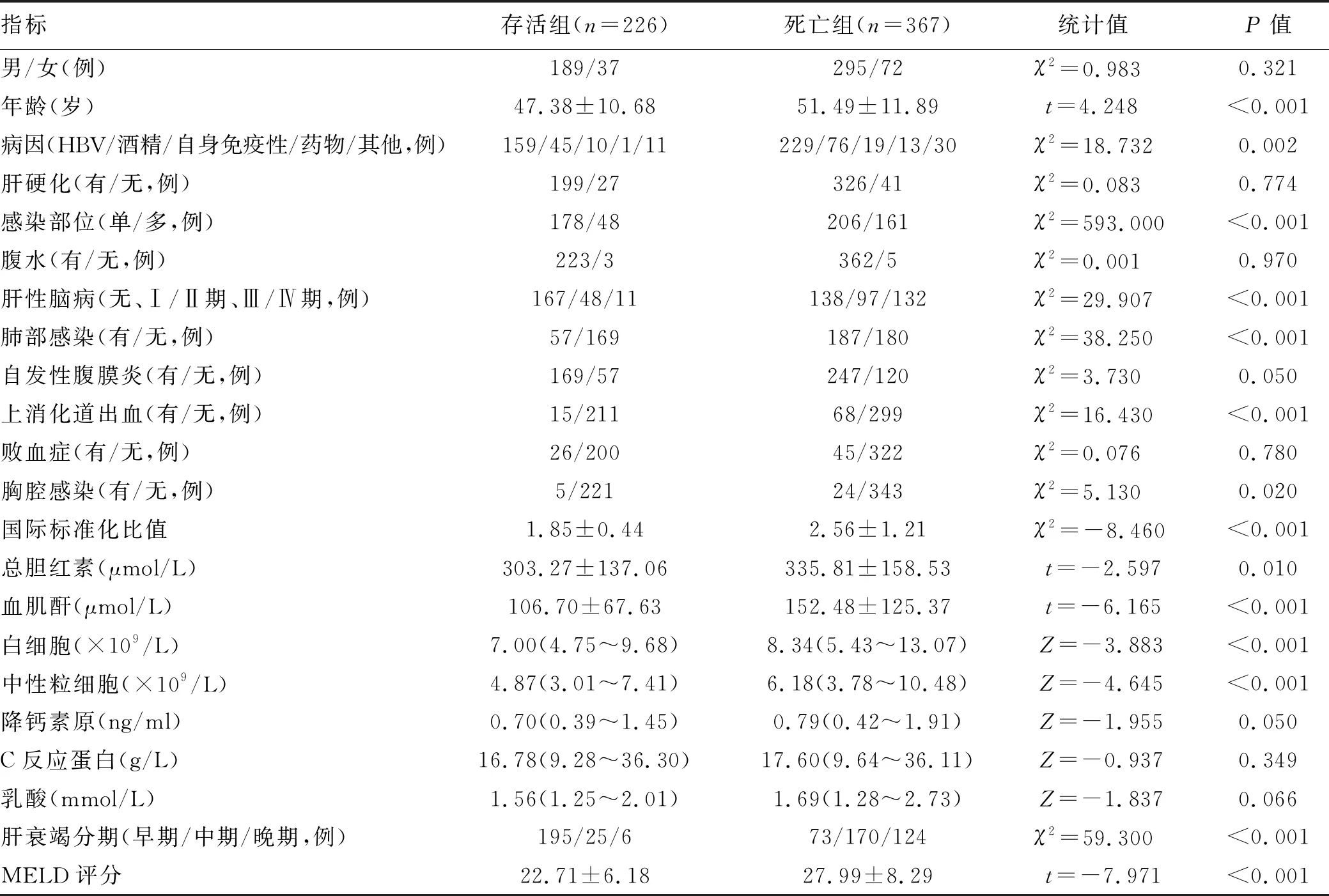
表3 生存组和死亡组单因素分析结果
2.5 多因素分析 将单因素分析结果中对预后有影响的部分指标进一步行多因素logistic回归分析,因国际标准化比值、MELD评分与肝衰竭分期相关,因此仅选择肝衰竭分期进入方程;血清肌酐是急性肾损伤的诊断指标,因此在方程中未将血肌酐作为因变量处理。结果显示,年龄、肝性脑病分期(Ⅲ/Ⅳ期)、肝衰竭分期(晚期)和急性肾损伤均为影响ACLF合并细菌感染患者90 d生存的独立危险因素(P值均<0.05)(表4)。
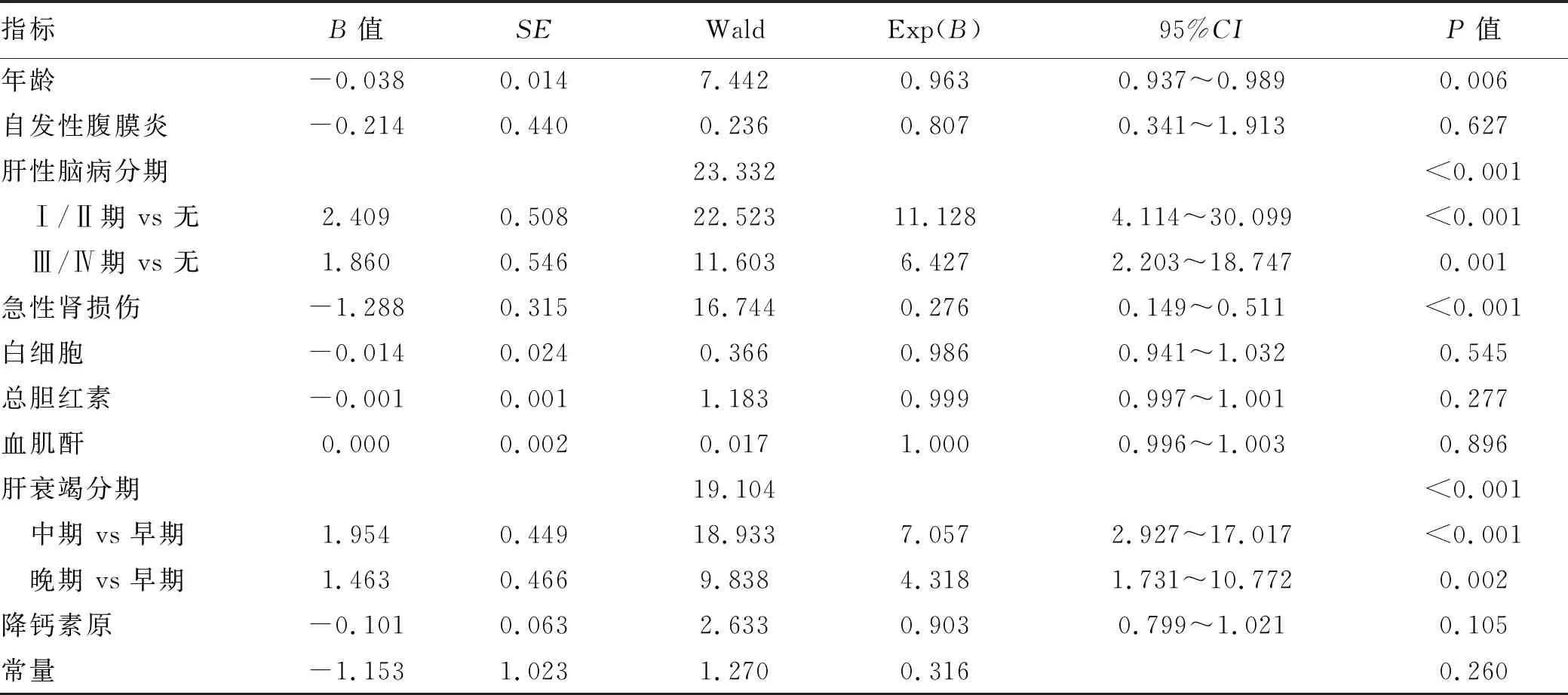
表4 影响ACLF合并感染患者90 d生存的多因素logistic回归分析
3 讨论
ACLF患者易合并细菌感染,感染率高达66.1%[8],发生感染患者的病死率是无感染患者的4倍[9]。目前,相关指南[7,10]提出了终末期肝病患者抗生素应用建议,但各地病原学流行情况、病原菌对抗生素的敏感度存在差异,常规进行血液和体液的病原学检测是合并感染时的基本准则。此外,与抗生素代谢和体内分布密切相关的感染部位的判定也具有重要的意义。因此,充分了解ACLF易合并感染的特点、部位、常见致病微生物,对患者合理治疗有着重要的影响。
本研究结果显示ACLF患者细菌感染率为56.7%,位居细菌感染前3位的分别是腹腔感染、肺部感染和败血症,这一结果与国外报道不同。来自欧洲的报道[3]显示,ACLF患者最常见的细菌感染为腹腔感染,其次为尿路及肺部感染;除泌尿系统感染外,其余部位均以革兰阴性菌为主。在不同感染部位,主要微生物菌群不同。本研究结果显示,腹腔感染及血流感染均以大肠埃希菌为主,肺炎克雷伯菌次之;而肺部感染中前3位是铜绿假单胞菌、肺炎克雷伯菌、鲍曼不动杆菌。因此,在经验性选择广谱抗生素时应有不同侧重。革兰阳性菌方面,主要为葡萄球菌、肠球菌和链球菌。虽然大部分患者尽可能给予微生物检查,但不足之处为细菌培养阳性率较低,腹水和痰培养阳性率分别为22.70%、52.82%,对指导临床用药的作用有限。
ACLF合并细菌感染者预后差,短期内病死率高,本研究中患者28 d、90 d生存率分别为56.66%和38.11%,与文献[9]报道相符。笔者对多项临床指标进行了单因素分析,发现年龄、病因、感染部位数、国际标准化比值、总胆红素、血肌酐、MELD评分、白细胞及中性粒细胞、降钙素原、肺部感染、肝性脑病、上消化道出血、胸腔感染、肝衰竭分期等为患者生存的影响因素。排除组间例数偏差较大(如病因)及重叠因素(如国际标准化比值与肝衰竭分期)等指标,对单因素分析中有显著性差异的部分指标进行多因素logistic回归分析,结果表明年龄、肝性脑病分期、肝衰竭分期和急性肾损伤是影响ACLF合并细菌感染患者90 d生存的独立危险因素,与临床报道[11-12]相符。因此,对高龄、出现肝性脑病以及急性肾损伤的感染患者,需高度警惕。作为目前在感染领域日益受到重视的降钙素原,本研究结果显示其并不是影响ACLF合并细菌感染患者生存的独立危险因素,考虑存在以下因素:(1)临床应用标准值偏低,文献[13]报道,在败血症的诊治中,以2.2 ng/ml作为临界值,敏感度达97.47%,而本研究中患者标准值上限为0.5 ng/ml;(2)降钙素原检测结果受多种因素干扰,在某些情况如肌酐升高也会出现非特异性升高[14]。由于本研究为回顾性研究,可能在ACLF患者总体感染率统计方面有所偏差,所得结论仍需大样本、前瞻性研究进一步明确。
综上,临床工作中应该警惕ACLF基础上发生的感染,对于怀疑感染者,做到早发现、早治疗,根据本地细菌流行特点,积极抗感染治疗,避免延误病情甚至造成不良后果。
利益冲突声明:本研究不存在研究者、伦理委员会成员、受试者监护人以及与公开研究成果有关的利益冲突。
作者贡献声明:苏海滨、刘晓燕负责课题设计,资料分析,撰写论文;胡瑾华、李晨、童晶晶、关崇丹、彭宇辉、宁鹏、严立龙、陈婧参与收集和整理数据;苏海滨负责拟定写作思路,指导撰写文章并最后定稿。
