基于水化学及当地稳定同位素的地下水硝酸盐污染空间分布特征及污染源解析
2021-09-24杨延梅郑明霞孙源媛傅雪梅
杨延梅, 张 田,, 郑明霞, 苏 婧, 孙源媛, 傅雪梅*
1.重庆交通大学河海学院, 重庆 400074 2.中国环境科学研究院, 国家环境保护地下水污染模拟与控制重点实验室, 北京 100012
进入20世纪以来,由于农业、生产等人类活动加剧,导致全球向河流输送的氮从34 Tg/a增至64 Tg/a[1],所有氮污染形态中,硝酸盐占主导地位,水体硝酸盐污染已成为世界范围内的环境问题. 硝酸盐污染来源多样,包括降雨、土壤有机氮、化学肥料、生活污水、粪肥和工业废水等[2-3]. 地下水作为重要水源供给,水质安全密切关系到人们的生活质量,硝酸盐作为地下水氮污染的主要形式[4-5],对水生态和人类健康构成严重威胁[6-7]. 由于地下水具有隐蔽性特征,且流动缓慢,交替程度弱,自净能力差,一旦被污染就难以恢复,且修复成本很高. 因此,精准识别地下水硝酸盐污染来源能够为硝酸盐污染防治工作提供有力支撑[8].
随着水体同位素测试手段不断完善,利用硝酸盐中氮、氧稳定同位素的特征值进行污染溯源,已成为氮污染溯源的研究热点[9-14]. 不同来源的硝酸盐具有不同的氮氧同位素[15],Heatont[16]通过研究,整理了典型的硝酸盐污染物氮同位素值域,对同位素技术在污染物溯源领域的发展起到了促进作用. 不同来源的同位素组成有部分的重叠区间,判断结果仍然具有不确定性,选取合适的模型计算不同来源的硝酸盐对污染的贡献率[17],能在一定程度上解决该问题,更好地为污染源的控制与管理服务[18]. 典型的定量解析模型主要包括基本质量守恒模型[19]、IsoSource模型、IsoError模型、SIAR模型. SIAR模型是目前应用最为广泛的定量解析硝酸盐贡献率的源解析模型[20],Xue等[21]等利用同位素技术结合贝叶斯公式对硝酸盐污染来源进行了溯源,并利用SIAR模型分析了各污染源的贡献比例. 对硝酸盐来源进行定量解析,不仅可以更精确地确定污染来源,而且能分析不同时间各污染源贡献率的变化,为地下水硝酸盐污染治理提供重要的理论依据. 近年来,越来越多的学者利用不同污染物来源硝酸盐中氮氧同位素特征值不同的特点[22-23],结合定量的源解析模型,实现了更为快速、准确的地下水氮污染来源的定性识别与量化.
目前应用同位素识别地下水污染源的研究通常采用经验值,但不同区域、不同污染来源的氮氧稳定同位素值都有所差异,且经验值的来源多样、范围多样,并没有统一的标准. 因此,仅通过氮氧同位素经验值的方式无法精准识别当地污染物来源,误差较大. 基于此,该文选取河北省张家口市宣化区洋河两岸的主要供水区为研究对象,基于当地土地利用类型,结合水化学分析方法,在充分调查研究区内不同特征污染物氮氧同位素特征值的基础上,通过绘制当地特征污染物氮氧同位素分布值域图,定性判断硝酸盐污染的不同来源,充实当地氮氧同位素特征值分布数据库. 采用SIAR模型计算当地不同硝酸盐污染来源的贡献比例,揭示宣化区洋河两岸地区硝酸盐污染空间分布情况及其来源,以期为控制当地地下水硝酸盐污染提供科学依据.
1 材料与方法
1.1 研究区概况
研究区位于张家口市宣化区洋河两岸10 km范围内,位于114°51′48.36″E~115°12′52.75″E、40°26′40.02″N~40°40′59.01″N,海拔590~1 200 m. 该地区属温带大陆性季风气候,四季分明,年均气温约8 ℃,全年以西北风为主,降雨主要集中在5—9月(汛期),降水量约占全年降水量的70%~80%,年均降水量380 mm,多年平均蒸发量 1 928 mm.
研究区是一个典型的新生代山间河谷断裂坳陷盆地,由西北-东南方向展布,中心部位由洋河自西北向东南穿流而过,汇水面积 2 400 km2,区内第四系较发育,覆盖范围约占盆地总面积的80%. 研究区属山间盆地水文地质区,主要分布山地基岩裂隙水和平原区第四系孔隙地下水,第四系含水层沿洋河河谷带状平原最厚,向两侧山区逐渐变薄,下部略具承压性;地下水补给接受来自上游冲洪积扇地下水的侧向流入补给及洋河径流补给,排泄方式以人工开采和向下游径流为主,地下水流方向自西向东,与洋河流向一致.
宣化区是张家口市的工业核心区,形成了以钢铁冶金、电力能源、装备机械制造等行业为主的工业体系;其次宣化区农业是典型的城郊型特色农业,形成了蔬菜、葡萄、规模化舍饲养殖“三大产业”. 研究区耕地占土地总面积的41%,建设用地占土地总面积的25%,根据2018—2020年《张家口市水资源公报》数据,宣化区工业、居民、城市公共、农业用水主要为地下水供水.
1.2 样品采集
为查明研究区地下水硝酸盐污染来源,分别于2019年10月、2020年5月在宣化区洋河两岸主要供水区对23处地下水监测井(P1~P23)进行采样,考虑氮的污染来源与监测井所在的土地利用类型存在相关性,利用土地利用矢量数据(见图1)确定研究区土地利用类型主要为建设用地、耕地和植被,并实地踏勘调查监测井周边的土地利用类型,发现监测井周边的土地利用类型分别为耕地(P1~P9、P20、P21、P23监测井)和建设用地(P10~P19、P22监测井).
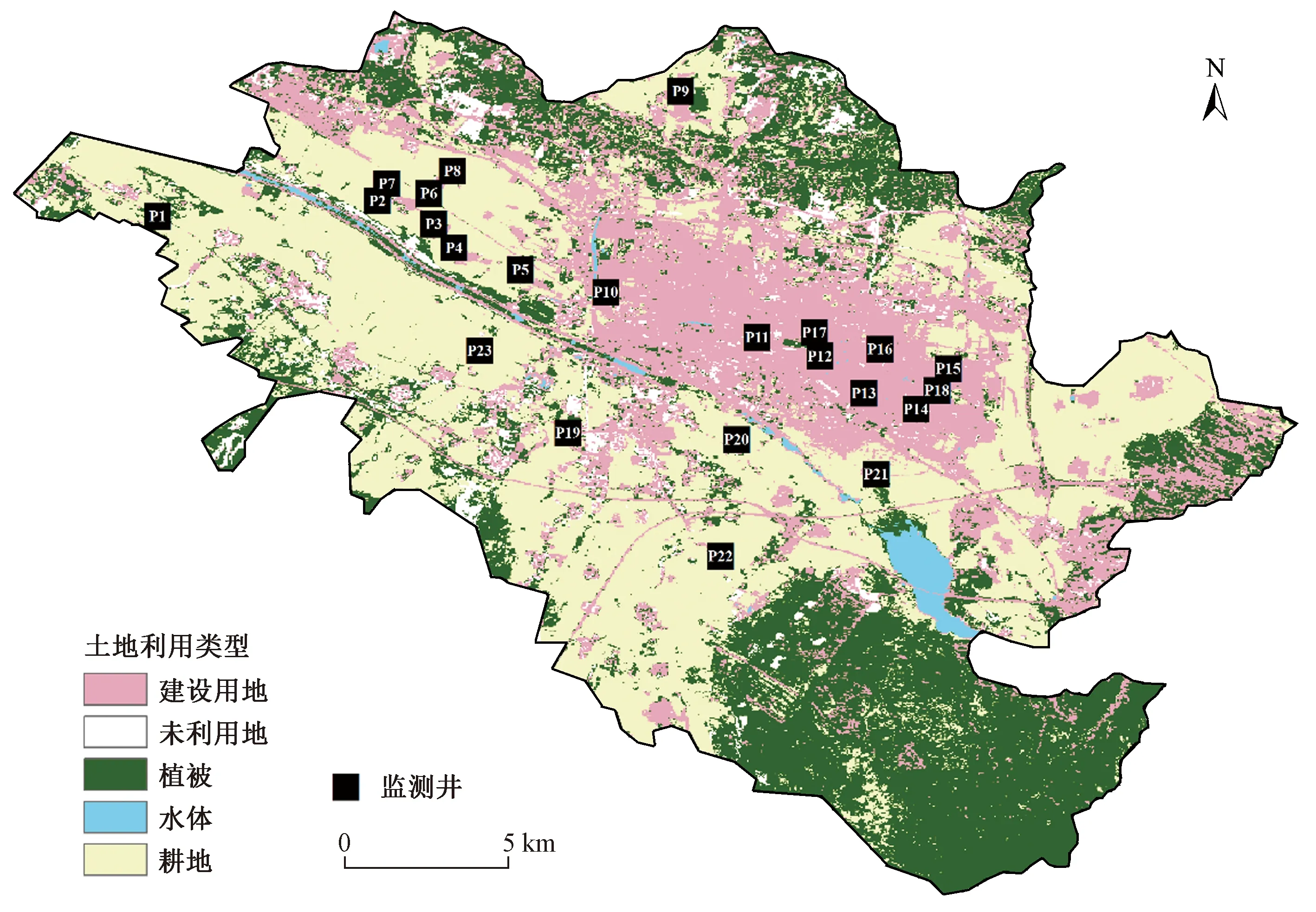
图1 研究区监测井的分布Fig.1 Monitoring points distribution in the study area
地下水样品采集前洗井15 min,采用In-SituBluetooth Device多功能测试仪现场测量pH、溶解氧浓度和电导率等,使用500 mL聚乙烯瓶采集水样带回实验室,0.45 μm滤膜过滤后在4 ℃下冷藏,分析地下水化学指标以及δ15N-NO3-、δ18O-NO3-指标. 样品测定严格按照《地下水质量标准》(GB/T 14848—2017)[24]中有关规定进行,利用电感耦合等离子体发射光谱仪(ICP-6000,Thermo,美国)对阳离子(K+、Na+、Ca2+、Mg2+)浓度进行分析测定;采用离子色谱仪(ICS-2000,DIONEX,美国)对阴离子Cl-和SO42-进行分析测定;NO3-浓度采用紫外分光光度法测定,NH4+浓度采用纳氏试剂分光光度法测定,NO2-浓度采用分光光度法测定,仪器均使用紫外分光度计(UV-2802,1718UNICO,美国);利用酸碱滴定管(采用稀盐酸-甲基橙/酚酞滴定法)对HCO3-浓度进行分析测定,以上指标均由张家口百信环境检测技术有限公司负责测试. 地下水样品及特征污染物中δ15N-NO3-、δ18O- NO3-的测定,首先利用特异性的反硝化细菌将硝态氮转化为N2O,然后采用气体浓缩仪(Trace-Gas,ISOPRIME LTD,英国)并结合连续流同位素比质谱仪(IRMS-100,Elementar,英国),测试工作在中国农业科学院农业环境稳定同位素实验室完成.
1.3 分析方法
为准确量化不同来源污染的贡献程度,选用基于贝叶斯方程的SIAR模型进行分析,在RStudio软件中运行SIAR程序包. 通过定义K个来源N个混合物的J种同位素,SIAR模型可表示如下:
(1)
Sij~N(μij,ωjk2)
(2)
Cij~N(λij,τjk2)
(3)
εij~N(0,σj2)
(4)
式中:Xij为第i种混合物的第j个同位素的值,i=1, 2, 3, …,N;j=1, 2, 3, …,J;Pk为需要SIAR模型计算的第k个来源的贡献比例;Sij为第i个来源的第j种同位素的δ值,服从期望为μ、方差为ω的正态分布;Cij为第i个来源的第j种同位素的分馏系数,服从期望为λ、方差为τ的正态分布;εij为残余误差,表示不同单个混合物之间不能确定的变量,其平均值和方差通常情况下为0.
该研究利用水环境化学方法结合氮、氧稳定同位素分析方法,对硝酸盐进行溯源分析. 水化学指标及氮氧同位素数据由Excel 2016、Origin 2017等软件进行分析处理;硝酸盐浓度的空间分布采用ArcGIS 10.3软件中反距离权重法插值完成;SIAR模型由R语言环境运行SIAR程序包计算.
2 结果与讨论
2.1 地下水水化学特征分析
2.1.1水化学总特征分析
研究区23处地下水监测井理化指标分析显示:pH的变化范围为7.00~8.34,平均值为7.56,属于弱碱性水质;电导率(EC)的变化范围为437.70~2 347.26 μS/cm,平均值为 1 251.5 μS/cm;ρ(TDS)变化范围为468.00~2 172.00 mg/L,平均值为684.70 mg/L;ρ(DO)变化范围为2.22~8.83 mg/L,平均值为6.44 mg/L,高浓度DO有利于水体氨化作用和硝化作用的进行,当ρ(DO)>5 mg/L时,DO对硝化作用无限制[25].
采用Piper三线图可以直观反映水化学溶质主要离子的相对含量和分布特征,并用于分析水化学成分的演化规律,辨别水化学形成与演化的控制因素. 如图2所示,地下水中阳离子浓度表现为ρ(Ca2+)>ρ(Na+)>ρ(Mg2+)>ρ(K+),阴离子浓度表现为ρ(HCO3-)>ρ(SO42-)>ρ(Cl-)>ρ(NO3-). 研究区地下水中阳离子主要以Ca2+、Na+为主,优势阴离子为HCO3-、SO42-,地下水化学相随时间变化主要由HCO3--Ca2+·Mg2+型向Cl-·SO42--Ca2+·Mg2+型演化,由于水体中Cl-来源主要为生活污水和化肥施用,SO42-来源主要为工业废水等,受人类活动影响较大. 人类生产活动过程中生活污水、工业废水、化肥施用是地下水硝酸盐污染潜在来源,初步分析研究区地下水硝酸盐污染来源受人类生产活动影响的因素较大.
2.1.2硝酸盐浓度时空变化特征
研究区地下水样品“三氮”检测浓度显示,硝酸盐浓度平均值为27.23 mg/L,亚硝酸盐浓度平均值为0.64 mg/L,氨氮浓度平均值为0.46 mg/L,表明地下水氮素主要存在形态为硝酸盐氮. 2019年11月和2020年5月硝酸盐浓度变化范围为1.22~130.10 mg/L,以GB/T 14848—2017《地下水质量标准》Ⅲ类水质标准(20 mg/L)为限,是Ⅲ类水质标准限值(20 mg/L)的1.36倍,23处样品平均超标率为42%,地下水受硝酸盐污染严重.
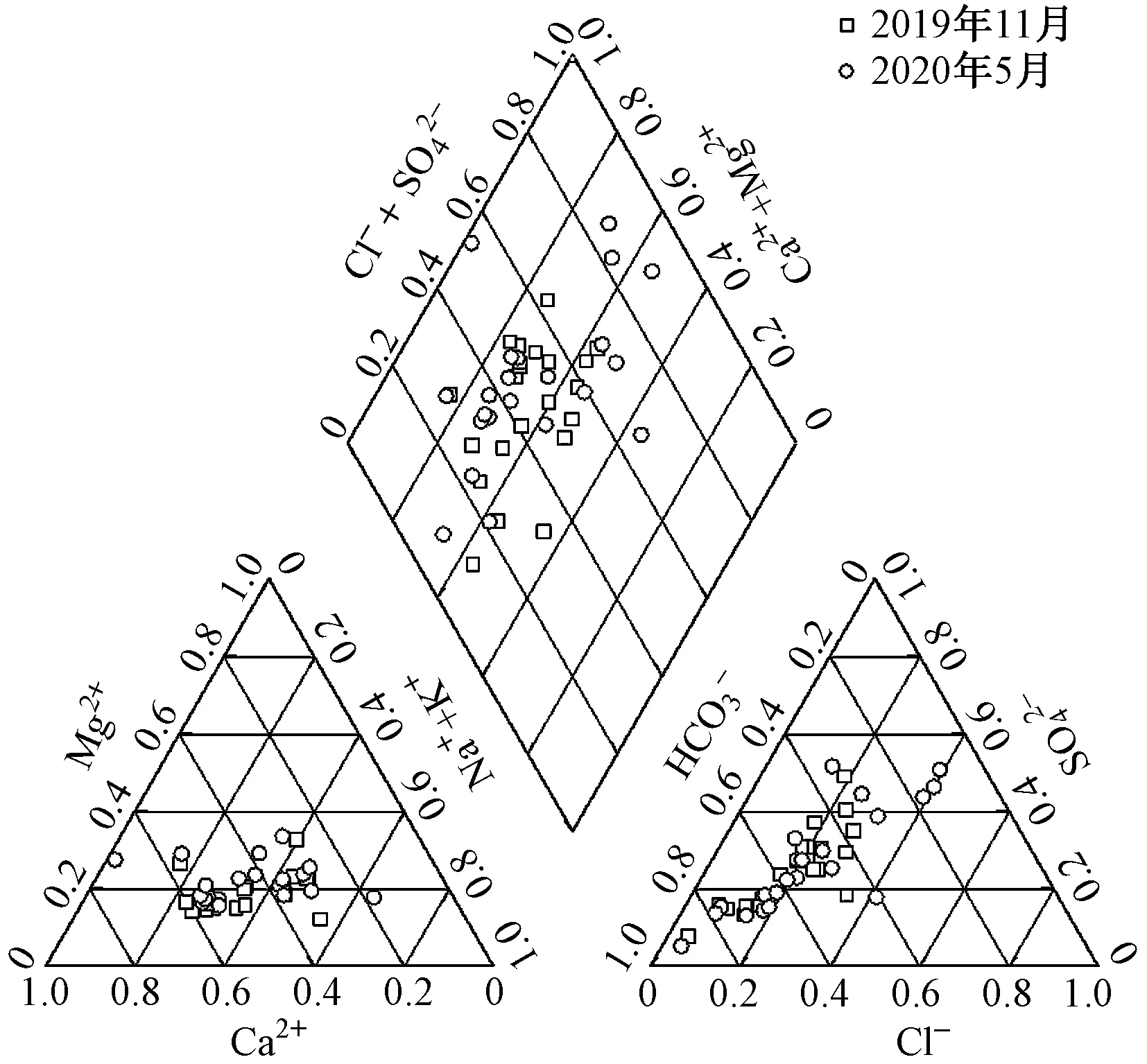
图2 研究区地下水Piper三线图Fig.2 Piper three-line map of groundwater in study area
研究区不同土地利用类型会对硝酸盐浓度产生影响,由图3可知,建设用地附近监测井地下水硝酸盐浓度大于耕地,表明该研究区人类生活、工业生产对地下水水质产生的影响大于农业生产. 2019年11月—2020年5月,建设用地硝酸盐浓度由37.81 mg/L减至30.55 mg/L,亚硝酸盐与氨氮浓度变化均较小,可能与11月—翌年5月地下水水量变化有关,硝酸盐浓度被稀释. 耕地硝酸盐浓度随时间变化呈增加的趋势,氨氮浓度则相反,一方面由于耕地的截污能力较差,春季农业施用无机化肥随农业灌溉进入地下水产生污染;另一方面可能与禽畜养殖粪便以及污水不当处理,造成5月硝酸盐浓度升高有关.
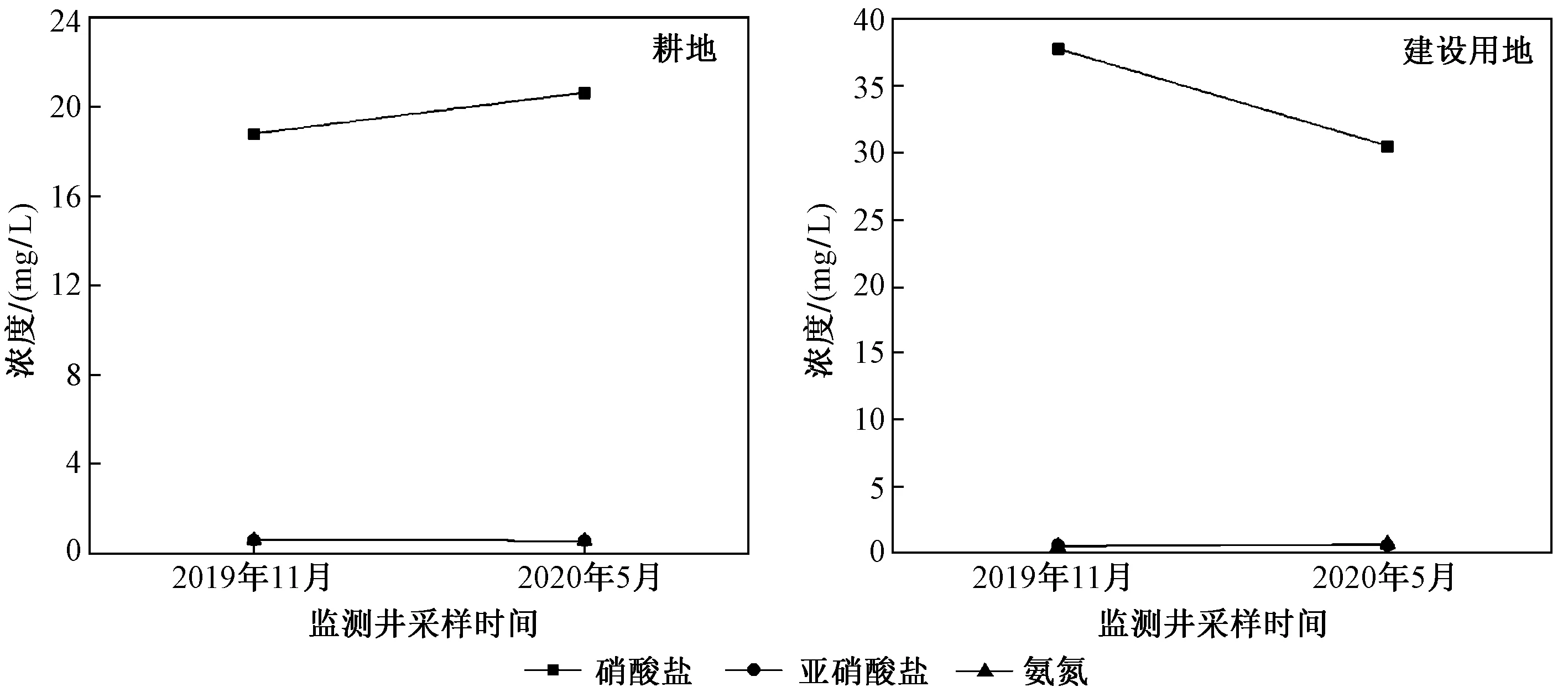
图3 不同土地利用类型“三氮”浓度的变化Fig.3 Changes of ‘trinitrogen’ concentrations in different land use types
基于ArcGIS 10.3软件反距离权重法插值,分析研究区硝酸盐浓度的空间分布变化,结果如图4所示. 由图4可见,上游水源地及下游沿河地区监测井硝酸盐浓度较低,两次监测地下水硝酸盐浓度高值均出现在P9、P18、P19监测井,结合监测井周边环境,对其进行分析. P9监测井位于宣化区东部四方台村,硝酸盐浓度为50.01 mg/L,周边为耕地和废弃工厂,硝酸盐污染原因可能受到早期工业污染以及化肥施用的影响; P18监测井位于宣化城区,周边人口密度较大、工业企业分布密集,硝酸盐浓度平均值为94.50 mg/L,表明该地区地下水硝酸盐浓度较高现象与居民生活、工业企业分布有关;P19监测井位于村镇小路边,周围有耕地及工厂,近距离10 m处有旱厕存在,粪便和污水以及村镇生活污水的不当处理是导致该监测井硝酸盐浓度(121.05 mg/L)偏高的主要原因. 两次监测值显示,硝酸盐污染较高地区其浓度变化不大,再次表明该地区地下水受到污染源持续污染.
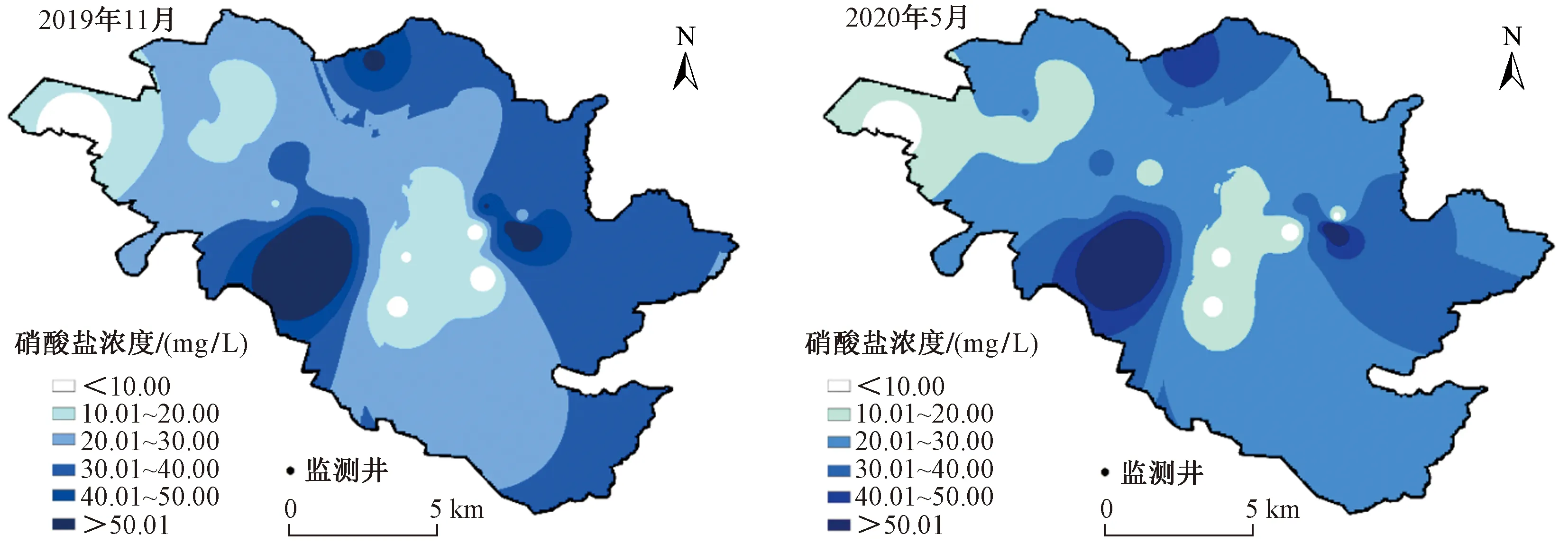
图4 研究区硝酸盐浓度的空间分布Fig.4 Spatial distribution of nitrate pollution concentration in the study area
2.1.3氮氧同位素时空分布特征
2019年11月δ15N-NO3-平均值为15.126‰,2020年5月δ15N-NO3-平均值为23.319‰,δ15N-NO3-特征值在-2.567‰~4.203‰之间波动;2019年11月δ18O-NO3-平均值为-0.989‰,2020年5月δ18O-NO3-平均值为5.210‰,δ18O-NO3-特征值在-10.802‰~49.203‰之间波动. 研究区地下水δ15N-NO3-、δ18O-NO3-明显的时间变化表明,宣化区地下水NO3-来源存在时间差异. 如图5所示,2019年11月δ15N-NO3-在P9、P22、P18监测井出现低值,分别为6.130‰、5.280‰、-0.700‰,2020年5月δ15N-NO3-在P1、P15、P18、P22监测井出现低值,分别为3.670‰、-2.570‰、1.320‰、5.270‰,低值区域主要存在于洋河上游耕地区域. 耕地区域地下水δ15N-NO3-变化范围为3.667‰~19.476‰,平均值为8.02‰;δ18O-NO3-变化范围为-4.085‰~10.933‰,平均值为0.58‰;建设用地地下水δ15N-NO3-变化范围为-2.566‰~49.203‰,平均值为11.074‰;δ18O-NO3-变化范围为-10.802‰~15.426‰,平均值为0.202‰. 研究区不同土地利用类型δ15N-NO3-、δ18O-NO3-变化表明,土壤氮、粪便及污水、无机化肥及工业废水对地下水硝酸盐污染的贡献率不同.
2.2 地下水硝酸盐污染来源的定性识别与迁移转化规律判断
2.2.1同位素经验值识别硝酸盐来源
根据硝酸盐中的氮氧同位素特征值可以识别水体中硝酸盐污染来源,为了判断研究区地下水硝酸盐污染的典型来源,对23个监测井地下水进行硝酸盐氮氧同位素分析. 选取特征污染物(土壤氮、粪便和污水、无机化肥及工业废水)δ15N-NO3-和δ18O-NO3-经验特征值分布区间,绘制监测井δ15N-NO3-和δ18O-NO3-同位素特征值分布图. 同位素特征值分布结果如图6所示. 由图6可见,2019年11月和2020年5月,δ15N-NO3-和δ18O-NO3-特征值主要落在土壤氮、粪便和污水、无机化肥及工业废水的值域范围,表明研究区地下水硝酸盐污染来源主要为土壤氮、粪便和污水、无机化肥及工业废水.
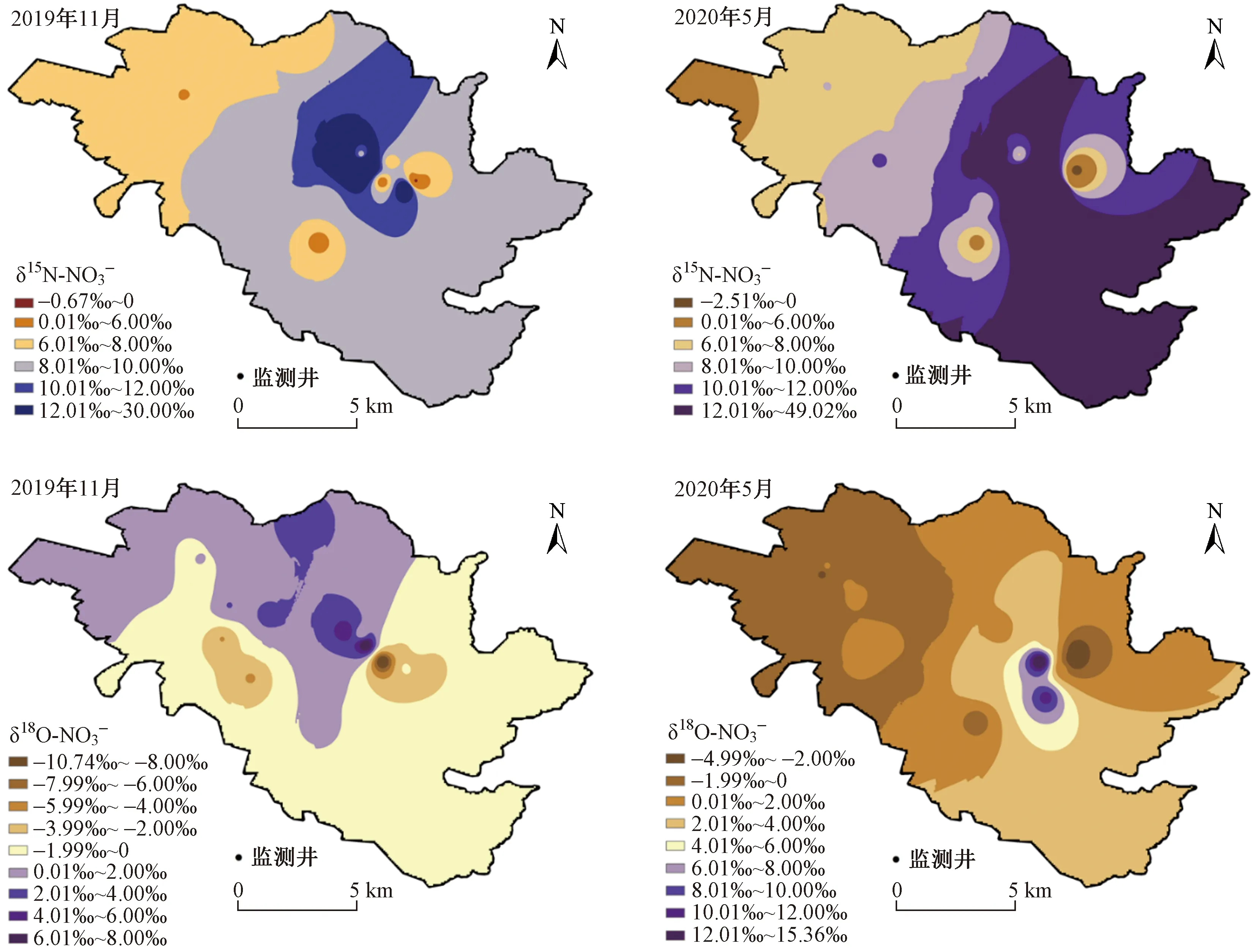
图5 δ15N-NO3-、δ18N-NO3-浓度时空分布Fig.5 The spatial and temporal distribution of δ15N-NO3- and δ18N-NO3- concentrations
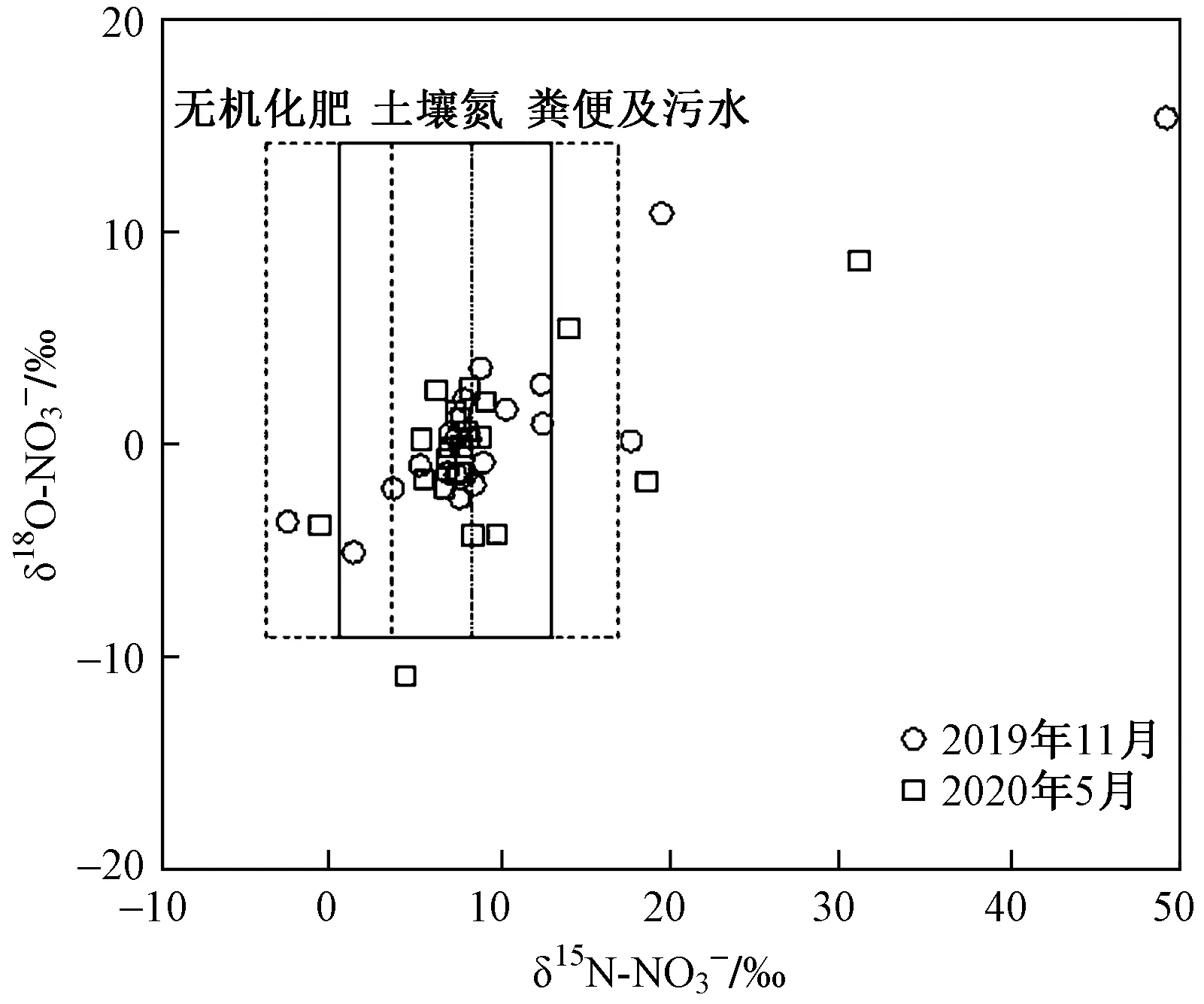
图6 监测井δ15N-NO3-、δ18O-NO3-同位素特征值Fig.6 δ15N-NO3-,δ18O-NO3- istopic characteristic values of monitoring wells
2.2.2同位素实测值识别硝酸盐来源
为了能够更为精确地刻画研究区硝酸盐污染来源的情况,对研究区当地特征污染物进行采样,在研究区不同区域采集12份土壤样品,7份污水及动物粪便样品,进行氮氧同位素测定,统计结果(见表1)表明,土壤氮中δ15N-NO3-的分布范围为1.46‰~7.71‰,粪便及污水中δ15N-NO3-的分布范围为9.49‰~17.58‰.
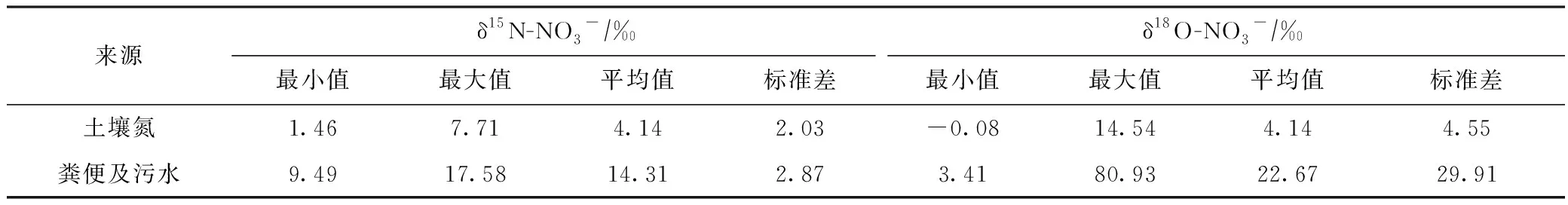
表1 研究区潜在污染源同位素特征值统计
采用研究区当地特征污染物δ15N-NO3-实测值,对特征污染物δ15N-NO3-值域范围进行调整,绘制δ15N-NO3-和δ18O-NO3-特征值分布图,与经验值分布相比,实测值域分布区间更适用于当地. 监测井氮氧同位素分布结果(见图7)表明,地下水硝酸盐污染主要为土壤氮、粪便及污水、无机化肥及工业废水. 土壤氮、粪便及污水是研究区内地下水硝酸盐污染的主要来源,符合建设用地NO3-浓度偏高的特征. 部分监测井分布于理论上的土壤氮来源区间,然而研究区内硝酸盐浓度平均值高达27.23 mg/L,远大于天然条件下硝酸盐浓度上限参考值(3 mg/L),天然条件下土壤氮的矿化及大气沉降氮等自然因素对研究区内地下水硝酸盐浓度的贡献是极其有限的,判断该监测井所在地区硝酸盐的来源情况复杂. 氮氧同位素经验值与实测值的对比分析表明,土壤氮、粪便及污水是研究区内地下水硝酸盐污染的主要来源.
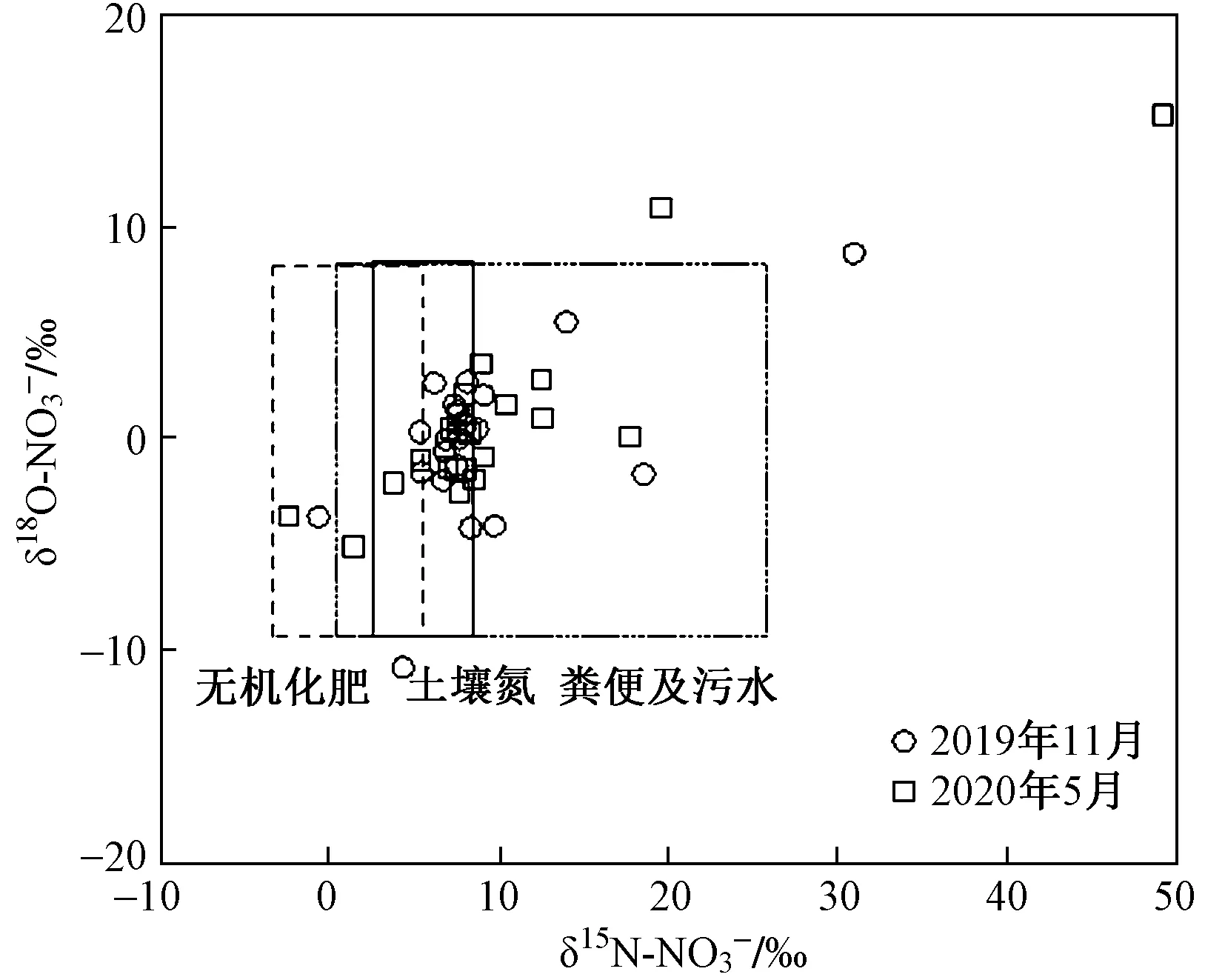
图7 监测井δ15N-NO3-、δ18O-NO3-同位素特征值Fig.7 δ15N-NO3-,δ18O-NO3- istopic characteristic values of monitoring wells
2.2.3研究区硝酸盐污染来源修正
结合研究区特征污染物同位素特征值经验值与实测值的分布区间,选取硝酸盐浓度高值监测井P9、P18、P19为代表,对污染来源结果进行分析修正(见表2). P9监测井的土地利用类型为耕地,由于早期工业污染及农业化肥施用,两次监测结果均显示来源为土壤氮,确定其硝酸盐来源为土壤氮混合污染;P18监测井的土地利用类型为建设用地,2020年5月氮氧同位素实测值与经验值结果不一致,结合该监测井周边多为居民生活用地、工业生产用地,确定污染来源为无机化肥及工业废水;P19监测井的土地利用类型为建设用地,监测井周边土地利用情况较为复杂,2020年5月结果显示,该监测井附近的旱厕对浅层地下水产生一定影响.
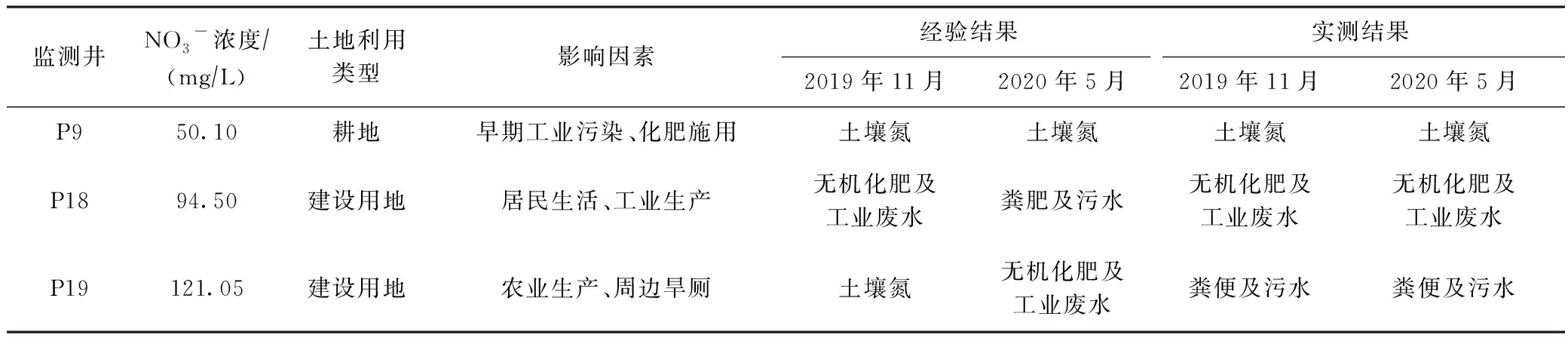
表2 同位素分析污染来源的结果对比
2.2.4地下水硝酸盐迁移转化过程识别
硝酸盐中的氮氧同位素组成不仅取决于不同的硝酸盐来源,同样也受到包气带中微生物活动的影响,如硝化、反硝化作用[26]. 硝化作用是指NH4+在氧化环境下经硝化细菌作用,形成硝酸盐的过程,属于耗氧反应,氧元素在反应过程中会有明显的变化[27],因此可以利用δ18O-NO3-的值判别是否发生硝化作用. 相对于大气沉降和化肥中的δ18O-NO3-组成,由硝化作用形成的硝酸盐δ18O特征值较低,根据Xue等[28]研究,硝化作用产生的δ18O-NO3-值范围为-10.00‰~10.00‰. 研究区95%监测井δ18O的变化范围为-10.80‰~8.82‰,平均值为-2.23‰,说明研究区硝化作用是地下水氮转化的主要过程.
反硝化作用会导致氮同位素分馏,对不同来源δ15N-NO3-分布范围产生影响[29],反硝化作用能还原NO3-释放N2或N2O使硝酸盐脱氮,导致NO3-基质的同位素富集[30]. 已有研究[31]表明,反硝化作用可引起δ18O、δ15N值同比升高,比率在1∶1.3~1∶2之间. 两次采样的δ18O/δ15N(同位素比值,下同)分别为0.152、-0.137,不在典型的反硝化δ18O/δ15N范围内,且研究区溶解氧浓度范围为2.22~8.83 mg/L,由于溶解氧充足,不利于反硝化作用的发生[32],基本可以证明研究区没有明显的反硝化作用存在.
2.3 SIAR模型计算硝酸盐污染各来源贡献率
通过对监测井δ15N-NO3-、δ18O-NO3-数据定性分析,该研究判断研究区的硝酸盐污染来源有3种:无机化肥及工业废水、土壤氮、粪便及污水. 由于δ18O-NO3-来源较为单一,实测值同位素特征值确定的值域有限,采用经验值更为可靠,δ18O-NO3-特征值的平均值和方差均来自文献;δ15N-NO3-特征值选取实测值(见表3),来源于当地硝酸盐特征污染物,主要为土壤氮、粪便及污水. 利用SIAR模型计算硝酸盐各污染源贡献率时,假设式(1)中分馏因子(Cij)为0,因为该研究区以硝化作用为主,没有反硝作用,不产生分馏影响,因此该假设成立.
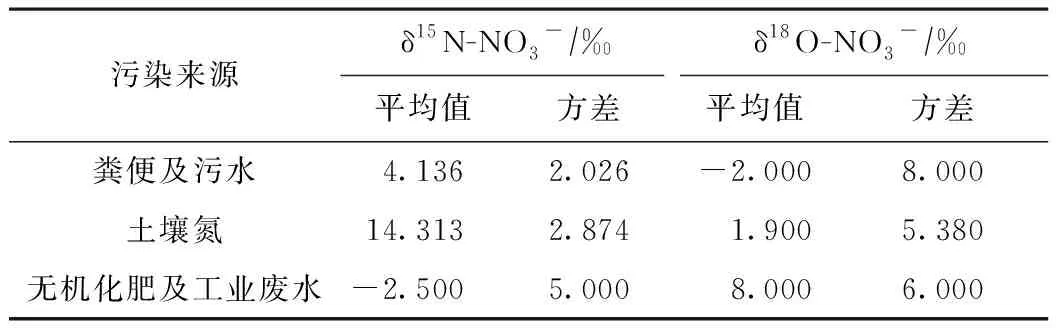
表3 SIAR模型参数确定
以23个监测井两次监测结果为样本,在R语言中运行SIAR程序包,计算各污染源的贡献率. SIAR模型输出结果(见图8)显示,土壤氮、粪便及污水为研究区最主要的硝酸盐污染来源. 2019年11月粪便及污水、土壤氮、无机化肥及工业废水的贡献率分别为49.39%、42.09%、8.51%,2020年5月的贡献率分别为46.63%、43.4%、9.97%.
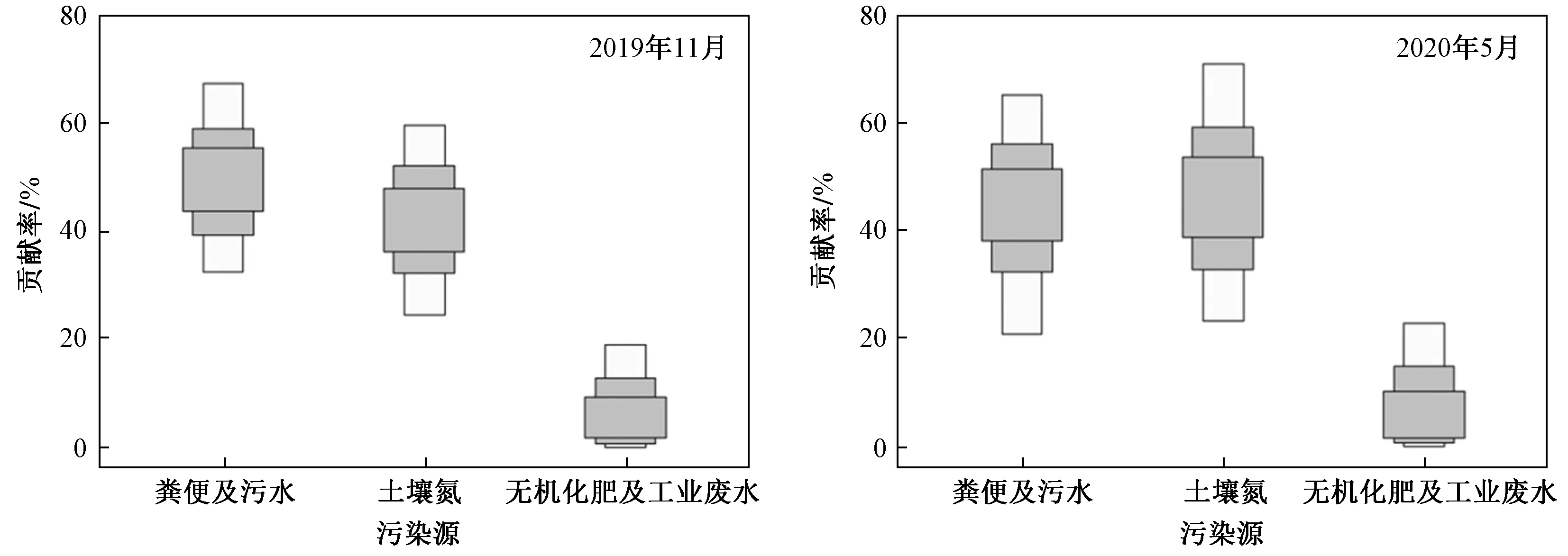
图8 SIAR模型计算各污染源贡献比例Fig.8 The SIAR model calculates the contribution ratio of each pollutant source
研究区地下水氮污染源以土壤氮、粪便及污水、无机化肥及工业废水为主,贡献率平均值分别为44.36%、43.35%、9.24%. 可见,2019年11月粪便及污水贡献率最高,2020年5月土壤氮贡献率最高,这与不同季节生活工业用水量、灌溉用水量、降水量等有关. 该研究发现,两次监测土壤氮贡献率的变化范围为42.09%~46.63%,显示农业活动已成为地下水环境氮污染的重要污染源,土壤氮的来源是由于耕地土壤较高的水溶性有机氮随着降雨、灌溉造成的水土流失进入包气带,在包气带发生硝化反应成为水体硝酸盐,输入地下水系统. 粪便及污水贡献率为43.39%~43.30%,通过分析,来源于生产生活过程中产生的污水、粪便对地下水造成污染,显示该研究区地下水硝酸盐污染的来源受人类活动影响较大. 因此,在地下水硝酸盐污染控制过程中应提高农业灌溉效率、加强城镇污水处理设施建设、控制化肥的使用量.
3 结论
a) 张家口市宣化区地下水中“三氮”污染以硝酸盐为主,其浓度变化范围为1.22~130.10 mg/L,平均值为27.23 mg/L,是GB/T 14848—2017 Ⅲ类水质标准限值(20 mg/L)的1.36倍,污染较严重;不同土地利用类型下,建设用地中硝酸盐浓度大于耕地中硝酸盐浓度.
b) 研究区地下水δ15N-NO3-和δ18O-NO3-特征值变化范围分别为-2.57‰~4.20‰、10.80‰~49.20‰,地下水氮迁移转化过程以硝化作用为主,基本不存在反硝化作用. 研究区特征污染物土壤氮δ15N-NO3-分布范围为1.46‰~7.71‰,粪便及污水中δ15N-NO3-分布范围为9.49‰~17.57‰,所绘制的当地特征污染物氮氧同位素分布值域图,可充实当地氮氧同位素特征值分布数据库.
c) SIAR模型输出结果显示,研究区地下水氮污染源以土壤氮、粪便及污水、无机化肥及工业废水为主,贡献率平均值分别为44.36%、43.35%、9.24%.
