非心脏手术围手术期心血管事件风险评估体系比较
2021-09-13王惠琴雷建国
王惠琴 雷建国
(1.川北医学院,四川 南充 637000; 2.成都市第五人民医院,四川 成都 610000)
随着医学持续发展,医疗技术不断进步,全球手术量日益增加,每年有超过3亿人行外科手术[1],约2亿人行非心脏手术[2],约180万成年人在非心脏手术术后30 d内死亡[2],围手术期心源性死亡率为1%~3%[3]。心血管事件主要包括急性冠脉综合征、恶性心律失常、心力衰竭、脑卒中和死亡等。围手术期心血管事件会导致患者预后不良、住院时间延长及医疗费用增加。若术前对风险进行预测并采取有效干预措施,便可提升手术的安全性。大量研究发现,高龄、术前多种心血管疾病病史、贫血、糖尿病和肾脏损害等都是心血管风险独立危险因素,但因个体差异、疾病多样性和手术复杂性等因素均会影响患者结局,单一因素不能全面评估和预测围手术期心血管事件风险,应根据患者具体情况进行综合评估。数十年来,产生了多种用于评估围手术期心血管事件风险的体系,见表1。现就非心脏手术围手术期心血管事件风险评估体系内容及其比较展开综述,以指导临床医生进行风险评估,做出临床决策,也有助于向患者及家属提供有依据的风险评估信息,让其充分了解手术风险,从而做出抉择。
1 非心脏手术围手术期心血管风险评估体系
1.1 Goldman指数
Goldman等[4]把患者术前各项心血管危险因素和围手术期结局相联系,用具体数值量化危险因素对结局影响程度的大小,提出了第一个非心脏手术围手术期心血管事件风险评估方法,其包含9项预测因素(见表2),根据总得分分为4级,Ⅰ级0~5分;Ⅱ级6~12分;Ⅲ级13~25分;Ⅳ级26~53分。Ⅰ~Ⅳ级围手术期严重心血管并发症的发生率分别为0.7%、5%、11%和22%,心源性死亡率分别为0.2%、2%、2%和56%,其灵敏度和特异度分别为55.2%和87.7%,阳性预测值和阴性预测值分别为21.6%和96.8%[5],表明其用于排除高危人群可发挥巨大作用,对于非高危人群价值不大。
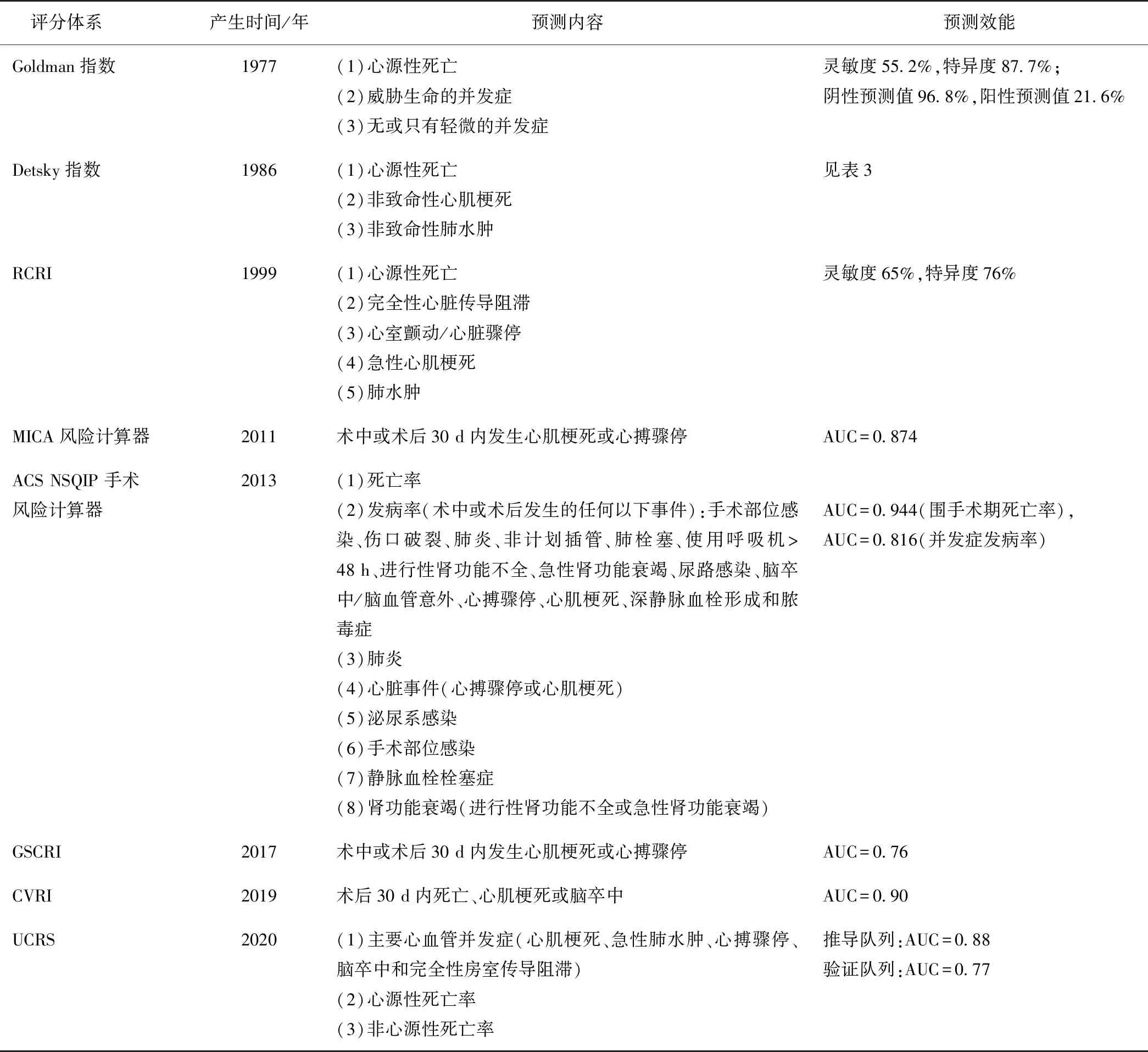
表1 8种评分体系
1.2 Detsky指数
在Goldman指数基础上,Detsky等[6]加入肺水肿病史和心绞痛分级2项新的预测因素,也将各项因素赋值评分,并根据手术类型将手术风险进行分类:经尿道手术及前列腺切除术、头颈部手术、胸腹腔手术、血管及骨科手术,发生心血管事件的概率分别为1.6%、2.6%、8.0%和13.2%,评分为0~5分时,心血管事件发生率将低于以上同类型手术;评分>10分时,心血管事件发生率将高于上述同类型手术。使用列线图是该评分系统的最大优势,在列线图上可找到相应分值对应的风险概率,可更加直观地了解心血管事件发生率,便于患者了解手术风险。见图1,某患者风险评分得分为10分时,其对应的似然比为1,则该患者发生围手术期心血管事件风险概率等于接受该同类型手术的患者的平均风险(25%)。

表2 Goldman指数预测因素及赋值[4]
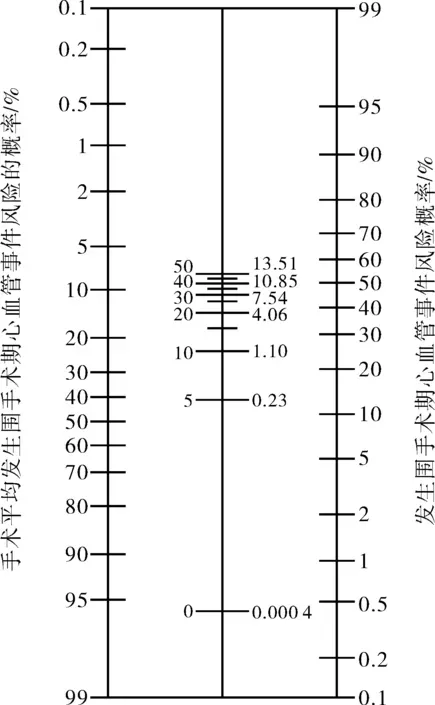
图1 Detsky指数似然比列线图
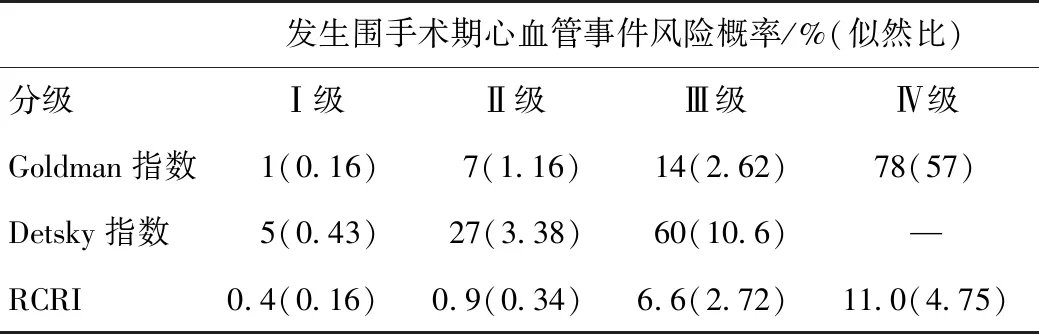
表3 Goldman指数、Detsky指数和RCRI发生围手术期心血管事件风险概率和似然比[5]
1.3 改良心脏风险指数
Lee等[7]确定了与围手术期心血管事件相关的6个独立预测因子:缺血性心脏病史、充血性心力衰竭病史、脑血管病史、高危手术、术前血肌酐>176.8 μmol/L和术前应用胰岛素治疗。每项因子赋值1分,当总分累计0、1、2和≥3分时,心血管事件发生率分别为0.5%、1.3%、3.6%和9.1%。验证改良心脏风险指数(revised cardiac risk index,RCRI)的系统评价[8]显示:RCRI特异度为76%,灵敏度为65%,表明RCRI具有较好的预测效能。RCRI相对简单,需6个临床资料,更加方便临床使用,现多国指南均推荐术前常规使用RCRI作为除急诊手术以外的评估工具[9-12]。但RCRI未考虑年龄、性别和手术类型等差异,多项研究结果显示,其会低估风险的发生率[13-14]。
1.4 心肌梗死或心搏骤停风险计算器
美国外科医师协会(ACS)利用国家外科质量改进项目(NSQIP)数据库开发了基于人工智能、大数据构建的心肌梗死或心搏骤停(myocardial infarction or cardiac arrest,MICA)风险计算器[15],其包含5个风险预测因素:年龄、血肌酐水平、美国麻醉医师协会(ASA)分级、手术类型和术前心肺功能状态。较少的参数使评估流程简化,MICA风险计算器的AUC优于RCRI(0.874 vs 0.747),在该研究中,其预测效能优于RCRI,但其也存在一定的局限性,该研究分析的变量仅限于NSQIP记录的变量,尽管数据集相当全面,但术前负荷试验、超声心动图、心律失常和主动脉瓣疾病等信息不全,且未系统地监测心肌标志物的水平,因而会低估实际风险的发生率。
1.5 ACS NSQIP手术风险计算器
ACS同样利用NSQIP数据库中的数据,开发了另一个基于网络的风险评估工具[16],使外科医生输入21种术前因素,包括:年龄、性别、体重指数、吸烟、手术类型、ASA分级、呼吸困难、糖尿病、急性肾衰竭、透析、充血性心力衰竭、基础心脏病、肿瘤发生转移、需药物治疗的高血压、慢性阻塞性肺疾病、腹水、败血症、需呼吸机、使用类固醇激素、活动能力和急诊手术,便可预测8种不良的结果。ACS NSQIP手术风险计算器对围手术期死亡率(AUC=0.944)和并发症(AUC=0.816)显示出了良好的预测效能。相比其他评估系统,ACS NSQIP手术风险计算器更加全面。但也让评估过程繁琐,加大了工作量,有学者比较了脊柱风险评估工具和ACS NSQIP手术风险计算器评估脊柱手术并发症发生的风险,发现ACS NSQIP手术风险计算器始终会低估并发症发生率[17]。
1.6 老年敏感性心脏风险指数
由于老年患者发生心脏并发症的风险更高,Alrezk等[18]利用NSQIP数据库中的年龄≥65岁的数据,开发了针对老年患者的心脏不良事件风险工具,其包含7项预测因素:ASA分级、手术类型、血肌酐>132.6 μmol/L、活动能力、充血性心力衰竭、糖尿病和脑卒中病史。相比年轻患者,老年患者肾小球滤过率和血肌酐水平通常较低,该模型选择了肌酐>132.6 μmol/L而非176.8 μmol/L作为预测因素,更具针对性和说服力,在验证队列中,老年敏感性心脏风险指数(geriatric sensitive cardiac risk index,GSCRI)的预测效能(AUC=0.76)分别优于RCRI(AUC=0.63)和MICA风险计算器(AUC=0.70)13%和6%。简约的评估模型确保了医生在临床工作中所需的易用性,但GSCRI是否是非心脏手术老年患者心脏风险的更好的预测指标尚需外部验证。
1.7 心血管风险指数
Dakik等[19]利用3 284例接受非心脏手术的成年患者作为推导队列,利用NSQIP数据库中的患者作为外部验证队列。在预测模型中纳入了6个数据元素:年龄≥75岁、血红蛋白<120 g/L、心绞痛或呼吸困难症状、心脏病史、血管手术和急诊手术。根据存在的数据元素数量,患者分别被分配至含有0、1、2、3和>3个数据元素的心血管风险指数(cardiovascular risk index,CVRI)组,在推导和验证队列中,AUC分别为0.90和0.82,从而证实了CVRI的识别和区分能力,CVRI有效地将患者分为低危组(CVRI 0~1)、中危组(CVRI 2~3)和高危组(CVRI>3),对非心脏手术患者的有效分流和管理具有重要意义。CVRI在简单性方面与RCRI[7]相似,且有更好的识别能力(CVRI的AUC=0.79)。并且CVRI研究纳入了所有接受非心脏手术的患者,包括未纳入RCRI队列的低风险患者和急诊手术患者。CVRI和ACS NSQIP手术风险计算器[16]都具有很高的识别能力(AUC分别为0.90和0.89),它们各具优缺点,CVRI给出每个患者的准确风险估计,将风险分层到不同的范围可能对医生和患者都更实用,ACS NSQIP评分使用的参数在评分者之间可能存在差异,除麻醉医师外,临床医生不常用。CVRI在来自NSQIP数据库的大型外部数据集中得到了很好地验证,但仍需更多的前瞻性研究进一步确定它在不同地理区域和不同患者群体中的有效性。
1.8 更新的心脏风险评分
Scorcu等[20]进行前瞻性队列研究,制定了更新的心脏风险评分(updated cardiac risk score,UCRS),确立了4个预测因素:高风险手术、术前估算肾小球滤过率<30 mL/(min·1.73 m2)、年龄≥75岁和有心力衰竭病史,根据这4个危险因素创建了1、2、3和4级风险,它们对应的30 d发生重大心血管并发症的风险分别为0.8%、2.5%、8.7%和27.2%。在研究队列和验证队列中,UCRS的AUC值均比RCRI大(0.88 vs 0.79和0.77 vs 0.72),显示出了高预测性能,适合在非心脏手术患者术前心脏风险评估中广泛使用,但该研究排除了临床不稳定的心脏病和紧急情况下接受非心脏手术的患者,因此,风险的估计不适用于所有的患者。
2 总结与展望
回溯几十年的临床研究,前辈们已开发出了上述数种风险评估体系,目前最常用的是RCRI[7]和ACS NSQIP评分[16]。在2014年欧洲心脏病学会指南[12]中,ACS NSQIP手术风险计算器与RCRI具有相同的使用推荐级别,但加拿大心血管协会在2017年的指南[10]更推荐使用RCRI。术前风险主要与患者性别、年龄、基础疾病、一般情况和手术类型等因素有关;术中主要与手术本身引起的低血压、交感神经兴奋、心律失常和麻醉方式、分级以及手术时间等有关;术后风险则主要与术后各种并发症相关。ACC/AHA在2014年发布的相关指南中强调了非心脏手术围手术期心血管并发症风险评估的重要性[21],并建议从手术缓急、手术本身具有的风险和心脏功能状态等多方面进行逐项评估。Smilowitz等[22]也建议在进行非心脏手术之前,应结合患者病史、体格检查、日常生活能力和心功能储备进行全面综合评估。同时,一些新的尚未纳入评估体系的实验室指标,如:脑利尿钠肽或N末端脑钠肽前体(N-terminal pro-brain natriuretic peptide,NT-proBNP)、超敏C反应蛋白(high sensitivity C-reactive protein,hs-CRP)、血红蛋白及血细胞比容、肌钙蛋白T和高敏肌钙蛋白等生物标志物均在研究中显示出良好的潜在预测价值。研究发现,将NT-proBNP=201 pg/mL设为临界值被确定为围手术期并发症的最佳预测指标,其灵敏度为80.0%,特异度为81.1%,多变量分析显示,NT-proBNP>201 pg/mL且RCRI≥2分是围手术期心血管并发症的独立预测因子[23],术后脑利尿钠肽和NT-proBNP测量均可增强非心脏手术后30 d和≥180 d死亡或非致命性心肌梗死的综合预测能力[24]。在一项骨科手术hs-CRP与预后的研究中,术前hs-CRP>3 mg/L比术前hs-CRP<3 mg/L的患者心血管事件的发生率高,并与住院时间长和术后并发症延迟相关[25]。有研究评估了血细胞比容对65岁以上老年人经历非心脏手术终点事件的影响,结果显示:当血细胞比容<39%时,血细胞比容每降低1个百分点,30 d内死亡率将增加1.6%。患者术前血红蛋白低于正常值(男性<130 g/L,女性<120 g/L),非心脏手术术后30 d内的死亡率和心脏并发症的发生率都会增加[26]。大型临床研究表明,术后肌钙蛋白T峰值分别为0.02 μg/L、0.03 μg/L和0.30 μg/L是术后30 d内死亡率的独立危险因素[27],且高敏肌钙蛋白比肌钙蛋白T有更高的敏感度,可提高围手术期风险评估体系的准确率[28],上述实验室指标显示出良好应用前景,有望在未来的研究中纳入评估体系,构建更加精准易行的评估工具。
