富血小板血浆联合负压封闭引流治疗慢性难愈性创面的疗效
2021-09-08李红普尚文煊
李红普,王 兵,尚文煊
1)河南中医药大学人民医院(郑州人民医院)血管外科 郑州 450003 2)郑州大学第五附属医院血管外科 郑州 450052
随着我国人口老龄化的进展,糖尿病足、褥疮、静脉性溃疡等慢性溃疡的发病率逐年增高,不仅严重影响人们的生活质量,而且为社会和家庭带来了沉重的经济负担[1-2]。慢性难愈性创面多见于下肢,常位于下肢胫前区及足靴区,因其周围软组织较少,肢体末端血供差,容易感染,加之重力因素影响静脉回流,形成溃疡后往往较难自行愈合。传统处理方法有清创、换药、抗感染等。负压封闭引流(vacuum sealing drainage,VSD)联合清创术可以使细胞分泌促生长因子,降低创面细菌数量,减轻组织水肿,为创面愈合提供有利的环境[3]。该技术已被广泛应用于急慢性创面的治疗并取得了较好的疗效[4]。富血小板血浆(platelet-rich plasma,PRP)是将自体全血离心,得到血小板浓度是正常的4倍以上的血浆。PRP应用于慢性难愈性创面的治疗取得了较好的疗效[5]。本研究旨在观察PRP联合VSD应用于慢性难愈性创面的效果,为临床治疗提供一种新的思路。
1 对象与方法
1.1 病例纳入及排除标准纳入标准:经外科正规治疗创面持续时间大于1个月;患者积极治疗原发病;仅有1处创面。排除标准:合并有骨髓炎者;伴有血液系统疾病,血小板数量减少或功能低下者;有认知功能障碍,依从性差者;合并慢性消耗性疾病心肺功能较差者。
1.2 病例资料根据纳入及排除标准从郑州人民医院2018年10月至 2020年5月收治的慢性难愈性创面病例中选取74例,其中男33例,女41例,年龄45~79岁;创面类别:静脉性溃疡24例,下肢动脉硬化闭塞症伴溃疡18例,糖尿病足伴感染16例,压疮9例,外伤伴感染性创面7例。依据患者治疗意向选择治疗方案,39例应用PRP联合VSD,35例应用VSD,治疗前均签署知情同意书。
1.3 治疗方法手术干预原发病进行病因治疗。静脉性溃疡行射频消融治疗大隐静脉曲张。糖尿病足、下肢动脉硬化闭塞症及动脉性溃疡给予经皮腔内血管成形术,保证其至少有一条流出道。
VSD:首先对创面分泌物进行细菌培养及药敏实验,分别用生理盐水、络合碘、过氧化氢反复冲洗创面,彻底清除坏死和失活组织,清理过程中注意保护血管和神经,注意止血。将聚乙烯乙醇化泡沫敷料(山东威高)依据创面大小修剪并拼接成合适大小,完全覆盖创面,擦干周围皮肤,用生物薄膜对贴密封,通过三通管连接负压吸引器。随后负压引流装置接中心负压持续引流,负压值为-9.30至-35.5 kPa。在持续负压引流期间用生理盐水冲管,避免管腔堵塞。视创面愈合情况分别于第7、14天更换负压引流装置,第14天进行细菌培养。
PRP治疗:使用加入4 mL枸橼酸钠的50 mL无菌注射器采集自体静脉血36 mL,充分混匀,使用21G针头将其注入TriCeLL PRP装置(北京恒信博科技有限公司),室温下离心2次。第1次3 200 r/min离心5~7 min,隔离红细胞层,缓慢多次转动PRP装置使血清和白膜层充分混匀;第2次3 300 r/min离心3 min,分离PRP层和贫血小板层;依据创面大小抽取适量PRP备用。待手术清创完毕后使用1 mL注射器多次分点在创面周围注射。在PRP中添加凝血酶激活剂使其凝集成为富血小板凝胶,覆盖于创面,然后用合适大小的负压泡沫敷料覆盖,余操作同VSD。引流第14天,视创面愈合情况予以拆除负压引流装置或重复上述治疗,同时进行细菌培养。
1.4 观察指标
1.4.1创面愈合时间及愈合率 以创面闭合、上皮组织覆盖且无感染为创面愈合标准。创面愈合时间为从创面接受正规治疗开始至愈合的时间,通过患者门诊换药、电话随访等方式记录。愈合率=治愈创面数量/创面总数量×100%。
1.4.2血清炎性指标检测 分别于治疗前及治疗第14天进行血清C-反应蛋白、白细胞计数测定。
1.4.3细菌培养 治疗前和治疗第14天后进行细菌培养。先用生理盐水冲洗创面,清除坏死组织,“Z”字形取样,用一次性细菌培养管从创面一端均匀蘸取渗液到另一端,随后送至检验科行细菌培养。细菌培养阳性率=阳性例数/送检例数×100%。
1.5 统计学处理采用SPSS 25.0处理数据。两组年龄、创面面积、愈合时间的比较采用两独立样本t检验,性别、创面类别构成、愈合率的比较采用χ2检验,细菌培养转阴率的比较采用精确概率法,治疗前后血清炎性指标水平的比较采用重复测量数据的方差分析。检验水准α=0.05。
2 结果
2.1 两组患者一般资料的比较两组患者年龄、创面面积、性别等差异无统计学意义,见表1。
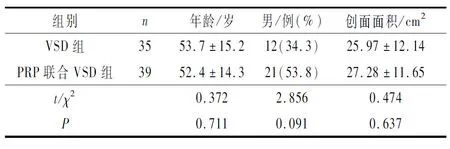
表1 两组患者一般资料比较
PRP联合VSD组中,静脉性溃疡13例,下肢动脉硬化闭塞症伴溃疡10例,糖尿病足伴感染8例,压疮5例,外伤伴感染性创面3例。VSD组中,静脉性溃疡11例,下肢动脉硬化闭塞症伴溃疡8例,糖尿病足伴感染8例,压疮4例,外伤伴感染性创面4例。两组创面类别构成差异亦无统计学意义(χ2=0.173,P=0.982)。
2.2 两组创面愈合率和愈合时间的比较PRP联合VSD组创面愈合率为92.3%(36/39),愈合时间为(39.15±4.18) d;VSD组创面愈合率为74.3%(26/35),愈合时间为(46.29±3.42) d;PRP联合VSD组创面愈合率大于VSD组(χ2=4.410,P=0.036),创面愈合时间短于VSD组(t=7.132,P<0.001)。未愈合的12例出院前创面较入院时均有不同程度减小,且没有发生粘连、再发感染等并发症。
2.3 两组患者感染水平比较PRP联合VSD组治疗前有15例细菌培养阳性,治疗第14天12例由阳转阴;VSD组治疗前13例细菌培养阳性,治疗第14天5例由阳转阴;两组均无阴转阳病例。PRP联合VSD组细菌培养转阴率高于VSD组(P=0.031)。两组治疗后血清C反应蛋白水平和白细胞计数均降低,但两组降低程度差异无统计学意义(表2)。
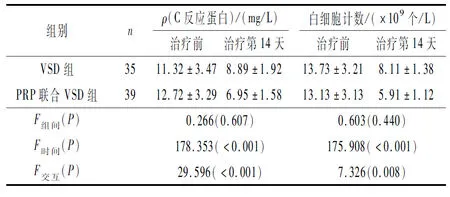
表2 两组治疗前后炎性指标的比较
3 讨论
PRP在创伤修复、血管再生、创面愈合等领域已得到大量研究,被广泛应用到骨科、整形外科、血管外科、神经外科、康复医学、美容等科室[6-7]。目前临床上应用较多的是自体全血2次离心法制备的PRP及其凝胶。研究[8]证实,PRP凝胶对慢性难愈性创面有明显的修复作用,安全有效。VSD可以通过扩张细胞膜引起信号的转导,促进细胞分裂、毛细血管增生、生长因子分泌,为创面愈合提供有利的环境[9]。有研究[10]发现VSD对于复杂性创面的愈合更有优势,例如糖尿病足合并感染、复杂外伤伤口等,但不适用于简单伤口。
本研究对PRP联合VSD对慢性难愈性创面的治疗效果进行了分析,结果显示PRP联合VSD在创面愈合率、创面愈合时间以及创面细菌培养转阴率方面疗效均优于单纯的VSD,与杨彪等[11]的研究结果一致。分析其原因可能为:PRP中富含大量的生长因子、大量的纤维蛋白,为创面的愈合提供了细胞支架,同时避免了自身免疫损伤。VSD加注射PRP或覆盖PRP凝胶,两者共同创造了抵御细菌感染的屏障,从而有效控制了感染;PRP和VSD可以共同抑制难愈性创面中的金属基质蛋白酶对胶原蛋白及生长因子的水解,有利于新生血管及肉芽组织的生长,促进创面愈合[12]。
目前关于PRP联合VSD治疗慢性难愈性创面的研究数据仍较少,且PRP的制备尚无统一的临床标准和指南。对于难愈性创面的治疗有间充质干细胞、蛆虫疗法、光学疗法、高压氧疗等多种方法[13],但是上述治疗方法缺少大量的临床前瞻性研究,且花费昂贵,临床开展较少。我们认为难愈性创面的治疗绝不仅仅是血管外科、骨科、整形外科或内分泌科某个单一科室所能完成的,应该保持多学科综合管理;应成立创面治疗中心,在多学科综合管理下,调整患者全身状态,积极对因治疗,处理原发病,分别在创面愈合的不同时期,采用多种技术联合治疗,针对每一个患者选择个体化治疗,营造良好的创面愈合环境,让患者有最大获益。病因治疗仍是创面管理的基础。此外,健康教育、有效的康复治疗、自我护理的加强均有利于创面的长期持续管理和愈合。