TBP辐解产物对U(Ⅳ)-肼和乙异羟肟酸反萃Pu(Ⅳ)的影响
2021-09-07宁勇智李传博
宁勇智,张 虎,陈 锦,李传博
中国原子能科学研究院 放射化学研究所,北京 102413
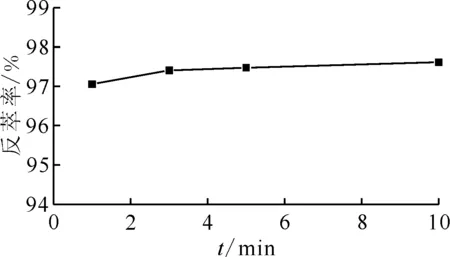
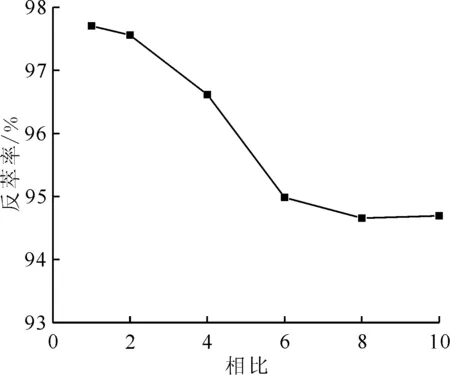
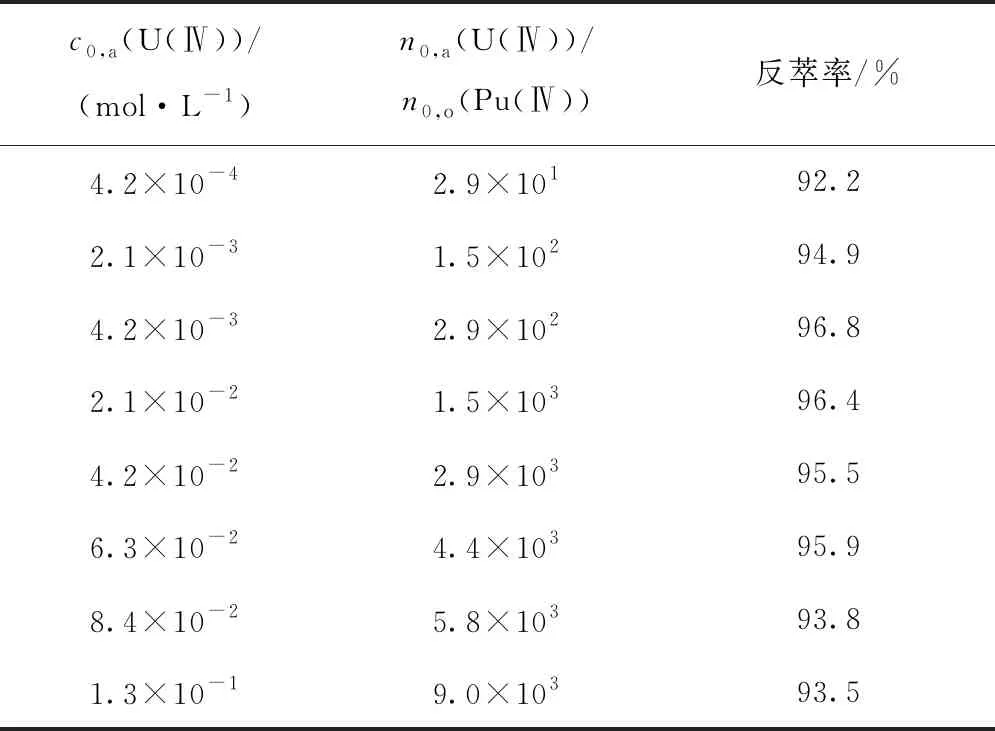
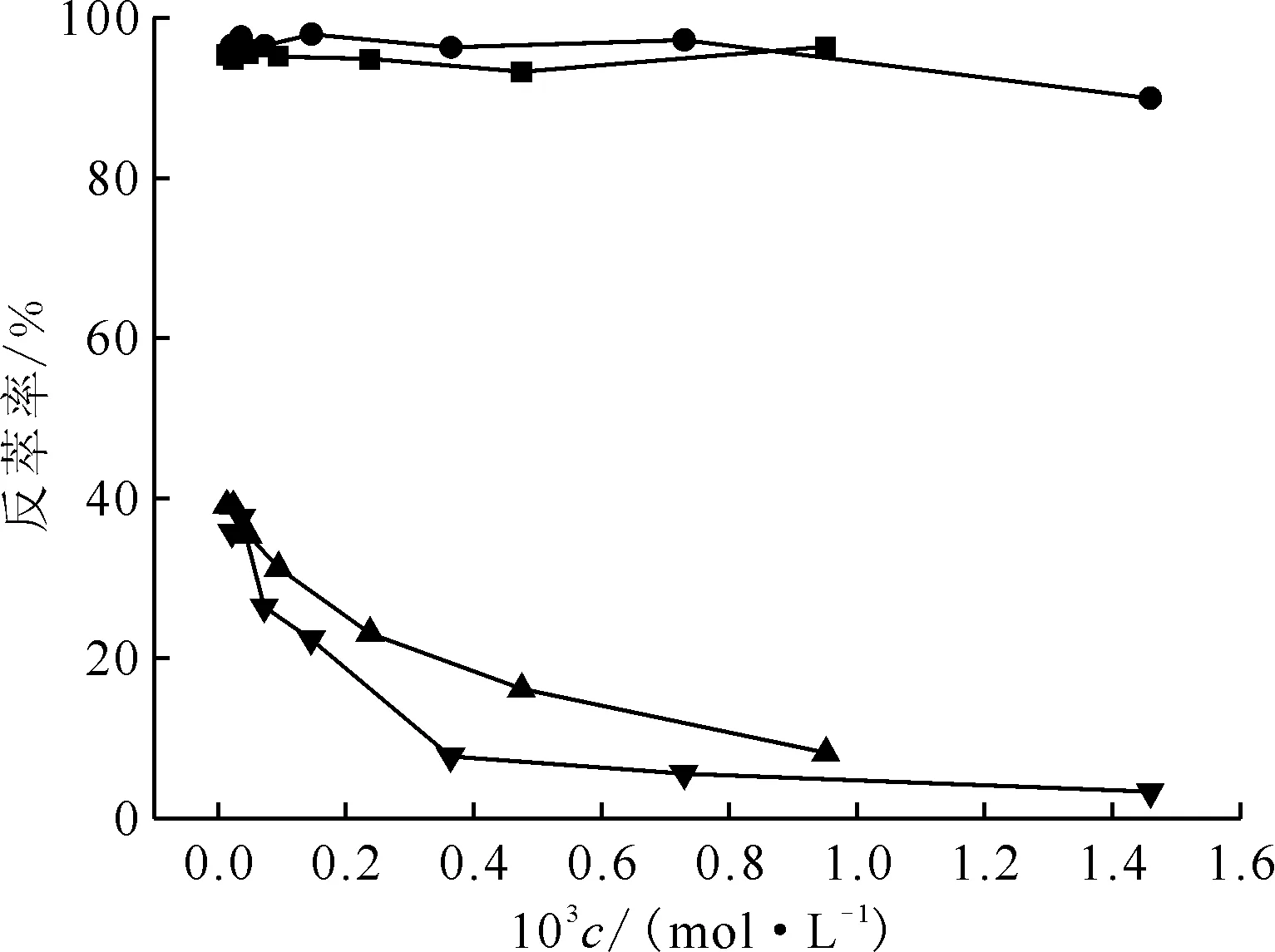
在乏燃料后处理PUREX流程的钚纯化循环中,通过设置钚障工艺,可以进一步提高Pu收率,降低Pu在有机溶剂中的保留。法国UP3厂和日本六个所[1]后处理厂的钚反萃取柱有机相出口处都设置有钚障槽,使用含U(Ⅳ)和肼的稀硝酸溶液补充反萃Pu。
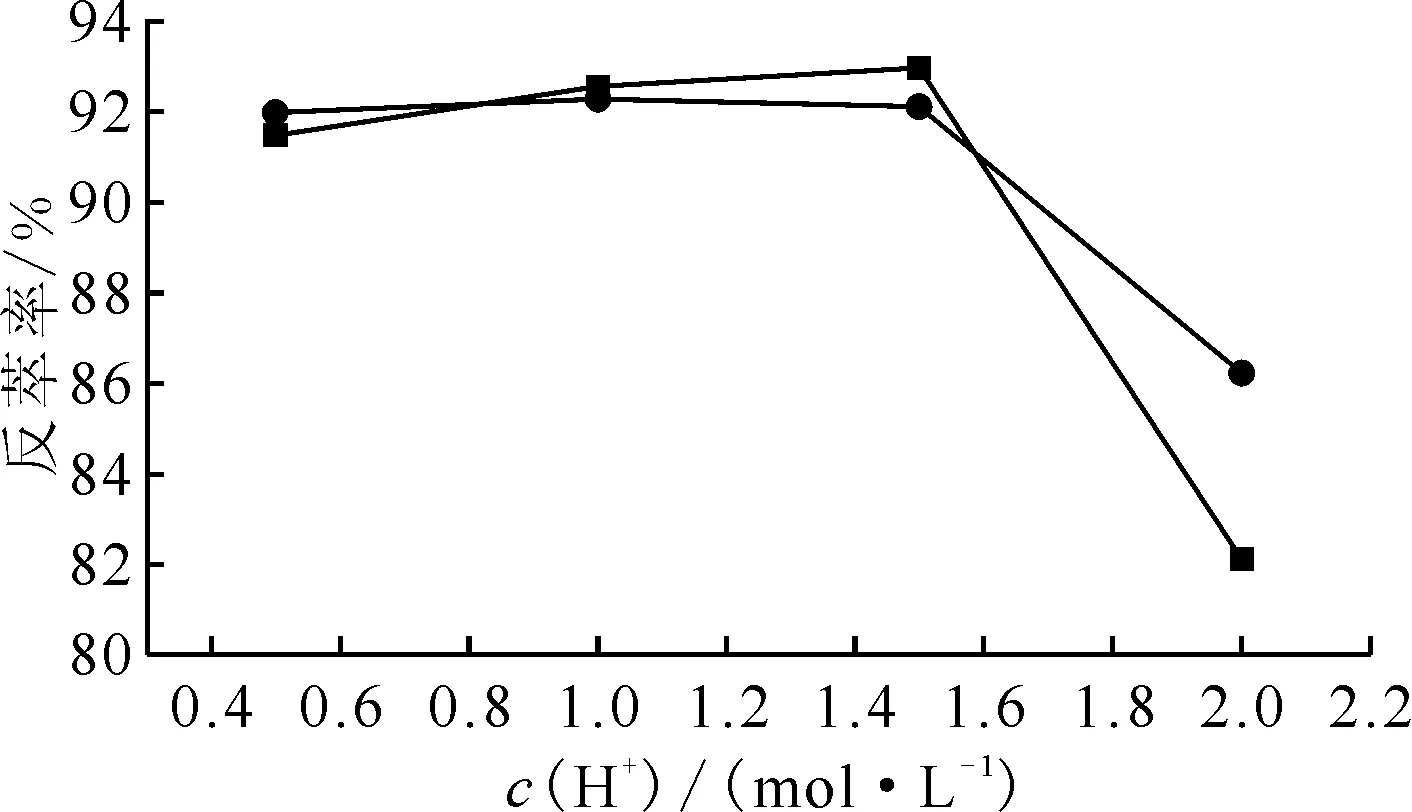
PUREX流程中的有机溶剂磷酸三丁酯(TBP)受到辐照后生成与Pu(Ⅳ)配位很强的辐解产物磷酸二丁酯(HDBP)、磷酸一丁酯(H2MBP),使Pu难以被完全反萃[2],造成有机相中Pu的保留。因此,溶剂中HDBP、H2MBP对Pu(Ⅳ)反萃的影响不容忽视。U(Ⅳ)是乏燃料后处理工艺中常用的还原反萃剂,还原效率高。乙异羟肟酸(AHA)是一种具有很强络合和还原能力的有机试剂,它在硝酸溶液中与锕系元素形成配合物的稳定性顺序[3-6]为U(Ⅵ) 已经有许多学者研究了U(Ⅳ)作为还原剂、AHA作为络合剂与Pu(Ⅳ)、Np(Ⅳ)等锕系金属离子的还原、络合作用,但是有关HDBP和H2MBP对其反萃Pu(Ⅳ)影响的研究报道较少。本工作拟研究TBP辐解产物HDBP和H2MBP对U(Ⅳ)-肼(N2H4)以及乙异羟肟酸(AHA)反萃Pu(Ⅳ)的影响,考察相接触时间、相比(o∶a)、还原剂浓度、HNO3浓度、N2H4浓度、HDBP和H2MBP浓度等条件对含有30%(体积分数)TBP/煤油中Pu(Ⅳ)反萃的影响。 二苯胺磺酸钠(指示剂级)、乙异羟肟酸(AHA,质量分数大于98%)、0.1 mol/L重铬酸钾分析滴定液(分析纯),上海阿拉丁生化科技股份有限公司;磷酸三丁酯(TBP)、浓硝酸、浓硫酸,分析纯,北京化学试剂公司;磷酸二丁酯(HDBP),纯度大于98%,国药集团化学试剂有限公司;磷酸一丁酯(H2MBP),纯度大于98%,加拿大多伦多化学研究责任有限公司;甲基红指示剂,分析纯,天津市大茂化学试剂厂;N-溴代丁二酰亚胺,分析纯,纯度大于99%,上海麦克林生化科技有限公司。30%TBP/煤油:用2.5%(质量分数)Na2CO3洗涤3次,再用0.1 mol/L HNO3洗涤3次,最后用去离子水洗至中性。 U(Ⅳ)溶液:采用电解还原U(Ⅵ)溶液的方法制备U(Ⅳ)储备液,得到0.7 mol/L U(Ⅳ)-0.69 mol/L HNO3-0.29 mol/L肼共100 mL。 含Pu(Ⅳ)有机相料液:取Pu(Ⅳ)硝酸溶液,用HNO3预平衡的30%TBP/煤油萃取3次,弃去水相,合并有机相,然后用30%TBP/煤油稀释定容。得到Pu(Ⅳ)有机相料液,Pu(Ⅳ)浓度为3.6×10-6mol/L,酸度为0.01 mol/L。 含HDBP、H2MBP的有机相溶液:将Pu(Ⅳ)萃入30%TBP/煤油中,加入计算量的HDBP或H2MBP到有机相中混匀,得到相应浓度的HDBP-30%TBP/煤油和H2MBP-30%TBP/煤油有机相溶液。有机相中Pu(Ⅳ)浓度为3.6×10-6mol/L,酸度为0.01 mol/L。 SL6000LL液闪仪,美国Bechman;PHS-3C型酸度计,上海雷磁仪器厂;VOATEX-5漩涡振荡器,海门市其林贝尔仪器制造有限公司;800B离心机,上海安亭科学仪器厂。 将配制好的含Pu(Ⅳ)有机相料液和反萃剂溶液按相比4∶1加入离心管中,在室温下振荡至预定时间,离心分相后分别取有机相、水相样品并测定两相中的Pu(Ⅳ)浓度,计算出Pu(Ⅳ)的反萃率。 U(Ⅳ)浓度的分析:用1.0 mol/L H2SO4-1 mol/L HNO3-0.1 mol/L NH2SO3H混合酸稀释U(Ⅳ)样品,加入3滴0.25 mol/L Fe2(SO4)3-2.0 mol/L H2SO4、2滴1%(质量分数)二苯胺磺酸钠-2.0 mol/L H2SO4后,0.1 mol/L K2Cr2O7滴定分析U(Ⅳ)浓度。 Pu质量浓度的测定:用液闪法测定α计数[7],推算得Pu的质量浓度。 HNO3浓度的分析:水相样品中HNO3浓度采用饱和草酸铵络合Pu,用标准NaOH进行滴定。有机相样品中HNO3先用去离子水反萃到水相,再用相同的方法测定。 铀中肼浓度分析:以甲基红为指示剂,用溴代丁二酰亚胺滴定法分析铀中肼浓度。 (1) 两相接触时间和相比的影响 (1) 由式(1)可知,该反应速率与反应物浓度成正比。从反应动力学来看,U(Ⅳ)能快速、定量地还原Pu(Ⅳ)。 c0,o(Pu(Ⅳ))=3.6×10-6 mol/L,c0,o(HNO3)=0.01 mol/L,c0,a(U(Ⅳ))=4.2×10-3 mol/L,c0,a(HNO3)=0.5 mol/L,c0,a(N2H4)=0.10 mol/L,25 ℃,o∶a=4∶1 在同样条件下改变相比为1∶1、2∶1、4∶1、6∶1、8∶1、10∶1,考察相比对Pu(Ⅳ)还原反萃取的影响,结果示于图2。由图2可知:当相比为1时,Pu(Ⅳ)的反萃率可达97.7%,而当相比大于6时,Pu(Ⅳ)的反萃率基本保持在94%以上。相比的增大,使得有机相中总Pu(Ⅳ)量和水相中总Pu(Ⅳ)量的比值增加,故反萃率降低。 c0,o(Pu(Ⅳ))=3.6×10-6 mol/L,c0,o(HNO3)=0.01 mol/L,c0,a(U(Ⅳ))=4.2×10-3 mol/L,c0,a(HNO3)=0.5 mol/L,c0,a(N2H4)=0.10 mol/L,25 ℃,t=5 min (2) 水相初始U(Ⅳ)浓度、HNO3浓度和肼浓度的影响 保持有机相中Pu(Ⅳ)和HNO3的初始浓度分别为3.6×10-6mol/L和0.01 mol/L,水相中HNO3和N2H4的初始浓度分别为0.5 mol/L和0.10 mol/L,在相接触时间为5 min、相比为4∶1、25 ℃的条件下,改变水相反萃剂U(Ⅳ)初始浓度,考察其对还原反萃取Pu(Ⅳ)的影响,结果列入表1。由表1可知:当U(Ⅳ)初始浓度从4.2×10-3mol/L升高到1.3×10-1mol/L时,根据公式(2)计算得到Pu(Ⅳ)反萃率的标准偏差s=1.7%,说明不同U(Ⅳ)初始浓度对Pu(Ⅳ)反萃率差距不大,且随着U(Ⅳ)初始浓度的升高,U(Ⅳ)对Pu(Ⅳ)均有很高的反萃率。因此在Pu(Ⅳ)浓度较低时,还原剂U(Ⅳ)浓度不再是主要影响因素。本实验选择还原反萃剂U(Ⅳ)的水相初始浓度为4.2×10-3mol/L。 (2) 当改变水相HNO3的初始浓度分别为0.3、0.5、0.7、1.0、1.2、1.5、2.0 mol/L时的实验结果示于图3。由图3可知,随着水相酸度增大,Pu(Ⅳ)反萃率显著降低。当水相酸度从0.3 mol/L增加到2.0 mol/L,Pu(Ⅳ)的反萃率从98.1%降低到86.5%。由U(Ⅳ)与Pu(Ⅳ)的反应动力学方程(式(1))可知,该反应速率与H+浓度的二次方成反比,还原剂的酸度对Pu(Ⅳ)反萃率影响较大。另一方面,随着水相酸度的增加,Pu(Ⅳ)的分配比变大。因此在避免Pu(Ⅳ)发生水解聚合的前提下,降低HNO3浓度有利于Pu(Ⅳ)的反萃[9]。 表1 水相中反萃剂U(Ⅳ)初始浓度对Pu(Ⅳ)反萃率的影响 图3 水相初始HNO3浓度对Pu(Ⅳ)反萃率的影响 图4 水相初始肼浓度对Pu(Ⅳ)反萃率的影响 (3) HDBP、H2MBP浓度的影响 c0,o(Pu(Ⅳ))=3.6×10-6 mol/L,c0,a(HNO3)=0.5 mol/L,c0,a(N2H4)=0.10 mol/L,25 ℃,t=5 min,o∶a=4∶1■——HDBP,c0,a(U(Ⅳ))=4.2×10-3 mol/L;●——H2MBP,c0,a(U(Ⅳ))=4.2×10-3 mol/L;▲——HDBP;▼——H2MBP 分别用0.5 mol/L HNO3溶液和4.2×10-3mol/L U(Ⅳ)-0.10 mol/L N2H4-0.5 mol/L HNO3溶液反萃取含不同浓度HDBP和H2MBP的含Pu(Ⅳ)有机溶液,在相接触时间5 min、相比4∶1的条件下,实验结果示于图5。由图5可知,0.5 mol/L HNO3不能有效反萃与HDBP、H2MBP配位的Pu(Ⅳ)。HDBP和H2MBP与Pu(Ⅳ)形成有机配合物,使Pu(Ⅳ)保留在有机相,从而影响反萃剂对其反萃的效率。当采用4.2×10-3mol/L U(Ⅳ)(0.10 mol/L N2H4-0.5 mol/L HNO3)还原反萃30%TBP/OK-HDBP或30%TBP/OK-H2MBP有机相中Pu(Ⅳ)时,反萃率均能达到96%以上。 图6和图7分别为相接触时间和U(Ⅳ)浓度的影响,实验结果表明,当U(Ⅳ)浓度大于4.2×10-3mol/L时,U(Ⅳ)能够快速完全地破坏HDBP或H2MBP与Pu(Ⅳ)形成的配合物,发生U(Ⅳ)与Pu(Ⅳ)的氧化还原反应,将Pu(Ⅳ)反萃到水相。发生反应(3)—(5): (3) (4) (5) c0,a(U(Ⅳ))=4.2×10-3 mol/L,c0,a(N2H4)=0.10 mol/L,c0,a(HNO3)=0.5 mol/L,25 ℃,o∶a=4∶1▲——HDBP,水相含U(Ⅳ);▼——H2MBP,水相含U(Ⅳ);●——HDBP;■——H2MBP 一方面,U(Ⅳ)有很强的还原能力,且其还原Pu(Ⅳ)的动力学速率比较快;另一方面,除了在水相发生还原反应,U(Ⅳ)还可被萃入有机相,在有机相中U(Ⅳ)还原Pu(Ⅳ)-DBP、Pu(Ⅳ)-MBP配合物中的Pu(Ⅳ),Pu(Ⅳ)被还原成Pu(Ⅲ)后进入水相。U(Ⅳ)的强还原性足以在有机相中还原被HDBP和H2MBP配位的Pu(Ⅳ)[10]。如图7,U(Ⅳ)浓度较低时,含HDBP或H2MBP的有机相中Pu(Ⅳ)反萃率均低于TBP有机相中Pu(Ⅳ)反萃率,这是因为Pu(Ⅳ)与DBP或MBP的络合常数均大于TBP的,Pu(Ⅳ)-DBP、Pu(Ⅳ)-MBP配合物稳定性均大于Pu(Ⅳ)-TBP。反应(4)和(5)相比反应(3)来说更加困难。 有机相含30%TBP/煤油,c0,o(HDBP)=4.8×10-4 mol/L,c0,o(H2MBP)=7.3×10-4 mol/L,c0,o(Pu(Ⅳ))=3.6×10-6 mol/L;c0,a(N2H4)=0.10 mol/L,c0,a(HNO3)=0.5 mol/L;25 ℃,t=5 min,o∶a=4∶1●——只有30%TBP/煤油,▲——含HDBP,■——含H2MBP (1) 两相接触时间的影响 配制三种不同组成的有机溶液:(1) 4.8×10-4mol/L HDBP-30%TBP/煤油;(2) 7.3×10-4mol/L H2MBP-30%TBP/煤油;(3) 30%TBP/煤油。三种有机溶液中Pu(Ⅳ)和HNO3的初始浓度分别为3.6×10-6mol/L和0.01 mol/L,水相中AHA和HNO3的初始浓度分别为0.10、0.1 mol/L。在相比为4∶1、25 ℃的条件下,考察Pu(Ⅳ)反萃率随两相接触时间变化的关系,结果示于图8。由图8可知:AHA反萃Pu(Ⅳ)时,Pu(Ⅳ)反萃率随相接触时间的增加而提高。在5、10 min和25 min时,含HDBP的有机相中Pu(Ⅳ)的反萃率分别为86.6%、99.3%和99.1%;含H2MBP的有机相中Pu(Ⅳ)反萃率分别为75.2%、85.0%和98.6%。AHA能够迅速将30%TBP/煤油中的Pu(Ⅳ)络合反萃到水相,5 min的反萃率即可达到99%以上。对于含HDBP的有机相,反萃10 min后Pu(Ⅳ)反萃率能达到99%以上,而对于含7.3×10-4mol/L H2MBP的有机相,30 min时Pu(Ⅳ)反萃率才达到99%。其原因是由于TBP辐解产物能够与Pu(Ⅳ)形成更稳定的配合物Pu(NO3)2(DBP)2[11]等,降低了AHA络合反萃Pu(Ⅳ)的效果。 有机相含30%TBP/煤油,c0,o(Pu(Ⅳ))=3.6×10-6 mol/L;c0,a(AHA)=0.10 mol/L,c0,a(HNO3)=0.1 mol/L;25 ℃,t=5 min,o∶a=4∶1■——不含HDBP 或H2MBP,▲——c0,o(HDBP)=4.8×10-4 mol/L,●——c0,o(H2MBP)=7.3×10-4 mol/L AHA反萃Pu(Ⅳ)的过程主要包括:(1) 在搅拌作用下,与TBP、HDBP或H2MBP配位的Pu(Ⅳ)扩散到两相界面,并发生解离;(2) 解离的Pu(Ⅳ)进入水相;(3) 进入水相的Pu(Ⅳ)或在相界面的Pu(Ⅳ)被AHA络合还原到Pu(Ⅲ);(4) 络合还原的Pu保留在水相。对于过程(1)和(2),在充分搅拌下,与TBP-Pu(Ⅳ)迅速达到平衡,但是Pu(Ⅳ)与DBP键长更短,相比TBP,Pu(Ⅳ)与DBP之间相互作用更强[12],此外,在较低酸度下HDBP与H2MBP易与Pu(Ⅳ)形成难溶配合物和胶体,使得有机溶液中有HDBP或H2MBP存在时,AHA反萃Pu(Ⅳ)更困难,达到平衡需要更长的时间。在用0.10 mol/L AHA反萃含7.3×10-4mol/L H2MBP有机相中的Pu(Ⅳ)时,30 min时仍未达到平衡状态。 (2) 乙异羟肟酸浓度和酸度的影响 分别用AHA浓度为0.05、0.10、0.15、0.20、0.25、0.30 mol/L,HNO3浓度为0.1 mol/L的水溶液络合反萃含4.8×10-4mol/L HDBP、7.3×10-4mol/L H2MBP的Pu(Ⅳ)有机相,Pu(Ⅳ)反萃率结果列入表2。由表2可知:当有机相中不含HDBP或H2MBP时,0.05~0.30 mol/L AHA对Pu(Ⅳ)反萃率均大于97%,说明AHA对有机相中Pu(Ⅳ)有很好的络合反萃作用[13];当有机相中含有HDBP或H2MBP时,Pu(Ⅳ)与之形成相对稳定的配合物,因此反萃过程中Pu(Ⅳ)配合物进入水相或相界面发生反应更加困难。当n(AHA)/n(HDBP)≈50时,Pu(Ⅳ)反萃率约为85%,而n(AHA)/n(H2MBP)≈50时,Pu(Ⅳ)反萃率已将近96%;当Pu(Ⅳ)反萃率达到97%时,AHA摩尔数需要过量HDBP约78倍、需过量H2MBP约52倍,且在AHA过量约100倍时均能达到99%左右的Pu(Ⅳ)反萃率。因此,采用AHA作为反萃剂可实现有机相中Pu(Ⅳ)的有效反萃,但相比H2MBP,AHA对有机相中含HDBP的Pu(Ⅳ)反萃更困难。 表2 有机相含HDBP、H2MBP、无HDBP/H2MBP AHA浓度对Pu(Ⅳ)反萃率的影响 HNO3浓度对AHA络合反萃Pu(Ⅳ)的影响示于图9。由图9可知:在水相酸度为0.5~1.5 mol/L,随着酸度的升高,AHA对HDBP或H2MBP络合的Pu(Ⅳ)的反萃率影响不大,均能达到92%以上,并且两者反萃率差异较小。但当HNO3浓度大于1.5 mol/L后,两种情况下的Pu(Ⅳ)反萃率均显著下降,HNO3浓度为2.0 mol/L时,AHA对HDBP或H2MBP络合的Pu(Ⅳ)的反萃率分别降低为86.2%和82.1%。主要是因为随着HNO3浓度的增加,Pu(Ⅳ)的分配比增大,不利于有机相中Pu(Ⅳ)的去除[14]。 c0,o(HDBP)=4.8×10-4 mol/L,c0,o(H2MBP)=7.3×10-4 mol/L,c0,o(Pu(Ⅳ))=3.6×10-6 mol/L;c0,a(AHA)=0.10 mol/L;25 ℃,t=5 min,o∶a=4∶1●——HDBP,■——H2MBP 对于水相酸度对Pu(Ⅳ)反萃的影响,还可利用AHA与Pu(Ⅳ)的络合反应方程式进行分析,其反应式如式(6),分配比的计算如式(7)[15]。 (6) (7) 其中:D0(Pu(Ⅳ))为c0(AHA)=0时Pu(Ⅳ)的萃取分配比;D(Pu(Ⅳ))为c0(AHA)≠0时Pu(Ⅳ)的萃取分配比,即Pu(Ⅳ)在有机相中总浓度与水相中总浓度之比。 由式(6)、(7)可以看出,降低AHA酸度,Pu(Ⅳ)的萃取分配比降低,有利于AHA对Pu(Ⅳ)的络合反萃,实验结果与此相符。因此,在使用AHA作为钚障槽的洗涤剂时,萃取系统酸度不应高于1.5 mol/L,且低酸有利于有机污溶剂的净化。 (1) U(Ⅳ)作为Pu(Ⅳ)的还原反萃剂对Pu(Ⅳ)有很强的还原反萃能力,且反应速率快。U(Ⅳ)可以有效地破坏HDBP、H2MBP与Pu(Ⅳ)的络合,消除HDBP和H2MBP对U(Ⅳ)反萃Pu(Ⅳ)的影响。提高相接触时间,降低相比、HNO3浓度、肼浓度均有利于U(Ⅳ)对Pu(Ⅳ)的反萃。 (2) 乙异羟肟酸(AHA)作为有机络合还原反萃剂能够有效地从含有HDBP或H2MBP的有机相中络合反萃Pu(Ⅳ),消除HDBP和H2MBP对Pu(Ⅳ)反萃的影响;相比H2MBP,AHA对有机相中含HDBP的Pu(Ⅳ)反萃更困难。 (3) 采用U(Ⅳ)和AHA作为反萃剂可实现有机相中Pu(Ⅳ)的有效反萃,可为PUREX流程中钚障槽工艺还原剂的选择提供数据支持。1 实验部分
1.1 试剂及仪器
1.2 实验方法
1.3 分析方法
2 结果与讨论
2.1 U(Ⅳ)-肼还原反萃Pu(Ⅳ)










2.2 乙异羟肟酸(AHA)反萃Pu(Ⅳ)



3 结 论
