对苯醌电化学捕获CO2机理研究及捕获产物的结构分析
2021-09-07杨钟煜范慧金葆康
杨钟煜,范慧,金葆康
(安徽大学化学化工学院,安徽合肥230601)
化石燃料作为工业和现代人类生活的主要能源,排放出大量的二氧化碳,而二氧化碳被认定为是全球变暖的主要原因。当前,解决这个问题的策略主要在两个方向:一是碳捕获和储存(CCS),即捕捉CO并将其储存;二是碳捕捉和利用(CCU),即二氧化碳捕获和利用,在实现降低二氧化碳排放的同时,将它转换为其他有用的化学物质,如甲醇和甲烷。可以实现CO捕获和利用的化学方法手段有很多,其中,利用电化学还原捕获CO显示出良好的前景。
醌羰基是醌类化合物(Q)电化学活性基团,具有易被还原的特性。Q的还原性质,易受到苯环上取代基的影响,同时介质对Q的还原过程有着较大影响。不同溶液中,醌类物质的氧化还原过程,经历一系列的电子转移、质子转移、氢键形成和中间体半醌自由基产生。还原中间体、还原终产物可以作为亲核试剂,进攻CO的亲电碳原子进而捕获CO,故而利用电化学的方法来还原醌物质并捕获CO的技术研究有着重要的理论意义和潜在的应用价值。
本文研究了苯醌(BQ)在乙腈体系中对CO的电化学捕获,采用现场红外光谱跟踪电化学捕获CO的历程,结合恒电位电解得到BQ捕获CO的产物,采用多种谱学技术对产物开展结构分析。
1 实验部分
1.1 仪器与试剂
CHI630E电化学工作站,上海辰华仪器有限公司;Nicolet is50型FTIR红外光谱仪,美国Nicolet公司;MODEL 363 POTENTIOSTAT GALVANOSTAT,PRINCETON AOOLIED RESEARCH恒电位仪,上海辰华仪器有限公司。
对苯醌(BQ),纯度98%,Sigma-Aldrich公司;乙腈(AN),HPLC级,Sigma-Aldrich公司;高氯酸四丁基铵盐(TBAP),HPLC级,上海Aladdin公司,用前烘1 h;氘代DMSO(DMSO-d),99.9%,萨恩化学技术有限公司;二氧化碳,纯度≥99.99%,南京上元工业气体厂;氮气,纯度≥99.99%,南京上元工业气体厂。
1.2 实验过程
1.2.1 电化学实验
利用CHI630E电化学工作站,采用三电极体系(金圆盘电极(Φ4 mm)为工作电极,Ag/AgCl为参比电极,铂丝为对电极)进行电化学实验。实验前,在抛光布上用AlO(粒径0.05~0.03μm)抛光工作电极,然后分别以二次水和乙醇清洗,并用高纯氮气吹干。
1.2.2 现场红外光谱实验
Nicolet is50型红外光谱仪,配以SMART iTR的镜面反射装置,液氮冷却HgCdTe(MCT/A)检测器,光谱分辨率为16 cm,所有光谱图都是以32张干涉图叠加所得到的。
实验前,分别配制含有0.2 mol/L的TBAP 10 mmol/L的BQ的乙腈溶液A和B(A与B相同)。A、B均通10 min高纯N,去除空气,随后B再通入40 min CO,得到CO饱和溶液。通过控制A、B溶液体积比,配制含不同CO浓度BQ溶液。电学实验与红外光谱实验同步进行,全部实验数据均以Grams/3D软件进一步处理。
1.2.3 恒电位电解实验
50 mL的0.2 mol/L TBAP和10 mmol/L BQ在乙腈溶液中,使用三电极体系进行电解;在“H”型的电解池中进行实验,工作电极选择1 cm金片电极,1 cm铂片电极选择对电极,银离子电极为参比电极。其中工作电极和对电极在使用前先用二次水和乙醇进行清洗,然后用二次水和乙醇(1∶1)超声清洗30 min;超声操作完毕后,再用二次水和乙醇清洗,接着用0.5 mol/L HSO以50 mV/s进行清扫;清扫完毕后,再次用二次水和乙醇(1∶1)超声清洗15 min。放入电解池中,电解池的阴极室在通电之前,需先通入CO1 h,保证阴极室电解开始时CO处于饱和状态,同时阳极室需通30 min的N作排空气处理。在-0.9 V下进行恒电位电解,实验时持续通入CO,当电解电流从初始的7 mA减小到5μA基本不再变化时停止电解,电解过程终有沉淀生成,总电解时长约为20 h。
1.2.4 电解产物的结构确认
电解结束后利用极性和溶解度的差异对产物进行提纯。具体而言,阴极室溶液先过滤,得到滤饼(沉淀产物),然后用乙腈对滤饼浸泡1 h后再次过滤,去除滤饼中的BQ;接着用二氯甲烷浸泡并过滤,去除残留的电解质TBAP。重复上述操作2次,最后对其进行真空干燥,得到纯净的产物。利用红外光谱仪确定产物主要官能团;利用元素分析仪(Vario EL-3)确定产物各元素间的比例;采用核磁共振谱仪(JNM-ECZ600R),以DMSO-d做溶剂进行表征,确定其结构。
2 结果与讨论
2.1 BQ在乙腈溶液中对CO2电化学捕获研究
图1 (A)是10 mmol/L BQ乙腈溶液在薄层池中的循环伏安曲线,曲线a是N条件下的CV曲线,曲线b是在饱和CO条件下的CV曲线,可以明显观察到,曲线a含有两对氧化(E)还原(E)峰:E=-0.42 V,E=-0.18 V,ΔE=0.24 V;E=-0.85 V,E=-0.62 V,ΔE=0.23 V,具有良好的对称性。整个反应历程符合EE机理,即第一步得到一电子后,生成阴离子自由基BQ中间体,随后在更负的电位下还原生成二价阴离子自由基BQ。氧化还原式电位分别是E=-0.39 V以及E=-0.73 V[E=(E+E)/2],这与文献报道的相符。但是在饱和CO的情况下,曲线b呈现的是一对氧化还原峰,还原峰电位E=-0.47 V,氧化电位E=-0.09 V,E=-0.28 V;与曲线a相比可以发现,还原峰的电流值I接近曲线a第一对还原峰电流值的两倍,可能原因是原来两步一电子转移转变为一步两电子的还原过程,表明CO的加入改变了对BQ电化学的氧化还原历程,第二步的还原过程电位产生正移,与第一个还原峰相重合,故曲线b呈现的是一对氧化还原峰,这和质子给体条件下的BQ电化学行为相似。需要指出的是,实验条件下不会发生CO自身的氧化还原,所以两对氧化还原峰重合,可能是CO和BQ的还原产物产生的化学反应所导致的。

图1 10 mmol/L BQ在乙腈溶液中的CV图(A)(其中,a为BQ的CV图,b为BQ在饱和CO2的条件下CV图)和CV曲线b所对应的红外光谱3D图(B)(0.2 mol/L的TBAP为支持电解质,扫速为10 mV/s)Fig.1 CV figure(A)of 10 mmol/L BQ in acetonitrile solution(where A is CV figure of BQ and b is CV figure of BQ under the condition of CO2 saturation)and 3D infrared spectrum figure(b)corresponding to CV curve b(0.2 mol/L TBAP was used as the supporting electrolyte and the scanning speed was 10 mV/s)
图1(B)是对应图1(A)中曲线b在进行循环伏安实验的同时,以0.2 V时的谱图为背景采集的现场红外光谱3D图。和BQ自身氧化还原的现场红外光谱3D图不同,CO存在时可以观察到两种类型的红外特征吸收峰。2 340 cm处负向吸收峰变化代表电化学过程中CO浓度的降低;正向吸收峰1 518 cm、1 356 cm、1 249 cm分别为[BQ-CO]的BQ的v的伸缩振动、v的伸缩振动以及v的弯曲振动,具体红外峰指认见表1。2 340 cm处吸收峰的变化表明BQ电化学还原过程中CO的浓度不断降低,考虑到该电位下CO不会发生自身的还原,因此合理的解释是,BQ的还原产物捕获了CO;另一方面,实验条件下并没有观察到阴离子自由基BQ中间体的红外特征吸收峰,表明生成的BQ立即与CO发生了反应,迅速生成[BQ-CO],产物不稳定,进一步获得电子。

表1 乙腈溶液中各红外吸收峰的归属Tab.1 The assignment of IR absorption peaks in CH3CN
图2 (A)是图1(B)处理得到的循环伏吸图(CVA)。图中1 356 cm、2 340 cm可分别跟踪[BQCO]和CO在电化学反应过程中的浓度变化。由图可知,还原过程中,CO的浓度约在40 s(-0.20 V)开始下降,并在70 s(-0.50 V)降到最小值;同时[BQ-CO]在40 s(-0.20 V)开始生成,并在70 s(-0.50 V)达到最大值。氧化过程中浓度的变化正好与还原过程相反。电位回扫到0.20 V的时候,2 340 cm、1 641 cm、1 356 cm处吸光度基本回到初始点。随着扫描的进行,BQ还原为BQ并立刻捕获CO,生成不稳定的[BQCO]再次得一电子还原成[BQ-CO]。而图2(B)是对应的导数循环伏吸图(DCVA),与CV曲线一致,从图中可以看出1 356 cm、2 340 cm分别代表的[BQCO]和CO基本和图1(A)图形类似,观察到一对氧化还原峰。
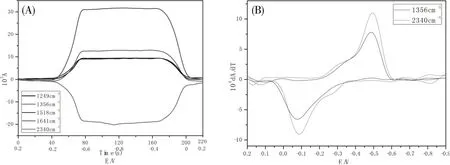
图2 BQ在2 340 cm-1、1 641 cm-1、1 518 cm-1、1 356 cm-1、1 249 cm-1处的CVA(A)和1 356 cm-1、2 340 cm-1处的DCVA(B),其中2 340 cm-1处的DCVA乘以-1Fig.2 CVA(A)and DCVA(B)of BQ at 2 340 cm-1,1 641 cm-1,1 518 cm-1,1 356 cm-1,1 249 cm-1 Where DCVA at 2 340 cm-1 is multiplied by-1
和BQ自身的两步单电子还原机理不同的是,有CO参与反应时,CV和DCVA结果均表明,BQ的两步单电子过程变得复杂,可能存在的电子转移机制为:

然而,仅仅基于红外光谱电化学,还不足以确认以上过程的正确性。为了进一步确证BQ捕获CO后形成[BQ-CO]的结构,开展了恒电位整体电解研究,期望获得最终电解产物的结构。
2.2 BQ对CO2电化学捕获产物的结构分析
利用CHI630E电化学工作站进行恒电位电解电位测定。电解前,利用线性扫描伏安法(LSV),确定恒电位电解实验时控制电位。电解池LSV结果如图3所示,在-0.9 V下已达到峰电流,因此恒电位电解时选择电位在-0.9 V下进行。电解过程中,通入CO,既保持其浓度,同时起到搅拌作用。随着电解的进行,电流逐渐减小,当电解电流从开始的7 mA减小到5μA时基本不再减小,停止电解,总电解时长约为20 h。

图3 10 mmol/L BQ与饱和CO2在AN中的循环伏安曲线(电位扫描速率为10 mV/s)Fig.3 Cyclic voltammetry curves of 10 mmol/L BQ and saturated CO2 in AN(with potentialscanning rate of 10 mV/s)
电解结束后,阴极室溶液颜色从电解开始的淡黄绿色变为褐色,并且从阴极室中可以明显观察到有沉淀生成,并且工作电极上也会吸附部分沉淀。对沉淀先进行过滤,然后用乙腈对滤饼浸泡1 h后再次过滤,去除滤饼中的BQ,利用真空干燥箱干燥去除残留的乙腈。接着用二氯甲烷浸泡并过滤,去除残留的电解质TBAP。多次重复上述操作,直到滤液无色为止,干燥后得到产物。
电解产物的核磁共振(NMR)谱图如图4所示。氢谱中0.9 mL/m、1.27 mL/m、1.53 mL/m、3.14 mL/m处的峰归属为四丁基铵根;6.51 mL/m处的峰为苯环上的氢,比例为3∶2∶2∶2∶1。C谱中158.25 mL/m属于羰基的峰,150.35 mL/m和116.19 mL/m属于苯环的峰,10~60 mL/m处的峰(除40 mL/m处属于DMSO-d
的峰)均属于四丁基铵根。证实了CO所进攻的是BQ上的羰基,产物的结构为稳定的羧酸式化合物;元素分析结果表明C∶H∶O∶N=20∶38∶3∶1,进一步证明产物中包含四丁基铵根,与核磁结果一致。为了进一步证实CO所进攻的是BQ上的羰基,对电解产物进行酸化(2 mol/L HCl)处理,进一步提纯并旋蒸处理,得到酸化后水解产物。
水解产物核磁共振(NMR)谱图如图5所示。结果与数据库文献中苯酚完全一致。与图4对比可以发现,代表四丁基铵根离子的氢谱和碳谱在图5中观察不到,并且代表CO处158.25 mL/m的碳谱也消失,表明酸化水解后生成对苯酚。以上结果证明,BQ电化学捕获CO的过程中,亲核进攻CO的是BQ羰基上的氧。
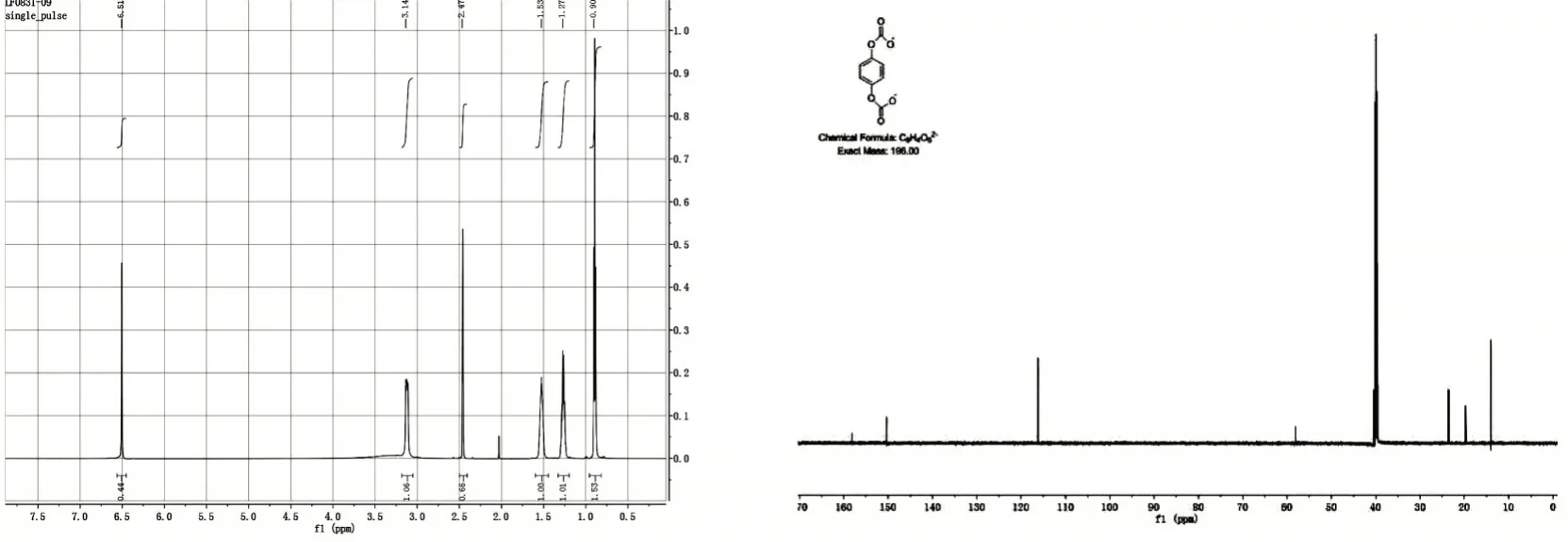
图4 氢谱和碳谱,氘代试剂为DMSOFig.4 1H NMR(600 MHz,DMSO-d6)δ6.51(s,1H).13C NMR(151 MHz,DMSO-d6)δ158.25,150.35,116.19.

图5 酸化后产物的氢谱与碳谱,氘代试剂为DMSOFig.5 1H NMR(600 MHz,DMSO-d6)δ8.60(s,2H),6.52(s,4H).13CNMR(151 MHz,DMSO-d6)δ150.25,116.20.
3 结论
红外光谱电化学及电解产物结构分析表明,乙腈溶液中BQ首先得一电子成为一价阴离子自由基BQ,然后捕获CO生成[BQ-CO],随后继续得到一电子生成终产物[BQ-CO]。研究发现,BQ捕获CO的化学计量关系为1∶2,亲核进攻CO的是BQ羰基上的氧,形成较为稳定的羧酸式结构。反应历程如下:
