酸浆全草甾体类化学成分研究
2021-09-06谭茂强郭远强丁丽琴
谭茂强,牛 峥,张 敏,郭远强,邱 峰*,丁丽琴
酸浆全草甾体类化学成分研究
谭茂强1, 2,牛 峥1, 2,张 敏1, 2,郭远强1, 3,邱 峰1, 2*,丁丽琴2*
1. 天津中医药大学中药学院,天津 301617 2. 天津中医药大学 组分中药国家重点实验室,天津 301617 3. 南开大学药学院,天津 300350
研究酸浆属植物酸浆var.的化学成分。对酸浆全草醋酸乙酯部位采用硅胶、Sephadex LH-20、ODS等多种柱色谱,并结合制备液相等方法进行分离和纯化,根据理化性质及波谱数据对其化学成分进行结构鉴定。从酸浆醋酸乙酯部位中共分离鉴定10个化合物,分别为4β-methoxy-7β-hydroxyneophysalin B(1)、酸浆苦素P(2)、7-氧代-β-谷甾醇(3)、7β-羟基谷甾醇(4)、3β-羟基豆甾-5,22-二烯-7-酮(5)、豆甾-5,22-二烯-3β,7β-二醇(6)、(24)-5,28-stigmastadiene-3β,24-diol-7-one(7)、(24)-5,28-stigmastadiene-3β,24-diol-7-one(8)、3β-羟基-胆甾-5-烯-7-酮(9)、sargassuol A(10)。化合物1为新化合物4β-methoxy-7β-hydroxyneophysalin B,中文俗名酸浆苦素XIII,化合物3~10均为首次从该属植物中分离得到。
酸浆全草;4β-methoxy-7β-hydroxyneophysalin B;酸浆苦素P;7-氧代-β-谷甾醇;结构鉴定;甾体类化合物
酸浆全草为茄科酸浆属植物酸浆L. var.(Mast.) Makino的干燥全草,味酸、苦,性寒,归肺、脾经;具有清热毒、利咽喉、通利二便的功效。酸浆中主要化学成分为甾体类、黄酮类、苯丙素类、生物碱类化合物和其他类化合物,其中甾体类(主要为变形麦角甾类)成分被认为是酸浆的特征性和主要生物活性物质[1-8]。现代药理研究表明酸浆具有抗肿瘤[9]、抗微生物[10]、抗疟疾[11]、免疫抑制[12]、免疫调节[13]和抗炎[14]等多种药理活性,而甾体类的抗肿瘤[15-17]、抗炎[14]活性较为显著。本实验通过多种色谱方法,对酸浆全草醋酸乙酯部位进行化学成分研究,共鉴定10个化合物(图1),分别为4β-methoxy-7β-hydroxyneophysalin B(1)、酸浆苦素P(physalin P,2)、7-氧代-β-谷甾醇(7-oxo- β-sitosterol,3)、7β-羟基谷甾醇(7β-hydroxysitosterol,4)、3β-羟基豆甾-5, 22-二烯-7-酮(3β-hydroxystigmasta- 5,22-dien-7-one,5)、豆甾-5,22-二烯-3β,7β-二醇(stigmast-5,22- dieβ,7β-diol,6)、(24)-5,28- stigmastadiene- 3β,24-diol-7-one(7)、(24)-5,28- stigmastadiene-3 β,24-diol-7-one(8)、3β-羟基-胆甾-5-烯-7-酮(3β-hydroxy-cholest-5-en-7-one,9)、sargassuol A(10),其中化合物1为新化合物,命名为4β-methoxy-7β-hydroxyneophysalin B,化合物3~10均为首次从酸浆属植物中分离得到。
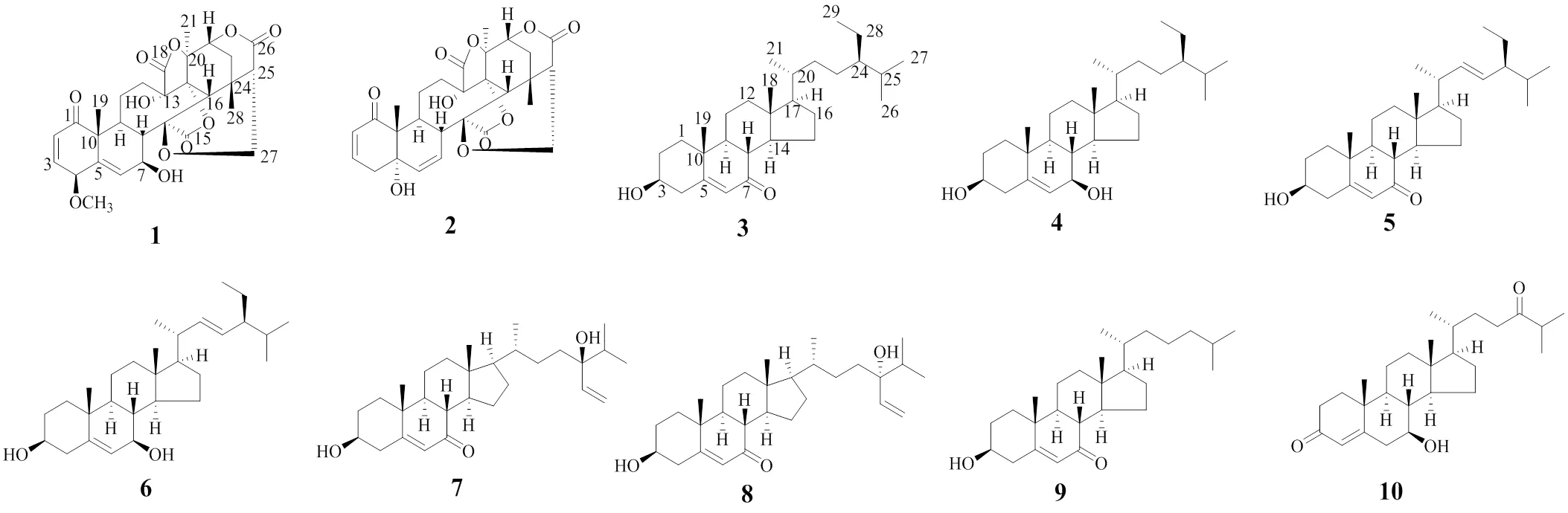
图1 酸浆全草醋酸乙酯部位化合物的结构
1 仪器与材料
1.1 仪器
A1204型万分之一电子天平 [梅特勒-托利多仪器(上海)有限公司],Bruker AVANCE III 600 MHz核磁共振波谱仪(瑞士Bruker公司),EYELA N-1100型系列旋转蒸发仪(日本东京理化EYELA公司),SB25-1DTN型超声清洗仪(宁波新芝生物科技有限公司),ZF-20D型暗箱式紫外分析仪(上海顾村电光仪器厂),Waters e2695分析型高效液相色谱仪(美国Waters公司),Waters 2535制备型高效液相色谱仪(美国Waters公司),Waters Xevo G2-S UPLC-Q/TOF(美国Waters公司),分析型及制备型YMC C18色谱柱(250 mm×4.6 mm,250 mm×20 mm,5 μm,日本);分析型及制备型PBr C18色谱柱(250 mm×4.6 mm,250 mm×20 mm,5 μm,日本)。
1.2 材料
柱色谱硅胶(100~200、200~300目,青岛海洋化工厂);ODS-A-HG 12 nm S-50 μm(日本YMC公司);Silica gel 60 F254(美国Merck公司);TLC Silica gel 60 RP-18 F254s(美国Merck公司);Sephadex LH-20(美国GE);薄层制备硅胶GF2540.4~0.5 mm(于成化工上海有限公司);色谱级甲醇、乙腈(天津市康科德科技有限公司),分析级环己烷、二氯甲烷、醋酸乙酯、甲醇(天津市康科德科技有限公司)。
样品(170 kg)购于吉林省延边朝鲜族自治州,药材经天津中医药大学中药学院中药资源学教研室张丽娟教授鉴定为酸浆L. var.(Mast.) Makino全草,留样现保存于天津中医药大学中医药研究院。
2 提取与分离
酸浆全草170 kg,用10倍量60%乙醇/水浸泡10 h,回流提取2次,每次2 h。合并提取液,减压回收溶剂浓缩,得到提取物浸膏。将总浸膏分散到5倍量的水中,分别用等体积的石油醚,醋酸乙酯萃取3次,减压得到石油醚萃取物、醋酸乙酯萃取物以及水层。醋酸乙酯萃取物(1.05 kg)经正相硅胶柱色谱,用二氯甲烷-甲醇(100∶0、50∶1、25∶1、10∶1、5∶1、3∶1、1∶1、0∶100)梯度洗脱,收集、浓缩后依据TLC检测合并得到13个流分(E1~E13)。
E3(66 g)经正相硅胶柱色谱,用环己烷-醋酸乙酯(100∶0、50∶1、25∶1、10∶1、5∶1、3∶1、1∶1、0∶100)梯度洗脱,收集、浓缩后依据TLC检测合并得到11个流分。E3-7经Sephadex LH-20柱色谱(二氯甲烷-甲醇1∶1)进行分离,经制备高效液相分离(甲醇-水25∶75,体积流量3 mL/min,检测波长205、236 nm)得到化合物6(3.2 mg)。
E8(35 g)经正相硅胶柱色谱,用环己烷-醋酸乙酯(100∶0、50∶1、25∶1、10∶1、5∶1、3∶1、1∶1、0∶100)梯度洗脱,收集、浓缩后依据TLC检测合并得到11个流分。E8-6经过二氯甲烷-甲醇重结晶后得到化合物2(435.6 mg)。E8-9经开放ODS柱色谱,水-甲醇(100∶0~0∶100)梯度洗脱后分为6个流分,E8-9-5经Sephadex LH-20柱色谱(二氯甲烷-甲醇 = 1∶1)和制备高效液相分离(甲醇-水-58∶42,体积流量3 mL/min,检测波长210、236 nm)得到化合物9(15.6 mg)。E8-10样品经Sephadex LH-20柱色谱(二氯甲烷-甲醇1∶1)进行分离,得到的E8-10-2经开放ODS柱色谱,水-甲醇(100∶0~0∶100)梯度洗脱后,得到的E8-10-2-5流分,经正相硅胶柱色谱,用环己烷-醋酸乙酯(100∶0、50∶1、25∶1、10∶1、5∶1、3∶1、1∶1、0∶100)梯度洗脱后,经制备高效液相分离(甲醇-水35∶65,体积流量3 mL/min,检测波长205、228 nm)得到化合物1(2.5 mg)。E8-5经开放ODS柱色谱,水-甲醇(100∶0~0∶100)梯度洗脱后,经Sephadex LH-20柱色谱(二氯甲烷-甲醇1∶1)和制备高效液相分离得到化合物3(23.6 mg)、4(2.6 mg)、5(66.0 mg)、7(2.0 mg)、8(2.5 mg)和10(8.8 mg)。
3 结构鉴定
1H-NMR (600 MHz,DMSO-6) 谱中(表1),在低场区显示3个烯烃质子信号H6.90 (1H, dd,= 10.0, 4.5 Hz, H-3), 5.94 (1H, d,= 10.0 Hz, H-2), 5.68 (1H, d,= 2.0 Hz, H-6);在高场区显示有1个甲氧基质子信号H3.30 (3H, s);3个甲基质子信号H1.75 (3H, s, H-21), 1.41 (3H, s, H-28) , 1.32 (3H, s, H-19)。13C-NMR (150 MHz, DMSO-6) 谱中提示29个碳信号,其中包括1个酮羰基碳信号C202.3 (C-1),3个酯羰基碳信号C172.9 (C-15), 171.9 (C-18), 170.9 (C-26);2组双键碳信号C142.7 (C-3), 135.5 (C-6), 131.6 (C-5), 128.5 (C-2);7个连氧碳信号C83.7 (C-13), 82.2 (C-20), 81.4 (C-14), 77.3 (C-17), 76.1 (C-22), 75.7 (C-4), 67.5 (C-7) 以及1个甲氧基碳信号C56.1。HSQC谱图(表1)将直接相连的碳氢信号进行归属,通过比对发现该化合物的核磁数据与3-hydroxy-2,3-dihydro-4, 7-didehydroneophysalin B数据接近[2],不同之处在于A、B环上取代基类型。

表1 化合物1的氢谱(600 MHz)、碳谱(150 MHz)数据归属
1H-1H COSY谱中(图2),给出A、B环上氢偶合关系。H-2/H-3/H-4依次相关,H-6/H-7/H-8/H-9依次相关,H-7/7-OH相关。在HMBC谱(图2)中,可以观察到如下远程相关信号:H-19 (H1.32)与C-1 (C202.3)、C-5 (C131.6)、C-10 (C51.6)、C-9 (C37.0)相关,从而确定H1.32处甲基信号为H-19信号;H-2 (H5.94)/C-1 (C202.3)、C-4 (C75.7)、C-10 (C51.6) 以及H-3 (H6.90)/C-1 (C202.3)、C-5 (C131.6)、C-4 (C75.7)确定与1位酮羰基共轭烯键存在;H-6 (H5.68)与C-4 (C75.7)、C-10 (C51.6) 相关确定另一双键取代位置;7-OH (H4.61)/C-6 (C135.5)、C-7 (C67.5)确定H4.61为羟基氢信号并确定其取代在C-7;-OCH3(H3.30)与C-4 (C75.7) 相关确定甲氧基取代于C-4。

图2 化合物1中主要1H-1H COSY和HMBC相关信号
在NOESY谱中(图3),H-4 (H4.14)与H-7 (H4.45)相关,H-19 (H1.32)与4-OCH3(H3.30)相关,提示H-19和4-OCH3是β构型,H-4 (H4.14)与H-7 (H4.45)是α构型,故推测7-OH为β构型,从而确定化合物1 A、B环的相对构型。通过X-ray单晶衍射,最终鉴定该化合物的绝对构型为(4β,7β,14α,16β,22α,25)-(16,24-cyclo-13,14-secoer gosta-2,5-diene-15,18,26-trioicacid,14,17:14,27-diepoxy-7, 13,20,22-tetrahydroxy-1-oxo--lactone--lactone(图4),经Sci-Finder检索,为未见报道的新化合物,命名为4β-methoxy-7β-hydroxyneophysalin B,中文俗名酸浆苦素XIII。
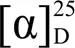

图3 化合物1中主要NOESY相关信号
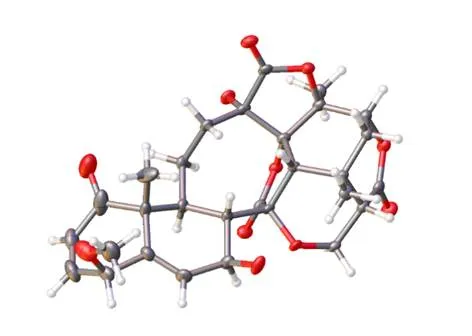
图4 化合物1的X-单晶衍射
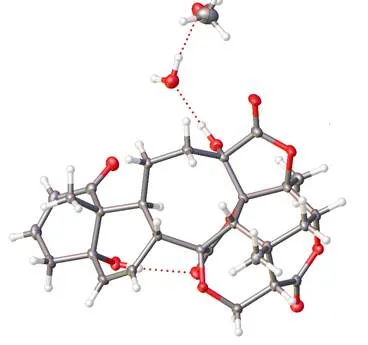
图5 化合物2的X-单晶衍射
4 讨论
甾体类(以变形麦角甾类为主)成分是酸浆中的主要特征性及活性成分,课题组前期曾发现此类成分具有显著的抗肿瘤活性[25-27]。本实验从酸浆全草醋酸乙酯部分分离得到10个甾体类成分,其中化合物1为新化合物,化合物3~10为首次从该属植物中分离得到,为进一步的活性评价奠定了物质基础,同时也为阐明酸浆的药效物质基础提供依据,对于酸浆的合理开发与应用具有一定的指导意义。
利益冲突 所有作者均声明不存在利益冲突
[1] Li A L, Chen B J, Li G H,.L. var.(Mast.) Makino: An ethnomedical, phytochemical and pharmacological review [J]., 2018, 210: 260-274.
[2] Qiu L, Zhao F, Jiang Z H,. Steroids and flavonoids fromvar.and their inhibitory effects on nitric oxide production [J]., 2008, 71(4): 642-646.
[3] Ma Y M, Han W, Li J,. Physalin B not only inhibits the ubiquitin-proteasome pathway but also induces incomplete autophagic response in human colon cancer cells[J]., 2015, 36(4): 517-527.
[4] Lin Y, Shi R X, Wang X,. Luteolin, a flavonoid with potential for cancer prevention and therapy [J]., 2008, 8(7): 634-646.
[5] 幸福, 蒋建勤. 锦灯笼的化学成分研究 [J]. 药学与临床研究, 2013, 21(4): 344-346.
[6] Itoh T, Tamura T, Matsumoto T. 4-Desmethylsgerols in the seeds of Solanaceae [J]., 1977, 30(3): 425-433.
[7] Chen L X, Xia G Y, Liu Q Y,. Chemical constituents from the calyces ofvar[J]., 2014, 54: 31-35.
[8] Asano N, Kato A, Kizu H,. 1β-amino-2α, 3β, 5β-trihydroxycycloheptane fromvar.[J]., 1996, 42(3): 719-721.
[9] Han H Y, Qiu L, Wang X H,. Physalins A and B inhibit androgen-independent prostate cancer cell growth through activation of cell apoptosis and downregulation of androgen receptor expression [J]., 2011, 34(10): 1584-1588.
[10] Silva M T, Simas S M, Batista T G,. Studies on antimicrobial activity,, ofL. (Solanaceae) fraction and physalin B bringing out the importance of assay determination [J]., 2005, 100(7): 779-782.
[11] Sá M S, de Menezes M N, Krettli A U,. Antimalarial activity of physalins B, D, F, and G [J]., 2011, 74(10): 2269-2272.
[12] Yu Y J, Sun L J, Ma L,. Investigation of the immunosuppressive activity of Physalin H on T lymphocytes [J]., 2010, 10(3): 290-297.
[13] Lin Y S, Chiang H C, Kan W S,. Immunomodulatory activity of various fractions derived fromL. extract [J]., 1992, 20(3/4): 233-243.
[14] Pinto N B, Morais T C, Carvalho K M,. Topical anti-inflammatory potential of Physalin E fromon experimental dermatitis in mice [J]., 2010, 17(10): 740-743.
[15] Chiang H C, Jaw S M, Chen C F,. Antitumor agent, physalin F fromL [J]., 1992, 12(3): 837-843.
[16] Wu S Y, Leu Y L, Chang Y L,. Physalin F induces cell apoptosis in human renal carcinoma cells by targeting NF-kappaB and generating reactive oxygen species [J]., 2012, 7(7): e40727.
[17] Magalhães H I, Veras M L, Torres M R,.andantitumour activity of physalins B and D from[J]., 2006, 58(2): 235-241.
[18] Peng X F, Wu Q, Gao C,. Chemical constituents from the fruit calyx ofvar.[J]., 2015, 24(9): 600-606.
[19] 白学莉. 抱茎苦荬菜的化学成分研究 [J]. 中国当代医药, 2016, 23(17): 4-7.
[20] 尚小雅, 王若兰, 尹素琴, 等. 紫红曲代谢产物中的甾体成分 [J]. 中国中药杂志, 2009, 34(14): 1809-1811.
[21] 贾陆, 郭明明, 李东, 等. 黄秋葵石油醚部位化学成分的研究Ⅱ [J]. 中国中药杂志, 2011, 36(7): 891-895.
[22] Feng M T, Wang T, Liu A H,. PTP1B inhibitory and cytotoxic C-24 epimers of Δ28-24-hydroxy stigmastane-type steroids from the brown algaHolmes [J]., 2018, 146: 25-35.
[23] Wang Y S, Wang L L, Hu Y,. Isolation and identification of two steroid compounds from[J]., 2010, 24(16): 1518-1522.
[24] Wang S Y, Xiang J, Huang X J,. Chemical constituents from(harv.)[J]., 2020, 17(6): e2000182.
[25] Chen L, Xia G, Qiu F,. Physapubescin selectively induces apoptosis in VHL-null renal cell carcinoma cells through down-regulation of HIF-2α and inhibits tumor growth [J]., 2016, 6: 32582.
[26] He H, Zang L H, Feng Y S,. Physalin A induces apoptotic cell death and protective autophagy in HT1080 human fibrosarcoma cells [J]., 2013, 76(5): 880-888.
[27] Sun C P, Qiu C Y, Yuan T,. Antiproliferative and anti-inflammatory withanolides from[J]., 2016, 79(6): 1586-1597.
Studies on the steroids from the whole herb ofvar.
TAN Mao-qiang1, 2, NIU Zheng1, 2, ZHANG Min1, 2, GUO Yuan-qiang1, 3, QIU Feng1, 2, DING Li-qin2
1. School of Chinese Materia Medica, Tianjin University of Traditional Chinese Medicine, Tianjin 301617, China 2. State Key Laboratory of Component-based Chinese Medicine, Tianjin University of Traditional Chinese Medicine, Tianjin 301617, China 3.College of Pharmacy, Nankai University, Tianjin 300350, China
To study the chemical constituents fromL. var.(Mast.) Makino.The compounds were isolated and purified by comprehensive column chromatography and preparative RP-HPLC. Their structures were elucidated by physicochemical properties and spectral analyses.10 compounds were obtained and identified as 4β-methoxy-7β-hydroxyneophysalin B (1), physalin P (2), 7-oxo-β-sitosterol (3), 7β-hydroxysitosterol (4), 3β-hydroxystigmasta- 5,22-dien-7-one (5), stigmast-5,22-dien-3β,7β-diol (6), (24)-5,28-stigmastadiene-3β,24-diol-7-one (7), (24)-5,28-stigmastadiene- 3β,24-diol-7-one (8), 3β-hydroxy-cholest-5-en-7-one (9), sargassuol A (10).Compound 1 was a new compound. Compounds 3—10 were isolated from thegenus for the first time.
whole plant ofL. var.(Mast.) Makino; 4β-methoxy-7β-hydroxyneophysalin B; physalin P ; 7-oxo-β-sitosterol; structural identification; steroids
R284.1
A
0253 - 2670(2021)17 - 5203 - 07
10.7501/j.issn.0253-2670.2021.17.011
2021-08-06
国家自然科学基金重点项目(82030116),国家自然科学基金面上项目(21472138)
谭茂强(1996—),男,硕士研究生,主要研究方向为天然药物化学。E-mail: 1316042069@qq.com
邱 峰(1967—),男,沈阳药科大学52期药学日语专业校友,博士研究生,教授,博/硕士生导师,研究方向为中药及天然产物药效物质基础。于1996年日本北海道药科大学博士毕业后,在沈阳药科大学从事博士后工作并留校,曾任天然药物化学系主任,校学位委员会委员、天然药物化学学科主席,教育部重点实验室副主任等。入选教育部长江学者特聘教授,国家高层次人才特殊支持计划领军人才和国家百千万人才工程,科技部重点领域创新团队带头人,兼任第七、八届国务院学位委员会中药学科评议组成员,世界中医药学会联合会中药化学专业委员会副会长,全国中医药高等教育学会中药教育研究会副理事长,教育部高等学校中药学类专业教育指导委员会委员,国家自然科学基金医学科学部中药学学科组会评专家等。Tel: 022-59596223 E-mail: fengqiu20070118@163.com
丁丽琴(1983—),女,博士研究生,副研究员,硕士生导师,研究方向为中药及天然产物药效物质基础的研究。Tel: 15522086884 E-mail: ruby70303@163.com
[责任编辑 时圣明]
