TNF-α抑制剂治疗强直性脊柱炎疗效及安全性的Meta分析
2021-09-03王莉民蒲彦川
王莉民,蒲彦川
(武威市人民医院,甘肃 武威 733000)
强直性脊柱炎(ankylosing spondylitis,AS)是常见的自身免疫性疾病中的一种,最常累及中轴关节,基本病变是附着点炎[1]。临床上主要以腰背部或骶髂部疼痛为特征,随病情进展,患者疼痛加重,活动逐步受限,严重影响患者的生活质量[2]。强直性脊柱炎的关节外表现也较常见,包括外周关节炎(25%~50%)、葡萄膜炎(25%~40%)、炎症性肠病(26%)[3]。脊柱关节病变很少直接引起死亡,而严重的关节外脏器损害可造成患者死亡[4]。
目前临床上AS 治疗的一线药物仍是非甾体抗炎药(NSAIDs),改善病情的抗风湿药物(DMARDs)包括柳氮磺吡啶、甲氨蝶呤、来氟米特等被广泛用于AS 的治疗。但DMARDs 治疗AS 的疗效欠佳,对于AS 关节外表现缺乏肯定的支持证据。研究表明肿瘤坏死因子α(TNF-α)抑制剂可明显改善AS患者的疼痛及生活质量等[5-6]。但是国内尚未有研究系统报道各TNF-α抑制剂对于AS 患者的有效性及安全性的Meta分析。因此,我们对TNF-α抑制剂的疗效及安全性进行评价及Meta分析,以供临床医生参考。
1 资料与方法
1.1 纳入与排除标准
1.1.1 研究类型
随机对照试验。
1.1.2 研究对象
纳入的AS 患者均符合1984 年修订的纽约AS诊断标准[7],性别不限。对在使用TNF-α 疗程中停药的患者,则不被纳入。
1.1.3 干预措施
TNF-α抑制剂与安慰剂对照或同一TNF-α抑制剂不同剂量对照。
1.1.4 结局指标
疗效评价指标:①主要指标:治疗终点时达到ASAS20 改善的例数;②次要指标:治疗终点时达到ASAS40/50/70 改善的例数,Bath 强直性脊柱炎活动指数(BASDAI),Bath 强直性脊柱炎功能指数(BASFI),血沉(ESR)、C 反应蛋白(CRP)的水平。安全性评价指标包括:过敏、感染等。
1.2 检索策略
1.2.1 检索范围
Cochrane library,Pubmed,EMbase,中国科技期刊全文数据库,中国期刊全文数据库,中国生物医学文献数据库,万方数据库。检索语言限定为中文和英文。
1.2.2 检索词
检索采用主题词与自由词结合的方式进行。简单检索用布尔逻辑运算连接检索词,高级检索遵循Cochrane 协作网出版的Handbook 提供的随机对照试验检索策略。中文检索词:依那西普、益赛普、英夫利昔单抗、阿达木单抗、戈利木单抗、赛妥珠单抗、TNFα抑制剂、强直性脊柱炎。英文检索词:Anti-TNF-alpha agents、Adalimumab、Etanercept、Infliximab、golimumab、ankylosing spondylitis。对检索到的文献的参考文献进行人工检索。
1.3 资料提取
由两名评价员独立提取纳入研究资料,包括试验设计期刊名称、作者、出版日期、发表国家、患者平均年龄、病程、干预措施、合并用药、疗效及安全性指标等,评价员对结果进行交叉核对,如遇分歧通过讨论或交由第三人解决。
1.4 方法学质量评价
两名评价员独立采用Cochrane 协作组提供的风险偏倚评估工具(The Cochrnae Collaboration’s tool for assessing rsk of bias)评价纳入试验的方法学质量。主要包括6 个项目:①是否描述随机方法;②是否分配隐藏及是否充分;③有无盲法,盲法实施对象具体为受试者,医务人员或结局测量者;④是否描述退出及失访情况;⑤是否有选择性报道结局指标;⑥是否存在其他可能影响试验质量的因素。
1.5 统计学分析
采用Cochrane 协作网提供的RevMan 5.0 统计软件进行Meta分析。计量资料采用加权均数差(WMD)或标准化均数差(SMD),各效应量均以95%可信区间表示。采用卡方检验判断各研究间的异质性,当组内各研究间有统计学和临床同质性时(P≥0.05,I2≤50%),采用固定效应模型,若存在统计学异质性时(P<0.05,I2>50%)时,分析异质性来源,确定是否能采用随机效应模型。
2 结果
2.1 检索结果
初检文献共3539 篇,其中PubMed 395 篇、EMbase 1171 篇、Cochrane library468 篇、中国科技期刊全文数据库289 篇、中国生物医学文献数据库157 篇、中国期刊全文数据库179 篇、万方数据库880 篇。通过ENDNOTE 自动去重(554 篇)后获得2985 篇,通过阅读题目和摘要排除2878 篇,通过仔细阅读全文排除92 篇,最终纳入15 篇文献。检索流程图如图1 所示。

图1 检索流程图
2.2 纳入研究基本情况
最终纳入15 篇文献,共计17 个RCT,共2499例患者。有8 个RCT 对比的是依那西普与安慰剂相比对AS 患者的疗效与安全性,4 个RCT 是戈利木单抗与安慰剂对比,2 个RCT 是英夫利昔单抗与安慰剂对比,1 个RCT 是阿达木单抗与安慰剂对比,2 个RCT 是益赛普与安慰剂对比。基本情况见表1。

2.3 纳入研究的方法学质量(见表2)

表2 纳入研究的方法学质量
2.4 Meta分析结果
2.4.1 药物疗效评价结果
(1)ASAS20 13 个研究报道了TNF-α抑制剂和安慰剂治疗达到ASAS20 改善的例数(P=0.01,I2=52%),采用随机效应模型合并效应量,结果显示两组差异有统计学意义[OR=4.55,95%CI(3.40,6.10)](如图2所示)。

图2 达到ASAS20 改善的例数
(2)ASAS40 7 个研究报道了TNF-α抑制剂和安慰剂治疗达到ASAS40 改善的例数,各研究间无统计学异质性(P=0.40,I2=4%),采用固定效应模型合并效应量,结果显示两组差异有统计学意义[OR=6.92,95%CI(5.00,9.59)](如图3 所示)。

图3 达到ASAS40 改善的例数
(3)ASAS50 4 个研究报道了TNF-α抑制剂和安慰剂治疗达到ASAS50 改善的例数,各研究间无统计学异质性(P=0.43,I2=0%),采用固定效应模型合并效应量,结果显示两组差异有统计学意义[OR=7.52,95%CI(4.25,13.29)](如图4 所示)。
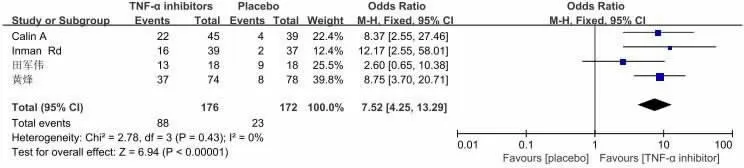
图4 达到ASAS50 改善的例数
(4)BASDAI50 8 个研究报道了TNF-α抑制剂和安慰剂治疗终点BASDAI50 改善的例数,各研究间无统计学异质性(P=0.11,I2=41%),故采用固定效应模型合并效应量,结果显示两组差异有统计学意义[OR=3.83,95%CI(3.01,4.88)](如图5 所示)。

图5 达到BASDAI50%改善的例数
(5)红细胞沉降率6 个研究报道了TNF-α抑制剂和安慰剂治疗终点红细胞沉降率的差异,各研究间无统计学异质性(P=0.17,I2=35%),故采用固定效应模型合并效应量,结果显示两组差异有统计学意义[OR=-7.59,95%CI(-9.54,-5.63)](如图6 所示)。
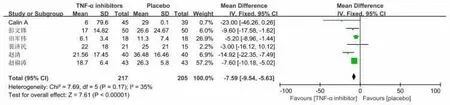
图6 TNF-α抑制剂与安慰剂比较ESR 的差异
(6)C 反应蛋白5 个研究报道了TNF-α抑制剂和安慰剂治疗终点C-反应蛋白的差异(P=0.002,I2=76%),故采用随机效应模型合并效应量,结果显示两组差异有统计学意义[OR=-1.36,95%CI(-1.84,-0.88)](如图7 所示)。
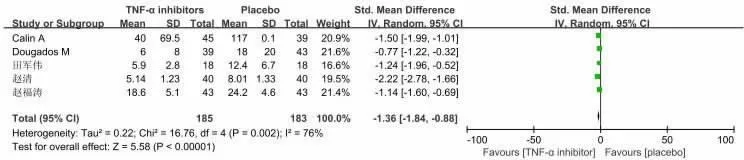
图7 TNF-α抑制剂与安慰剂比较CRP 的差异
2.4.2 药物不良反应评价
(1)注射部位反应9 个研究报道了TNF-α抑制剂组和安慰剂组注射部位的不良反应,其中红肿、瘙痒等较为常见(I2=59%,P=0.01),故采用随机效应模型合并效应量,Meta分析结果显示两组差异有统计学意义[OR=3.01,95%CI(0.96,9.44)](如图8 所示)。

图8 TNF-α抑制剂与安慰剂比较注射部位不良反应发生率的Meta分析
(2)感染8 个研究报道了TNF-α抑制剂组和安慰剂组相比发生感染的差异,其中上呼吸道感染较为常见,各研究间无统计学异质性(I2=0%,P=0.93),故采用固定效应模型合并效应量,Meta分析结果显示两组差异有统计学意义[OR=1.45,95%CI(1.10,1.90)](如图9 所示)。
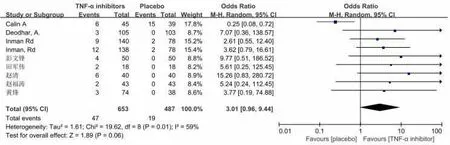
图9 TNF-α抑制剂与安慰剂比较感染发生率的Meta分析
3 讨论
强直性脊柱炎(AS)是以炎性腰背痛为主要特征的自身免疫性疾病。如不经及时治疗,患者活动将受限,最终丧失劳动能力,甚至自理能力。因此,早期诊断和有效的治疗能减轻强直性脊柱炎患者的疼痛及家庭负担。2016 年ASAS-EULAR[23]对于高疾病活动度的AS 患者推荐使用生物制剂。肿瘤坏死因子α(TNF-α)是由单核-巨噬细胞产生,具有调节炎症、免疫反应等的多重效应细胞因子,参与骨细胞的破骨、成纤维细胞的增生等过程[24],因此在AS 患者的发病机制中起重要作用。本研究旨在系统评价目前常用的TNF-α抑制剂对AS 患者的疗效及安全性。
本研究共纳入17 个RCT,共2499 例患者,比较了TNF-α抑制剂与安慰剂相比治疗强直性脊柱炎患者的有效性和安全性,纳入研究所用TNF-α抑制剂包含依那西普、阿达木单抗、戈利木单抗、英夫利昔单抗和益赛普。结果表明TNF-α抑制剂与安慰剂相比可显著改善强直性脊柱炎患者的疼痛、功能及炎性指标。纳入研究报道的较为常见的不良反应包括注射部位不良反应、感染等,所有纳入研究均未报道发生严重不良反应事件,如:严重感染、肿瘤、结核等,但以上未报道的严重不良反应可能与随访病程较短有关。因此,提示临床医生应在使用TNF-α抑制剂之前进行结核的筛选,并对于免疫力低下,存在感染的患者应谨慎使用。
本系统评价共纳入17 个RCT,但纳入研究的质量差异较大。其中6 篇文献未提及具体的随机方法,8 篇文献未提及是否分配隐藏,2 篇文献观察终点时间较短,分别为6 周和8 周。因此,可能造成选择性偏倚,并导致临床异质性和结果的偏倚。此外,纳入的17 个RCT 中,有8 个RCT 对比的是依那西普与安慰剂相比对AS 患者的疗效与安全性,4 个RCT 是戈利木单抗与安慰剂对比,2 个RCT 是英夫利昔单抗与安慰剂对比,1 个RCT 是阿达木单抗与安慰剂对比,2 个RCT 是益赛普与安慰剂对比。因此要得到更可靠的证据,尚需除依那西普外其他类型的TNF-α抑制剂多中心、大样本的临床试验。
综上所述,TNF-α抑制剂能显著提高治疗有效率,降低红细胞沉降率、C 反应蛋白等炎性指标的水平,且无严重的不良反应发生,对于临床上高疾病活动度的AS 患者可首先考虑。
