负载镍锌氧体木质素基活性炭吸附磺胺噻唑
2021-09-03仇仕杰梁祖雪刘以凡叶晓霞刘明华福州大学环境与资源学院福建福州350108
仇仕杰,梁祖雪,华 洁,刘以凡,叶晓霞,刘明华 (福州大学环境与资源学院,福建 福州 350108)
磺胺类抗生素是一类广谱抗菌药物,作为抑菌剂能够针对由革兰氏阳性和阴性菌引起的细菌感染以及一些由原生动物引发的疟疾,弓形体病等,被广泛应用在医药、畜牧和水产养殖中[1-2].因其具有结构稳定性及环境持久性,容易在各环境介质中长期残留,破坏生态坏境,甚至还可能通过食物链富集作用危害到人体健康[3].因此,控制水体环境中抗生素含量,降低磺胺类抗生素对生态环境和人类健康的影响至关重要.
相比于其他方法,吸附法是现在研究应用较多且比较成熟的物理处理方法,具有操作简单、成本低、对污染物的去除效率普遍较高且在处理过程中不容易产生高毒性的副产物等优点,极具应用前景[4].而活性炭具有丰富的孔隙结构与巨大的比表面积,吸附容量大,且成本低廉技术成熟,因此具备相对优势[5].目前,已经有诸多研究报道了活性炭对于磺胺类抗生素的高效去除并取得良好的效果.Meng等[6]利用棉花壳热解与磷酸原位活化制备生物炭,对磺胺嘧啶(SDZ)的最大吸附量为 86.90mg/g. Wan等[7]以污泥为原料合成了新型磁性活性炭材料,对磺胺甲恶唑(SMX)的吸附容量可达 157.3mg/g.而金属氧化物复合吸附剂也是近年来的发展趋势. Su等[8]研究了铂饰氧化锌纳米管对于磺胺噻唑类药物的吸附,在很大程度上提高了其吸附敏感性.温俊峰等[9]采用原位水热法制备了纳米NiO/沙柳活性炭复合材料,对苯酚的去除率可达 80%以上.金属氧化物复合吸附剂是理想的有机废水处理材料.然而,目前对于磺胺类污染物吸附机理的研究仍不够成熟,利用低成本生物质制备对磺高吸附容量活性炭材料的技术也亟需改善.
本研究采用来源广、成本低的生物质废弃物中的碱木素作为原材料制得负载镍锌氧体的木质素基活性炭(NiZn-DO/LAC),对NiZn-DO/LAC的结构进行表征分析,同时探究了NiZn-DO/LAC对磺胺噻唑(ST)的吸附效果及吸附机理.以期为磺胺类污染物的治理提供新颖的吸附材料和相关的理论技术应用提供新的思路.
1 材料与方法
1.1 化学试剂
绿竹碱木素(福建三明某企业);无水乙醇、盐酸、氢氧化钠、氢氧化钾均为分析纯,购自上海阿拉丁生化科技股份有限公司;六水合硝酸锌、六水合硝酸镍、磺胺噻唑均为分析纯,购自国药集团化学试剂有限公司.实验用水均为超纯水.
1.2 材料合成
1.2.1 LAC的制备 称取10g碱木素溶于50mL超纯水中,反应2h后,用氢氧化钾(1mol/L)以1:1的浸渍比浸渍 8h.再将得到的样品冷冻干燥后,在 800℃管式炉中通入氮气反应2h,升温速率为10℃/min,待样品冷却后取出,干燥研磨即可得到碱木素基活性炭,记为LAC.
1.2.2 NiZn-DO/LAC的制备 取2g LAC与2.908g六水合硝酸镍和 1.894g六水合硝酸锌混合溶解于50mL超纯水,缓慢滴加 1mol/L氢氧化钠至沉淀后转入反应釜,在180℃温度下反应20h,倒出上清液后用无水乙醇和超纯水洗涤,经干燥研磨后即可得负载镍锌氧体的碱木素基活性炭,记为NiZn-DO/LAC,设2组平行实验.
1.3 主要仪器
多点磁力搅拌器(RO 10power3691035,IKA)、紫外可见分光光度计(T6新世纪,北京普析通用仪器有限责任公司)、扫描电镜(SEM,SUPRA 55,德国卡尔蔡司公司)、X射线粉末衍射仪(XRD,X'Pert Pro MPD,荷兰 Philips)、物理吸附仪(BET,Micromeritics ASAP2020HD88,美国Micromeritics公司)、X射线光电子能谱仪(XPS,Thermo Scientific ESCALAB 250X,美国Thermo Fisher Scientific公司)、pH计(PHS-3C,上海仪电科学仪器股份有限公司)、电子天平(XB10200D,上海精科天美贸易有限公司)、Zeta电位分析仪(Nano Brook Omni,美国布鲁克海文仪器公司).
1.4 吸附实验
将1000mg/L磺胺噻唑储备液稀释成50mL不同浓度梯度的溶液,投加 0.01g相应活性炭样品,置于智能恒温培养振荡器中,在室温(25±2)℃ ,pH=(5±0.2)条件下以160r/min的振荡速率振荡12h.反应完毕后,用玻璃注射器取出溶液,然后用 0.22 μm 玻璃纤维过滤器过滤.随后采用紫外分光光度计在吸光度281nm处测定磺胺噻唑剩余浓度,根据公式(1),计算活性炭样品的平衡吸附容量.

式中: Qe为平衡吸附容量,mg/g; Ce为吸附质的初始质量浓度,mg/L; C0为吸附后,吸附质的质量浓度,mg/L; V为溶液的体积,L; X为吸附剂的投加量,g.
1.5 吸附再生实验
称取已达饱和吸附量的NiZn-DO/LAC 0.1g于锥形瓶中,采用50ml NaOH溶液(0.1mol/L)为解吸液,在恒温振动器中重复再生4次,2份为平行实验.每次再生后抽滤、用超纯水洗至中性并干燥,然后重复吸附实验同 1.4.使用 (1)计算每次再生吸附后的吸附容量.
2 结果与讨论
2.1 NiZn-DO/LAC的表征
2.1.1 SEM-Mapping分析 LAC及 NiZn-DO/LAC 5000×和20000×放大倍数的SEM图如图1所示.由图 1(a)可知,原始的碱木素基活性炭表面较为光滑且形成了大量不同尺寸和形状的孔洞,呈现出多孔的结构,且以微孔与介孔为主,这表明KOH活化可以有效地产生孔隙[9],从而使吸附剂存在较大的比表面积,利于吸附过程的进行.KOH活化的主要机理为KOH可以通过氧化还原反应腐蚀碳从而产生孔结构,反应产物H2O与CO2气体还能进一步拓展孔隙[10].而当热解温度超过金属钾的沸点(762℃)时,钾蒸汽会使碳的芳香层膨胀,产生更多孔隙[11].负载镍锌氧化物之后[图 1(b)],活性炭表面粗糙,有部分团聚现象,部分孔隙被负载物堵塞,可能由于活性炭表面被有一层金属的氧化物或氢氧化物包裹[12].整体而言,改性活性炭呈蓬松多孔的立体结构,微孔和介孔仍然保持完整.有利于降低吸附质分子的吸附阻力,加强吸附质在吸附剂表面的传输运动,从而进一步提高材料的吸附性能[13].图2为NiZn-DO/LAC复合材料的Mapping图谱.由Mapping图可知,制备的活性炭复合材料主要由C、O、Ni、Zn四种元素组成.另外,在相关的元素含量表中可得 C、O、Ni和Zn的重量百分比分别为65.92%、27.33%、4.53%和2.21%,且四种元素分布均匀.此外,NiZn-DO/LAC中不含其他元素也表明了本实验制备出了较为纯净的碱木素基活性炭材料.

图1 LAC与NiZn-DO/LAC的SEM图Fig.1 SEM diagrams of LAC and NiZn-DO/LAC

图2 NiZn-DO/LAC的能谱Mapping图Fig.2 mapping images of NiZn-DO/LAC composites
2.1.2 BET分析 活性炭是一种典型的多孔材料,可以采用N2吸-脱附等温曲线对样品的孔隙特征进行更加深入的研究和分析.LAC和 NiZn-DO/LAC的吸附-脱附曲线及孔隙特征如图3(a)和表1所示.根据IUPAC气体吸附等温线的分类标准,由吸附-脱附等温线图所示,LAC与 NiZn-DO/LAC的吸附曲线都符合IV型,具有H4型滞后环[13].表明多孔吸附剂出现了毛细凝聚的现象,且吸附材料是一种典型的介孔结构[14],改性后对材料的结构完整性造成的影响可以忽略不计.样品的孔隙特征数据如表 1所示.LAC的比表面积和总孔容分别为 1197m2/g和0.7298cm3/g,而NiZn-DO/LAC的比表面积和总孔容分别下降至 759.1m2/g与 0.4288cm3/g.分析可知,LAC比NiZn-DO/LAC的比表面积和平均孔容更大,这是由于负载金属氧化物之后会对 LAC的孔道造成一定的堵塞现象,占用了相应的活性位点,从而导致相应的表面积也会有所下降[15].这与SEM所观察到现象也相吻合.

表1 LAC与NiZn-DO/LAC的孔隙特征Table 1 Porosity characteristics of LAC and NiZn-DO/LAC

图3 吸附材料的BET与XRD分析图谱Fig.3 BET and XRD of adsorbing material
2.1.3 XRD分析 LAC和NiZn-DO/LAC的XRD图谱如图3(b)所示.NiZn-DO/LAC的XRD图谱分别在 2θ为 31.77°、34.42°、36.26°、47.54°、56.60°、62.86°、67.95°和 76.97°等处出现了明显的衍射峰,分别对应 ZnO(PDF#65-3411)的(100)、(002)、(101)、(102)、(110)、(103)、(112)、(202)晶面[16].另外,在 2θ为 19.26°、33.06°、38.54°、52.10°、59.05°、62.73°、和 69.35°等处也出现了明显的衍射峰,分别对应Ni(OH)2(PDF#14-0117)的(001)、(100)、(101)、(102)、(110)、(103)、(111)、(200)晶面[17].这表明金属的氧化物或者氢氧化物已经成功负载在了活性炭表面,而对于制备出的碱木素基活性炭(LAC)而言,LAC的XRD谱图的噪声较大,LAC材料基本为无定形的形式存在.
2.2 NiZn-DO/LAC对ST的吸附行为分析
2.2.1 吸附动力学 吸附动力学研究主要是通过动力学模型对数据进行拟合,描述吸附剂吸附溶质的速率快慢,从而对其吸附机理进行深入探讨.为了构建ST在NiZn-DO/LAC上的吸附动力学模型,本文监测了吸附容量随时间的变化(图 4(a)),并称取若干份0.01g的活性炭吸附剂,分别加入到质量浓度为60mg/L、体积为50mL的ST溶液平行样品瓶中.在25℃,150r/min条件下,置于恒温培养振荡器上振荡反应.间隔一定的时间对样品进行取样分析,测定样品中残余ST的质量浓度.通过准一级动力学方程、准二级动力学方程和颗粒内扩散模型对数据进行拟合(图 4(b-d)).其中,Lagergren准一级动力学方程公式如下:

式中:t为吸附时间,min;qe为平衡吸附量,mg/g;qt为吸附时间为t时的吸附量,mg/g;qe,c为计算得到的平衡吸附量,mg/g;k1为准一级吸附速率常数,min-1.
通过以 ln(qe-qt)为纵坐标,t为横坐标作图所得拟合直线的斜率和截距可计算求出 k1和 qe,c值.Lagergren准二级动力学方程的公式如下:
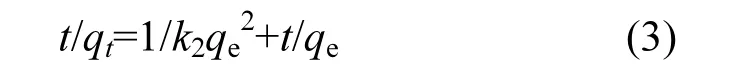
式中:t为吸附时间,min;qe为平衡吸附量,mg/g;qt为吸附时间为 t时的吸附量,mg/g;k2为准二级吸附速率常数,min-1.
通过以 t/qt为纵坐标,t为横坐标作图所得拟合直线的斜率和截距可计算求出 k2值.颗粒内扩散模型认为吸附过程主要由膜扩散和内扩散这两个阶段控制,其方程如下:

式中:t为吸附时间,min;qt为吸附时间为t时的吸附量,mg/g;Kp为颗粒内扩散速率常数,mg/(g·min1/2);B为与界面层厚度相关的系数.
通过以 qt为纵坐标,t1/2为横坐标作图所得拟合直线的斜率和截距可计算出b和Kp值.
如图4(a)所示,NiZn-DO/LAC在吸附ST的过程中,在300min左右可以达到吸附平衡,平衡吸附容量约为264.6mg/g,优于其他报道中的吸附剂(如表3所示).此外由线性拟合结果(表 2)可知,准一级动力学和准二级动力学方程都适用于材料对ST的吸附动力学过程.这意味着NiZn-DO/LAC与ST之间的吸附过程既存在物理吸附,也发生了化学吸附过程[18].颗粒内扩散模型结果如图 4(d)所示,排除吸附初期物质传递的差异,可以认为 qt-t1/2线性图通过原点,因此可以认为试验吸附过程符合颗粒内扩散模型,颗粒内扩散是控制吸附过程的限速步骤.吸附过程可以明确的分为 3个线性区域.第一阶段是边界层扩散阶段,ST从水溶液自由扩散到活性炭表面,吸附能力迅速提高.第二阶段是空隙扩散阶段,污染物继续扩散到活性炭的吸附位点,但在此阶段线性斜率下降,吸附能力缓慢增加,这主要受颗粒内扩散控制.第三阶段是吸附反应阶段.该线的斜率趋于水平,并且吸附容量保持恒定,这意味着在该阶段已经达到吸附平衡[19].

图4 NiZn-DO/LAC对ST的吸附动力学拟合曲线Fig.4 Adsorption kinetics of ST on NiZn-DO/LAC

表2 NiZn-DO/LAC对ST的吸附动力学参数Table 2 Adsorption kinetics parameters for ST adsorption on NiZn-DO/LAC
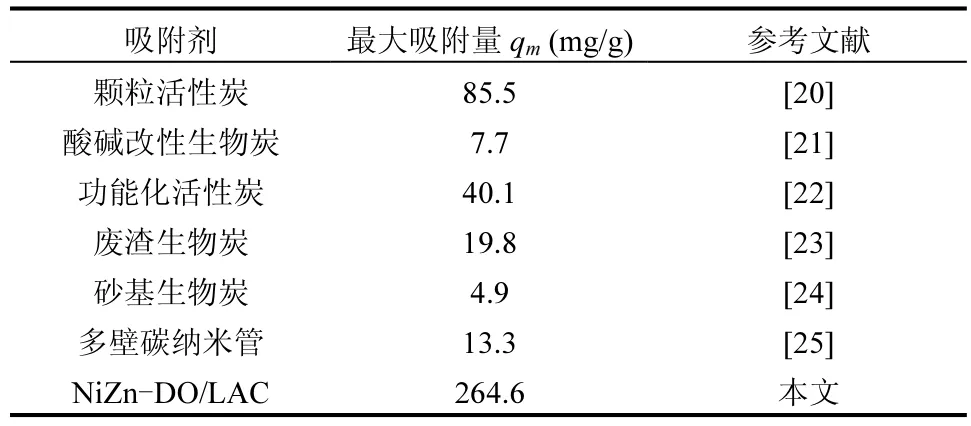
表3 不同吸附剂对于ST的最大吸附量Table 3 Maximum adsorption capacity for ST with different forms of adsorbent
为了进一步确认ST在NiZn-DO/LAC上已经被成功吸附,本文采用 XPS对吸附前后的样品进行表征.如图 5所示,NiZn-DO/LAC在吸附 ST后,398eV处的N1s及164eV处的S2p出现了明显的峰, 证明ST已经成功的被吸附到了NiZn-DO/LAC上.

图5 NiZn-DO/LAC吸附ST前后的XPS全谱Fig.5 XPS survey scans of NiZn-DO/LAC before and after ST adsorption
2.2.2 吸附等温线与吸附热力学 在pH值为5,转速 150r/min条件下,设置恒温振荡器温度分别为298.15,308.15和318.15K,对质量浓度分别为10,20,40,60,80,100,120,140,160,180和200mg/L的ST溶液,分别投加吸附剂0.01g,进行吸附平衡实验,吸附时间400min,结果如图 6所示.对 ST吸附数据使用Langmuir和Freundlich模型进行拟合, Langmuir吸附等温线模型可以表征吸附初始浓度对吸附过程的影响.其方程式为:

式中:Ce为平衡浓度,mg/L;qe为单位质量吸附剂的平衡吸附量,mg/g;KL为Langmuir吸附常数,L/mg;qm为单位质量吸附剂表面覆盖单分子层时的最大吸附量,mg/g.
以吸附平衡浓度Ce为横坐标,Ce/qe为纵坐标得到拟合直线斜率和截距,由此求出KL和qm.另一个常用的模型为Freundlich吸附等温线模型,其吸附方程式为:

式中:Kf表示与吸附量有关的常数,mg/g(L/mg)1/n; n表示与吸附强度有关的参数.
以 lnCe为横坐标,lnqe为纵坐标,可以由拟合直线的斜率和截距算出 Kf和 n.如表 4所示,与Langmuir模型(R2= 0.932、0.912、0.906)相比,Freundlich模型(R2= 0.990、0.987、0.983)的相关系数值较高,表明ST在NiZn-DO/LAC上的吸附更符合Freundlich模型,也可以推断出NiZn-DO/LAC对ST的吸附属于多分子层吸附[26].同时,NiZn-DO/LAC对ST的吸附过程中Kf值均随温度升高而降低,说明低温有助于吸附.此外,n>1表明NiZn-DO/LAC对ST的吸附过程较容易进行[27].如图6所示,相比较于Langmuir模型,NiZn-DO/LAC对ST的吸附过程在Freundlich模型下可以更好地进行拟合,且其对污染物的平衡吸附容量随着温度的升高而降低,表明升温不利于吸附地进行.这也与上述拟合数据分析出的结果一致.

表4 NiZn-DO/LAC对ST的Langmuir及Freundlich吸附拟合参数Table 4 The Langmuir and Freundlich adsorption isotherm equations for ST by NiZn-DO/LAC

图6 NiZn-DO/LAC对ST的吸附等温线Fig.6 Adsorption isotherms of ST on NiZn-DO/LAC
为了进一步探讨吸附过程的热力学反应,通过不同温度下的吸附等温线获得了相关的热力学参数,如吉布斯自由能(ΔG),焓(ΔH)和熵(ΔS)和范霍夫曲线(图7).相关计算公式如下:

图7 ST的范霍夫曲线Fig.7 Van’t Hoff plots with ST
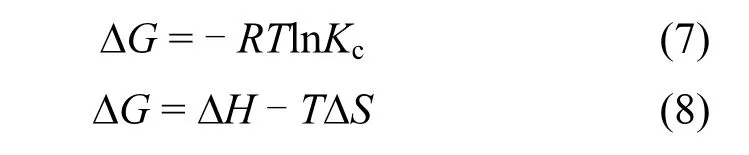
式中: Kc为吸附平衡常数,通常带入Langmuir的KL进行计算,L/mg;R为理想气体常数,8.314J/mol/K;ΔG 为吉布斯自由能,kJ/mol;ΔH 为焓,kJ/mol;ΔS为熵,J/mol/K.

通过以ln Kc为纵坐标,1/T为横坐标,以拟合直线的截距和斜率,可以求得ΔH和ΔS.ΔG均小于0,说明NiZn-DO/LAC对ST的吸附是可以自发进行的,吸附质容易被吸附到吸附剂表面,且温度越高,ΔG值越小,这表明温度升高使得自由能减小,反应速率因此而加快[28].ΔH<0,则说明该吸附过程为放热反应,低温有利于 NiZn-DO/LAC对 ST的吸附.此外,负ΔS值表明NiZn-DO/LAC对ST的吸附过程中发生了熵的下降[29].
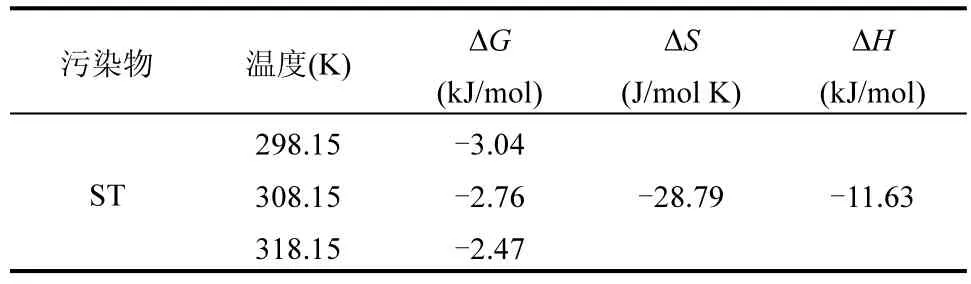
表5 NiZn-DO/LAC对ST的吸附热力学参数Table 5 The thermodynamic parameters on the adsorption of ST by NiZn-DO/LAC
2.2.3 NiZn-DO/LAC的可重复利用性 可重复使用性是评估吸附材料性能的重要标准之一,这对于吸附材料在实际应用中的效果具有十分重要的意义.绝大部分活性炭吸附剂,主要选用氢氧化钠(NaOH)作为解吸剂[30].结合XRD分析(图8(b)),吸附前后NiZn-DO/LAC材料具有良好的化学稳定性,pH值并不会影响其晶型结构和金属化合物的形态[31],因此本实验选用NaOH作为解吸剂.如图8(a)所示,吸附饱和的NiZn-DO/LAC材料经过4次循环再生之后,解析率相应从93.20%降低至79.43%.这意味着合成的NiZn-DO/LAC具有比较好的可重复使用性,能够连续有效的对污染物进行去除,从而显著的降低使用成本.

图8 NiZn-DO/LAC对ST的可重复利用性与吸附前后XRD图谱Fig.8 XRD pattern and Reusability of NiZn-DO/LAC before and after ST adsorption
2.3 NiZn-DO/LAC对ST的吸附机理研究
2.3.1 静电作用 静电相互作用通常被认为是解释带电污染物吸附行为的重要机制.为了探究污染物ST与NiZn-DO/LAC之间的静电相互作用,考察不同pH值(pH = 1~12)条件下的吸附情况.如图9(a)所示, ST的去除效率在pH = 1~5时随着pH值的增大而增大,并在 pH=5时,吸附效率达到最大值,吸附容量能达到328.2mg/g.ST的去除效率在pH = 5~12时逐渐减小.特别值得注意的是,当pH>10时,平衡吸附容量开始急剧下降,由此可以推断,过高的 pH值不利于ST的吸附.通过zeta电位(图9(b))分析可知NiZn-DO/LAC吸附剂的等电点 pHpzc=4.43,当溶液的 pH<pHpzc时,吸附剂表面呈正电,而当 pH>pHpzc时,吸附剂NiZn-DO/LAC表面带负电.而ST在水溶液中的存在形态与溶液中的 pH值也密切相关,当pH≤2.2时,ST主要以阳离子的形态存在,当2.2<pH<7.24时,随着溶液pH值的增加,ST的阳离子形态含量的比例逐渐减小,中性分子形态的比例逐渐增加.且当pH=5时,溶液中仍存在一定数量阳离子形态的ST.当pH≥7.24时,主要以阴离子形态存在[32]. ST受pH值的影响主要是因为苯环上的两个官能团(图10)——氨基(-NH2)与磺酸氨(-NH-),pH值低时,氨基处于质子化,pH 值高时,磺酸氨处于去质子化[33].因此,在 pH=5时的高吸附平衡与带负电荷的 NiZn-DO/LAC与带正电荷的 ST分子之间的静电吸引有关.而在较高的pH值下,吸附量的下降可能与静电斥力有关.在强碱性条件下,吸附剂和吸附质表面均带负电荷,且吸附剂维持了良好的晶型结构,具有相当的稳定性,两者之间的静电斥力导致平衡吸附下降.在强酸性条件下,吸附剂晶型遭到破坏,且存在静电斥力的作用,从而导致吸附效果下降.由此可见,静电作用在NiZn-DO/LAC吸附ST的过程中发挥了一定的作用[34].但根据图9所示,平衡吸附容量与Zeta电位值之间不存在线性关系,这一点说明还存在着其他相互作用促进了ST的吸附过程.

图9 pH值对ST在NiZn-DO/LAC上的吸附性能的影响与在不同pH条件下材料的Zeta电位(pH = 1-12)以及在不同pH条件的XRD图谱Fig.9 Effects of pH on the adsorption of ST on NiZn-DO/LAC with the addition of Zeta potentials and XRD pattern of adsorption materials at different pH conditions

图10 ST结构式Fig.10 structural formula of Sulfathiazole
2.3.2 π-π键作用 为了阐明ST在NiZn-DO/LAC界面上的分子相互作用,进一步探讨其吸附机理,进行 XPS分析实验.根据相关的文献,π-π堆积相互作用在吸附含有芳香环污染物方面起着至关重要的作用[35].一般来说,具有C=C双键或芳香环的有机化合物中含有π电子,π电子与碳结构中的π电子相互作用,形成π-π电子耦合连接[36].此外,由于制备原料中的木质素属于芳香族化合物又含有大量的C元素,存在大量的苯环可以与吸附质之间的苯环产生相互作用,其中涉及的 π-π堆积相互作用可能是一种存在的吸附机理,如图 11(b)所示,NiZn-DO/LAC在吸附ST前的C1s谱图主要由和 π-π 基团(291.5eV)组成.吸附后一方面 C-C/C=C的比例从 50.25%上升至 71.94%,这些主要来源于NiZn-DO/LAC 表面吸附的 ST.另一方面,吸附后可以看到,π-π基团的比例从5.53%下降到4.32%,说明π-π基团是ST吸附过程中的有效吸附位点.因此可以合理地假设 ST与 NiZn-DO/LAC之间存在 π-π相互作用,促进ST的吸附.
2.3.3 络合作用 金属离子与碳基底结合主要是通过复合材料上的官能团(羟基、羧基或者其他基团)的方式相结合,此外这些官能团还可以通过螯合或离子交换与各种金属结合[37].而水体中磺胺类抗生素与金属离子共存时,在某些条件下易产生络合形成抗生素—金属离子络合物,会对磺胺类抗生素的吸附去除产生显著影响.NiZn-DO/LAC中同时含有锌和镍的氧化物,这两部分可能表现出表面对ST吸附的络合作用,金属离子与 ST之间能形成Me(SMR-)+式[38].为了进一步确定这一点,XPS分析的测量扫描显示了锌和镍的特征峰.如图 11(a)和(c)所示,吸附前 Zn元素的结合能为 1020.8,1022.8和1043.9eV,1045.6eV处分别为Zn 2p 3/2和Zn 2p 1/2的特征峰.而吸附后Zn元素的结合能分别为1021.8和 1044.8eV.而在镍的图谱中,特征峰有不同程度的下降.这可能是由于发生了络合作用形成了稳定的抗生素—金属离子络合物.T Sekimoto等[39]的研究也表明,络合作用在磺胺类污染物的吸附过程中发挥了重要的作用.
2.3.4 氢键作用 氢键是在有机污染物的吸附过程中最常见的机理之一.NiZn-DO/LAC表面含有羟基、羧基、内酯基等含氧官能团,这些基团与ST的苯环电子以及-NH2容易形成氢键,增强了其对ST的吸附能力.因此,可推断氢键可能在NiZn-DO/LAC对ST的吸附过程中起着重要作用.如图11(b)所示,C1s谱图中吸附ST之后,=O的含量从25.63%下降到7.91%,而如XPS图谱中高分辨率 O1s图谱所示(图 11(c)),529.90eV处的离子氧()与530.70eV处的双键键合到碳上的氧(C=)都有不同比例的消失或降低,这表明了这些基团可能参与了氢键的形成.

图11 NiZn-DO/LAC吸附ST前后的XPS高分辨图谱Fig.11 High-resolution XPS spectra of NiZn-DO/LAC before and after ST adsorption
2.3.5 疏水作用 活性炭表面通常分布着一定的疏水位点,其表面的石墨层和ST之间可以产生疏水作用.疏水作用也受到很多因素的影响,其中,当活性炭在吸附体系中所带的净电荷密度为零时,即其表面的含氧官能团不发生电离,且ST分子处于中性分子态时,二者之间表现出最强的疏水作用.当二者带 有电荷时,疏水作用会明显受到抑制[40].
3 结论
3.1 以碱木素为原料,通过水热合成法成功制备NiZn-DO/LAC,比表面积为 759.1m2/g,吸附前后XRD图谱表明NiZn-DO/LAC在吸附过程中具有良好的化学稳定性.且当ST初始浓度为 60mg/L、pH值为5、温度为25℃时,投加0.01gNiZn-DO/LAC吸附 300min后,可达到最大吸附容量 328.2mg/g,高于未改性前LAC的吸附容量254.7mg/g.且吸附再生实验表明在循环4次之后,解析率为79.43%,仍可达到较理想的吸附效果.
3.2 NiZn-DO/LAC对 ST的吸附符合 Freundlich等温吸附方程.该吸附过程是自发进行的吸热反应,且吸附过程属于多分子层吸附.而准一级动力学和准二级动力学方程都符合拟合结果,这说明该吸附过程是物理和化学吸附互相作用的结果.
3.3 NiZn-DO/LAC对ST的吸附机理主要为静电作用、π-π堆积作用、络合作用、氢键作用及疏水性作用的协同作用.
