同位素稀释-气相色谱/质谱法测定婴幼儿辅食中四种呋喃类化合物
2021-09-02李凤华郑凤家曹艳平辛成龙
李凤华,郑凤家,曹艳平,李 蔚,王 林,辛成龙
(山东大学预防医学研究院,山东省疾病预防控制中心,山东济南 250014)
呋喃及甲基呋喃(2-甲基呋喃、3-甲基呋喃、2,5-二甲基呋喃)是一类无色、易挥发的小分子化合物,具有麻醉和刺激性,有毒且易燃,吸入后可引起头痛、头晕、恶心、呼吸衰竭[1−2]。国际癌症研究机构研究认为,呋喃对人类具有潜在的致癌性,将呋喃归为2B类致癌物[3−4]。呋喃的检测和评估一直是国内外研究机构关注的热点,美国食品药品监督管理局(US FDA)和欧盟食品安全局(EFSA)等权威机构发现多种食品中存在呋喃[5−8]。呋喃可由抗坏血酸、氨基酸、碳水化合物、不饱和脂肪酸等前体物质产生[9−10],广泛存在于咖啡、罐头等食品中[11−15]。而2-甲基呋喃、3-甲基呋喃、2,5-二甲基呋喃与呋喃性质类似,都可能由食品在热加工过程中产生,且来源与食物中呋喃的形式相同,对人与动物都具有相似的毒性。
到目前为止,甲基呋喃国内研究的较少,有关食品和饮料甚至婴幼儿食品中的含量信息有限。EFSA在2017年风险评估过程中针对食品中呋喃、2-甲基呋喃、3-甲基呋喃、2,5-二甲基呋喃四种呋喃类化合物进行评估,但是只得到了呋喃的分析结果,并未获得其它三种甲基呋喃的数据,专家组经过评估发现,对于婴儿食品,主要的呋喃暴露途径为即食食品,由于这类食品大多经过高温处理和密闭封装,呋喃的含量水平较高[16−18],而婴幼儿的食物比较单一,可能为呋喃及甲基呋喃的高暴露人群。因此需要建立合适的方法,收集更多关于食品中呋喃及甲基呋喃类化合物含量的数据以便进行人体健康风险的暴露评估。
目前针对呋喃的测定研究比较多,应用的方法主要是电化学分析法[19]、顶空气相色谱-质谱法[20−22]和顶空固相微萃取-气质联用法[23−26]。由于呋喃、甲基呋喃分子量小,易挥发,定量容易受到基质干扰,顶空进样是分析此类化合物的最合适的方法。本实验通过优化顶空气相色谱-质谱条件,利用顶空装置将样品中的目标化合物提取出来,消除基质干扰,采用气相色谱分离,质谱定性定量,建立了同时测定婴幼儿辅助食品中四种呋喃类化合物的方法,并应用本方法对市售婴幼儿辅食中的四种呋喃类化合物的含量状况进行了调查,为食品安全风险评估监测研究提供技术支持。
1 材料与方法
1.1 材料与仪器
婴幼儿辅食 按照国家食品安全风险监测标准要求采集市售婴幼儿辅食样品共139份,包括26份饼干,10份米粉,13份蛋糕,75份水果泥,15份肉(鱼)泥,均为定型包装样品;甲醇 色谱纯,德国Merck公司;氯化钠 优级纯,国药集团;试验用水Millipore纯水机制取超纯水;标准品呋喃(100μg/mL)、D4-呋喃(100μg/ mL)、3-甲基呋喃、2,5-二甲基呋喃德国Dr.公司;2-甲基呋喃、D3-3-甲基呋喃、D3-2,5-二甲基呋喃 加拿大TRC公司;D6-2-甲基呋喃 加拿大CDN Isotopes公司。
Thermo Trace1310-ISQ气相色谱-质谱联用仪配有EI源、Triplus三合一(液体、顶空、固相微萃取)自动进样器,美国Thermo公司;Millipore—Q超纯水机 美国Millipore公司;精密移液器 美国Thermo公司;Vortex-Genie2涡旋混匀器 美国Scientific公司;Sartorius CPA225D电子天平 德国Sartorius公司。
1.2 实验方法
1.2.1 样品预处理 饼干和蛋糕样品放入−20℃冷冻2 h,用食品粉碎机粉碎,−20℃密封冷冻保存并尽快测定,其余样品在分析前放入4℃冰箱中冷藏过夜。
1.2.2 标准溶液的配制3种甲基呋喃混合标准储备液的配制:分别称取2-甲基呋喃、3-甲基呋喃、2,5-二甲基呋喃标准品适量,用甲醇溶解并定容,配制成浓度为100μg/mL的混合标准储备液,0~8℃避光保存。
D6-2-甲基呋喃、D3-3-甲基呋喃、D3-2,5-二甲基呋喃混合同位素内标储备液的配制:分别称取标准品适量,用甲醇配制成浓度为100μg/ mL的标准储备液,0~8℃避光保存。
高浓度呋喃及甲基呋喃混合标准使用液的配制:移取呋喃及3种甲基呋喃混合标准储备液适量,置于10 mL容量瓶中,用甲醇稀释至刻度,混匀,配制成1.0μg/mL的4种混合标准使用液,0~8℃避光保存。
低浓度呋喃及甲基呋喃混合标准使用液的配制:移取高浓度混合标准使用液1.0 mL,加入甲醇稀释定容至10.0 mL,配制成浓度为0.1μg/mL的混合标准使用液,0~8℃避光保存。
同位素内标混合溶液的配制:移取D4-呋喃及甲基呋喃混合同位素内标储备液适量,用甲醇稀释并定容至50.0 mL,配制成浓度为1.0μg/mL的同位素内标混合使用液,0~8℃避光保存。
1.2.3 样品测定 迅速称取4℃冷藏过夜的混匀固体样品1.0 g(精确至0.01 g),罐装半固体样品2.50 g(精确至0.01 g)于20 mL顶空瓶中,加入10 mL 20%氯化钠溶液,加入浓度为1.0μg/mL的4种内标混合标准溶液100μL,并立即盖上顶空瓶盖子,混匀,放置到顶空进样装置上,GC/MS自动进样分析,结果以重复性条件下获得的三次独立测定结果的算术平均值计算。
1.2.4 色谱质谱条件
1.2.4.1 顶空条件 顶空孵化室平衡温度60℃,加热时间30 min;进样针温度:70℃。
1.2.4.2 色谱条件 HP-PLOTQ毛细管色谱柱:30 m×0.32 mm(内径)×20μm(膜厚);进样口温度:200℃;程序升温:初温60℃,保持1 min,以10℃/min升至230℃,保持2 min;载气:氦气,流速:1.7 mL/min;分流进样,分流比3:1。
1.2.4.3 质谱条件 离子源:电子轰击(EI)离子源,电子能量70 eV;离子源温度:230℃;传输线温度:280℃;溶剂延迟10 min;检测方式:选择离子(SIM)扫描。保留时间及监测离子参数见表1。
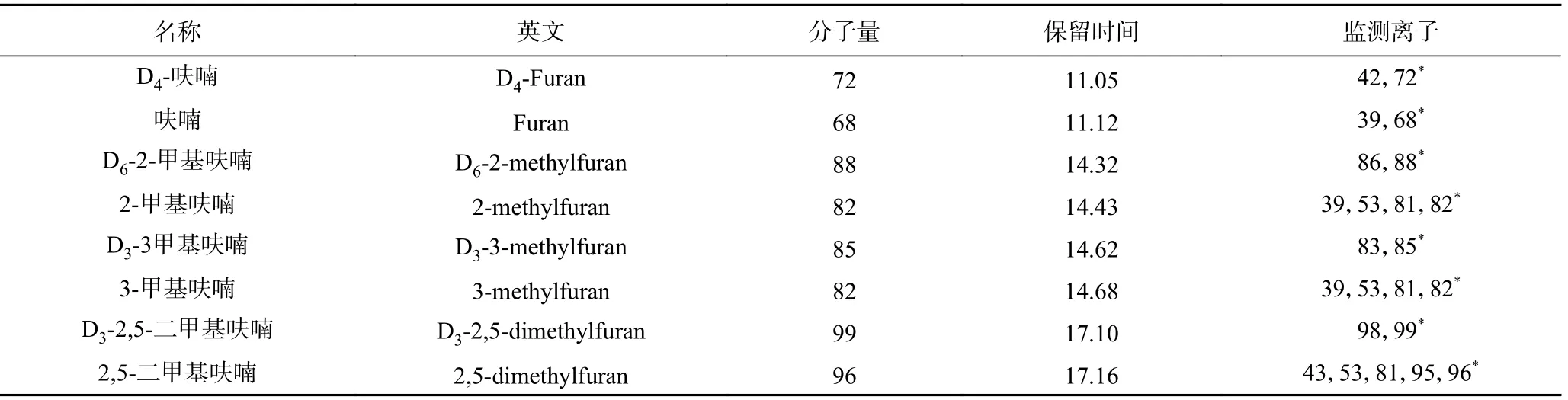
表1 四种呋喃类化合物及同位素内标SIM模式下检测条件Table 1 Selected ion monitoring (SIM)conditions for the determination of furans
1.2.5 方法学考察
1.2.5.1 线性关系、检出限与定量限的考察 取8个20 mL顶空进样瓶,分别加入10 mL 20%氯化钠溶液,1.0μg/mL 4种内标混合应用液100μL,依次加入不同体积的高低浓度的混合标准使用液,制成含1.0、3.0、5.0、10.0、20.0、40.0、100和200 ng的标准系列,GC/MS进样分析,以不同浓度的各目标物的峰面积与其内标峰面积比值对应相应的质量浓度进行线性回归,绘制标准曲线。按照三倍信噪比(3 S/N)计算检出限,10倍信噪比(10 S/N)为定量限,确定四种呋喃类化合物的检出限和定量限。
1.2.5.2 加标回收率、精密度试验 精密称取已知含量不同种类的婴幼儿辅食样品适量,进行回收率和精密度试验,分别添加三个不同质量浓度的混合标准溶液,按照1.2.3项下方法进行前处理和测定,每个浓度平行测定6次,计算其加标回收率和相对标准偏差,以验证该方法的准确性。
1.3 数据处理
采用内标法进行定量,应用仪器配置工作站Xcalibur系统进行数据采集处理,并使用excel 2010进行数据分析。
2 结果与分析
2.1 色谱分离条件的优化
根据检测目标物呋喃及甲基呋喃的特点和色谱柱的性质以及查阅文献,本试验选择了HP-PLOTQ色谱柱。将配制好的浓度为1.0μg/mL的单标溶液按照方法进行全扫描采集,确定8个目标物的定性定量离子,并采用选择离子扫描方式(SIM)分段采集检测不同保留时间的待测物,以提高样品检测的灵敏度并消除部分杂质的干扰。通过优化色谱分离条件,获得最优的色质谱仪器条件。应用已建立的方法,SIM监测模式下四种呋喃及同位素内标物混合标准溶液的总离子流图见图1。
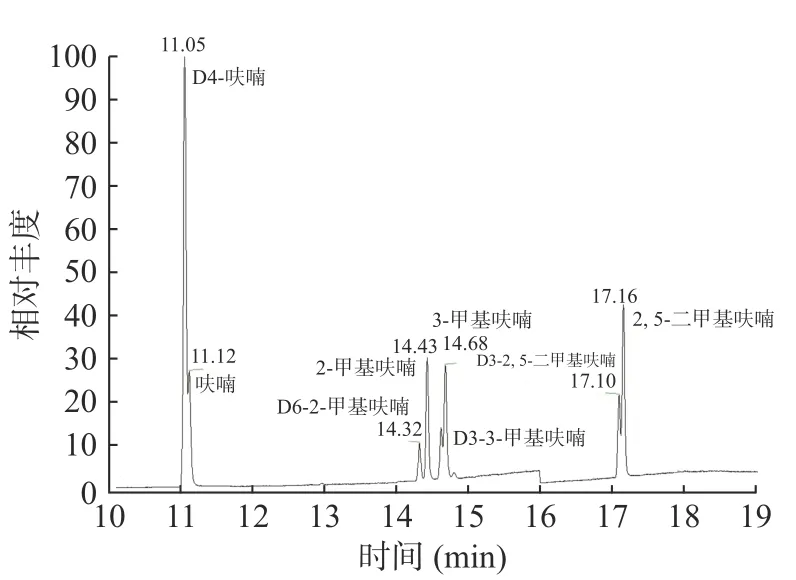
图1 混合标准溶液的总离子流色谱图Fig.1 Total ion chromatogram of mixed standardssolution
2.2 顶空条件的优化
由于顶空孵育平衡温度和时间的选择直接影响样品中四种呋喃类化合物定量的准确性,本试验按照方法将四种呋喃类化合物的标准溶液加入顶空瓶中,使得顶空瓶中四种目标化合物的加入量为100 ng,将顶空瓶密封好后分别在40、50、60、70、80℃的温度下平衡30 min,分析四种目标化合物的峰面积,结果见图2a。结果表明,四种目标化合物在60℃下回收最好,确定选择样品的平衡温度为60℃。
另外将顶空瓶密封好后分别在60℃下平衡15、20、30、40、50 min,分析四种呋喃类化合物的峰面积,发现平衡时间20~50 min,峰面积没有明显的改变,见图2b。因此选择样品的平衡时间为30 min。
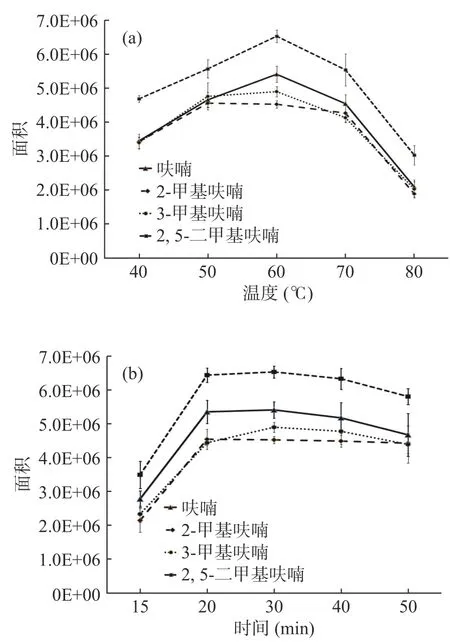
图2 顶空参数的优化Fig.2 Optimization of HS parameters
2.3 无机盐氯化钠浓度的选择
本试验考察了不加氯化钠,加入10%氯化钠和20%氯化钠对各目标物峰面积的影响,发现顶空分析中加入氯化钠,各目标物的峰面积均有成倍的增长,见图3。且线性关系良好,说明加入氯化钠可以促进样品中的目标物进入顶空相,所以本试验确定加入20%氯化钠以提高检测方法的灵敏度。
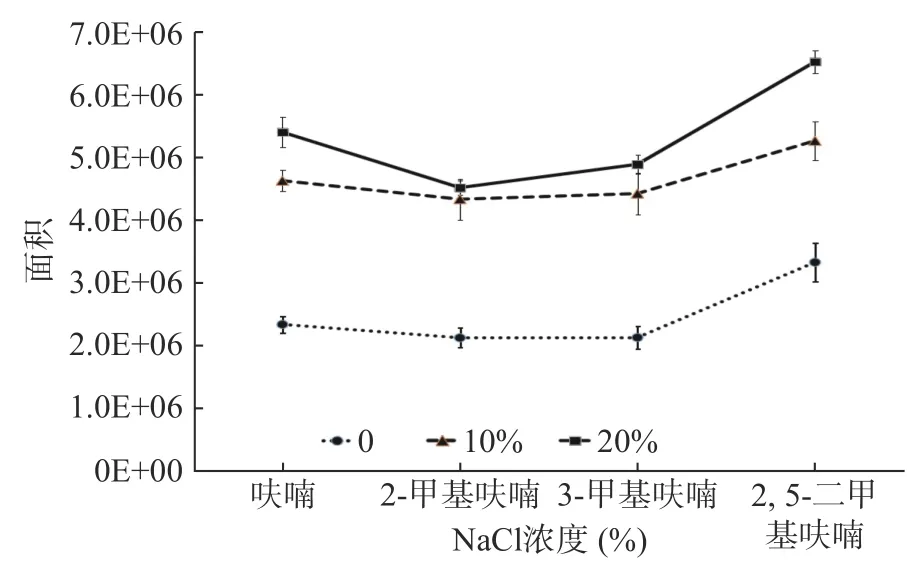
图3 无机盐氯化钠浓度的优化Fig.3 Optimization of NaCl concentration
2.4 定量方法的选择
由于氘代同位素内标与目标物有相似的物理化学性质,因此在样品分析的过程中,加入氘代同位素内标能校正分析过程中各种因素对待测目标物的影响,提高了检测结果的稳定性和准确性。
采用标准加入法和纯溶剂标准曲线法两种方法测定婴幼儿饼干、米粉、蛋糕、水果泥和肉泥中四种呋喃类化合物含量的平均结果(平行测定三次)见表2。由5种不同基质样品的检测结果对比表明标准加入法和纯溶剂标准曲线法两种方法没有显著性差异,证明两种定量方法基本等效,为了避免重复样品操作的繁琐,提高分析的效率,当分析测定大批量样品时,推荐采用纯溶剂标准曲线法定量。
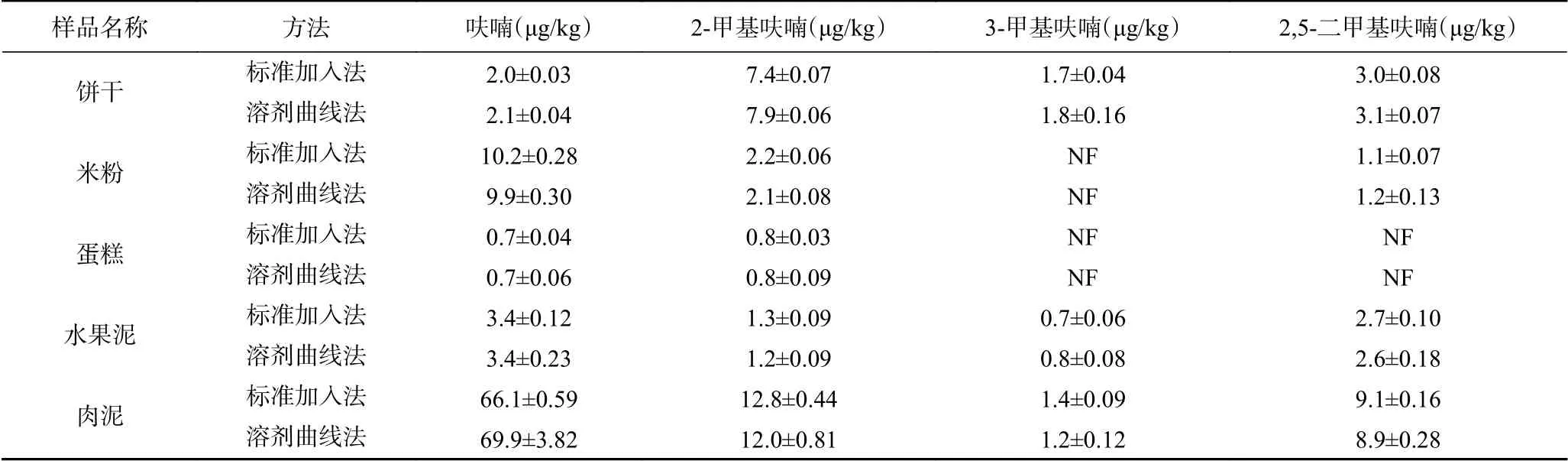
表2 标准加入法和纯溶剂标准曲线法定量样品中四种呋喃的检测平均结果(n=3)Table 2 Resultsof 4 furansin sampleswith standard addition method and solvent standard curvemethod (n=3)
2.5 工作曲线和检出限、定量限
以目标物的质量为横坐标,目标物的峰面积与同位素内标的峰面积之比为纵坐标绘制工作曲线。结果表明,各化合物在1~200 ng范围内呈良好的线性关系,线性回归方程、相关系数见表3。以3倍信噪比(3 S/N)和10倍信噪比(10 S/N)计算方法的检出限和定量限,饼干、米粉、蛋糕称取1.00 g,4种化合物的检出限均为0.2μg/kg,定量限为0.5μg/kg;水果泥和肉泥称取2.5 g,检出限均为0.1μg/kg,定量限为0.3μg/kg。

表3 线性参数Table3 Linearity parameters
2.6 精密度与回收率试验
分别称取一定质量的饼干、米粉、蛋糕、果泥、肉泥样品,加入不同质量浓度混合标准溶液,按照方法处理,使得添加水平相当于样品中10、40、200 ng,测定不同基底样品高低浓度的回收率,结果见表4。不同基底样品高低浓度的加标回收率为81.6%~110.5%,相对标准偏差(RSD,n=6)为3.44%~14.2%,说明方法具有良好的回收率与精密度。
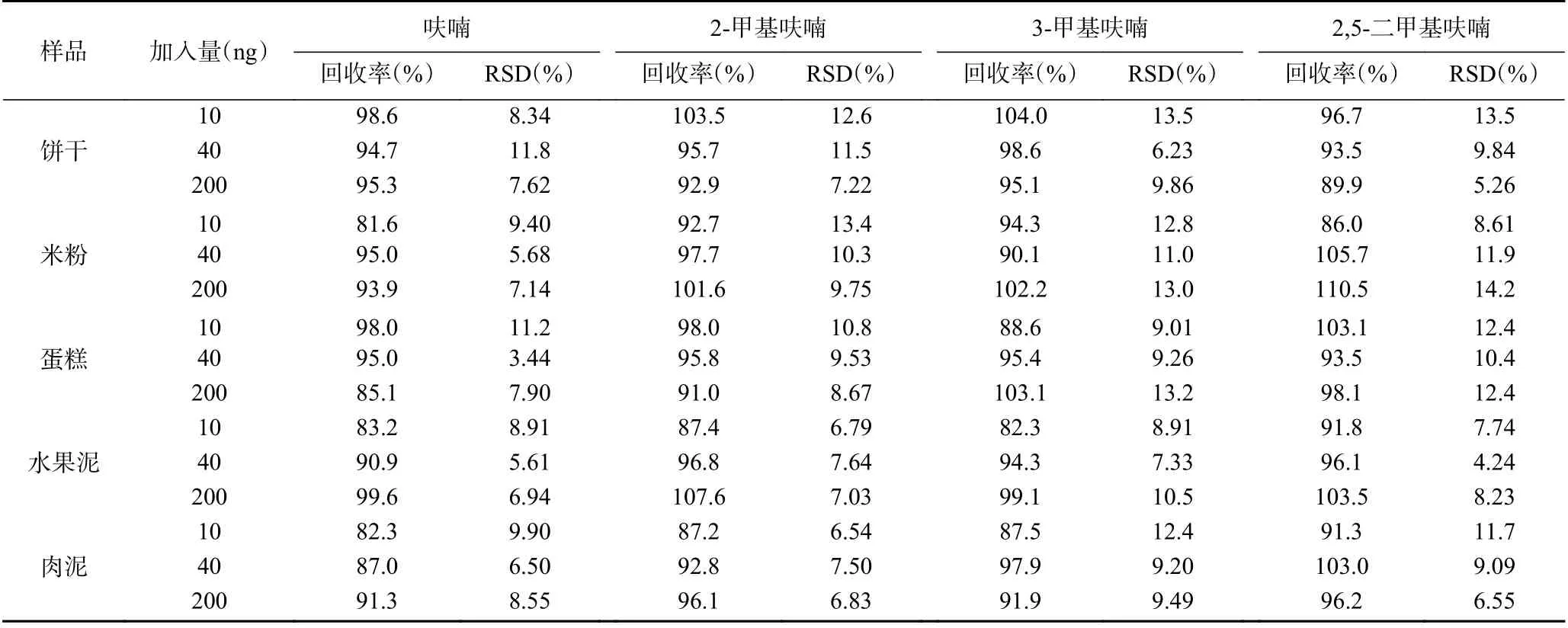
表4 精密度及回收率试验结果(n=6)Table 4 Results of test for precision and recovery (n=6)
2.7 实际样品的检测
利用已建立的方法,采集市售的婴幼儿辅食样品共139份,其检出结果见表5,所有样品检出率最高的是呋喃,为98.6%。肉泥样品中检出四种目标物的中位值最大,其中一份饼干样品中呋喃和2-甲基呋喃的含量最高,分别达到了177.2和313.4μg/kg。
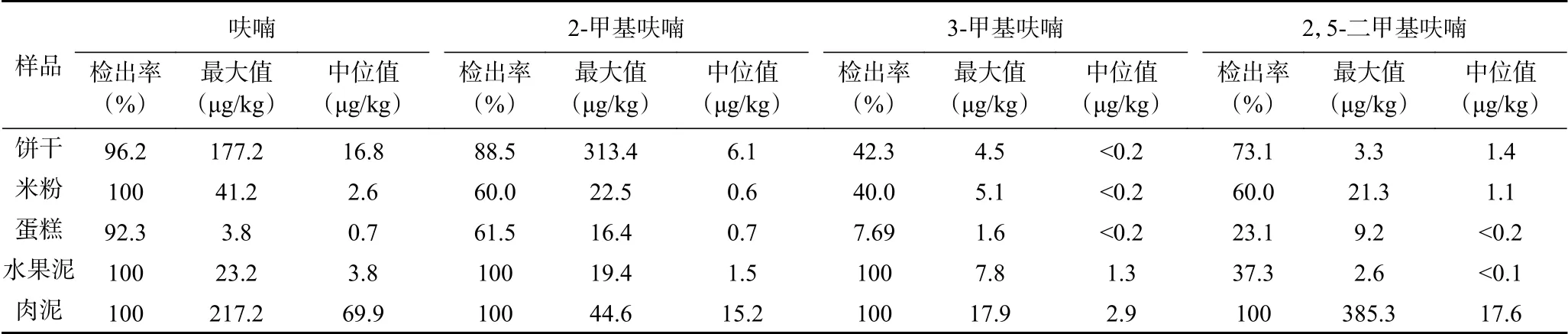
表5 样品中四种呋喃类化合物的检测结果Table5 Detection resultsof 4 furansin 139 samples
3 结论
本文建立了同位素稀释-顶空气相色谱/质谱法检测婴幼儿辅食中四种呋喃类化合物的检测方法。通过优化色谱条件和质谱条件以及样品前处理方法,目标化合物得到完全分离,线性关系良好,而且方法操作简单,灵敏度高,准确、可靠,适用于婴幼儿辅食样品中呋喃及甲基呋喃类化合物的检测,满足此类样品污染状况调查工作开展的要求,实验所得数据可以为制定食品安全标准和婴幼儿人群膳食暴露评估提供数据支持。
