硅钼蓝法测定电解锰中硅含量的试验
2021-09-01何传琼黄丽珍
何传琼,黄丽珍,卢 燕,黄 慧
(南方锰业集团有限责任公司 大新锰矿分公司,广西 大新 532315)
0 前 言
电解锰纯度高,用途广,主要用于有色金属合金如铝锰合金、铜锰合金,铬锰系不锈钢冶炼[1];还用于电焊条材料、化工、医药、食品、电子等工业。而行业标准YB/T 051—2015[2]明确规定了其技术要求、试验方法等,其中硅含量是其重要技术指标之一。随着冶金工业技术进步和产业精细化、多样化发展提出了特殊的要求,例如:电子工业中生产软磁铁氧体的高纯Mn3O4,对电解锰杂质含量有着较高的要求,特别是电解锰中硅含量的高低直接影响Mn3O4产品的含硅量,最终影响软磁铁氧体的性能质量[3]。因此,准确测定电解锰中硅的含量有着重要意义,值得不断探讨、优化、试验其检测方法。
目前,行业中大多采用高氯酸脱水重量法、氟硅酸钾碱滴定法、钼蓝分光光度法测定硅。滴定法滴定过程氟硅酸钾不稳定易挥发;重量法操作烦琐,分析流程长且脱水冒高氯酸烟时,污染环境;而分光光度法分析具有精密度好、灵敏度高、选择性好等优点。总的来说,经典的光度法仍是测定硅含量的主要方法[4]。钼蓝光度法,适用于电解金属锰中硅含量的测定[5-10]。通过大量试验和研究,总结出优化的硅钼蓝光度法。
1 试验部分
1.1 仪器和试剂
1)XP-205天平,紫外可见分光光度计UV-1800PC,恒温水浴锅。
2)硫酸(9+91):量取90 mL浓硫酸缓慢加入到盛有910 mL二级水大烧杯中用玻璃棒搅拌均匀冷却备用。
3)40 g草酸溶于800 mL(7+73)二级水硫酸溶液中。
4)称取75 g钼酸铵加1 000 mL溶解混匀。
5)称取150 g硫酸亚铁铵溶解于1 000 mL加有10 mL硫酸的二级水中,混匀。
6)硅标准溶液500 μg/mL(国家钢铁材料测试中心钢铁研究总院),所用试剂均为优级纯,水为实验用二级水。
1.2 试验方法
准确称取0.800 g电解锰试样(应通过0.149 mm筛孔)于250 mL烧杯中,少水润湿,缓慢加入20 mL硫酸(9+91),待试样剧烈反应结束后加水约至40 mL。置于电热板上加热煮沸,取下稍冷, 转移至100 mL容量瓶中,少水洗烧杯5~6次,溶液体积控制在50 mL左右。恒温水浴中加热至试液温度为50 ℃,加入10 mL(7.5%)钼酸铵溶液,于恒温水浴中加热6 min,且不时摇动,取下冷却至室温。加入15 mL草硫混酸(4+7)混匀,一定时间内加入5 mL(15%)硫酸亚铁铵溶液,混匀,用水稀释至刻度,混匀,静置15 min待测。于分光光度计波长810 nm处测量其吸光值,以随同试样的空白溶液为参比,从工作曲线上查出相应的硅量。硅的含量计算公式:
(1)
式(1)中:m1为从工作曲线上查得的硅量,mg;m0为试样量,g。
2 结果及分析
2.1 标准曲线的制作
分别准确移取浓度为10 μg/mL的硅标准溶液0.00,0.50,1.00,3.00,5.00,7.00,10.00 mL置于100 mL容量瓶中,分别按试验方法步骤加入试剂,以试剂空白为参比,于分光光度计波长810 nm处测量其吸光度。以测定的吸光度值为纵坐标,硅含量为横坐标绘制工作曲线,如图1。
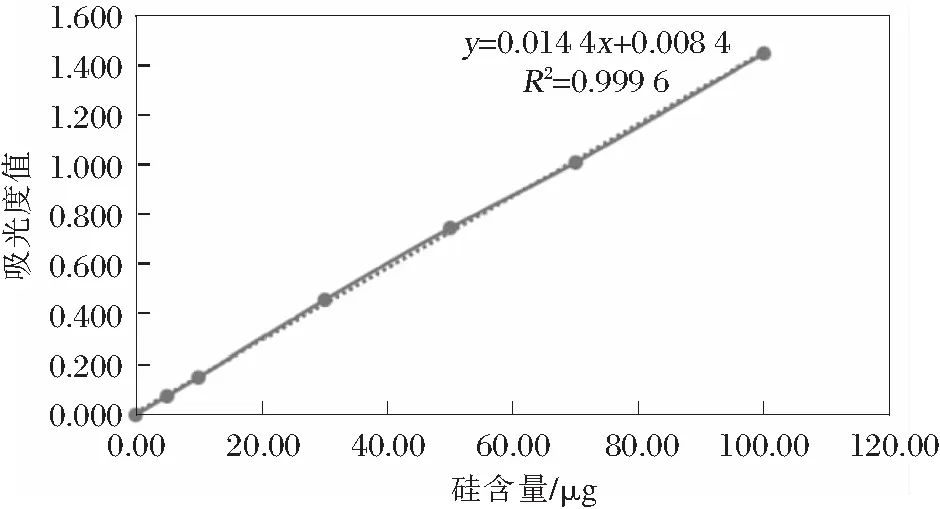
图1 硅标准曲线
由图1通过线性回归关系计算得回归方程为:y=0.014 4x+0.008 4,R2=0.999 6。
2.2 结果分析
2.2.1 不同硫酸加入量对测定结果的影响
称取相同试样,加入不同量的硫酸(9+91),结果见表1。

表1 硫酸用量试验
硫酸加入量决定溶液酸度,而溶液酸度影响硅钼酸离子络合程度。酸度过大,钼酸铵与硅不起反应;酸度过小,会生成大量钼酸铁沉淀,使硅钼酸生成不完全。
由表1可知,硫酸(9+91)的加入量在17~22 mL范围内,吸光度值最大,硅含量较为稳定,故选择加入20 mL硫酸(9+91)作为最佳用量。
2.2.2 钼酸铵用量对测定结果的影响
称取6个相同试样,相同试验条件下,加入不同量的钼酸铵,结果见表2。
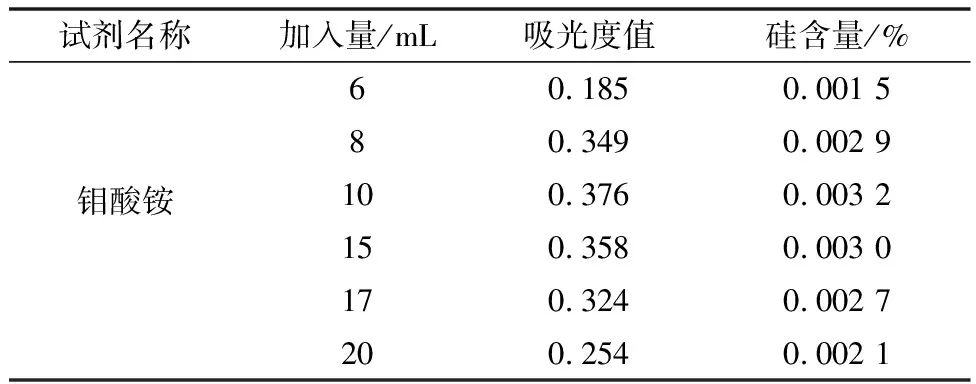
表2 钼酸铵用量试验
钼酸铵的加入量会影响钼蓝的色泽强度。大量的钼酸铵会影响体系的酸度,导致硅含量偏低;但也不可加得太少,否则会降低硅的色泽强度,使吸光度测定不灵敏,结果偏低。
由表2数据可知,钼酸铵的加入量在8~15 mL范围内,吸光度值最大且硅含量较为稳定,故选择加入10 mL钼酸铵作为最佳用量。
2.2.3 草硫混酸用量对测定结果的影响
称取6个相同试样,相同试验条件下,加入不同量的草硫混酸,结果见表3。
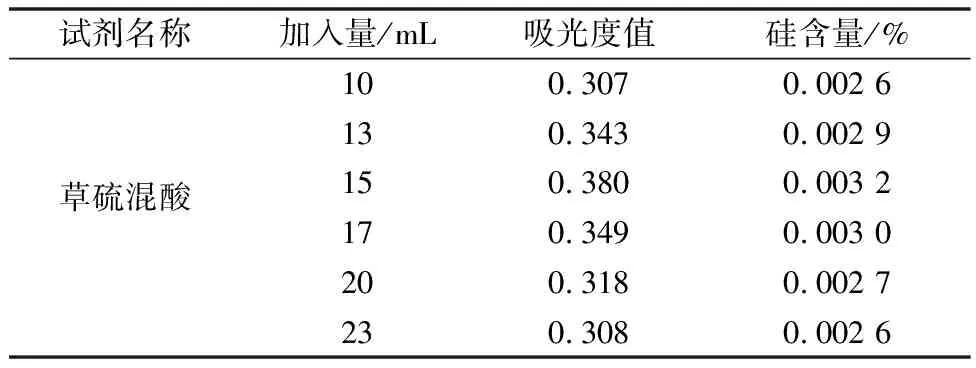
表3 草硫混酸用量试验
草硫混酸的加入量影响杂质掩蔽的效果。大量的草硫混酸会增加体系酸度,影响硅钼酸离子络合程度;而少量的草硫混酸无法完全消除磷、砷杂质的影响,使测量结果偏低。
由表3可知,草硫混酸的加入量在13~17 mL范围内,吸光度值最大,硅含量较为稳定,故本试验选择加入15 mL草硫混酸作为最佳用量。
2.2.4 硫酸亚铁铵用量对测定结果的影响
称取6个相同试样,相同试验条件下,加入不同量的硫酸亚铁铵,结果见表4。
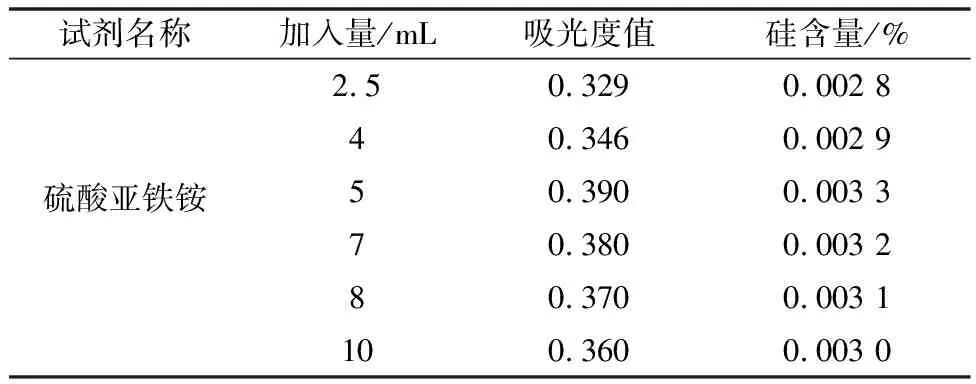
表4 硫酸亚铁铵用量试验
对于分光光度测试灵敏度来说,硅钼蓝的蓝色色泽比硅钼杂多酸的黄色色泽灵敏度高,加入硫酸亚铁铵还原黄色硅钼杂多酸为硅钼蓝。过量的硫酸亚铁铵在试液中不会增加还原能力,只起缓冲作用;而少量硫酸亚铁铵无法完全还原硅钼杂多酸为硅钼蓝,结果偏低。
由表4可知,硫酸亚铁铵的加入量在5~10 mL范围内,吸光度值最大,硅含量较为稳定,故本试验选择加入5 mL硫酸亚铁铵作为最佳用量。
2.2.5 不同水浴放置时间对测定结果的影响
称取相同试样,相同试验条件下,不同的水浴锅放置时间,结果见表5。
由表5可知,水浴放置时间控制在5~7 min范围内,吸光度值最大,硅含量较为稳定,故本试验选择水浴放置时间为6 min。
2.2.6 不同显色静置时间对测定结果的影响
称取相同试样,相同试验条件下,不同的显色静置时间,结果见表6。

表6 不同显色静置时间测定结果
由表6可知,显色放置时间控制在15~20 min范围内,硅含量较为稳定,故本试验选择显色静置时间为15 min。
2.3 检出限
按照试验方法最佳条件进行操作,做11次空白试验连续测定,记录空白试验的吸光度值,以标准偏差的3倍作为该方法的检出限。结果见表7。
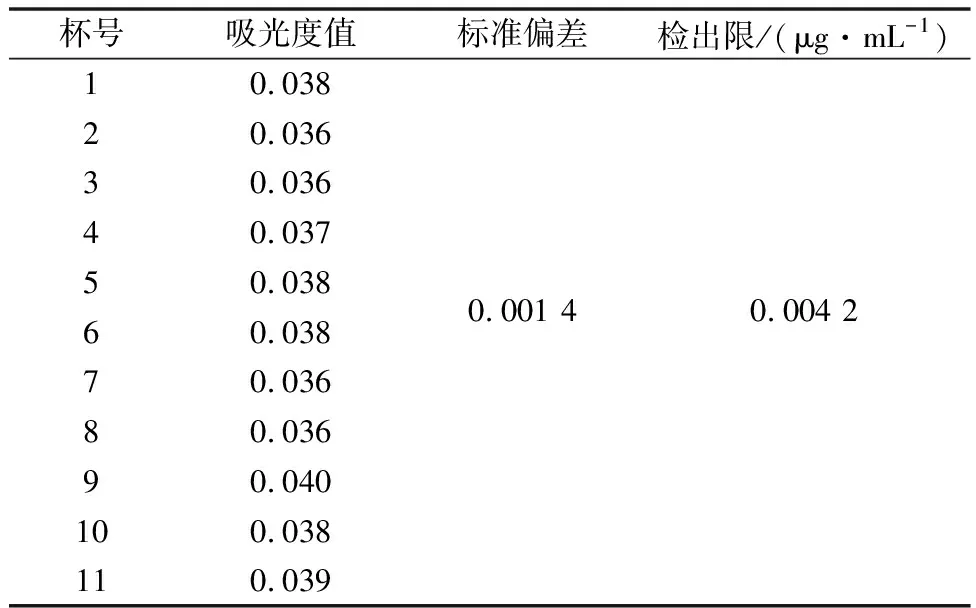
表7 检出限的测定结果
由表7可以看出,该方法的检出限为0.004 2 μg/mL,能够满足电解锰产品中硅含量的检测要求。
2.4 精密度试验
称取相同试样10份,按照试验方法最佳条件进行硅含量测定,计算相对标准偏差,结果见表8。
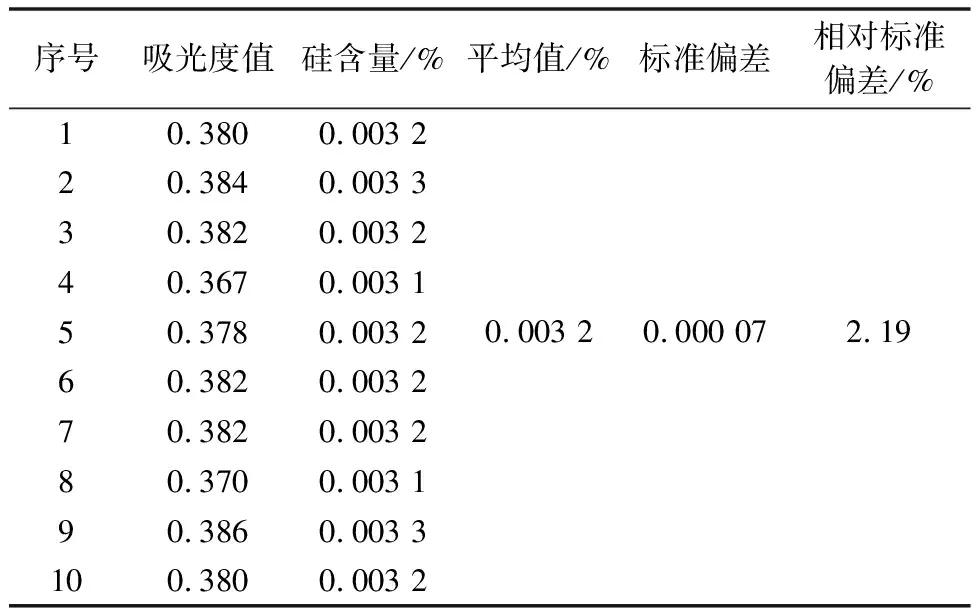
表8 精密度试验数据结果
由表8中数据结果可得,该试验方法对测定电解锰试样中硅含量的相对标准偏差为2.19%,具有较高的精密度。
2.5 加标回收率试验
取1号、2号、3号试样做3组加标回收试验:每组试样称取3份共9份,其中加标的试样在溶样前分别准确加入10 μg/mL硅标准溶液0.00,3.00,5.00 mL按最佳试验条件进行分析,平行测定试样,计算硅的回收率。试验数据结果见表9。
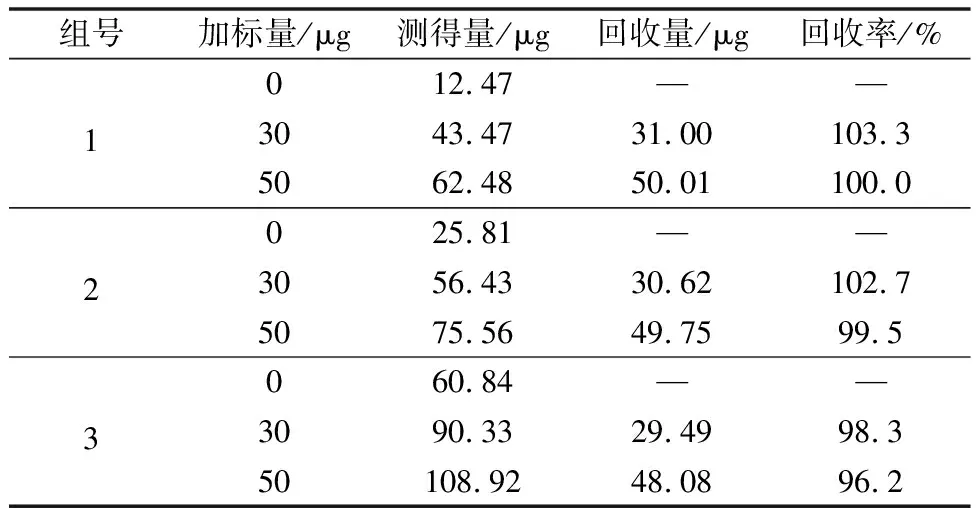
表9 加标回收率数据结果
由表9数据结果可得,方法优化后测定电解金属锰中硅的加标回收率在96.2%~103.3%之间,说明该方法的分析准确度较高,可行性好。
3 结 论
通过试验:准确称取0.800 g试样,加入20 mL硫酸(9+91)溶解,加10 mL(7.5%)钼酸铵反应生成硅钼杂多酸,加15 mL草硫混酸(4+7)掩蔽杂质,加入5 mL(15%)硫酸亚铁铵还原硅钼蓝,于分光光度计波长810 nm处测量溶液吸光度值。试验证明方法的检出限为0.004 2 μg/mL、相对标准偏差为2.19%、加标回收率测定在96.2%~103.3%之间。结果表明该试验方法检出限低,精密度良好,回收率高且仪器检测分析快速、操作简便、结果准确,适用于实际生产检测需求。
