磁固相萃取联合荧光法测定生物样品中的卡维地洛
2021-08-24秦艳芳赵冰欣李晓姣徐风云
秦艳芳,赵冰欣,李晓姣,徐风云,吴 昊*
(1.长治幼儿师范高等专科学校,山西 长治046000;2.山西师范大学 化学与材料科学学院,山西 临汾041004)
卡维地洛(Carvedilol,CAR,图1)属于α和β受体阻断剂,可扩张血管,保护心肌和神经元,在临床上广泛用于高血压、心绞痛和心力衰竭等疾病的治疗,能显著降低心血管患者的发病率和死亡率[1-2]。
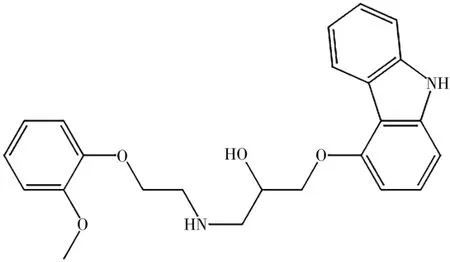
图1 卡维地洛的结构式Fig.1 The structure of carvedilol
磁固相萃取(MSPE)是21世纪发展起来的一项新型固相萃取技术,与传统的固相萃取相比,具有操作简便快速、成本低等优点[3-4]。共价有机骨架材料(COFs)是一类由轻质元素通过共价键连接的新型多孔有机材料,具有化学和热稳定性良好、比表面积大和孔径可控等优点[5],在样品预处理领域具有广阔的应用前景[6]。
本研究采用Fe3O4纳米材料、1,3,5-三甲基间苯三酚(Tp)和联苯胺(BD),通过溶剂热法合成了Fe3O4@COF(TpBD)复合材料。相比已有文献[7],其合成方法所用试剂少,过程简单易操作,实验成本低。以Fe3O4@COF(TpBD)为MSPE吸附剂联合荧光分光光度法建立了一种检测血浆和尿液中的CAR含量的新方法,通过优化相关实验参数,在最优实验条件下对该分析方法进行了评估。
1 实验部分
1.1 试剂与仪器
FeCl3·6H2O、乙二醇、无水乙酸钠、1,2-乙二胺、1,3,5-三甲基间苯三酚(Tp)、联苯胺(BD)(上海阿拉丁生化科技有限公司);无水乙醇、冰醋酸、高效液相色谱级甲醇、乙醇、乙腈(北京百灵威科技有限公司);CAR标准物质(中国药品生物制品检定所);尿液及血浆取自长治幼儿师范高等专科学校校医院。
Cary Eclipse荧光分光光度计(Agilent Technologies,美国);pHS-3C pH计(上海强生科技有限公司);KQ-500DV超声波洗涤器(江苏昆山禾创超声仪器有限公司);JEM-2100透射电子显微镜(TEM)(JEOL,日本);D8 Advance X射线衍射仪(XRD)(Bruker,德国);7407振动样品磁强计(Lake Shore,美国);FT-IR360傅里叶变换红外光谱仪(FT-IR)(Nicolet,美国);ASAP 2020比表面和孔隙度分析仪(Micromeritics,美国)。
荧光测量条件:(25±0.5)℃;λex=240 nm,λem=356 nm;激发和发射狭缝宽度为5 nm;扫描速度为1 000 nm·min-1。
1.2 磁性材料Fe3O4@COF(TpBD)的制备
Fe3O4纳米材料参照文献[4]制备:将1.0 g FeCl3·6H2O分散于20 mL乙二醇中超声处理,随后缓慢加入3.0 g无水乙酸钠,磁力搅拌30 min;加入10 mL 1,2-乙二胺搅拌30 min后,将混合溶液移至高压反应釜中加热至200℃并保持8 h,自然冷却至室温。最后将黑色产物用去离子水和乙醇洗涤数次,并在真空烘箱中60℃干燥24 h。
Fe3O4@COF(TpBD)复合材料通过溶剂热法制备:取60 mg Fe3O4加至30 mL无水乙醇中超声分散,然后依次加入63 mg(0.3 mmol)Tp和55.2 mg(0.3 mmol)BD,混合物超声35 min后,移至高压反应釜中加热至180℃,保持48 h。最后将产物用去离子水和乙醇洗涤数次,并在真空烘箱中60℃干燥24 h。
1.3 样品处理
CAR标准溶液(0.1 mg/mL):精确称取10 mg CAR,加1 mL的冰醋酸溶解,再加适量超纯水定容至100 mL。
血样处理:在具塞离心管中依次加入10 μL不同质量浓度的CAR标准溶液、2.0 mL血浆和8 mL乙腈脱蛋白,以4 000×g离心15 min。收集透明的上清液,待测。
尿样处理:在具塞离心管中依次加入10 μL不同质量浓度的CAR标准溶液和10 mL新鲜人尿,4 000×g离心10 min。收集透明的上清液,待测。
1.4 磁固相萃取过程
准确称取5 mg吸附剂Fe3O4@COF(TpBD)置于50 mL含CAR样品溶液的比色管中,超声4 min,将钕铁硼磁铁置于比色管底部对吸附剂进行分离,弃去上清液后,将吸附剂在40℃氮气中吹干。然后准确量取0.5 mL乙醇置于比色管底部进行解吸,超声5 min后使用钕铁硼磁铁分离解吸剂和吸附剂,重复解吸步骤2次,合并两次解吸剂。最后将解吸剂用0.22 μm的针式过滤器过滤,滤液用于荧光分析。
2 结果与讨论
2.1 Fe3O4@COF(TpBD)表征
利用TEM分别对Fe3O4和Fe3O4@COF(TpBD)的形貌进行了表征。如图2A与图2B所示,Fe3O4呈球形,且大小均匀,表面被COF(TpBD)均匀包裹。元素分布图像(图2C)也表明Fe3O4@COF(TpBD)中Fe3O4(元素Fe、O)和COF(TpBD)(元素C、N、O)均匀紧密地结合。
由Fe3O4和Fe3O4@COF(TpBD)的N2吸附-解吸等温线(图2D)可知,Fe3O4的BET比表面积和孔体积分别为11.00 cm2/g和0.14 cm2/g,Fe3O4@COF(TpBD)的分别为32.26 cm2/g和0.18 cm3/g,相比Fe3O4均明显增加。
Fe3O4和Fe3O4@COF(TpBD)的磁化曲线(图2E)表明,两者均具有良好的磁性能,Fe3O4@COF(TpBD)的饱和磁化强度为27.7 emu/g,在外磁场作用下容易分离。
从Fe3O4、COF(TpBD)和Fe3O4@COF(TpBD)的XRD谱图(图2F)可以看到,Fe3O4有6个特征峰(2θ=30.1、35.3、43.1、53.2、57.0、62.4)分别对应于(220)、(311)、(400)、(422)、(511)和(440)晶面,COF(TpBD)在2θ=25.5处的特征峰对应其(001)晶面。Fe3O4@COF(TpBD)图谱中这两种材料的峰都有体现,说明二者形成了复合材料,同时结晶度未发生变化。
如Fe3O4、COF(TpBD)和Fe3O4@COF(TpBD)的FT-IR谱图(图2G)所示,Fe3O4@COF(TpBD)在584 cm-1处的吸收带为Fe—O振动,3 432 cm-1和1 442 cm-1处的吸收带分别是O—H基团和芳香C====C单元的特征拉伸带,1 292 cm-1和1 605 cm-1处吸收带分别与C—N拉伸和C====N键有关。表明Fe3O4已成功被COF(TpBD)包裹。

图2 Fe3O4(A)和Fe3O4@COF(TpBD)(B)的TEM图,Fe3O4@COF(TpBD)的元素分布图(C),Fe3O4和Fe3O4@COF(TpBD)的N2吸附-解吸等温线(D),Fe3O4和Fe3O4@COF(TpBD)的磁化曲线(E),Fe3O4、COF(TpBD)和Fe3O4@COF(TpBD)的XRD图谱(F)以及Fe3O4、COF(TpBD)和Fe3O4@COF(TpBD)的FT-IR图谱(G)Fig.2 TEM images of Fe3O4 nanocrystal clusters(A)and Fe3O4@COF(TpBD)(B),element mapping images of Fe3O4@COF(TpBD)(C),N2 adsorption-desorption isotherms of Fe3O4 and Fe3O4@COF(TpBD)(D),magnetic curves of Fe3O4 and Fe3O4@COF(TpBD)(E),XRD spectra of Fe3O4,COF(TpBD)and Fe3O4@COF(TpBD)(F),and FT-IR spectra of Fe3O4,COF(TpBD)and Fe3O4@COF(TpBD)(G)
2.2 实验条件优化
2.2.1 pH值溶液的pH值会对药物与吸附剂间的吸附平衡产生影响。实验中溶液的pH值用B-R缓冲溶液调节。在溶液pH 2.0~12.0范围内进行MSPE和荧光检测。结果如图3A所示,随pH值的升高,CAR的荧光强度变化不大。为了方便操作,实验选择萃取溶液的pH值为6.0。
2.2.2 吸附剂用量考察了吸附剂用量在1~8 mg范围内对荧光强度的影响(图3B)。结果表明,当吸附剂用量为5 mg时,CAR的荧光强度最大。因此,实验选用5 mg吸附剂。
2.2.3 萃取时间考察了萃取时间为1~10 min时对CAR荧光强度的影响(图3C)。结果显示,荧光强度随着萃取时间的延长逐渐增加,当萃取时间为4 min时,CAR的荧光强度达到最大值,吸附过程达到平衡。因此,萃取时间确定为4 min。
2.2.4 解吸条件分别考察了乙酸、甲醇、乙醇和乙腈4种有机溶剂对CAR的解吸效果(图3D)。当选用乙醇为解吸剂时CAR的荧光强度最大。并考察了乙醇用量(0.2~0.8 mL)对CAR荧光强度的影响(图3E)。结果表明,改变乙醇用量,CAR的荧光强度变化不明显,为了方便操作,选用乙醇的体积为0.5 mL。另外,采用0.5 mL乙醇为解吸剂,考察了解吸时间在1~10 min范围内时对CAR荧光强度的影响(图3F)。结果表明,解吸时间为5 min时,CAR荧光强度最大。故选择最佳解吸时间为5 min。

图3 溶液pH值(A)、吸附剂的用量(B)、萃取时间(C)、解吸剂(D)、解吸剂的体积(E)和解吸时间(F)对CAR荧光强度的影响Fig.3 Effects of sample solution pH value(A),adsorbent amoun(tB),adsorption time(C),desorption solvent types(D),desorption solution volume(E)and desorption time(F)
2.3 方法选择性
在优化实验条件下,考察了某些共存物质以及常见离子对CAR(10 ng/mL)测定的影响。控制测量误差在±5%以内,1 000倍的尿素,800倍的Mg2+,700倍的K+、HPO42-,600倍的Na+、SO42-,400倍的Cl-,160倍的Ac-,120倍的Ca2+,56倍的Al3+,8倍的Cu2+等不会对测定造成干扰。可见该方法具有很好的选择性。
2.4 方法分析
在最优实验条件下,制备了一系列CAR溶液,以荧光强度(y)对质量浓度(x,ng/mL)绘制标准工作曲线,线性回归方程为y=8.138x+4.555,R=0.999 2。结果表明方法在1~100 ng/mL质量浓度范围内呈良好线性。CAR的检出限(S/N=3)为0.19 ng/mL,定量下限(S/N=10)为0.63 ng/mL,对溶液中CAR的富集倍数为113倍。可见该方法的灵敏度高,线性范围宽。
为考察方法的重现性,按照磁固相萃取步骤对1 ng/mL CAR标准溶液于日内和日间进行6次平行测定。计算结果表明,其日内相对标准偏差(RSD)为3.4%,日间RSD为3.6%。
2.5 样品分析
为了验证本方法的可行性及有效性,在尿样和血样中分别加入高、中、低3种不同质量浓度的CAR标准溶液,经“1.3”方法处理后,按照磁固相萃取过程进行加标回收实验。回收率测定结果如表1 所示,其范围为95.9%~98.7%。说明方法的准确性较好,可有效测定尿样和血样中CAR的含量。

表1 加标尿样和加标血样中CAR的荧光测定(n=3)Table 1 Fluorimetric determination of CAR in spiked urine and spiked plasma(n=3)
2.6 方法比较
相比其他文献方法(表2),本文所建立的方法线性范围宽,在加标样品中回收率高。
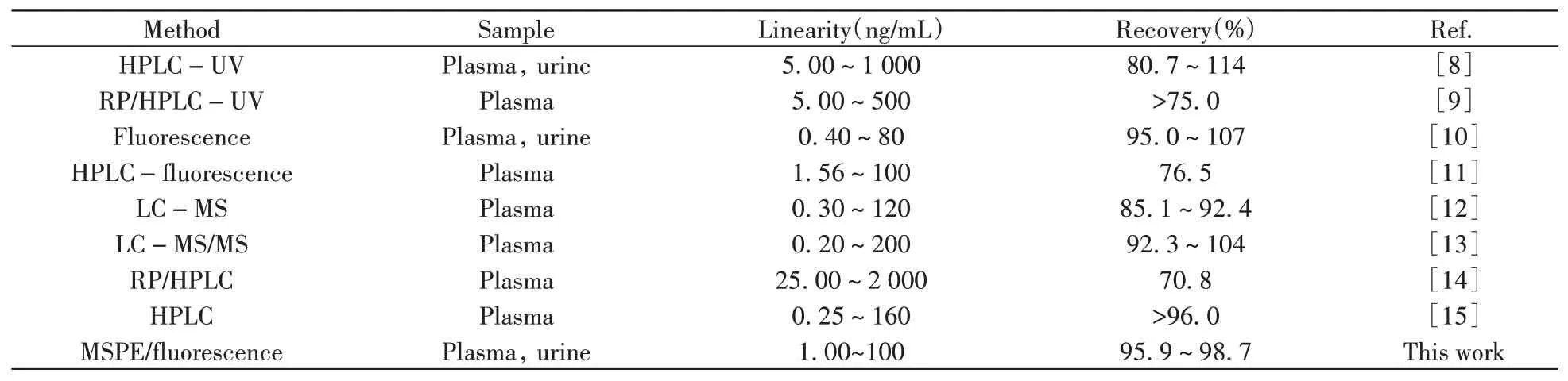
表2 生物样品中CAR检测方法比较Table 2 Comparison of determination for CAR in biological samples
3 结论
本研究合成了Fe3O4@COF(TpBD)复合材料,并以Fe3O4@COF(TpBD)作为MSPE吸附剂,联合荧光分光光度法建立了一种检测CAR含量的新方法。结果表明,该方法检测范围宽、灵敏度高且回收率好,适用于尿样和血样中CAR含量的测定。
