家族性玻璃体淀粉样变性一家系临床特征及基因突变分析
2021-08-23余强黄星杨主敏王鲜
余强 黄星 杨主敏 王鲜
贵州医科大学附属医院眼科,贵阳 550004 余强现在德阳市人民医院 618000
家族性玻璃体淀粉样变性(familial vitreous amyloidosis,FVA)是一种引起患者视力逐渐下降的常染色体显性遗传病。目前,与玻璃体淀粉样变性致病性密切相关的是转甲状腺素蛋白(transthyretin,TTR)基因[1]。已知TTR基因有100多个基因突变位点与淀粉样变性相关[2],最常见的是Val30Met突变,即缬氨酸被甲硫氨酸取代[3]。国内对此病的报道相对较少。本研究对贵州省FVA一家系的临床特征和基因突变进行分析,以期为此类疾病的治疗及预后分析提供一定的参考。
1 资料与方法
1.1 一般资料
采用家系调查研究方法,回顾性分析2005年5月至2019年3月于贵州医科大学附属医院就诊的贵州省汉族FVA一家系的基本资料。研究对象为该家系20名家系成员,包括5例患者和15例未发病成员。5例9眼FVA患者纳入标准参照文献[4],排除葡萄膜炎、眼内炎、玻璃体积血等其他因素导致的玻璃体混浊,其中先证者就诊前1眼因玻璃体混浊已于外院行玻璃体切割术。本研究遵循《赫尔辛基宣言》,经贵州医科大学附属医院伦理委员会审核批准(批文号:2019-296),所有家系成员均对本研究知情并签署知情同意书。
1.2 方法
1.2.1眼部检查及手术过程 20名家系成员均行最佳矫正视力(best corrected visual acuity,BCVA)、眼压检查,采用裂隙灯显微镜(日本Topcon公司)和90 D前置镜检查眼前节和眼底。5例9眼患者均采取闭合式三通道玻璃体切割术,术中尽量切除后极部光学区及周边混浊玻璃体,与视网膜及血管黏附紧密的玻璃体不予完全切割,术中所有术眼玻璃体腔均用平衡盐溶液填充。术中采集玻璃体标本送检至病理科行刚果红染色,术后1周、6个月复查BCVA、眼压、眼前节及眼底,并进行长期随访。
1.2.2基因检测及变异位点致病性分析 抽取该家系20名成员外周静脉全血4 ml,采用QIAamp DNA Mini试剂盒(上海Qiagen公司)按照说明从先证者全血中提取基因组DNA,根据说明书将≥3 μg的DNA用于文库制备。选择350~450 bp的DNA片段和包含接头序列的DNA片段构建DNA文库。采用GenCap试剂盒,通过基因捕获策略选择与眼科疾病相关的661个基因。生物素标记的捕获探针被用于杂交所有具有非重复区域的外显子。将1 μg DNA文库与BL缓冲液(北京迈基诺基因科技股份有限公司)和生物素标记的探针混合,采用ABI-2720 PCR仪(美国赛默飞公司)进行PCR反应。反应条件:95 ℃变性7 min,65 ℃退火2 min。加入23 μl预热至65 ℃的HY缓冲液,65 ℃杂交22 h。用500 μl 1倍结合缓冲液和50 μl MyOne磁珠,洗脱3次,重悬于80 μl 1倍结合缓冲液。加入64 μl 2倍结合缓冲液至杂交混合物中,转移至含有80 μl MyOne磁珠的试管中,旋转混匀1 h。采用WB1缓冲液室温洗脱磁珠15 min,WB3缓冲液65 ℃洗脱3次,每次15 min,采用洗脱缓冲液将结合的DNA洗脱下来。洗脱的DNA进行PCR反应,反应条件:98 ℃预变性30 s;98 ℃变性25 s,65 ℃退火30 s,72 ℃延伸30 s,共进行15个循环;72 ℃延伸5 min。根据产品说明书用SPRI beads纯化PCR产物。富集的DNA文库用Illumina HiSeq 2000第2代测序仪进行双端测序。将原始测序数据去除污染和接头序列,采用BWA软件(http://bio-bwa.sourceforge.net/)将过滤后的序列比对到NCBI数据库人类基因组参考序列上,采用GATK软件(https://software.broadinstitute.org/gatk/)分析得出单核苷酸变异(single nucleotide variation,SNV)和插入缺失突变(inserts and deletions,INDEL)的相关信息。通过ANNOVAR软件(http://annovar.openbioinformatics.org/en/latest/)对所有的SNV和INDEL进行注释。筛除正常人数据库中频率小于0.05的突变位点。采用SIFT、PolyPhen-2、REVEL生物信息学蛋白功能预测软件进行变异位点致病性预测和保守性预测。经过分析筛选得到的候选变异位点采用PCR和Sanger测序验证。采用Primer 3.0在线软件(http://primer3.ut.ee/)设计TTR基因PCR引物,正向引物序列为5’-TTTGCCATTTAATTTCAGTTAGGAG-3’,反向引物序列为5’-GGGAACCTTTGGTCATTCATC-3’。反应条件:98 ℃预变性2 min;98 ℃变性30 s,65 ℃退火30 s,72 ℃延伸30 s,循环30次。PCR产物经过Sanger测序并在ABI 3130 Genetic Analyzer(Applied Biosystems)上进行分析。对先证者及其余受试者进行Sanger测序验证。采用ACMG指南对发现的变异位点进行致病性分析。
2 结果
2.1 该FVA家系临床特征
2.1.1家系遗传特点 该家系前2代患者(男性1例,女性2例)均已去世,家系成员述其生前经医院诊断为“玻璃体混浊”,发病年龄约为40岁,未予治疗,去世年龄及原因不详。纳入研究的20名家系成员中包括5例患者和15例未发病成员,其中男性患者2例,女性患者3例,均以视力下降、视物模糊就诊,无四肢麻木、远端无力、胃肠道功能障碍、蛋白尿、下肢水肿、活动耐力减低、皮肤病变等相关系统病变主诉。5例患者发病年龄为32~43岁。15例未发病成员中,男6例,女9例;年龄为2~31岁。本家系的遗传方式符合常染色体显性遗传(图1)。
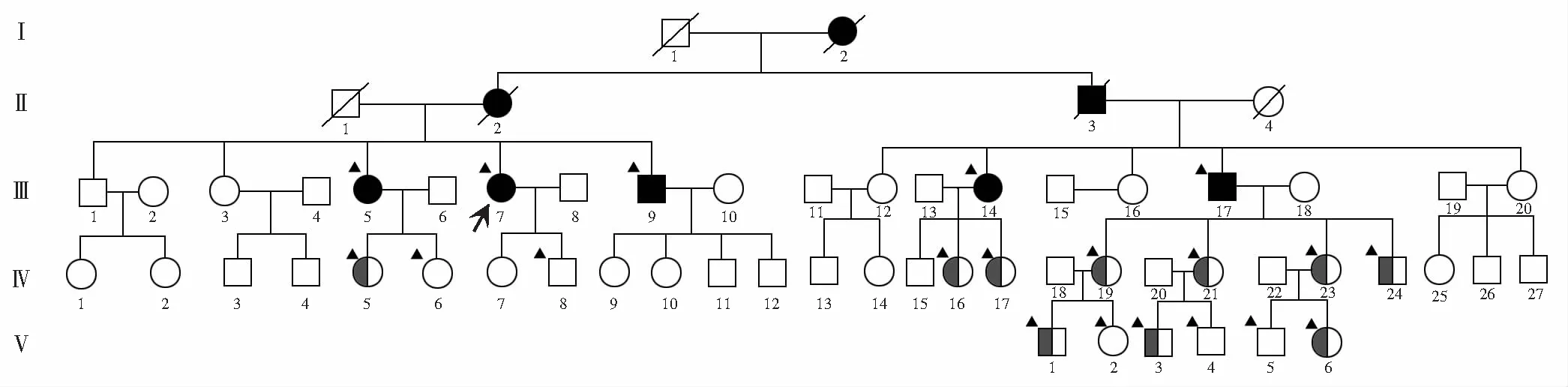
图1 该FVA家系图 □:健康男性;○:健康女性;■:男性患者;●:女性患者;:男性携带者;:女性携带者;/:已故;:先证者;▲:受检者Figure 1 Pedigree diagram of FVA □:healthy male;○:healthy female;■:male patient;●:female patient;:male carrier of the gene variation site;:female carrier of the gene variation site;/:deceased;:the proband;▲:subject
2.1.2眼部检查 5例9眼FVA患者玻璃体切割术前,6眼BCVA为0.1~0.2,3眼为数指/50 cm,平均眼压为(15.18±1.32)mmHg(1 mmHg=0.133 kPa);前房角镜检查未发现异常物质沉积于前房角,各位点房角开放;晶状体后囊膜下轻度混浊,后囊膜白色“足盘样”点状颗粒附着(图2),玻璃体灰白色絮状混浊,眼底窥不清。术后1周,8眼BCVA为0.8,1眼为0.6,平均眼压为(15.32±2.11)mmHg。术后6个月,6眼BCVA为0.8,2眼为0.6,1眼为光感,平均眼压为(16.13±1.25)mmHg,其中1眼玻璃体切割术后3个月视力下降未及时就诊,术后6个月就诊时发现视网膜脱离,视力降至光感。玻璃体切割术后6年眼底检查可见视网膜散在残余淀粉样混浊玻璃体附着(图3),未见出血、渗出等病变,玻璃体切割术后7年光相干断层扫描(optical coherence tomography,OCT)检查黄斑区各层结构未见明显异常(图4)。15例30眼未发病成员中2例4眼为小儿,检查不配合,其余13例26眼BCVA为0.8~1.0,平均眼压为(15.52±1.15)mmHg,眼前节及眼底检查未见明显异常。
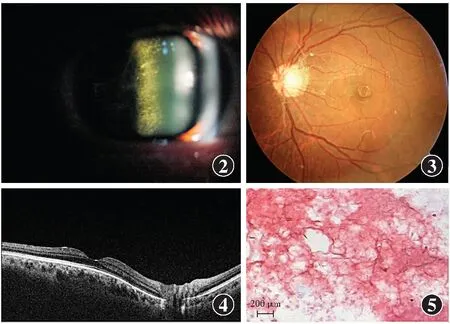
图2 Ⅲ5患眼术前裂隙灯显微镜检查 晶状体后囊膜下轻度混浊,后囊膜白色“足盘样”点状颗粒附着 图3 Ⅲ9玻璃体切割术后6年眼底照相 视网膜散在残余淀粉样混浊玻璃体附着 图4 Ⅲ5患眼玻璃体切割术后7年OCT 视网膜各层结构未见明显异常 图5 Ⅲ7患眼玻璃体标本组织病理学检查(刚果红 ×200,标尺=200 μm) 玻璃体样本刚果红染色呈阳性反应,呈红色弥散染色Figure 2 Slit lamp microscopy image microscopy of the affected eye of Ⅲ5 before operation Mild posterior subcapsular cataract behind the lens with white pedal disc punctate particles attachment was observed Figure 3 Fundus image of Ⅲ9 at six years after vitrectomy Scattered residual amyloid opacity of the vitreous body attached to the retina Figure 4 OCT image of Ⅲ5 at seven years after vitrectomy No obvious abnormality was found in the retina Figure 5 Histopathological examination of vitreous specimen of Ⅲ7(Congo red ×200,bar=200 μm) Positive staining result with red diffuse staining
2.1.3玻璃体样本组织病理学检查 所有患者术中玻璃体样本行刚果红染色呈阳性反应,呈红色弥散染色(图5)。
2.1.4术后长期随访 5例8眼(1眼因视网膜脱离后眼球萎缩)患者均在玻璃体切割术后3~14年发生继发性青光眼,眼压为38.3~50.2 mmHg,前房角镜检查显示房角开放且未见异常物质沉积,静态视野检查显示存在象限性视野缺损(图6),眼底可见视盘苍白(图7),早期均以药物控制眼压,后期2眼行小梁切除术,6眼行青光眼引流阀植入术。此外,先证者于外院行玻璃体切割术的1眼亦发生青光眼,予以药物控制眼压。对携带突变但未发病的家系成员均进行随访,均未有相关系统疾病的主诉,眼部检查均正常,暂未发现有发病病例及青光眼病例。
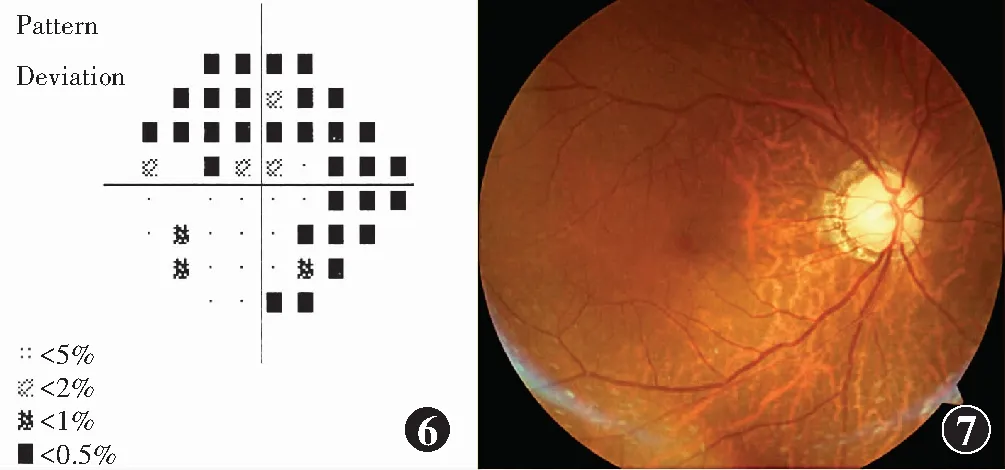
图6 Ⅲ14玻璃体切割术后3年静态视野检查 提示象限性视野缺损 图7 Ⅲ5玻璃体切割术后10年眼底照相 可见视盘边界清,颜色苍白Figure 6 Static perimetry result of Ⅲ14 at three years after vitrectomy Quadrantal visual field defect was indicated Figure 7 Fundus image of patient Ⅲ5 at ten years after vitrectomy The optic disc with clear boundary was pale in color
2.2 该FVA家系基因检测及致病性分析
基因测序发现5例患者及10名未发病成员均发生TTR基因杂合突变,即第3号外显子第307位核苷酸由鸟嘌呤变异为胞嘧啶(c.307G>C),导致其编码的第103位氨基酸由甘氨酸变异为精氨酸(p.Gly103Arg);5名未发病家系成员未检测到TTR基因突变(图8)。根据ACMG指南,HGMD数据库已有该位点的致病性报道,评为PS1;在正常人群数据库中未发现变异,评为PM2;生物信息学蛋白功能预测软件SIFT、PolyPhen_2、REVEL均预测为有害变异,评为PP3,因此该变异总评分为PS1+PM2+PP3,为可能致病性变异。在猩猩、猕猴、牛等物种中,该位点是保守的。
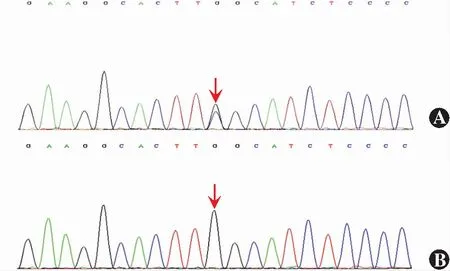
图8 TTR基因c.307G >C突变测序图 A:突变型 B:野生型 箭头所示为突变位点Figure 8 Sequencing of mutation c.307G >C in TTR gene A:Mutant type B:Wild type The arrow showed the mutation site
3 讨论
淀粉样变性可分为4种类型:(1)系统性淀粉样变性,包括原发性淀粉样变性、多发性骨髓瘤伴发的淀粉样变性等;(2)继发性淀粉样变性,常见于自身免疫性疾病、慢性炎症等;(3)β2-M淀粉样变性,即透析相关性淀粉样变性,淀粉样蛋白由β2-微球蛋白衍生而来;(4)遗传性淀粉样变性[5]。FVA是由遗传基因突变导致相应不溶性淀粉样蛋白异常沉积于玻璃体而引起的常染色体显性遗传病。
本研究中,术前5例患者均存在玻璃体絮状混浊,晶状体后囊膜下轻度混浊,玻璃体切割术后1周和6个月视力均好于术前(除1眼术后3个月发生视网膜脱离)。可见玻璃体混浊为影响患者视力的主要因素,行玻璃体切割术是治疗玻璃体淀粉样变性的有效方法,与既往文献报道观点一致[3,6]。
FVA与继发性青光眼有一定关联[7-8]。Beirão等[9]报道未予玻璃体切割术治疗的患者青光眼发生率为10.5%,明显低于行玻璃体切割手术患者的56.1%。石一宁等[10]对FVA一家系研究表明,眼前节均无异常的患者行玻璃体切割手术治疗后1~2年发生青光眼。本研究中,15例未发病成员眼压及房角均正常;5例9眼患者术前眼压正常,房角开放且未见异常物质沉积,术后1周和6个月眼压正常,但8眼行玻璃体切割术后3~14年均发生继发性青光眼;此外,先证者于外院行玻璃体切割术的1眼亦发生继发性青光眼,可见此家系玻璃体切割术后继发性青光眼的发生率较高。分析原因可能为玻璃体切割术破坏了玻璃体前界膜,导致玻璃体腔淀粉样物质扩散至前房并沉积于小梁组织,引起房水外流受阻,继而引起青光眼,但本研究缺少相关小梁组织的病理学检查,尚有待进一步验证;同时也不能排除该FVA家系成员本身就存在青光眼的情况,因为睫状体色素上皮亦可合成淀粉样物质[11],后者经房水引流通道亦可阻滞小梁组织,玻璃体切割术可能加速了淀粉样物质沉积于小梁组织,因此加速了青光眼的发生。该家系成员玻璃体切割术后3~14年发生青光眼,建议对此类疾病患者行玻璃体切割术后进行长期随访,有利于青光眼的早期发现和干预。
本研究发现该FVA家系存在TTR基因p.Gly103Arg杂合突变。国外尚未有关其导致FVA及家族性淀粉样多发神经病变的报道。谢渊等[12]认为,TTR基因Gly103Arg杂合突变可能与其所研究的黎族FVA家系的发病有关。查阅NCBI发现,p.Gly103Arg的碱基序列与p.Gly83Arg的碱基序列完全相同。陈凌燕等[13]报道1例遗传性玻璃体淀粉样变性患者,发现TTR基因Gly83Arg突变可能是玻璃体淀粉样变性的致病原因。Zhang等[14]研究发现,TTR基因Gly83Arg突变与中国的FVA相关。Liu等[15]研究报道玻璃体混浊在TTR基因Gly83Arg突变患者中非常普遍。谢兵等[1]证实了FVA一汉族家系是由TTR基因Gly83Arg杂合子突变所致。本研究发现5例患者和10名表型正常者均存在TTR基因p.Gly103Arg杂合突变,但由于患者的父母均已去世,故缺少基因变异来源验证。FVA属于常染色体显性遗传病,本研究中存在未发病的TTR基因突变携带者,暂不能用遗传学共分离现象解释,但符合常染色体显性遗传性疾病的亚型之一“延迟显性”,即携带有该突变基因的个体早期不显现出临床症状,当到了一定年龄时致病基因的作用才表现出来,继而引起相应临床表现。结合本家系的临床表现和基因突变结果,考虑TTR基因p.Gly103Arg杂合突变可能是该FVA家系的致病突变位点,但有待于今后对携带突变基因的未发病成员长期随访验证。TTR基因为FVA主要致病基因,结合患者的主要临床表现,考虑到该家系人员庞大,研究成本过高,故在基因检测初期只对TTR基因进行了突变检测。
本研究收集了汉族FVA一家系,对20名家系成员进行眼科检查和基因检测,并对其中5例患者行玻璃体切割术治疗,长期随访结果显示,玻璃体切割术是治疗FVA的有效方法,但术后继发性青光眼发病率较高。TTR基因p.Gly103Arg杂合突变可能是该FVA家系的致病突变位点。
利益冲突所有作者均声明不存在任何利益冲突
