运用数据挖掘和网络药理学探讨糖尿病认知功能障碍中医用药规律和作用机制
2021-08-07石崯力
石崯力,王 旭,盛 沛,张 擎,梁 婕
南京中医药大学第一临床医学院,南京 210029
糖尿病(diabetes mellitus,DM)是由遗传和环境多重因素造成胰岛素分泌或生物作用缺陷,临床以慢性高血糖为特征的一组代谢性疾病。流行病学调查发现近三分之一DM患者合并不同程度的认知功能障碍[1],多表现出健忘、学习及记忆能力减退、认知缺失等症状,严重者病情可进展至不可逆性痴呆。中医将糖尿病认知功能障碍(diabetic cognitive dysfunction,DCD)归于“消渴”“呆病”范畴,认为该病多由年迈肾虚、情志所伤、饮食失调、久病耗损等内外病因综合影响所致[2]。近年来运用中药治疗DCD的研究逐渐增加,积累大量临床数据,将其规范、总结是现代医学研究的大方向。通过对治疗DCD的中医处方进行探寻,挖掘潜在配伍药物组合并提炼用药规律,为今后临床选方用药提供借鉴。本研究基于对文献数据库进行检索,通过数据挖掘技术进行关联、聚类和因子分析,研究其用药规律,并通过网络药理学对核心组方治疗DCD的有效活性成分和潜在靶点进行初步预测,筛选出相关生物学功能相关通路,对核心组方治疗DCD的复杂作用机制进行初步探究,为科研和临床提供新思路和可靠依据。
1 资料与方法
1.1 文献来源与检索策略
以(主题=糖尿病认知功能障碍or主题=糖尿病认知障碍or主题=糖尿病脑病)and(关键词=中医or关键词=中医药)匹配,检索中国知网(CNKI)、万方数据(WF)、维普期刊全文数据库(VIP)、生物医学文献数据库(CBM)、及中国科学引文数据库(CSCD)自1999年1月至2020年10月收载的文献。
1.1.1 纳入标准
采用以下纳入标准对文献进行筛选:(1)治疗DCD的公开发表的中医临床研究文献,包括证治探讨、名家经验和临床观察等,DCD的诊断应符合国内外公认的标准[3,4];(2)研究对象未合并其他病症;(3)文献所报道的中药复方、中成药资料完整;(4)中药在对照实验研究中具有显著明确的临床疗效;(5)作者使用同一观点重复发表的文献只取一篇。
1.1.2 排除标准
采用以下排除标准对已纳入的文献进行进一步筛选:(1)综述类、动物实验、源于会议、科普类文献;(2)采用针灸、推拿、食疗、护理等非中医处方治疗或中西医结合治疗DCD的文献;(3)非糖尿病所引起的认知功能障碍的文献。
1.2 中药材数据的规范化
参照全国高等中医药院校“十二五”规划教材《中药学》[5]将表达相同的中药进行归类处理,并将中药别名或俗称予以规范。如将“丹皮”“牡丹皮”统一为“牡丹皮”,“生地”“生地黄”统一为“生地黄”,“法半夏”“半夏”统一为“半夏”等。
1.3 数据处理和分析
根据标准排除筛选后将纳入的文献内中药处方及中药材逐一输入至Microsoft Excel 2019,进行排序、校对和整理,建立中药治疗DCD数据库。运用IBM SPSS Modeler 18.0、SPSS Statistics 25.0软件对高频中药进行因子、聚类分析以及关联规则网络图的制作。
1.4 通过网络药理学进行作用机制分析
1.4.1 核心组方化合物的筛选和预测
运用TCMSP数据库(http://tcmspw.com/tcmsp.php)搜索核心组方化学成分,以口服生物利用度(oral bioavailability,OB)≥30%和类药性(drug like,DL)≥0.18为阈值条件[6]进行初步筛选,纳入中药有效活性成分,建立中药化学成分数据集。通过SuperPred数据库(http://prediction.charite.de/)对筛选出的化合物进行相关靶点预测[7],利用UniProt数据库(http://www.uniprot.org/),将种属设置为“homo sapiens”,对去重后的有效靶点信息进行规范化。
1.4.2 DCD疾病靶点的预测
以“diabetic cognitive dysfunction”“diabetic encephalopathy”等为关键词,通过OMIM(http://www.omim.org/)、TTD(http://db.idrblab.net/ttd/)、Genecards(https://www.genecards.org/)、PharmGkb(http://www.pharmgkb.org/)和Drugbank数据库(http://www.drugbank.ca/)获取DCD潜在疾病靶点并建立疾病信息数据集[8]。
1.4.3 核心组方药物-有效成分-靶点-疾病网络的构建
将筛选出的有效化合物、其潜在的靶点蛋白和疾病的导入至Cytoscape 3.8.0软件(http://www.cytoscape.org/)构建“核心组方药物-有效成分-靶点-疾病”共有机制网络,并使用Network Analyzer功能对核心组方中的有效成分进行分析。
1.4.4 蛋白质—蛋白质相互作用(PPI)网络构建
利用Stitch和String数据库(https://string-db.org/cgi/input.pl)分别构建核心组方潜在靶点与疾病靶点的PPI网络,选择种属为“homo sapiens”,筛选条件为“minimum required interaction score>0.7”,将得到的蛋白质互作关系导入Cytoscape 3.8.0软件构建成分靶点和疾病靶点相互作用 PPI网络[9],并通过CytoNCA插件进行网络拓扑分析,以网络拓扑参数点度中心性(degree centrality,DC)、中介中心性(betweenness centrality,BC)和接近中心性(closeness centrality,CC)均大于中位数为标准,筛选发挥药效的主要活性成分以及核心靶点[10]。
1.4.5 关键靶点的代谢通路与生物过程分析
将核心靶点导入DAVID 6.8数据库(https://david.ncifcrf.gov/)[11],将“gene list”及“background”设置为“homo sapiens”。运用R Studio软件下载“ggplot2”扩展包[12],设定阈值P< 0.01,FDR < 0.01,进行京都基因与基因组百科全书(KEGG)通路富集分析;下载“dplyr”和“org.Hs.eg.db”安装包,以阈值P< 0.01、FDR < 0.01进行关键基因基因本体(GO)功能分析,最终以条形图和气泡图的形式输出结果。
1.4.6 分子对接验证
通过分子对接技术对核心组方内的关键成分和关键靶点之间的互作关系进行进一步的探究。研究表明[13],二甲双胍(metformin)作为经典的降糖药物,能一定程度改善糖尿病患者认知障碍,因此以其作为阳性对照药物。具体步骤为:通过Pubchem网站(https://pubchem.ncbi.nlm.nih.gov/)检索获取关键成分的3D结构,下载SDF文件并利用Open Babel 2.3.2软件将SDF文件转化为PDB文件,从Protein Data Bank(http://www.rcsb.org/pdb)数据库中检索关键靶点的受体蛋白,利用AutoDockTools软件对受体蛋白进行去水、去配体、加氢、平衡电荷等修饰,用Grid程序下的Grid Box命令打开Grid Option工具对每个受体蛋白进行处理,利用AutoDock Vina 1.1.2对受体蛋白与配体小分子分别进行分子对接。分子对接的结果以一种结合能(affinity)的形式输出,是衡量配体是否能与受体分子有效结合的重要指标,一般认为对接得分小于-4.25 kcal/mol可认为配体与靶点之间具有结合活性,得分小于-5.0 kcal/mol则认为结合活性较佳,得分小于-7.0 kcal/mol则认为两者之间有强烈的对接活性。
2 数据挖掘结果
2.1 治疗DCD的中药使用频次统计
根据标准排除筛选,共纳入符合的文献33篇,涉及中药加减处方共123首,中药共137味,总使用频数为1 381次,使用中药频次最高的前十位依次是:当归、熟地黄、甘草、川芎、茯苓、枸杞子、桃仁、黄芪、石菖蒲和白芍,并对中药在中药组方中出现的频率进行统计。使用频数大于25次的中药共20味(见表1)。

表1 治疗糖尿病认知功能障碍的处方频数大于25次的中药材统计
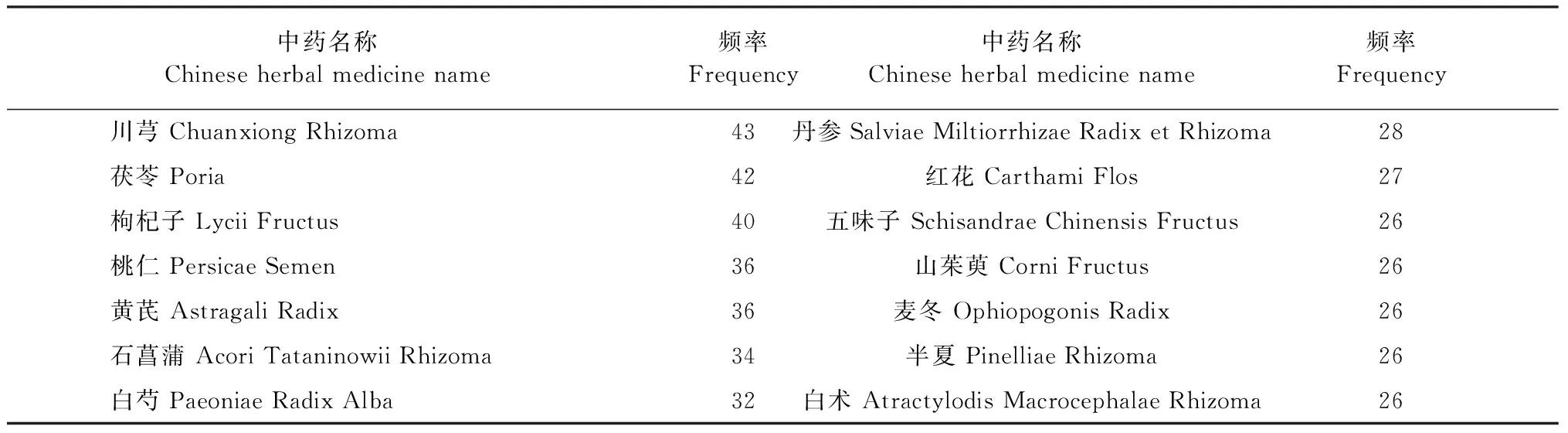
续表1
2.2 治疗DCD的中药关联分析
通过 SPSS Modeler 18.0软件应用apriori算法对使用频数大于25次的20味高频中药进行建模,以查找各中药间的相关性与因果关系。设置关联参数:最小支持度大于20%,最小置信度大于80%,支持度提示药对或药物组合同时出现的频率,置信度则提示当药物组合前项出现时,后项药物出现的概率。结果得到桃仁-红花、川芎-红花、当归-桃仁-川芎、川芎-红花-桃仁、熟地黄-菟丝子-枸杞子等核心药物组合共26组(见表2)。
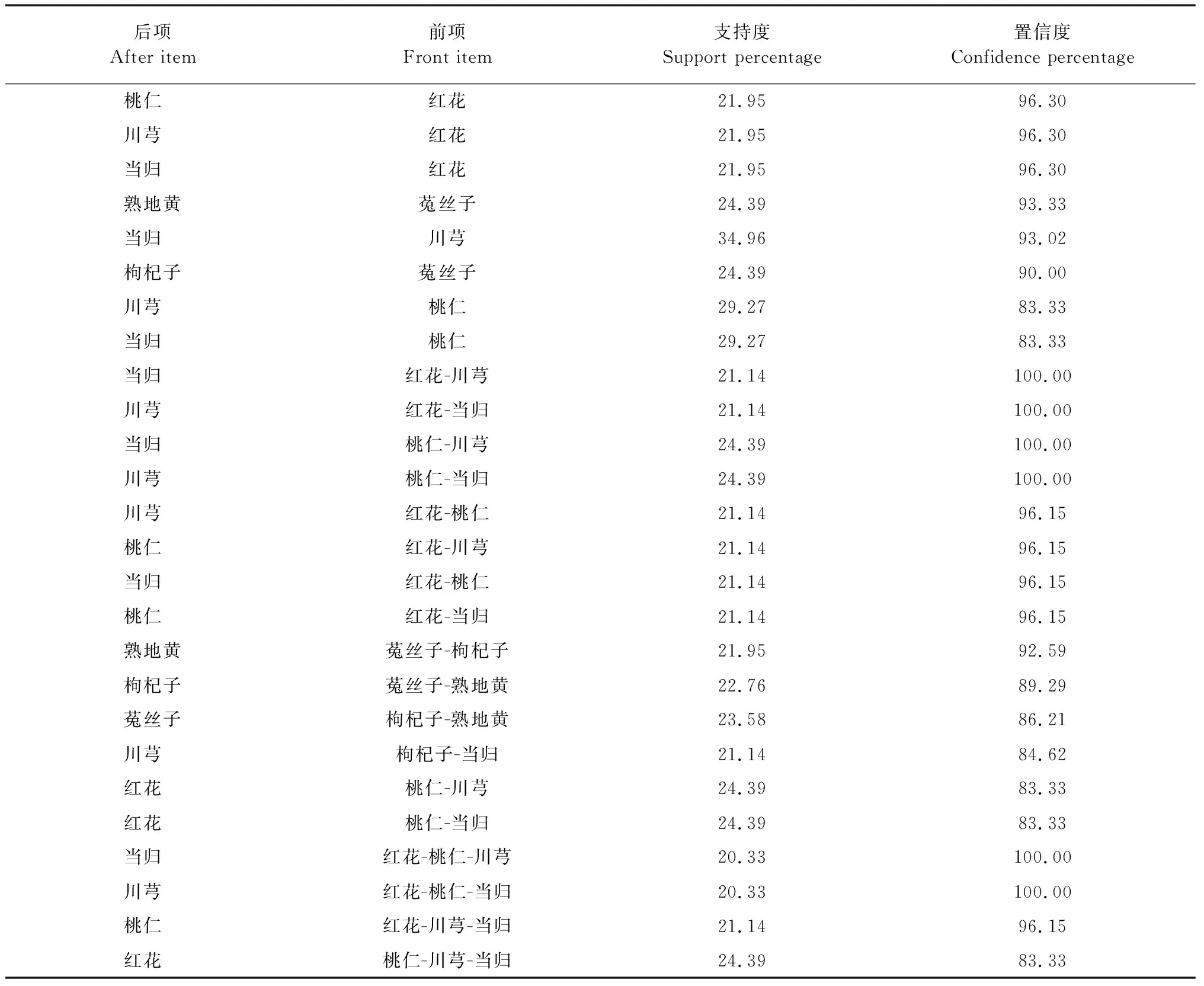
表2 糖尿病认知功能障碍处方高频中药关联分析
2.3 治疗DCD的中药聚类分析
使用SPSS Statistics 25.0统计软件对使用频数大于25次的20味高频中药进行聚类分析。采用组间连接的系统聚类算法,运算后可得到6类,即为DCD的核心配伍药物组合用于临证加减(见图1)。分别是:(1)桃仁、红花、当归、川芎;(2)枸杞子、菟丝子、熟地黄;(3)甘草、白芍、丹参;(4)石菖蒲、远志、黄芪;(5)半夏、白术、茯苓;(6)山药、山茱萸、五味子、麦冬。
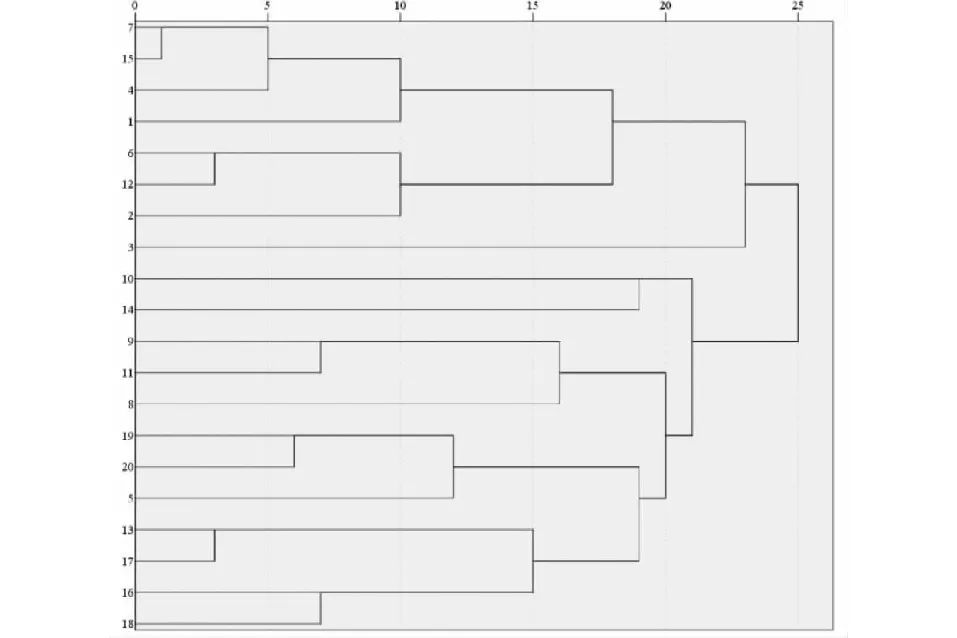
图1 糖尿病认知功能障碍处方中药聚类分析图Fig.1 Cluster analysis of diabetes cognitive dysfunction prescription注:右侧中药材由上至下的顺序为:桃仁、红花、川芎、当归、枸杞子、菟丝子、熟地黄、甘草、白芍、丹参、石菖蒲、远志、黄芪、半夏、白术、茯苓、山药、山茱萸、五味子、麦冬。以下图中数字对应的中药材与图1相一致。Note:The order of Chinese herbal medicines from top to bottom is:Persicae Semen;Carthami Flos;Chuanxiong Rhizoma;Angelicae Sinensis Radix;Lycii Fructus;Cuscutae Semen;Rehmanniae Radix Praeparata;Glycyrrhizae Radix et Rhizoma;Paeoniae Radix Alba;Salviae Miltiorrhizae Radix et Rhizoma;Acori Tataninowii Rhizoma;Polygalae Radix;Astragali Radix;Pinelliae Rhizoma;Atractylodis Macrocephalae Rhizoma;Poria;Dioscoreae Rhizoma;Corni Fructus;Schisandrae Chinensis Fructus;Ophiopogonis Radix.The Chinese herbal medicines corresponding to the numbers in the figures below are the same as those in figure 1.
2.4 治疗DCD的中药因子分析
为了探寻高频中药间潜在的结构关系,运用SPSS Statistics 25.0统计软件对高频中药进行因子分析,通过KMO检验和Bartlet球形检验比较变量间相关系数的差异,结果显示抽样适合性检验KMO=0.600,Bartlet球形检验P=0.000,差异具有显著性P<0.05,认为变量间存在较强的依赖性,符合因子分析标准。采用主成分分析法,设置提取初始特征值大于1,可提取公因子数为8个,累计贡献率为78.53%。设置最小载荷量为0.5,得出桃仁(0.896)、红花(0.861)、川芎(0.841)、当归(0.645)在成分F1上载荷量较高;在成分F2上载荷量前四位为熟地黄(0.755)、枸杞子(0.801)、菟丝子(0.842)、半夏(0.513);五味子(0.701)和麦冬(0.869)在成分F3上载荷量较高;在成分F4上载荷量较高的中药为山药(0.843)、山茱萸(0.876);在成分F5上载荷量较高的中药为石菖蒲(0.856)、远志(0.540)和白芍(0.682);在成分F6上载荷量最高的前三位分别是甘草(0.808)、茯苓(0.565)和白术(0.576);在成分F7-8上载荷最高分别为黄芪(0.815)和丹参(0.904),由此将各成分上载荷量较高的中药提炼为公因子(见表3)。通过kaiser标准化的全体旋转法得到旋转因子载荷图(见图2)。
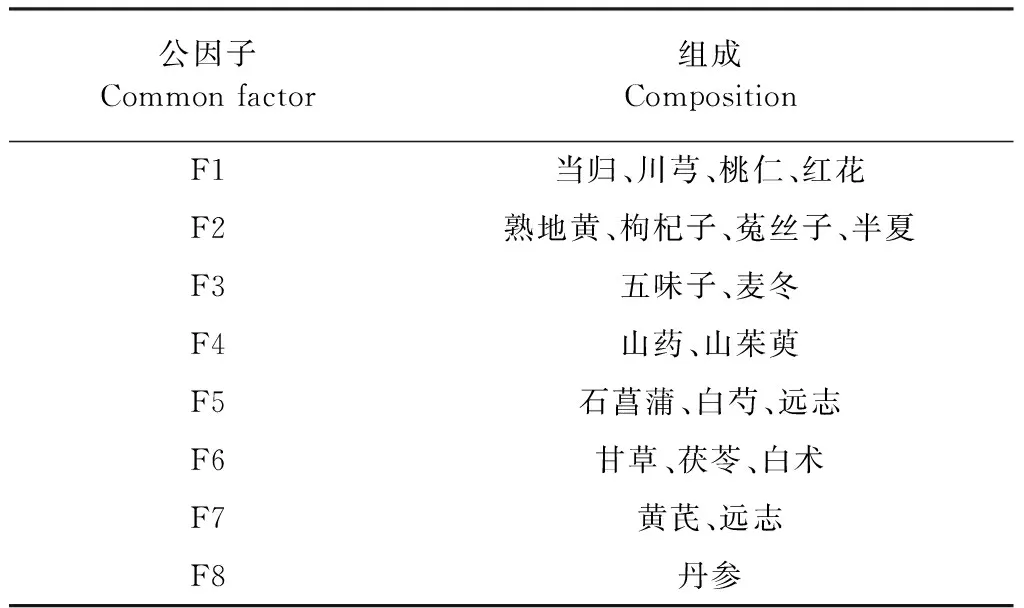
表3 公因子信息表

图2 糖尿病认知功能障碍中药处方旋转因子载荷图Fig.2 Rotational load diagram for prescription factor analysis of diabetic cognitive dysfunction
3 网络药理学结果
3.1 核心组方化学成分筛选
根据关联、聚类和因子分析,综合得到“当归、桃仁、红花、川芎、熟地黄、枸杞子、菟丝子、石菖蒲、白芍”9味中药组成的核心组方。从TCMSP数据库中根据OB、DL值筛选核心组方的潜在活性化学成分共109个(见表4)。

表4 核心组方中109个候选化合物的基本信息

续表4(Continued Tab.4)

续表4(Continued Tab.4)
3.2 DCD疾病靶点筛选
通过OMIM、TTD、PharmGkb和Drugbank数据库分别收集DCD相关靶点基因590、282、44、61个,通过Genecards数据库获得“diabetic cognitive dysfunction”为关键词的靶点5 236个、“diabetic encephalopathy”为关键词的靶点2 556个,将二者靶点合并后去重;relevance score代表靶点与疾病的密切程度,根据其由高到低排序,取前1 000个作为DCD的潜在靶点;经去重后共收集到1 490个DCD疾病相关靶点。
3.3 “核心组方药物-有效成分-靶点-疾病”共有网络的构建
将上述的经剔除无对应靶点的核心组方有效化学成分、重复靶点和疾病的相关靶点导入至Cytoscape 3.8.0软件,构建“核心组方药物-有效成分-靶点-疾病”网络图,其包含了349个节点和1 723条关系(见图3)。网络中节点的大小与度值呈正比关系,其中度值(degree)排在前三位的化合物为槲皮素(quercetin)、山奈酚(kaempferol)和β-谷甾醇(β-sitosterol)。
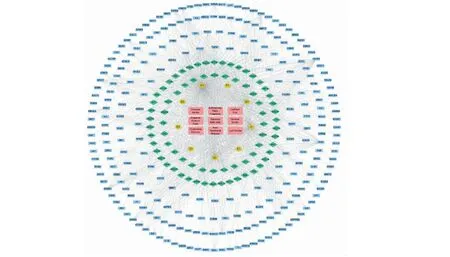
图3 “核心组方药物-有效成分-靶点-疾病”共有网络图Fig.3 Common network of "core prescription drugs-active ingredients-targets-disease"注:蓝色表示疾病靶点;红色表示核心组方中药物名称;绿色表示核心组方有效成分;棕色表示共有化合物成分。Note:The blue section represents the disease target;The red portion represents the core prescription drug;The green portion represents the active ingredient;The brown portion represents a common compound ingredient.
3.4 PPI网络的构建与分析
利用Stitch和String数据库分别获得核心组方和疾病潜在靶点PPI网络;通过Cytoscape 3.8.0软件进行合并,去除19个单独的靶点GABRA2、GABRA5、PLAT、PSMD3、NR3C2、ECE1、GABRA1、G6PD、THBD、CHRNA7、MGAM、DPP4、SCN5A、ADRA2A、ACHE、NR1I3、PTGS1、RXRA、PPP3CA后获得核心组方治疗DCD相关潜在作用靶点76个。运用Cytoscape软件中CytoNCA插件通过对中心网络进行拓扑分析,筛选最终得到24个核心靶点(见图4),其中degree值排名前3位的靶点依次为:TP53、IL6、FOS,由此推测其是作为核心药物治疗DCD中发挥重要作用的关键靶点,将用于后续的分子对接验证。
3.5 关键靶点的代谢通路与生物过程分析
3.5.1 药物-疾病核心靶点GO分析
将获得的核心组方治疗DCD交互的潜在靶点利用DAVID数据库进行GO分析,结果可获得237条GO富集功能,其中生物过程(biological process,BP)相关的条目最多,共183条,23条细胞组成(cellular component,CC)和31条分子生物学功能(molecular function,MF)。以P<0.01,FDR<0.01为筛选条件选取GO条目,其涉及调控糖脂代谢、细胞凋亡、炎症反应、蛋白质磷酸化、蛋白酶结合、血管生成等生物学过程。运用R Studio软件下的“dplyr”“org.Hs.eg.db”和“ggplot2”扩展包对上述的分析结果前20条进行可视化处理(见图5)。

图4 核心组方治疗DCD靶点的PPI网络Fig.4 The core prescription drugs PPI network for the treatment of DCD targets
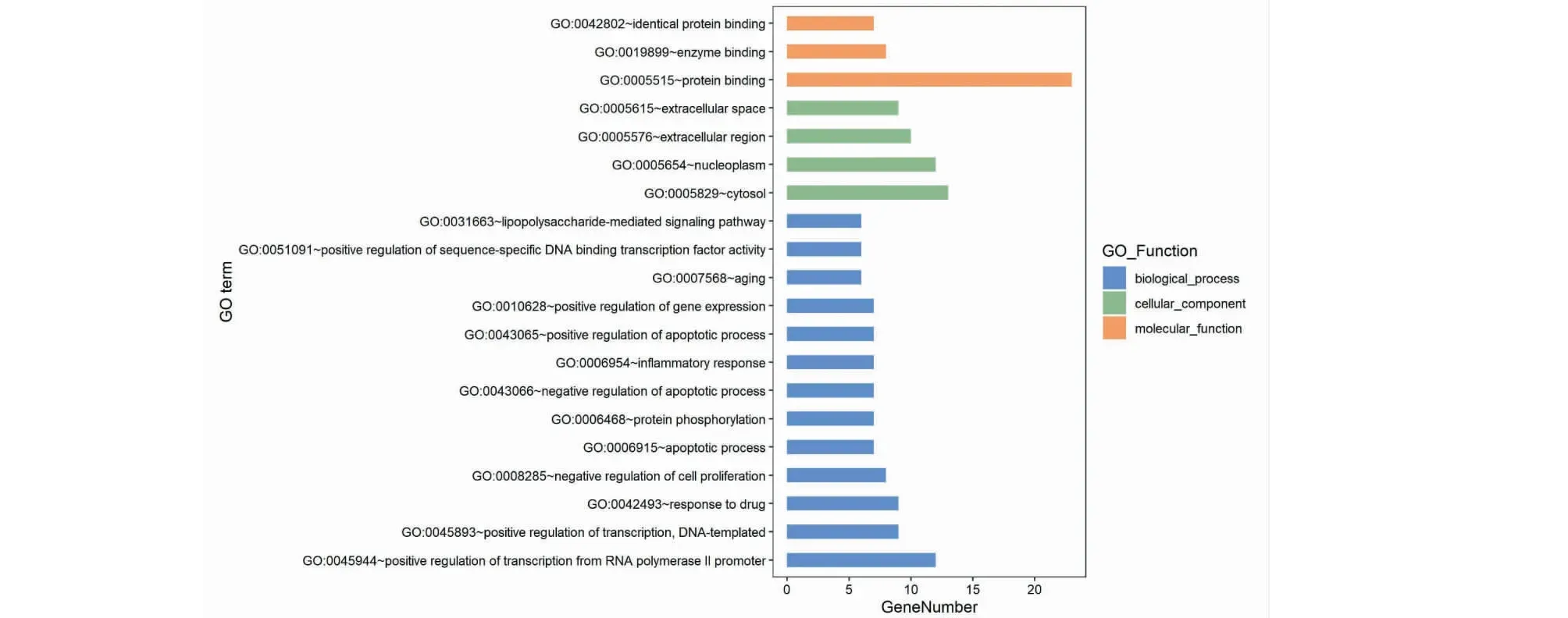
图5 核心组方治疗DCD潜在核心靶点的GO功能分析(前20位)Fig.5 GO function analysis of core prescription drugs for treating DCD potential core targets (Top 20)
3.5.2 药物-疾病KEGG通路富集分析
利用DAVID数据库对核心组方治疗DCD交互的核心靶点进行KEGG通路分析,共获得96条富集通路,以P<0.01,FDR<0.01为筛选条件选取共66条KEGG条目。分析结果提示核心靶点与TNF信号通路、MAPK信号通路、Toll样受体信号通路、FoxO信号通路、HIF-1信号通路、鞘脂信号通路、VEGF信号通路和胰岛素信号通路等有关,与此同时还发现核心靶点与多种癌症、病毒感染性疾病、寄生虫病等存在联系。运用R Studio软件对筛选后的前30条KEGG通路结果进行可视化处理(见图5)。
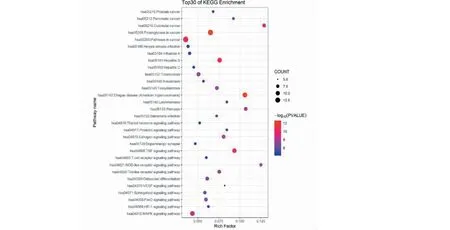
图6 核心组方治疗DCD潜在核心靶点的KEGG富集功能分析(前30位)Fig.6 KEGG enrichment function analysis of core prescription drugs for treating DCD potential core targets (Top 30)
3.6 分子对接验证
通过对核心组方中主要活性成分进行分子对接验证,结果显示,配体小分子均稳定地位于对接口袋内(见表5)。与二甲双胍相比,核心组方的主要活性成分与关键靶点之间对接更为紧密,其中与TP53和FOS结合能最低的活性成分为槲皮素,与IL6结合能最低的活性成分为β-谷甾醇。运用PyMOL作三维图展示槲皮素与配体小分子FOS(PDB ID:1fos)之间的相互作用(见图7)。

表5 核心组方有效成分和二甲双胍与TP53、FOS、IL6分子对接结果

图7 FOS与槲皮素的分子对接模式图Fig.7 Molecular docking diagram of FOS and quercetin
4 讨论与结论
DCD是糖尿病常见的慢性并发症之一,对患者的疾病预后、生活质量造成不良的影响。中医对DCD无专门病名,多将其归于“消渴”“呆病”“痴呆”范畴,现多认为其发病病机为本虚标实,病位在脑,涉及脾、肾等多脏腑。脾失健运,不能游溢精微,积于中焦使其运化机能受损,意舍不清,影响心神[14];病程日久,或因痰蒙神窍,或因瘀血阻络,或因痰瘀毒互结,集聚脑络,脑失所养,导致DCD的发生发展,患者多表现出健忘、精神恍惚、认知减退。病程日久,痰湿、瘀血、浊毒等病理产物相互作用耗损阴阳,终致肾精不足,髓海空虚[15,16]。
前针对DCD尚无明确完善的西医治疗方案,而中医药在治疗DCD方面优势突出,在降低血糖血脂、延缓记忆减退、减轻毒副作用、提高生活质量等方面均取得良好的临床疗效。本研究基于对中医临床处方进行数据挖掘分析,通过频次统计发现DCD用药多为川芎、桃仁、丹参、红花、当归、黄芪、熟地黄等具有活血化瘀、补气补血之味和半夏、石菖蒲、远志等理气化湿、醒神益智之品。活血化瘀与补虚药物性味多甘、温,配伍使用可化脑络瘀阻,调气血通畅,补正气虚损。肝为瘀血生成之枢,善用肝经药物引经报使,行气活血,通利化瘀。理气开窍药与安神药甘苦同用,肺脾同治,气行则湿化,气顺则痰消,则化浊开窍,醒脑通络。关联分析结果提示桃仁-红花、川芎-红花、当归-红花、枸杞子-菟丝子具有高频率和强相关性。聚类分析和因子分析发现,公因子F1、F8(包括桃仁、红花、川芎、当归、丹参)以活血化瘀通络为主,是为“逐瘀汤”的基础,并归气血,养活同施,既可除病因通脑络,又可匡扶正气,主治瘀血所致之证;公因子F2、F4(包括熟地黄、山药、山茱萸、枸杞子、菟丝子等)以补虚为主,其中熟地黄、山药、山茱萸三阴并补,补肾益精,养肝健脾,为“地黄丸”重要组成部分,主治肝肾亏损之证;公因子F2、F3、F5、F6、F7(包括半夏、茯苓、白术、甘草、石菖蒲等)以理气化湿醒脑为主,其中半夏和茯苓相结合,为“二陈汤”的基础,取燥湿散结与利水渗湿之效,主治痰浊所致之证。聚类分析与因子分析结果相似,客观地证明治疗DCD中药配伍有规可循。
根据数据挖掘分析结果得出,当归、桃仁、红花、川芎、熟地黄、枸杞子、菟丝子、石菖蒲、白芍9味药组成的核心组方能从多角度、多维度、多层面反映中医药从“活血化瘀、补肾填髓、开窍醒脑”基本法则治疗DCD。从微观角度,核心组方中槲皮素、山奈酚和β-谷甾醇等化合物发挥了重要的作用。槲皮素不仅能降低胰岛素抵抗和空腹血糖水平,而且可调节海马区SIRT1活性蛋白和NLRP3炎症小体表达,不仅可以缓解内质网应激(endoplasmic reticulum stress,ERS),而且还可抑制海马区异常炎症反应,保护神经元异常退变[17]。山奈酚是一种天然类黄酮化合物,不仅能通过抑制NO降解实现对细胞的抗氧化保护,还可通过调节MAPK、PI3K-Akt通路降低炎症因子表达,抑制内质网过度应激[18]。β-谷甾醇[19]可通过激活胰岛素下游信号分子以降低IRS-1磷酸化,上调IR-1和AKT蛋白的表达,抑制PKCq和NF-κB通路传导,削弱海马区炎症反应。PPI网络及拓扑分析表明,核心组方通过TP53、FOS、IL6、MAPK14、CASP3、ERS1、IL1B等核心靶点治疗DCD的可能性较大,涉及糖脂代谢、血管生成、炎症反应、细胞老化和凋亡等生物学过程。
通过FOS、IL6、IL1B、MAPK14、CASP3等基因可诱导下游转录因子,激活TNF信号通路、MAPK信号通路、Toll样通路、FoxO信号通路发挥作用,使得炎性因子磷酸化以调控细胞炎症反应[20]。这些信号通路不仅与细胞凋亡、炎症反应之间关系紧密,也与ERS和细胞自噬相关。当机体能量供给不足引起内质网平衡紊乱,通过MAPK信号通路、FoxO信号通路多重调节细胞自噬,清除细胞质中的异常蛋白,调控自噬通量,抑制ERS,减少淀粉样蛋白在海马区的异常沉积以保护神经元[21,22]。雌激素信号通路介导多种雌激素核受体抑制海马神经元内部的ERS,维持内质网稳定,阻断Caspase级联反应,调控CASP3基因以保护细胞存活,对认知功能障碍产生一定程度的良性调节[23]。Toll样受体(TLRs)被证明可通过胰岛素信号通路和Toll样通路激活胰岛素下游信号分子,上调胰岛β细胞周围蛋白的活性,调控全身胰岛素敏感性和血脂分布[24]。
通过数据挖掘发现目前中医组方治疗DCD多从行气活血化瘀、化痰醒脑开窍、滋阴填精固肾的大方向入手,从中挖掘出当归-桃仁-川芎、当归-红花-川芎、川芎-红花-桃仁、熟地黄-菟丝子-枸杞子等核心药物配伍,为日后临床应用提供宝贵治疗经验和参考;基于网络药理学对中医治疗DCD遣方用药中的核心组方潜在作用机制进行初步分析,由此对中医医家治疗疾病过程中所用的药物给出科学的解释。同时,本研究还存在一定的不足和缺陷,包括纳入中医临床处方数量有限、文献质量参差不齐等,数据挖掘和网络药理学尚停留于理论层面,对核心药物有效成分作用DCD的具体作用机制还需进一步的基础实验加以验证。
