苗药芭蕉根化学成分研究(Ⅲ)*
2021-08-05黄鸿运杨贵香李勇军
黄鸿运,蒋 礼,杨贵香,汪 洋,马 雪,潘 洁,李勇军△
(1.贵州医科大学民族药与中药开发应用教育部工程研究中心·省部共建药用植物功效与利用国家重点实验室,贵州 贵阳 550004; 2.贵州医科大学药学院,贵州 贵阳 550004; 3.贵州医科大学贵州省药物制剂重点实验室,贵州 贵阳 550004)
芭蕉根是芭蕉科植物芭蕉Musa basjooSieb.et Zucc的干燥根茎,味甘、性大寒、无毒,是贵州苗族的习用药材[1],收载于2003年版《贵州省中药材·民族药材质量标准》。《本草备要》中记载,芭蕉根捣汁温服可治疗产后血胀,取其汁液可涂于疮口。芭蕉根的化学成分丰富,含苯醌、蒽醌、香豆素等成分[2-4]。研究表明,芭蕉根在抗炎、镇痛、抑菌等方面均有一定作用[5-6]。为进一步利用芭蕉根药材,提升其质量控制标准,探讨其药效物质基础,课题组在前期研究[2,7]的基础上,继续分离、鉴定了7个化学成分。现报道如下。
1 仪器与试药
1.1 仪器
ACQUITY-TQD型质谱仪(美国Waters公司);BUCHI R-200型旋转蒸发仪(瑞士Buchi公司);JEOL-ECS-400 MHz型核磁共振波谱仪(日本电子株式会社)。
1.2 试药
D101型大孔树脂、柱层析硅胶及硅胶GF254预制板(青岛海洋化工有限公司);Sephadex LH-20型凝胶(瑞士Pharmacia Biotech公司);Toyopearl HW-40C型凝胶、Toyopearl HW-40F型凝胶(日本东曹株式会社);试验所用试剂均为分析纯,水为纯化水。芭蕉根药材于2016年购自云南,经贵州医科大学龙庆德副教授鉴定为正品,标本保存于贵州医科大学贵州省药物制剂重点实验室。
2 方法与结果
2.1 提取分离
取干燥的芭蕉根药材,粉碎成粗粉,取20 kg,用70%乙醇回流提取3次,每次1.5h,第1次、第2次用7倍量溶剂,第3次用5倍量溶剂,合并3次的提取液,减压回收溶剂,挥至无醇味,得浸膏(1 129.2 g),过D101型大孔吸附树脂,以水、50%乙醇、95%乙醇依次洗脱。
50%乙醇段(42.0 g)采用正相硅胶柱分离,以二氯甲烷-甲醇(15∶1→1∶1,V/V)为流动相进行梯度洗脱,经薄层色谱(TLC)分析、合并相似流分,得10个组分(Fr.1~Fr.10)。
Fr.1采用正相硅胶柱分离,以石油醚-乙酸乙酯(9∶1→5∶5,V/V)为流动相进行梯度洗脱,经TLC分析、合并后浓缩,得2个组分(Fr.1.1~1.2)。Fr.1.1采用正相硅胶、Sephadex LH-20型凝胶等填料进行反复柱色谱分离;经TLC分析、合并后浓缩,得化合物1(10.0 mg)。Fr.1.2采用Toyopearl HW-40F型凝胶(甲醇)、Sephadex LH-20型凝胶(氯仿-甲醇,1∶1,V/V)等填料反复柱层析,得化合物2(1.2 mg)。
Fr.4采用正相硅胶柱,以石油醚-氯仿(5∶1,V/V)洗脱,经TLC分析、合并后浓缩,得3个组分(Fr.4.1~4.3)。Fr.4.2采用Toyopearl HW-40C型凝胶柱(氯仿-甲醇,1∶1,V/V),Toyopearl HW-40F型凝胶柱(甲醇)等填料进行反复柱层析,经TLC分析、合并后浓缩,得化合物3(2.6 mg)。Fr.4.3采用正相硅胶、Sephadex LH-20型凝胶(甲醇)、Toyopearl HW-40F型凝胶(甲醇)等填料分离,经TLC分析、合并后浓缩,得化合物4(18.3 mg)。
Fr.8采用Toyopearl HW-40 C型凝胶柱(氯仿-甲醇,1∶1,V/V),经TLC分析、合并后浓缩,得2个组分(Fr.8.1~8.2)。Fr.8.2采用Sephadex LH-20型凝胶柱(氯仿-甲醇,1∶1,V/V),Toyopearl HW-40C型凝胶柱(氯仿-甲醇,1∶1,V/V),Toyopearl HW-40F型凝胶柱(甲醇)分离,经TLC分析、合并后浓缩,得化合物5(68.3 mg)。
Fr.10采用Sephadex LH-20型凝胶柱(甲醇)、Toyopearl HW-40F型凝胶柱(甲醇)、ODS反相(甲醇-水)分离,经TLC分析、合并后浓缩,得化合物6(11.8 mg)、化合物7(9.8 mg)。
2.2 结构鉴定
2.2.1 化合物1
C31H50O。白色粉末。1H-NMR(400 MHz,CDCl3)δ:4.63(2H,brs,H-27),2.38(2H,m,H-2),2.20(1H,m,H-4),0.96(3H,s,H-18),0.87(3H,s,H-30),0.84(3H,dd,J=6.5 Hz,H-21),0.58(1H,d,J=4.2 Hz,H-19),0.36(1H,d,J=4.2 Hz,H-19);13C-NMR(100MHz,CDCl3)δ:32.8(C-1),41.0(C-2),213.4(C-3),50.0(C-4),47.1(C-5),25.9(C-6),25.2(C-7),46.0(C-8),24.9(C-9),29.2(C-10),27.0(C-11),32.7(C-12),45.3(C-13),48.7(C-14),35.4(C-15),27.1(C-16),52.1(C-17),18.3(C-18),28.0(C-19),36.0(C-20),17.9(C-21),33.8(C-22),31.4(C-23),41.6(C-24),150.1(C-25),19.1(C-26),109.4(C-27),10.7(C-28),18.6(C-29),20.2(C-30)。以上数据与文献[8]的报道基本一致,故鉴定该化合物1为cyclomusalenone。
2.2.2 化合物2
C32H52O5。无色针状。1H-NMR(400 MHz,pyridined5)δ:4.69(1H,dt,J=11.5,4.0 Hz,H-3),3.38(1H,td,J=14.41,3.0 Hz,H-19),2.58(1H,dd,J=14.0,3.4 Hz,H-7),1.83(3H,d,J=3.4 Hz,H-6),1.37(2H,m,H-22),1.21(2H,m,H-21);13C-NMR(100 MHz,pyridine-d5)δ:38.3(C-1),23.9(C-2),80.5(C-3),37.9(C-4),55.1(C-5),18.6(C-6),38.1(C-7),44.8(C-8),46.1(C-9),37.8(C-10),39.1(C-11),210.5(C-12),85.8(C-13),51.0(C-14),66.6(C-15),43.9(C-16),35.0(C-17),51.5(C-18),35.1(C-19),31.7(C-20),34.5(C-21),39.5(C-22),27.9(C-23),16.7(C-24),15.9(C-25),20.4(C-26),14.4(C-27),31.9(C-28),32.2(C-29),25.8(C-30),21.1(Ac-Me),170.6(Ac-CO)。以上数据与文献[9]的报道基本一致,故鉴定化合物2为rubiprasin A。
2.2.3 化合物3
C6H10。淡黄色固体。1H-NMR中δH1.66(3H,s,H-6)为甲基质子信号;δH1.23(2H,s,H-4),2.02(4H,s,H-3,5)为亚甲基质子;δH5.07(1H,s,H-2)为双键质子信号。13C-NMR中δC26.4(C-3),29.7(C-4),32.2(C-5)为亚甲基碳信号;δC23.4(C-6)为甲基碳信号;δC125.0(C-2)和135.2(C-1)为双键碳信号;由于未找到化合物的核磁数据,根据二维波谱数据(HMQC,HMBC)归属该化合物各碳氢信号(见表1),在HMBC重要相关中,δH1.66(3H,s,H-6)甲基氢信号与δC135.2(C-1),125.0(C-2),32.2(C-5)碳信号存在远程相关和δH5.07(1H,s,H-2)双键质子信号与δC26.4(C-3),32.2(C-5),可见甲基连接在C-1碳上。再由分子量和已知的结构片段可知该化合物除以上所述片段外再无其他结构片段,由此将各基团进行连接。综合上述分析,化合物3的结构鉴定为1-甲基-环戊烯。化合物3的重要相关HMBC图见图1。

表1 化合物3的1H-NMR(400 MHz,CDCl3)和13C-NMR(100 MHz,CDCl3)数据Tab.1 1H-NMR(400 MHz,CDCl3)data and 13C-NMR(100 MHz,CDCl3)data of compound 3
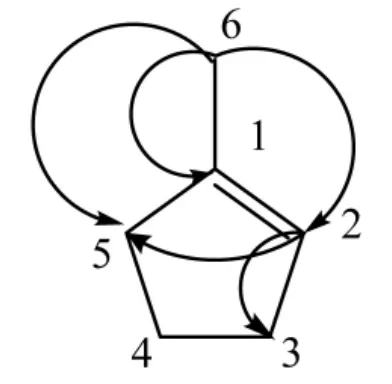
图1 化合物3的重要相关HMBC图Fig.1 Important related HMBC spectra of compound 3
2.2.4 化合物4
C14H20O9。白色粉末。1H-NMR(400 MHz,CD3OD)δ:6.11(2H,s,H-3,5),4.66(1H,d,J=6.8 Hz,H-1′),3.84(1H,m,H-5′),3.78(6H,s,2,6-OCH3),3.66(1H,dd,J=12.0,5.2 Hz,H-6′),3.19(1H,m,H-3′);13C-NMR(100 MHz,CD3OD)δ:129.5(C-1),154.7(C-2,6),94.3(C-3,5),156.0(C-4),106.1(C-1′),75.7(C-2′),78.2(C-3′),71.2(C-4′),77.7(C-5′),62.5(C-6′),56.7(2,6-OCH3)。以上数据与文献[10]的报道基本一致,故鉴定化合物4为leonuriside A。
2.2.5 化合物5
C19H12O2。红色针状。1H-NMR(400 MHz,CDCl3)δ:8.23(1H,d,J=8.3 Hz,H-7),7.94(1H,dd,J=8.0,1.2 Hz,H-6),7.73(1H,dd,J=7.3,1.0 Hz,H-4),7.60(1H,m,H-5),7.59(1H,d,J=8.3 Hz,H-8),7.48(3H,m,H-3′,5′,4′),7.36(2H,m,H-2′,6′),7.12(1H,s,H-3);13C-NMR(100 MHz,CDCl3)δ:180.5(C-1),150.0(C-2),113.0(C-3),131.8(C-3a),131.0(C-4),131.3(C-5),130.0(C-6),129.0(C-6a),135.9(C-7),127.2(C-8),149.3(C-9),125.2(C-9a),123.8(C-9b),142.6(C-1′),128.5(C-2′,6′),128.0(C-3′,5′),127.8(C-4′)。以上数据与文献[11]的报道基本一致,故鉴定化合物5为2-hydroxy-9-phenyl-phenalen-1-one。
2.2.6 化合物6
C15H12O5。紫红色固体。1H-NMR(400 MHz,CD3OD)δ:9.65(1H,s,H-10),6.28(2H,m,H-4,6),6.90(1H,d,J=8.0 Hz,H-7),6.87(1H,s,H-2′),6.74(2H,d,J=8.0 Hz,H-5′,6′),5.19(1H,s,H-2);13C-NMR(100 MHz,CD3OD)δ:104.7(C-2),115.2(C-4),130.6(C-5),126.6(C-6),116.2(C-7),147.0(C-8),153.6(C-9),193.2(C-10),146.5(C-1′),114.7(C-2′),145.9(C-3′),131.0(C-4′),115.8(C-5′),119.5(C-6′)。以上数据与文献[12]的报道基本一致,故鉴定化合物6为2-(3′,4′-二羟基苯基)-1,3-苯并二茂恶-5-甲醛。
2.2.7化合物7
C13H8O2。橘黄色粉末。1H-NMR(400 MHz,CD3COCD3)δ:8.65(d,J=7.6 Hz,H-9),8.44(d,J=8.0 Hz,H-7),8.07(d,J=7.6 Hz,H-6),7.89(1H,t,dd,J=8.0,7.6 Hz,H-8),7.85(1H,d,J=7.2 Hz,H-4),7.66(1H,t,dd,J=7.6,7.2 Hz,H-5),7.20(1H,s,H-3);13C-NMR(100 MHz,CD3COCD3)δ:180.4(C-1),149.5(C-2),136.6(C-7),132(C-6a),131.1(C-9),130.5(C-4),129.8(C-6),128.3(C-3a),127.4(C-9a),127.2(C-5),126.8(C-8),124.4(C-9b),113.9(C-3)。以上数据与文献[13]的报道基本一致,故鉴定化合物7为2-hydroxy-1Hphenalen-1-one。
3 讨论
芭蕉可药食两用。研究发现,芭蕉花石油醚提取物中石油醚和乙酸乙酯萃取部位可抑制肝癌细胞的增殖[14];芭蕉茎中羽扇豆酮的含量明显高于芭蕉根茎和叶,故可以芭蕉茎替代根茎作为羽扇豆酮的原材料来源[15]。将芭蕉根与酢浆草、补骨脂等药材配伍,研发了“骨康胶囊”“肿痛舒喷雾剂”等中成药制剂[16],用于治疗骨质疏松和骨折[17]及化肿消瘀等[16-17]。目前,对于芭蕉发挥药效的物质基础尚不明确,对其作用机制研究较少,本研究中在课题组前期研究的基础上,继续分离得到7个化合物,其中化合物4,7为首次从芭蕉根中分离得到,化合物2,3,6为首次从该属植物中分离得到,化合物3首次归属了其碳氢波谱数据。
综上所述,本研究丰富了芭蕉根化学成分,可为芭蕉根的进一步研究提供参考。
