乳腺癌根治术后放疗靶区外放边界的分析及验证
2021-08-03申正文李师谭霞田秀梅罗焕丽靳富万跃
申正文,李师,谭霞,田秀梅,罗焕丽,靳富,万跃
重庆大学附属肿瘤医院肿瘤放射治疗中心,重庆400030
前 言
精准放疗技术是在保证靶区接受高剂量照射的同时,尽量减少周围正常组织受到的照射剂量。目前肿瘤放射治疗已经广泛采用调强放射治疗(Intensity‐Modulated Radiotherapy,IMRT)技术,但是IMRT技术对摆位的精度要求更高。影像引导放射治疗(Image‐Guided Radiotherapy,IGRT)技术的出现有利于开展精准放疗,IGRT可以在治疗过程中确定肿瘤位置及分次间的变化[1]。由于摆位误差、器官运动、几何形变等原因,为了保证处方剂量覆盖足够的肿瘤靶区,需要在临床靶区(Clinical Target Volume,CTV)周围外放足够的边界得到计划靶区(Planning Target Volume,PTV),边界过大会增加正常组织受照剂量,边界过小又不能保证足够的靶区覆盖。采用IGRT技术可以减少摆位误差,最大限度地减少CTV到PTV的外放边界[2‐3]。
由于各放疗中心设备或软件不同、质控水平差异以及技师的摆位标准不一致等,各中心的摆位误差都有所差别[4‐9]。针对本中心所开展的放疗技术、治疗技师摆位水平等情况不同,特别是肿瘤部位的不同,计算出适合的靶区外放边界,具体问题具体分析。胸部肿瘤受呼吸运动影响大,腹部肿瘤受呼吸运动影响小,但受胃肠蠕动、膀胱充盈程度影响大,所以胸、腹部的外放边界最好能区分开来。乳腺癌患者的肿瘤靶区运动幅度较大,上臂的运动会影响乳房肌肉,摆位难度较大。带有IGRT 功能的直线加速器可以通过采集锥形束CT(Cone Beam CT,CBCT)图像,与计划CT 图像配准得到摆位误差,通过调整治疗床减小摆位误差。本研究利用CBCT 采集的乳腺癌根治术后体膜固定下的摆位误差进行分析,确定合适的外放值。通过在治疗计划系统(Treatment Planning System, TPS)中模拟摆位误差,比较剂量学差异,对此外放值的合理性进行验证。
1 材料与方法
1.1 患者基本情况
随机选取2020年4~9月于重庆大学附属肿瘤医院放射治疗中心接受乳腺癌根治术后放疗的患者40例,其中左乳腺癌20 例,右乳腺癌20 例。体位均为仰卧位,双手抱肘放于额前,热塑体膜固定。使用荷兰飞利浦公司Big Bore大孔径CT模拟定位机对患者行CT 扫描,扫描层厚为5 mm。在美国瓦里安公司(Varian)Eclipse TPS 上,由医师勾画靶区和危及器官,物理师制定计划,采用6 MV X 射线IMRT 滑窗技术,处方剂量为50 Gy/25 F。所有治疗计划均在Varian IX直线加速器上执行。
1.2 图像引导放疗
采用CBCT进行位置验证,患者在放疗期间每周行1 次CBCT,共5 次。在放疗前按患者体表标记摆位,利用Varian IX 加速器CBCT 扫描,获取患者影像,与计划CT 影像进行配准。采用自动算法配准,自动配准后根据骨性标志和靶区的形状位置进行手动微调,直至结果满意为止。记录患者左右、头脚、腹背3个方向的摆位误差,移动加速器治疗床修正摆位误差后进行治疗。
1.3 外扩边界计算
摆位误差可分为系统误差和随机误差。系统误差用分次治疗误差的平均值Σ表示,随机误差用分次治疗误差的标准差σ表示。根据Van Herk 提出的PTV 外放边界公式M=2.5Σ+0.7σ计算外放边界[10]。此经验公式考虑了系统误差和随机误差,保证90%的患者95%的处方剂量包全CTV。
1.4 模拟摆位误差
根据计算得到的外放值,外扩本研究所选取40例患者的CTV,生成新的PTV,重新制作计划,命名为标准计划Plan_O。通过下述3种方式,在TPS中模拟摆位误差。A:根据5次摆位误差的平均值移动治疗等中心,直接获得新的剂量分布;B:因患者每周行1次CBCT,1周5次计划为1组,将5次摆位误差分别带入到每组计划中计算剂量分布,最后叠加获得总剂量分布;C:将标准计划的等中心分别向左、右、头、脚、腹、背各方向移动1、3、5 mm,获得各方向不同大小摆位误差下的剂量分布。将它们分别命名为模拟计划Plan_A、Plan_B、Plan_C。因为模拟计划只改变了患者的治疗中心,没有重新优化,其它所有条件与标准计划保持不变,所以剂量分布的变化反映了因摆位误差产生的剂量分布变化。
1.5 评价剂量变化
比较Plan_O 和Plan_A、Plan_B 之间靶区和危及器官的剂量学差异。所选择比较参数包括:CTV 和PTV 的95%和98%体积的受照射剂量D95和D98、最大剂量Dmax、最小剂量Dmin、平均剂量Dmean;患侧肺的V5(受到5 Gy 及以上照射的体积百分比,其他以此类推)、V20、V30、Dmean;患侧肱骨头的Dmean;对侧乳腺的Dmax、Dmean;心 脏 的V30、V40、Dmean;脊髓的Dmax。以Plan_O 的剂量分布为基准,计算Plan_C 的γ 通过率。γ 通过率被广泛地应用于IMRT 计划验证[11‐12],它包括了百分剂量差异(Dose Difference, DD)和一致性距离(Distance To Agreement, DTA)。美国医学物理师协会TG‐218 报告推荐在DD=3%和DTA=2 mm 的条件下,计划的γ通过率应大于95%[13]。
1.6 统计学方法
采用SPSS 25.0统计学软件对实验数据进行配对t检验,P<0.05为差异有统计学意义。
2 结果
2.1 摆位误差
每位患者每周行1次CBCT,40位患者共拍摄200套CBCT影像。统计得到左右、头脚、腹背方向的摆位误差为(2.09±2.48)、(2.57±2.52)和(2.88±2.54)mm,其中左乳腺癌和右乳腺癌患者在3 个方向的摆位误差相近(表1)。
表1 左右乳腺癌患者各方向摆位误差比较(mm,± s)Tab.1 Setup errors of patients with left-sided or rightsided breast cancer(mm,Mean±SD)
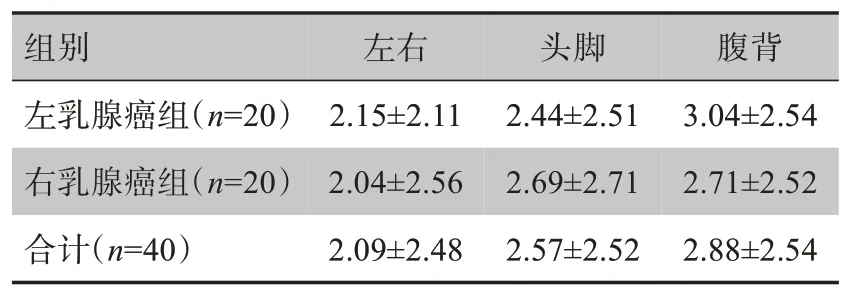
表1 左右乳腺癌患者各方向摆位误差比较(mm,± s)Tab.1 Setup errors of patients with left-sided or rightsided breast cancer(mm,Mean±SD)
组别左右头脚腹背左乳腺癌组(n=20)右乳腺癌组(n=20)合计(n=40)2.15±2.11 2.04±2.56 2.09±2.48 2.44±2.51 2.69±2.71 2.57±2.52 3.04±2.54 2.71±2.52 2.88±2.54
2.2 外扩边界
根据靶区边界外放公式M=2.5Σ+0.7σ计算出各方向上靶区边界的外放值,在左右、头脚、腹背方向的M值分别为6.24、7.99、7.17 mm(表2)。因左右乳腺癌患者摆位误差接近,所以采用同样的外放值。

表2 由摆位误差计算不同方向的外放值(mm)Tab.2 Margins in different directions computed by setup errors(mm)
2.3 .剂量影响
在TPS 中采用A 和B 两种方式模拟摆位误差,Plan_O 和Plan_A、Plan_B 之间靶区和危及器官的剂量学差异分别见表3。采用C 方式模拟摆位误差,Plan_C的γ通过率(3%/2 mm)见表4。
表3 摆位误差对靶区剂量的影响(± s)Tab.3 Dosimetric effects of setup errors on target areas(Mean±SD)
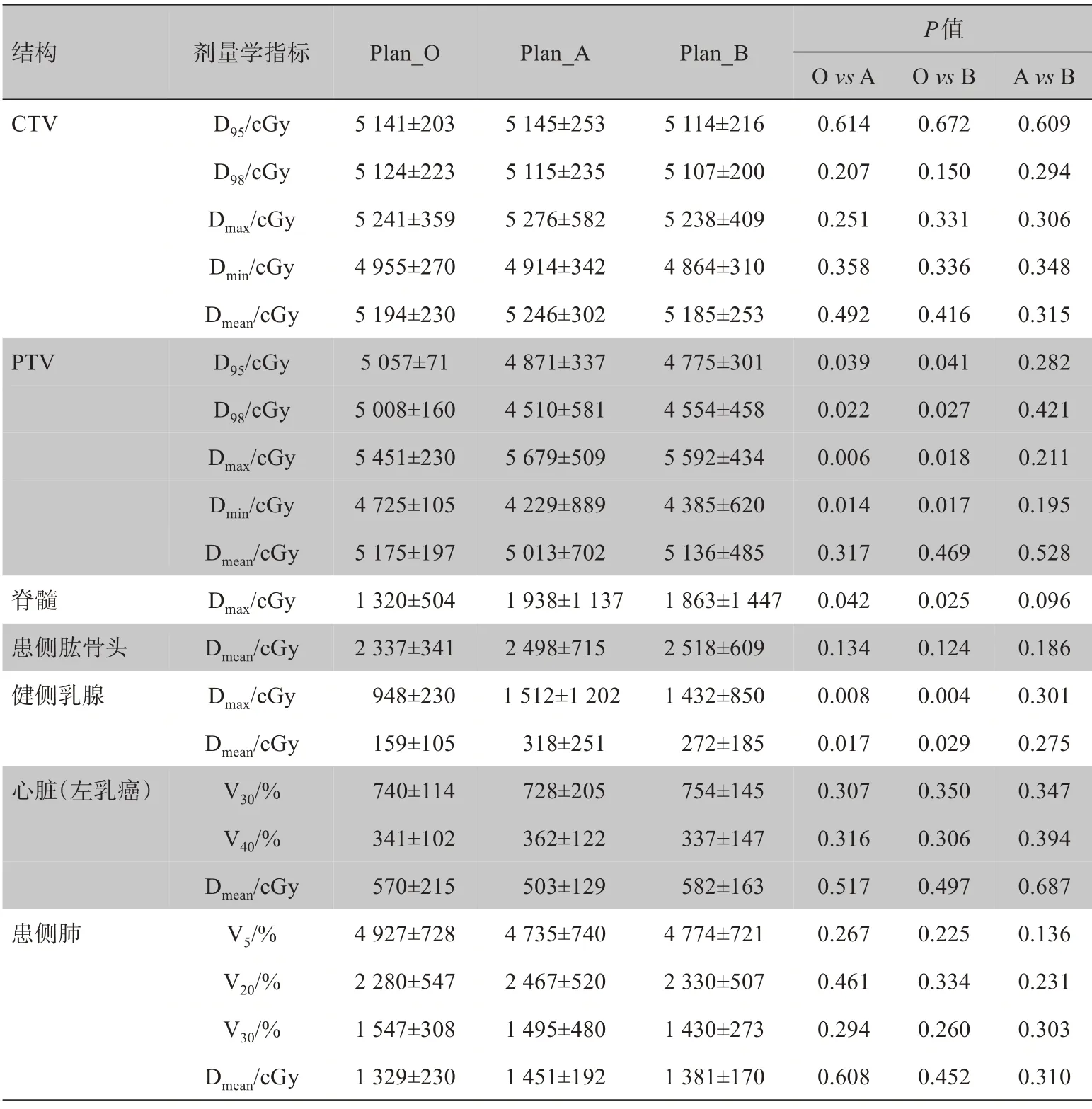
表3 摆位误差对靶区剂量的影响(± s)Tab.3 Dosimetric effects of setup errors on target areas(Mean±SD)
结构剂量学指标Plan_O P值Plan_A Plan_B CTV PTV脊髓患侧肱骨头健侧乳腺心脏(左乳癌)患侧肺D95/cGy D98/cGy Dmax/cGy Dmin/cGy Dmean/cGy D95/cGy D98/cGy Dmax/cGy Dmin/cGy Dmean/cGy Dmax/cGy Dmean/cGy Dmax/cGy Dmean/cGy V30/%V40/%Dmean/cGy V5/%V20/%V30/%Dmean/cGy 5 141±203 5 124±223 5 241±359 4 955±270 5 194±230 5 057±71 5 008±160 5 451±230 4 725±105 5 175±197 1 320±504 2 337±341 948±230 159±105 740±114 341±102 570±215 4 927±728 2 280±547 1 547±308 1 329±230 5 145±253 5 115±235 5 276±582 4 914±342 5 246±302 4 871±337 4 510±581 5 679±509 4 229±889 5 013±702 1 938±1 137 2 498±715 1 512±1 202 318±251 728±205 362±122 503±129 4 735±740 2 467±520 1 495±480 1 451±192 5 114±216 5 107±200 5 238±409 4 864±310 5 185±253 4 775±301 4 554±458 5 592±434 4 385±620 5 136±485 1 863±1 447 2 518±609 1 432±850 272±185 754±145 337±147 582±163 4 774±721 2 330±507 1 430±273 1 381±170 O vs A 0.614 0.207 0.251 0.358 0.492 0.039 0.022 0.006 0.014 0.317 0.042 0.134 0.008 0.017 0.307 0.316 0.517 0.267 0.461 0.294 0.608 O vs B 0.672 0.150 0.331 0.336 0.416 0.041 0.027 0.018 0.017 0.469 0.025 0.124 0.004 0.029 0.350 0.306 0.497 0.225 0.334 0.260 0.452 A vs B 0.609 0.294 0.306 0.348 0.315 0.282 0.421 0.211 0.195 0.528 0.096 0.186 0.301 0.275 0.347 0.394 0.687 0.136 0.231 0.303 0.310
表4 不同摆位误差下模拟计划的γ通过率(%,± s)Tab.4 Gamma passing rates of simulation plans with different setup errors(%,Mean±SD)
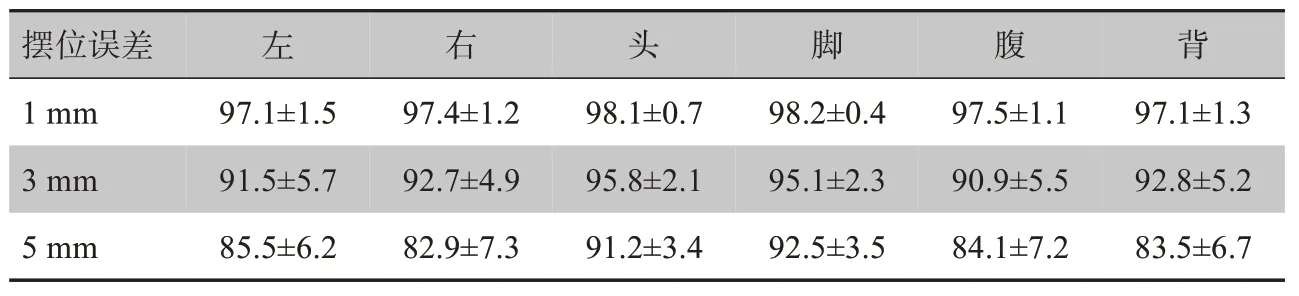
表4 不同摆位误差下模拟计划的γ通过率(%,± s)Tab.4 Gamma passing rates of simulation plans with different setup errors(%,Mean±SD)
摆位误差左右头脚腹背1 mm 3 mm 5 mm 97.1±1.5 91.5±5.7 85.5±6.2 97.4±1.2 92.7±4.9 82.9±7.3 98.1±0.7 95.8±2.1 91.2±3.4 98.2±0.4 95.1±2.3 92.5±3.5 97.5±1.1 90.9±5.5 84.1±7.2 97.1±1.3 92.8±5.2 83.5±6.7
3 讨论
利用CBCT采集患者治疗前的影像,与体位固定影像配准,通过移动治疗床,可以校准摆位误差。摆位误差与体位固定方式有关。本中心乳腺癌根治术后放疗体位固定采用的是热塑体膜固定。统计分析摆位误差发现热塑体膜固定方式与文献[14‐15]报道的采用乳腺托架和真空垫固定方式无明显差别。目前乳腺癌根治术后放疗采用的体位固定方式主要有热塑体膜、乳腺托架和真空垫3 种,每种固定方式都存在一定程度的缺点:热塑膜会增加皮肤反应而且牵拉会导致乳腺变形,乳腺托架会增加颈部旋转和下颌抬高角度的不确定性,真空垫可能因破损漏气产生变形。
放疗患者治疗中的摆位误差是影响放疗计划精确实施的关键因素。摆位误差决定了PTV 的外放大小,如果从CTV到PTV外扩范围过大,周围正常组织受到过量照射,会增加正常组织并发症概率,外扩范围过小,肿瘤受到的照射剂量会不足,使肿瘤局部控制率下降。靶区外放边界的计算方法有很多,各计算方法的原理和应用场景也相同,其中Van Herk 提出的靶区边界外放计算公式得到了最广泛的认可。Van Herk 研究表明摆位误差包括系统误差和随机误差:系统误差在放疗过程中是不变的,主要包括模拟定位系统的扫描误差和机械误差、加速器的机械误差以及激光灯的误差等;随机误差是指患者分次间治疗体位重复的差异性,主要包括技师的摆位操作、患者器官运动等产生的差异,随机误差虽不能完全消除,但可以尽量减小[16‐17]。
目前研究摆位误差对剂量分布的影响主要有以下几种方式:利用IGRT 采集到的各分次摆位误差,取其平均值带入TPS 重新计算,观察剂量学差异[18];将各分次摆位误差分别带入TPS,重新计算后进行叠加比较剂量学差异[19];在TPS 中模拟不同大小的摆位误差来分析摆位误差对靶区及危及器官的剂量学影响[20];将IGRT 采集到的影像回传TPS,与定位CT进行形变配准得到实际照射剂量,比较剂量学差异[21]。本研究模拟方式A 根据5 次CBCT 摆位误差的平均值移动治疗等中心作为模拟计划,与文献[18]类似。但是由于剂量累积与等中心的偏差并非线性关系,所以笔者还采用了模拟方式B,与文献[19]类似,生成每次摆位误差的模拟剂量分布,然后叠加各分次剂量。本文对这两种模拟方式得出的剂量分布进行了比较,发现PTV 的D95、D98、Dmax、Dmin有统计学差异,其他剂量学参数没有统计学差异。另外与文献[20]类似,模拟了不同方向和大小的摆位误差,但与其不同的是采用计算模拟计划Plan_C 的γ通过率比较剂量分布差异,笔者发现左右和腹背方向的摆位误差对剂量分布的影响大于头脚方向;摆位误差超过3 mm以后对剂量分布会产生明显影响。
观察摆位误差对剂量分布的影响最准确的方法是患者在每次治疗前都利用CBCT进行位置验证,将每次的摆位误差带入TPS重新计算出每次的剂量,把各分次的剂量叠加得到实际的剂量分布,而且有研究已经表明患者每次治疗前行CBCT 验证校准摆位误差,得到的实际剂量分布优于每周行1 次CBCT[22]。但是考虑到患者承受的额外辐射剂量和经济负担,以及加速器机房的治疗效率,本中心的CBCT 引导频率为每周1 次,略显不足。临床上通常选择每周行1~2 次CBCT 或者前3~5 次治疗都行CBCT,校准摆位误差后再每周行1次CBCT。
放射治疗中3%~5%的剂量改变就会导致肿瘤局控率下降以及正常组织并发症概率增加。精确放疗的根本目的就是在保证靶区接受足量照射的同时,最大限度降低危及器官的受量。临床上通常将CTV外扩一定距离形成PTV,从而保证CTV 接受足量照射。根据回顾性分析摆位误差计算出的靶区外放边界来指导外扩CTV,在实际治疗时的摆位误差是否会影响CTV 接受足量照射是本研究的主要目的之一。本研究采用了3种不同的模拟摆位误差方式,观察它们对剂量分布的影响。结果显示标准计划Plan_O 和模拟计划Plan_A、Plan_B 之间CTV 的各项剂量学指标无显著差别,但PTV 的各项剂量学指标,除Dmean外都有显著变化,说明摆位误差对于PTV 剂量的影响显著。在危及器官方面,模拟的摆位误差对于肺、心脏、肱骨头的剂量学影响都无显著差别,但脊髓、健侧乳腺受量受摆位误差影响显著。
综上,根据治疗前由CBCT 采集到的摆位误差,计算出CTV 外扩至PTV 的外放边界为8 mm,在此外放边界下模拟摆位误差,CTV 的各项剂量学指标无统计学差异,可以用于指导本中心乳腺癌根治术后的靶区外扩。但摆位误差对PTV、脊髓和对侧乳腺的剂量有较大影响,左右和腹背方向的摆位误差对剂量分布的影响大于头脚方向,当摆位误差超过3 mm就会对剂量分布产生明显影响,必须对摆位误差进行修正。
