BiPAP压力滴定及Auto-CPAP在治疗重叠综合征合并呼吸衰竭的疗效观察
2021-08-03李玉静
王 亮,李玉静,杨 超,孟 静
(1.河北省胸科医院呼吸与危重症医学科,河北 石家庄 050041;2.河北省胸科医院检验科;3.石家庄市第二医院妇产科)
慢性阻塞性肺疾病(chronic obstructive pulmoriary disease,COPD)在老年群体中常见,部分病人可合并阻塞性睡眠呼吸暂停综合征(obstructive Sleep Apnea Syndrome,OSAS),临床称之位重叠综合征(overlap Syndrome,OS)。无创正压通气是治疗OS的主要手段,COPD病人常选用双水平正压通气(bilevel positive airway pressure,Bi PAP)模式治疗,而OSAS病人则更倾向于选用自动压力模式持续气道正压通气(auto-continuous positive airway pressure,Auto-CPAP)[1]。BiPAP可使吸气相和呼气相均保持一定压力,有利于改善通气及促进O2和CO2在肺泡内的交换,在改善OS所诱发的Ⅱ型呼吸衰竭上优势明显[1,2]。Auto-CPAP是一种单行正压通气呼吸模式,根据实际需要自动进行压力调节,能够感知病人的呼吸事件,电子压力调控设备会自动调高所输出的压力水平,直到病人的呼吸相关事件被清除或达到预先设置的最高水平[3]。要想实现最佳通气,呼吸机的模式选择及压力设定尤为关键;目前,BiPAP模式常用采用人工压力滴定的方法确定压力[1,4],而Auto-CPAP则根据病人需要自动设定所需压力[1,3]。那么,上述两种通气模式在治疗OS上否存在疗效差异呢?目前尚未形成统一结论。为此,本研究选取110例OS伴呼吸衰竭的病人,按照呼吸机正压通气模式分为两组,进而明确不同通气模式是否会对临床疗效产生影响。
1 资料与方法
1.1 一般资料
选取2018-06~2020-10在河北省胸科医院睡眠呼吸监测诊疗中心接受治疗的110例OS伴呼吸衰竭的病人为研究对象,根据治疗期间所接受的正压通气方式不同,将病人分为两组,A组(65例):其中男49例,女16例,年龄28~65岁,平均(46.46±16.51)岁,BMI(33.23±2.25)kg/m2,行压力滴定下的BiPAP治疗;B组(45例):其中男33例,女12例,年龄26~66岁,平均(45.37±15.83)岁,BMI(34.02±2.48)kg/m2,采用Auto-CPAP治疗。两组病人在年龄、性别比例、病程、身体质量指数(BMI)、是否吸烟及是否伴有合并症等基线资料比较无统计学差异(P>0.05),具有可比性(见表1)。所有病人均签署知情同意书,表示对本实验内容知情,并愿意参加此研究;本研究获得医院伦理委员会批准同意。
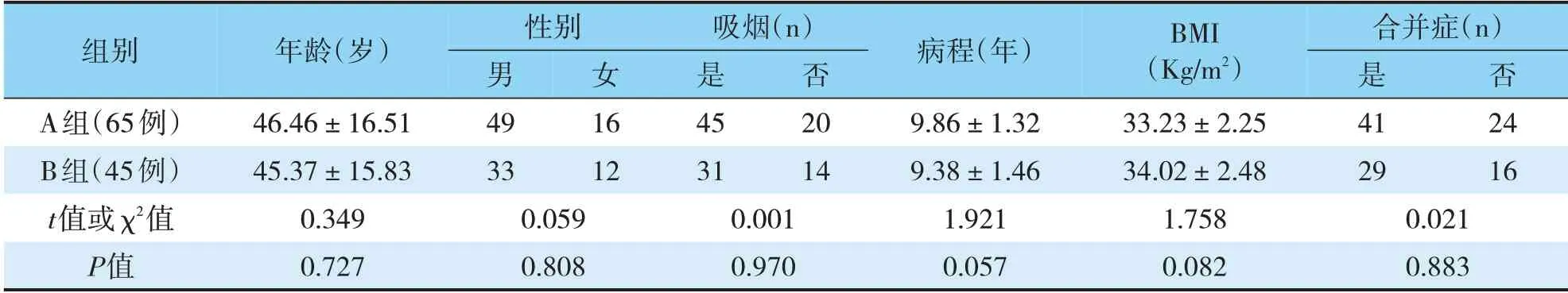
表1 两组病人一般资料比较
1.2 纳入及排除标准
(1)纳入标准:①所有病人都符合中华中医药学2019年会发布的《慢性阻塞性肺疾病中医诊疗指南》对COPD的诊断标准,即吸入支气管扩张药物后,FEV1/FVC%<70%,存在明确的气流受限[5];②OSAS的诊断符合中华医学会全科医学分会《成人阻塞性睡眠呼吸暂停基层诊疗指南》制定的OSAS诊断标准[6],即7h的夜间睡眠过程中出现呼吸暂停及低通气>30次,或呼吸暂停低通气指数(apnea hypopnea index,AHI)≥5次/h;③符合呼吸衰竭标准:静息状态下,动脉血氧分压(PaO2)<60mmHg,伴或不伴有动脉血二氧化碳分压(PaCO2)>50mmHg;④具有正压通气的指征:出现中度或重度呼吸困难,已出现胸腹不规律运动,轻中度酸中毒(PH值7.25~7.35),高碳酸血症(PaCO250~80mmHg),呼吸频率小于25次/min[2,7];⑤病人依从性较好,自愿参加本次研究;(2)排除标准:①已出现意识障碍,不能配合治疗;②痰液分泌多,出现上呼吸道阻塞;③PaO2<40mmHg,已危及生命;④合并肺大泡、支气管扩张、哮喘、肺间质纤维化等呼吸系统疾病。
1.3 治疗方法
两组病人均完善肺功能相关检查,给予抗炎、抗感染、祛痰、平喘、解痉挛药物治疗,A组采用BiPAP通气模式,调至S/T模式,氧流量4~8L/min,采用压力滴定技术确定通气压力:在多导睡眠监测仪监测下,技术人员进行整夜人工压力滴定,确定最佳吸气相压力和呼气相压力,理想压力滴定的标准是消除各种睡眠期和各种体位时的睡眠呼吸事件,使呼吸暂停低通气指数(apnea hyponea index,AHI)<5次/h,同时不能伴有自发性微觉醒。B组采用Auto-CPAP通气模式,在病人进入睡眠后,根据呼吸事件的发生情况触发并调节呼吸机的压力输出,第二日将治疗数据进行分析,然后以最高有效治疗压力的95%水平设定为治疗压力。
两组病人呼吸机通气期间均联合抗炎、抗感染、祛痰、平喘、解痉挛药物治疗;呼吸机治疗时间初步定为2周,可视病情恢复情况进行延长,前3天带机时间至少在8~10h,且夜间睡眠带机时间需≥4h。若出现呼吸困难、血气分析相关指标无改善或出现意识状态变差则认为正压通气治疗失败,需及时行气管插管辅助通气治疗。
1.4 观察指标
借助多导睡眠监测仪(美国飞利浦伟康公司,Alice6)(PSG)对睡眠状态下的受试者进行相关指标监测,包括总睡眠时间、AHI、微觉醒指数、夜间最低氧饱和度等。
于治疗前后不同时间点分别抽取股动脉血,离心后取上清,借助试剂盒行血气分析,检测项目包括PH值、PaO2、PaCO2、血氧饱和度(SaO2)等;同时,检测肺功能状态,包括用力肺活量(FVC)、第1秒用力呼气容积(FEV1)、1秒率(FEV1/FVC%)等。
以Epworth日间多睡量表(Epworth Sleepiness Scale,ESS)来评估病人的嗜睡程度:包括8个项目,每个项目评分0~3分,满分24分;0~5分为正常;5~10分属轻度嗜睡;10~15分属中度嗜睡;16~24分属重度嗜睡[1]。
1.5 统计学处理
采用SPSS 18.0软件包进行统计分析,计量资料符合正态分布,以均数±标准差表示,组间比较采用两样本t检验或χ2检验,组内比较采用重复测量的方差分析,检验水准为α=0.05,P<0.05时判定差异有统计学意义。
2 结果
2.1 PSG监测指标比较
两组病人在总睡眠时间、AHI、微觉醒指数和夜间最低氧饱和度上均较治疗前有显著改善(P<0.05),且B组在总睡眠时间和微觉醒指数上明显优于A组(P<0.05);但A组在夜间最低氧饱和度上优于B组(P<0.05)(见表2)。

表2 两组病人PSG监测指标比较
2.2 血气分析比较
两组病人的PaCO2较治疗前有显著降低,PaO2、SaO2及PH值则较前有显著升高(P<0.05),组间比较无显著统计学差异(P>0.05)(见表3)。
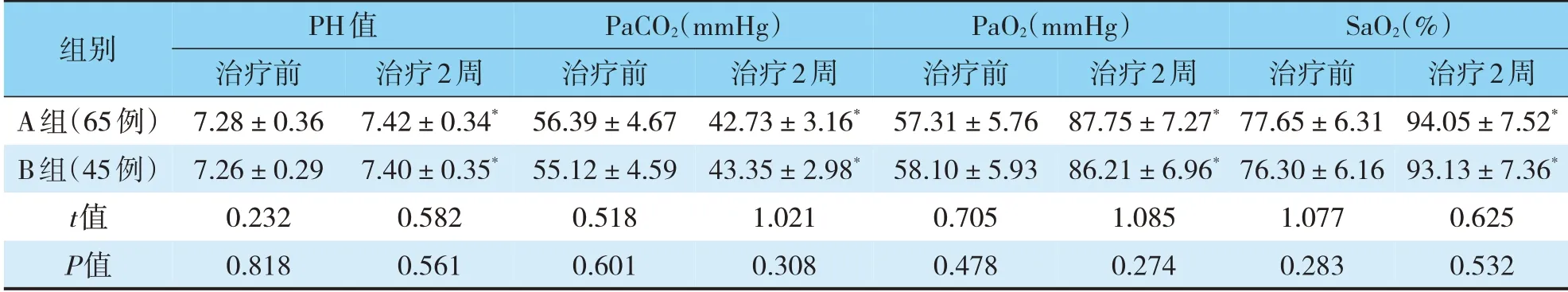
表3 两组病人血气分析比较
2.3 肺功能及睡眠质量改善情况比较
两组病人治疗后的FVC、FEV1、FEV1/FVC均有显著升高,治疗前后比较有显著统计学意义(P<0.05);组间比较无显著统计学差异(P>0.05)。两组ESS评分显著降低,治疗前后比较差异显著(P<0.05);且A组评分明显优于B组(P<0.05)(见表4)。

表4 两组病人肺功能及睡眠质量改善情况比较
3 讨论
COPD是以小气道阻塞为特征的一种呼吸系统疾病,通气障碍是其主要临床表现,且在呼吸道感染、呼吸肌疲劳等因素的作用下诱发呼吸衰竭[1,2]。OSAS最早出现的病变部位是上气道的狭窄和阻塞,且气道高反应的严重程度与OSAS病情呈正相关[8]。OS病人主要体现在上下呼吸到同时存在梗阻,在夜间睡眠可发生中上气道狭窄和上气道阻力增高现象,导致肺通气不足、气道阻力增加、功能残气量升高,加重缺氧并最终导致II型呼吸衰竭的发生[1,2,9]。两种呼吸道疾病同时存在可互为因果,危害更大。有研究报道,COPD病人在快速动眼睡眠阶段,呼吸驱动力会降低,而气道阻力和功能残气量会显著增加,若合并严重的OSAS,则极易出现低氧血症和高碳酸血症,继发性肺动脉高压和心血管意外的风险也更高[2,4]。因此,一旦明确诊断需要在药物治疗的基础上积极应用人工辅助通气技术支持治疗[1~8,10]。
目前临床应用较多的通气模式有Bi PAP和Auto-CPAP[1,8]。两种模式在应用时均需要进行压力设定,BiPAP模式多采用PSG监测下的人工滴定技术[11],而Auto-CPAP模式则以最高有效治疗压力的95%水平设定为治疗压力[8]。对于OS合并呼吸衰竭的病人应该采用何种通气模式,临床上仍存在较大的争论。叶环等[1]认为,与BiPAP相比,Auto-CPAP模式所需的压力低,病人依从性更好。岳英明等[8]通过对比研究法发现,在治疗重度OSAS病人时,Auto-CPAP模式对病人的睡眠结构改善更佳且依从性更好。在本研究中,通过PSG监测发现,两组病人在总睡眠时间、AHI、微觉醒指数和夜间最低氧饱和度上均较治疗前有显著改善,但B组在延长总睡眠时间和降低微觉醒上明显优于A组,这一结果与叶环等[1]及岳英明等[8]所得结论基本相同。合适的压力设定是保证疗效的关键,最有效的治疗压力应该可以消除在各睡眠时期及各种睡眠体位时出现的呼吸暂停,并能够保持整夜睡眠中的SaO2大于90%,当有效压力过高时,病人的舒适性降低,每晚呼吸机使用时间缩短,治疗收益变小[1]。本研究中,Auto-CPAP所设定的压力低,这明显增加了病人的舒适性,因此病人可以获得更长的睡眠时间及更低的微觉醒次数。那么,较低的压力设定是否会影响到肺通气效果呢?
在本研究中,通过血气分析发现,两组病人的PaCO2较治疗前有显著降低,PaO2、SaO2及PH值则较前有显著升高,组间比较无显著统计学差异。值得注意的是,虽然血气分析中的SaO2无明显差异,但A组的夜间最低氧饱和度要显著高于B组(95.76%vs 93.25%)。笔者认为,两种通气模式均可以有效增加肺通气,进而改善病人的呼吸衰竭状态;同时,亦能够通过降低PaCO2来纠正呼吸性酸中毒,达到升高PH值效果。BiPAP本质是压力支持通气和CPAP的结合形式,在自主吸气时提供一个较高的吸气压,帮助病人克服气道阻力,增加肺泡通气量,降低吸气肌负荷,减少呼吸肌做功和耗氧量,有利于呼吸肌的休息;呼气时提供一个较低的呼气压,可对抗内源性呼气末正压,起到机械性支气管扩张作用,防止细支气管陷闭,增加通气量,增大功能残气量,改善通气与血流比例,从而有利于O2和CO2在肺泡内的交换[4,9]。在夜间,病人的迷走神经呈兴奋状态,这导致肺通气功能更差;BiPAP模式可以通过设定较高的吸气压力来增加肺泡通气量,进而提升病人的夜间最低氧饱和度。通过PSG所获取的数据能及时、准确、动态的反映病人夜间的通气状况[12],而晨起所抽取的动脉血仅能反映清晨时的氧饱和度情况,此时迷走神经兴奋性降低,两种通气模式均可以实现良好的通气。
有文献报道,无创正压通气技术不仅对慢性呼吸系统疾病有很好的治疗效果,对其伴随的呼吸衰竭、肺心病及心力衰竭均有较好的协同治疗作用[2,7,9,10,13~15]。刘璐等[14]发现,BiPAP在治疗COPD合并慢性呼吸衰竭时疗效满意,可显著改善血气的相关指标及肺功能,缓解病人临床症状并提高其生活质量。在本研究中,无论是采用BiPAP模式还是采用Auto-CPAP模式,病人的呼吸功能相关指标(FVC、FEV1、FEV1/FVC)均较前获得显著改善,且组间比较无显著性差异。但在促进日间嗜睡状态的改善上,采用BiPAP模式的A组其ESS评分要显著优于采用Auto-CPAP模式的B组。笔者认为,夜间睡眠时间长并不能代表睡眠质量高,日间嗜睡程度是评价睡眠质量的最佳标准。有文献报道,ESS评分除了能反映病人的日间嗜睡程度外,还可用于评价病人的主观生存质量[1]。因此,Bi PAP模式在改善病人日间嗜睡状态及提升生活质量上更具优势。
综上所述,BiPAP及Auto-CPAP均是治疗OS合并呼吸衰竭的有效通气方法,Auto-CPAP在延长夜间睡眠时间及降低微觉醒上优势明显,而BiPAP在提升夜间氧饱和度、改善日间嗜睡状态上效果更佳。
