儿童重症腺病毒肺炎合并肺部后遗症的高危因素研究*
2021-07-31曹佳颖周浩泉潘家华
徐 露,曹佳颖,周浩泉,潘家华△
(1.安徽医科大学附属省立医院儿科,安徽 合肥 230000;2.上海市儿童医院重症医学科,上海 200000)
近年来,我国关于腺病毒肺炎病例的报道逐渐增多,重庆市[1]、湖南省[2]、台湾地区[3]及广州市[4]等地均有相关病例报道。腺病毒感染常可导致重症肺炎,尤其是3、7、55型等血清型,具有病死率高和后遗症发生率高等特点。目前,国际上尚无针对腺病毒肺炎后遗症的统一标准,但是有学者将其定义为:任何形式的慢性肺病,包括闭塞细支气管炎(BO)、斯-占综合征(SJ)、支气管扩张、肺纤维化、持续性大叶萎陷和反复喘息[5-7]。既往研究表明,腺病毒肺炎预后不良的危险因素包括:住院时间大于30 d、高碳酸血症、多灶性肺炎[8];有创通气,发热时间超过10.5 d[1];低氧血症[4];腺病毒7型[9]。然而,上述危险因素常不能敏感地预测腺病毒肺炎预后。对于重症腺病毒肺炎(SAP)预后需要进一步研究。本研究回顾性分析了47例SAP患者,旨在找出可以预测SAP预后不佳的危险因素。现报道如下。
1 资料与方法
1.1一般资料 选取安徽医科大学附属省立医院2018年7月至2019年12月间SAP患者47例(总48例,其中1例患儿于住院期间死亡)作为研究对象,年龄在4个月至11岁,顺利出院后随访时间为半年至一年半不等。根据是否有后遗症,分为有后遗症组(n=18)和无后遗症组(n=29)。纳入标准:腺病毒肺炎诊断标准符合《儿童病毒肺炎诊疗规范(2019年版)》且合并腺病毒感染。腺病毒感染定义为:(1)鼻咽拭子检测结果显示腺病毒抗原阳性;(2)鼻咽拭子腺病毒DNA为阳性;(3)送检肺泡灌洗液或者血液进行宏基因测序提示腺病毒。重症肺炎诊断标准符合《儿童社区获得性肺炎诊疗规范(2019年版)》,具体内容包括:(1)发热、咳嗽、喘息。(2)有意识障碍。(3)有低氧血症,包括发绀、呼吸增快,呼吸率(RR)大于或等于70次/分(婴儿),RR≥50次/分(>1岁);辅助呼吸(呻吟、鼻扇、三凹征);间歇性呼吸暂停;氧饱和度小于0.92。(4)脱水征或拒食。(5)胸部X线片或胸部计算机断层扫描(CT)示多肺叶浸润、超过2/3肺浸润、胸腔积液、肺不张、气胸、肺脓肿、肺坏死。(6)存在肺外并发症。排除标准:脐血干细胞移植术后患儿;营养不良;免疫缺陷;哮喘;有肺部基础病变及遗传代谢病。
1.2方法 收集资料包括住院病例和院外随访。出院后随访主要包括门诊复诊和电话随访。包括基本信息、临床表现、实验室检查、病原学检查、影像学检查、治疗方法等。巨细胞病毒(CMV)感染定义为:(1)血、尿样本中CMV-DNA载量大于1×105;(2)血清标本中CMV抗体IgM阳性。
1.3统计学处理 采用SPSS25.0软件进行统计分析,计量资料用中位数(范围)表示,组间比较采用秩和检验;计数资料以率或百分比表示,组间比较采用χ2检验。采用logistic回归模型确定发生SAP的独立危险因素。P<0.05为差异有统计学意义。
2 结 果
2.1SAP临床特征
2.1.1临床表现 患者临床表现严重。主要表现为高热、发热时间长、咳嗽、喘息等。肺部并发症包括胸腔积液、呼吸衰竭、肺不张、气胸等,肺外在并发症主要为肝功能损伤、凝血功能异常、心肌损伤等。C反应蛋白、白细胞等炎症指标明显升高,部分患者危重患者表现为粒细胞减少。见表1。
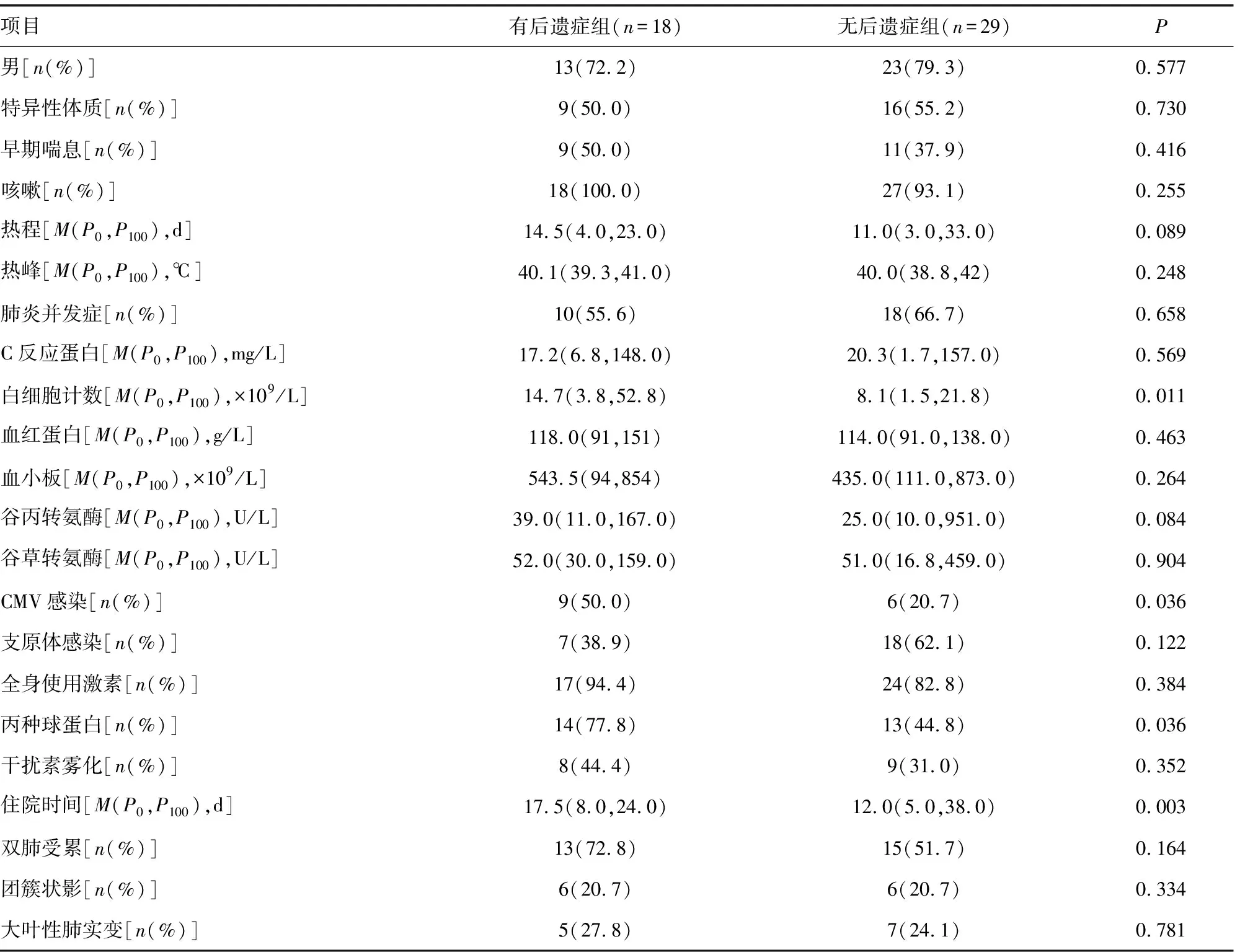
表1 2组临床表现比较
2.1.2影像学特点 影像学特点为多变。在病情危重患者中,影像学变化更为迅速。SAP的主要影像学改变为:肺实变(82.9%)、絮状影(53.2%)、团簇状影(25.5%)、大叶实变影(25.5%)等。既往有学者报道,腺病毒肺炎患者种团簇状影占比可达71%[10]。其原因可能是由于在病程的不同时期,所得影像及病毒感染严重程度不同。当肺炎累积至整个肺叶时,临床上极难与细菌性肺炎鉴别。临床上,当使用抗菌药物无效时需考虑到腺病毒感染。此时,病原学检测是鉴别两者的重要手段。
2.1.3治疗 所有的患儿均接受肺炎的标准治疗。目前并没有针对SAP的特效抗病毒药物。在本研究中,作者主要以丙种球蛋白和全身性糖皮质激素抗炎支持治疗,部分患者使用干扰素雾化治疗。但是,糖皮质激素和干扰素的使用并没有减少出院后肺部后遗症的发生率。在使用丙种球蛋白的患者中,患儿住院时间缩短(P<0.001)、出院后肺部后遗症(反复喘息)减少(P=0.036),但是,患儿肺内和肺外并发症发生率未见明显降低。
2.2并发肺部后遗症的高危因素
2.2.1单因素回归分析结果 所有SAP患者出院后门诊及电话随访结果显示,18例患者出现反复喘息症状。对有相应症状的患者进一步检查,10例患者肺部影像学表现为马赛克灌注征,剩下8例患者未见明显异常影像学表现。结合患者病史及相关检查,作者将有反复喘息、有马赛克灌注征、肺功能异常的患者,诊断为闭塞性细支气管炎(BO),予激素雾化联合阿奇霉素、孟鲁斯特治疗,必要时辅以口服激素治疗。其余合并反复喘息的患者,则予辅舒酮、孟鲁斯特长期治疗。单因素回归分析显示:病程中白细胞计数大于17×109/L[P=0.018,比值比(OR)=1.134,95%置信区间(CI)1.022~1.259]、合并CMV感染(P=0.041,OR=3.833,95%CI1.057~13.909)、住院时间大于13 d(P=0.033,OR=1.132,95%CI1.010~1.270)、使用丙种球蛋白(P=0.031,OR=4.308,95%CI1.139~16.296)是SAP出现肺部后遗症的危险因素,见表1。
2.2.2多元logistic回归分析结果 将单因素分析有意义的指标(白细胞计数、合并CMV感染、静脉使用丙种球蛋白及住院时间)纳入多元logistic回归分析。结果显示,仅合并CMV感染(P=0.045,OR=5.161,95%CI1.040~25.602)是SAP合并反复喘息的独立危险因素,见表2。

表2 预测参数的logistic回归分析
3 讨 论
腺病毒感染引起的临床症状差别很大,包括不明显的感染、自限性上呼吸道疾病、坏死性毛细支气管炎、急性呼吸窘迫综合征,甚至死亡。免疫系统的激活、大量趋化因子和细胞因子的产生在炎症的激活中明显发挥作用,包括肿瘤坏死因子-α(TNF-α)、白细胞介素(IL)-1、IL-6,、IL-8,、IL-10、IL-12、干扰素γ(IFN-γ)等[11]。大量炎性细胞因子导致细支气管上皮细胞坏死,细支气管周围渗出明显。气道上皮的不完全修复和过度纤维增生会导致细支气管局部的管腔狭窄、闭塞[12]。腺病毒肺炎患者出院以后,关于肺部炎症的持续时间,目前尚缺乏统一结论。但是有学者提出,在肺部感染数年后,肺泡灌洗液中仍可见到中性粒细胞炎症,且第一秒用力呼气量占所有呼气量的比例下降,提示肺部发育不良[13]。因此,在腺病毒感染之后,患儿仍需要长期的随访。医生在随访过程中需注意患儿有无肺部后遗症的发生,包括反复咳喘、运动不耐受等,警惕发生BO的可能。通过早期识别腺病毒肺炎预后不良的高危因素,理论上可以早期治疗甚至预防肺部后遗症的发生。
当SAP患儿入院时检测合并CMV感染时,患儿出院后的肺部后遗症发生率更高,需要长期使用吸入型糖皮质激素、孟鲁斯特等药物治疗,部分患者需要还需要使用普米克雾化、口服糖皮质激素治疗。既往研究显示,在移植术后患者中,CMV感染是发生闭塞性细支气管炎综合征(BOS)的独立危险因素之一[14-16]。但是,在非免疫抑制状态下,临床上很少重视患者是否合并CMV感染,以及合并该病毒感染是否会对疾病的预后产生影响。本研究发现,合并CMV感染是SAP预后不良的独立危险因素,但其具体原因不详。可能是CMV作为一种免疫调节病毒,会持续刺激T淋巴细胞,促进多种炎性细胞因子(如TNF-α、IL-6、IFN-γ等)的释放,从而加重肺炎后的局部炎症水平[15,17],增加肺部后遗症的发生概率。因此,CMV在判断肺炎预后时具有更高的敏感度。
除发热时间长、住院时间长、低氧血症、高碳酸血症这些在腺病毒肺炎中晚期出现的高危因素外,腺病毒7型及病毒载量也是SAP预后不良的高危因素[9,18]。本研究中,明确诊断腺病毒7型患者有22例,11例患者有明显后遗症,包括反复喘息、BO等。因此,对于腺病毒肺炎患者,需早期对病毒临床分型,不但可以判断病情的严重性,还可以预估临床后遗症的发生率。
但是,应对目前的研究结果持谨慎态度。(1)本研究是回顾性分析,不可避免地有一定的回忆偏倚和选择偏倚.(2)本研究属于单中心研究,样本量偏小,不能完全反映真实情况。(3)本研究并没有证明抗CMV治疗是否对腺病毒肺炎预后有影响。(4)对于可能对腺病毒肺炎产生不良预后的病毒载量阈值,由于研究资料所限,并未能进一步研究。
