合成生物医学应用领域态势分析
2021-07-30李玉娟仇华炳柳天晴
李玉娟 仇华炳 柳天晴 夏 霖*
1(中国科学院深圳先进技术研究院 深圳合成生物学创新研究院 深圳 518055)
2(深圳市合成生物学协会 深圳 518055)
3(中国科学院武汉文献情报中心 武汉 430071)
1 引 言
合成生物学是生命科学领域的一门新兴热门工程科学,其实质是在工程学思想指导下,按照特定目标理性设计、改造乃至从头重新合成生物体系,通过构造人工生物系统来研究生命科学中的基本问题或应对人类面临的重大挑战,其核心旨在通过研究以期理解生命本质(造物致知)和创造社会经济价值(造物致用)[1]。合成生物技术被多国评价为未来的颠覆性技术之一。
合成生物学在生物医学、农业、工业、能源、环境和国防等领域具有广阔的应用前景[2-3]。在医学应用领域,合成生物技术为疾病诊疗提供了新思路,为临床复杂疾病提供高效、特异、智能化、安全的全新解决方案。例如,人工合成的活体药物为癌症、遗传病等无药可治的人类健康挑战及新突发传染病提供高效治疗手段;人工基因组合成技术、基因编辑技术可治疗地中海贫血症、艾滋病等重大疾病;噬菌体治疗可从根本上解决无药可救的超级细菌难题,为肺炎等感染性疾病摆脱抗生素缺乏的困境;使用智能细菌(高效广谱的实体瘤溶瘤细菌)、益生菌等细菌靶向治疗肿瘤、糖尿病和肥胖等复杂疾病,提高国民健康水平,降低化学药物依赖;CAR-NK 等人工改造的免疫细胞,能有效治疗癌症、衰老等世界性医学难题[4-5]。未来十年(2021—2030),合成生物等前沿生物技术或将彻底变革医疗领域[6]。
2020 年,COVID-19 新冠病毒大流行席卷全球,生命健康成为全球首要关注的问题。人们对健康与生物医药产业的关注达到前所未有的高度,在这一全球公共卫生事件的刺激下,合成生物医药行业爆发出巨大的活力。随着生物医药行业的蓬勃发展,越来越多的公司关注“利用生物合成的方式重塑传统生产方式”,这开启了生物合成的新纪元。本文结合合成生物医学发展态势,对合成生物医学领域进行文献计量及专利分析,旨在为我国合成生物医学领域发展及布局提供参考依据。
2 合成生物医学文献计量
在 Web of Science 核心数据库中检索合成生物医学应用内容相关数据,2001—2021 年共有 10 803 篇相关文献,其中 2020 年度为 2 270篇。领域高被引文章 350 篇,热点论文 11 篇(数据截至 2021 年 3 月 15 日)。其中,热点论文(Hot Papers)是指基于 22 个基本科学指标数据库(Essential Science Indicators,ESI)中某一学科领域最近两年发表的论文数据,最近两个月内被引次数排在前 0.1% 的论文。高被引论文(Highly Cited Papers)是指基于 ESI 库中某一学科领域最近 10 年的引文数据,同学科同年度中被引次数排在前 1% 的论文[7]。
文献计量检索式:TS=(((“synthe* biology”or “Gen* editing” or CRISPR or “synthe* genome”or “synthe* chromosome” or “gene assembly”or “DNA assembly” or “synthe* genomics”or “synthe* life” or “chromosome biology” or“genome engineering” or “DNA-based data storage” OR “DNA comput*” or “unnatural nucleotide” or “unnatural amino acid” or “de novo protein” or “directed evolution protein” or “genetic*circuit” or “genetic* logic gate” or “biosynthetic*pathway” or “protocell” or “artificial cell” or“reconstitut* cell” or “metabolic engineering” or“synthe* microbiome” or “synthe* microbiota”or “synthe* microbial communities” or “synthe*microbial consortia” or “microbiome engineering”)or (“synthe* biology” and “AI”) or (“synthe*biology” and “machine learning” ) or (“synthe*biology” and “rational design”) or (“synthe*biology” and modeling) or(“synthe* biology”and “quantitative*”) or (“synthe* biology” and“automat*”) or (“synthe* biology” and “robot*”))and (“medic*” or “therap*”))[8]。
2.1 发文量年度变化趋势
通过计量分析可知(图 1),合成生物医学领域发文数量逐年增长(2021 年统计不完整,数据截至 2021 年 3 月 15 日)。随着全球对合成生物学的重视,各国战略规划与系列鼓励政策密集出台,尤其在是医学领域的大力投入,使得从2014 年开始,合成生物医学相关论文呈现爆发式增长。
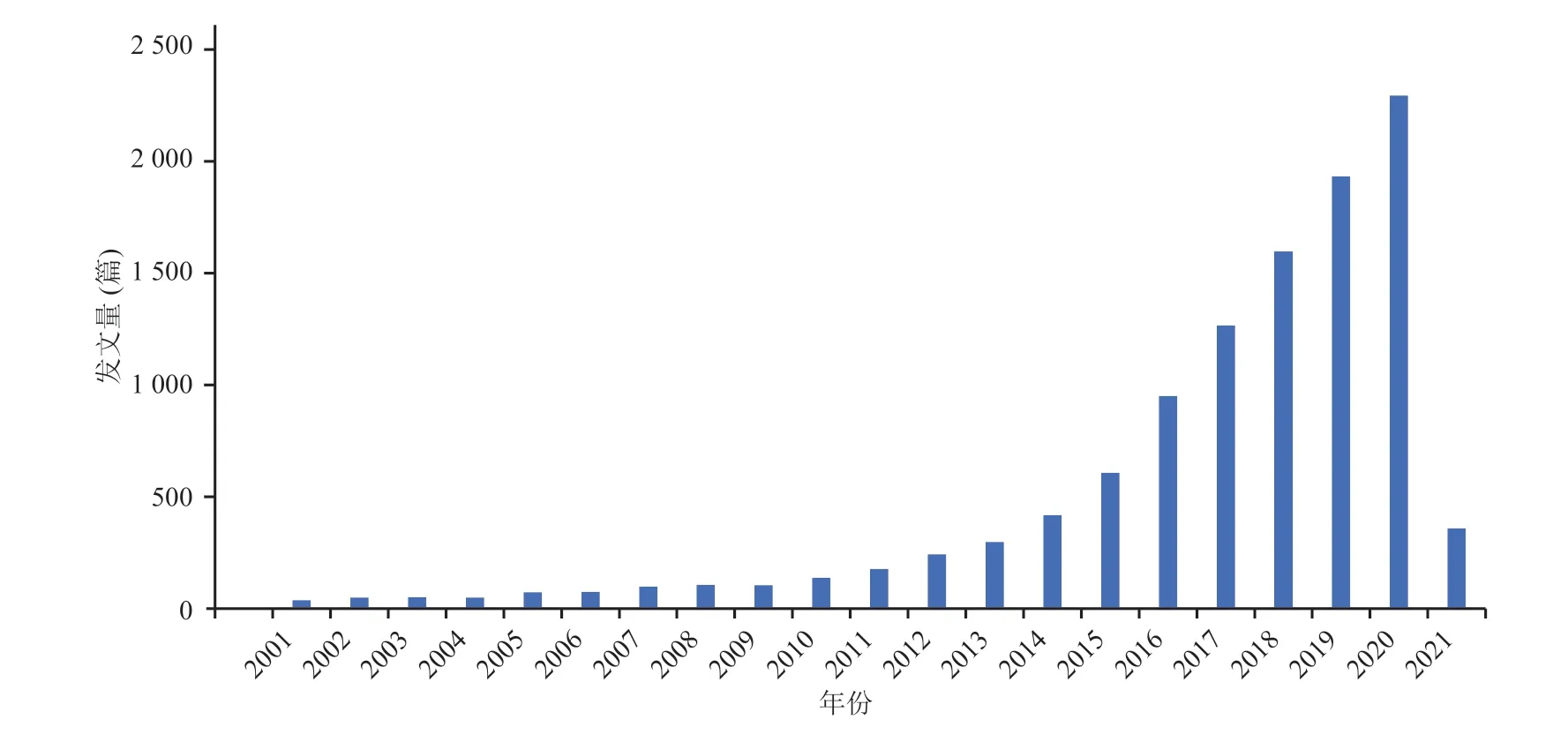
图1 合成生物医学领域发文量年度分布Fig. 1 Annual distribution of papers published in the field of synthetic biomedicine
2.2 发文量主要国家分析
从主要国家分布来看(图 2),合成生物医学领域发文量前 10 的国家依次为美国(44.5%)、中国(21.9%)、德国(7.5%)、英国(7.2%)、日本(5.3%)、法国(4.4%)、加拿大(4.4%)、印度(3.5%)、韩国(3.4%)和意大利(3.3%),美国以4 532 篇的发文量遥遥领先于其他国家,中国发文量共计 2 228,位居第二。中美两国的发文量总计占全球 2/3 以上(注:根据数据库统计源分类规则,本文中国不含港澳台地区,下同)。
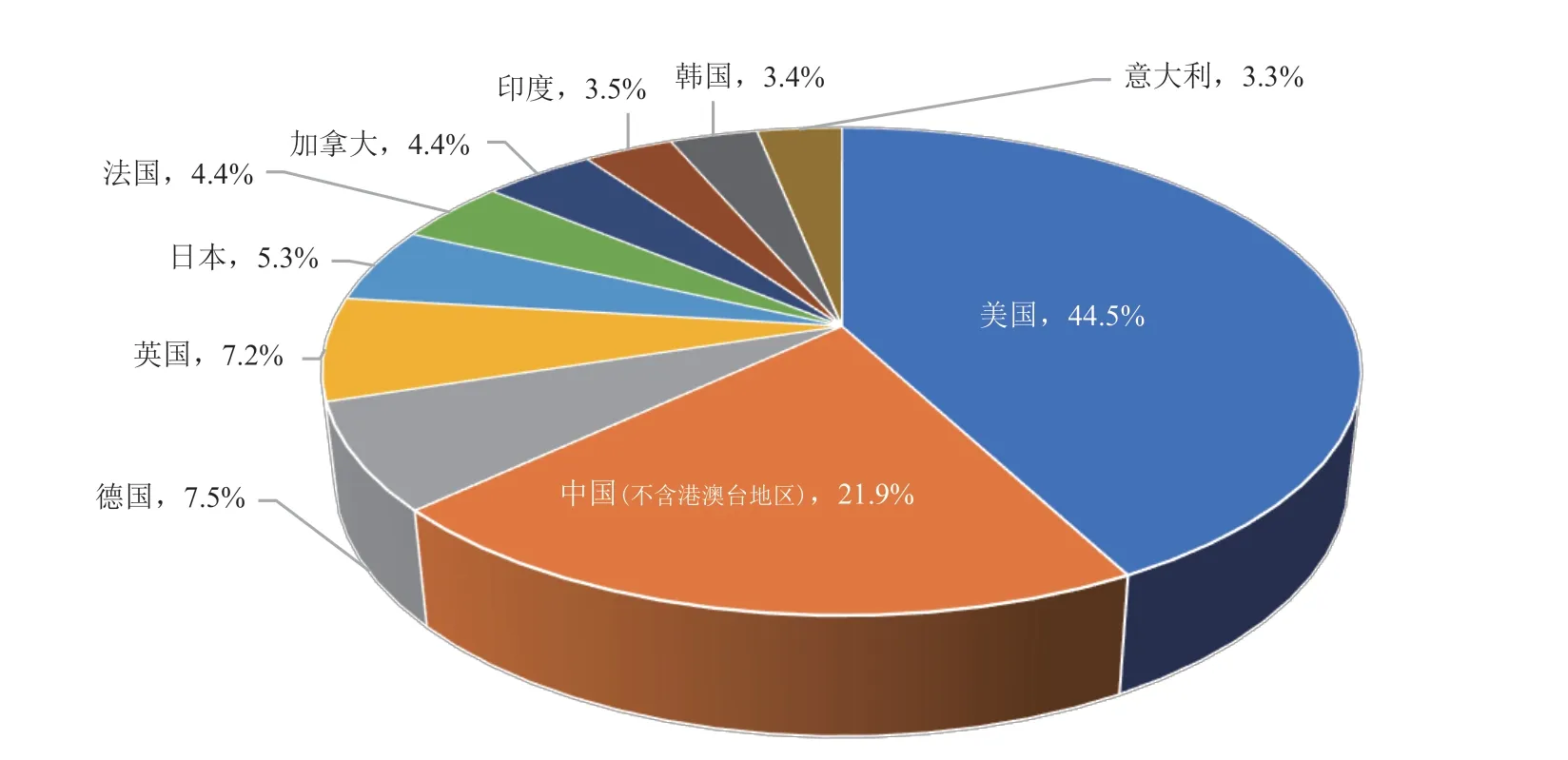
图2 合成生物医学领域主要发文国家(前 10)Fig. 2 Main countries that published in the field of synthetic biomedicine (Top 10)
2.3 主要机构分析
从开展合成生物医学研究各机构来看(表 1),美国机构发文数量仍处于领先地位,中国科学院在合成生物医学领域发文 555 篇,位居第三。从表 1 不难看出,加州大学、哈佛大学及麻省理工学院等高校,不仅发文量位列前沿,高被引论文数量及占比也非常引人注目。值得一提的是,霍华德•休斯医学研究所、宾夕法尼亚大学及博德研究所,在合成生物医学领域发文数量虽然不多,但其高被引论文数量分别排名第 4 位、第 5位和第 7 位,其发文质量可见一斑。
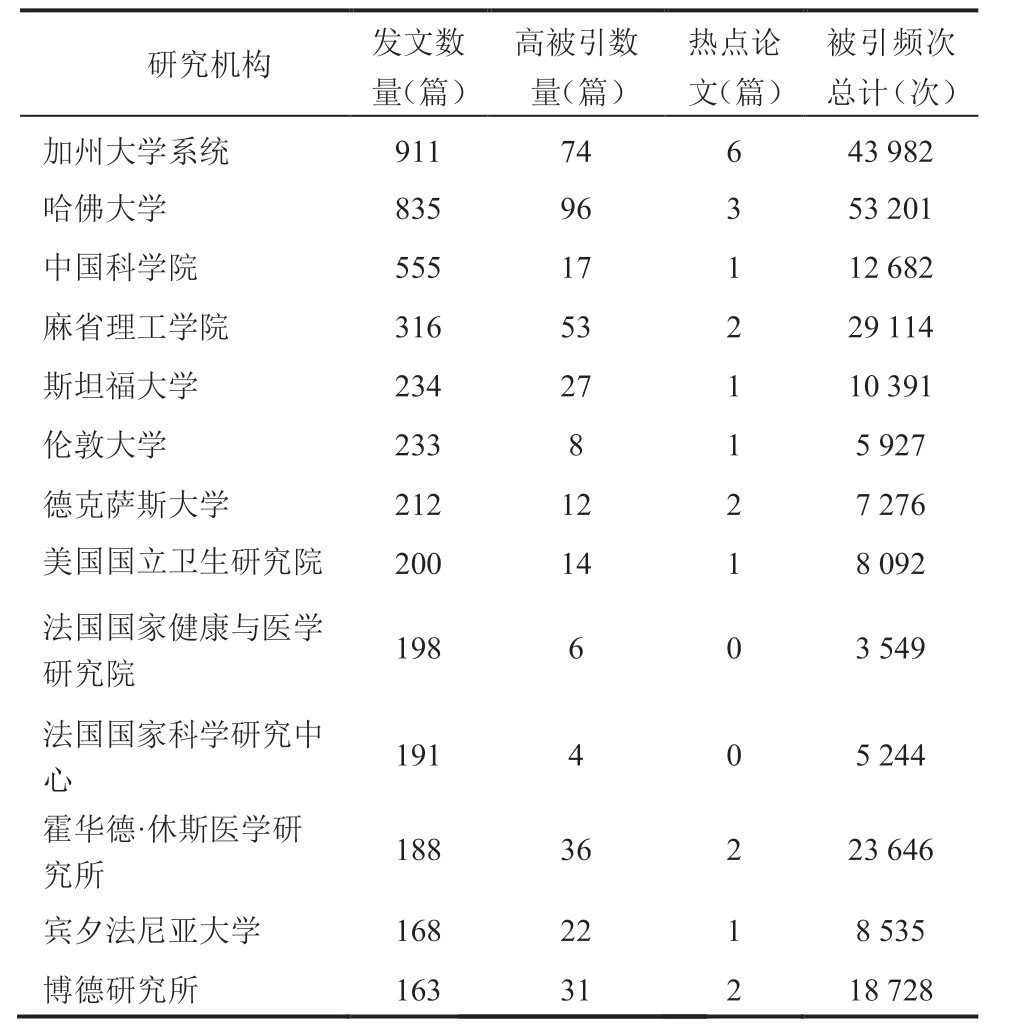
表1 合成生物医学领域各主要机构发文数量、高被引及热点论文情况Table 1 Summary of total scientific publications, highly cited papers and hot papers published by major research institutions in the field of synthetic biomedicine
2.4 高被引论文计量分析
对 350 篇高被引论文进行人工清洗后的计量分析结果显示,领域高被引论文发文量排名前10的发文作者所属机构均是美国的,而尤其值得指出的是,博德研究所的作者在其中占了 3 位(表 2)。而在机构性质上,所属研究机构以研究院校居多,但也有 2 家公司上榜。这表明不仅科研院所重视合成生物医学领域的基础研究与应用研究,企业也非常重视合成生物医学的产业研究与应用。
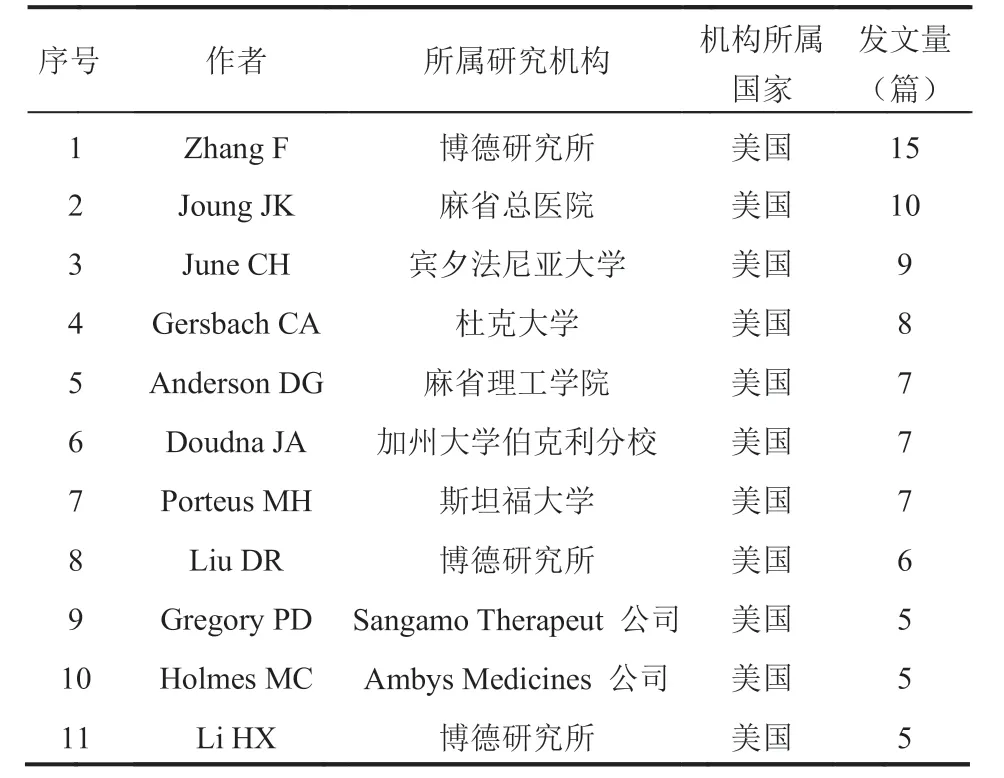
表2 合成生物医学领域高被引论文数量排名前 10 的发文作者分布Table 2 Distribution of authors with the top 10 highly cited papers in the field of synthetic biomedicine
2.5 代表性文献
根据 Web of Science 核心数据库检索结果,按被引频次高低例举重点文献分析如下(表 3):
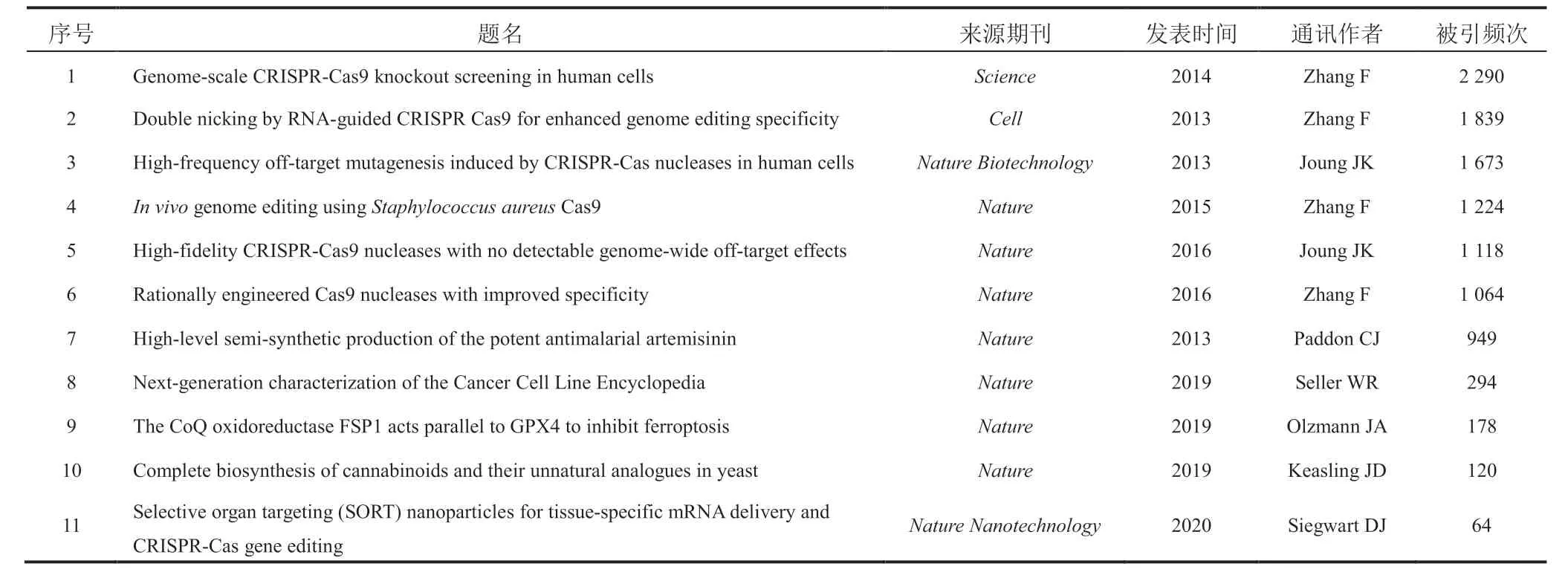
表3 合成生物医学领域代表性文献Table 3 Representative literature in the field of synthetic biomedicine
(1)麻省理工学院和哈佛大学的博德研究所Zhang 团队在Science发表题为“Genome-scale CRISPR-Cas9 knockout screening in human cells”的文章,报告了慢病毒传递的基因组规模的CRISPR-Cas9 敲除(GeCKO)文库(用 64 751 个独特的引导序列靶向 18 080 个基因),可以在人细胞中进行阴性和阳性选择筛选。该实验首先使用GeCKO 文库来鉴定对于癌症和多能干细胞的细胞生存力至关重要的基因,接着在黑色素瘤模型中筛选基因,这些基因的丢失与对治疗 RAF 抑制剂 Vemurafenib 的抗性有关。排名最高的候选基因包括先前验证的基因NF1和MED12以及新命中的基因NF2、CUL3、TADA2B和TADA1。该研究观察到针对相同基因的独立向导 RNA 和高命中率之间的高度一致性,证明了用 Cas9 进行基因组规模筛选的可行性[9]。
(2)麻省理工学院和哈佛大学的博德研究所Zhang 团队在Cell发表题为“Double nicking by RNA-guided CRISPR Cas9 for enhanced genome editing specificity”的文章,描述了一种结合Cas9 切口酶突变体和配对向导 RNA 来引入目标双链断裂的方法。该研究表明,使用配对切口可以在细胞系中将脱靶活性降低 50~1 500 倍,并促进不牺牲靶切割效率的情况下对小鼠受精卵基因敲除。这种通用策略可实现需要高特异性的各种基因组编辑应用程序[10]。
(3)哈佛大学麻省总医院 Joung 团队在Nature Biotechnology发表题为“High-frequency oあ-target mutagenesis induced by CRISPR-Cas nucleases in human cells”的文章,使用基于人类细胞的报告分析来表征基于 Cas9 与 CRISPR 有关的 RNA 引导性核酸酶(RGN)的脱靶裂解。研究发现单个和双重错配的耐受程度不同,这取决于它们沿着引导 RNA(gRNA)-DNA 界面的位置。通过检测部分错配位点,很容易地检测到由 6 个 RGN 中的4 个诱导的脱靶改变,这些 RGN 靶向人细胞中的内源基因座。实验发现的脱靶位点有多达 5 个不匹配,许多突变频率与预期靶点上观察到的频率相当(或更高)。该研究表明,即使人类细胞中存在不完全匹配的 RNA-DNA 接口,RGN 也可以非常活跃,这一发现可能会混淆 RGN 在研究和治疗中的应用[11]。
(4)麻省理工学院和哈佛大学的博德研究所Zhang 团队在Nature发表题为“In vivogenome editing usingStaphylococcus aureusCas9”的文章,报告了来自金黄色葡萄球菌(SaCas9)的 Cas9可以编辑基因组,其效率与 SpCas9 相似,但短了 1 000 碱基对以上。该研究将 SaCas9 及其单导 RNA 表达盒包装到单个腺相关病毒(AAV)载体中,并靶向小鼠肝脏中的胆固醇调节基因Pcsk9。在注射后的一周内,观察到超过 40% 的基因修饰,并伴随着血清 Pcsk9 和总胆固醇水平的显著降低。随着使用 BLESS 的方法进一步评估SaCas9 和 SpCas9 的全基因组靶向特异性,该研究证明 SaCas9 介导的体内基因组编辑具有高效和特异性的潜力[12]。
(5)马萨诸塞州总医院 Joung 团队在Nature发表题为“High-fidelity CRISPR-Cas9 nucleases with no detectable genome-wide oあ-target eあects”的文章,描述了一种高保真 Cas9 变异体 SpCas9-HF1,旨在减少非特异性 DNA 接触。SpCas9-HF1 保留了与野生型 SpCas9 相当的靶活性,在人类细胞中测试的单导 RNAs (sgRNAs)超过 85%。当 sgRNA 靶向标准非重复序列时,SpCas9-HF1 可以将脱靶效应降低至即使采用最敏感的方法也无法检测到的水平。即使对于非典型的、重复的靶位点,SpCas9-HF1 也未检测到由野生型 SpCas9 诱导的绝大多数脱靶突变。SpCas9-HF1 为研究和治疗应用提供了野生型SpCas9 的替代品。该研究结果提出一种通用策略得以优化其他 CRISPR-RNA 引导的核酸酶的全基因组特异性[13]。
(6)麻省理工学院和哈佛大学的博德研究所 Zhang 团队在Nature发表题为“Rationally engineered Cas9 nucleases with improved specificity”的文章,使用结构引导的蛋白质工程来提高化脓性链球菌 Cas9 (SpCas9)的特异性。通过使用靶向深度测序和无偏见的全基因组脱靶分析评估人细胞中 Cas9 介导的 DNA 裂解,该研究证明“增强的特异性”SpCas9 (eSpCas9)变体可减少脱靶效应并维持强大的靶裂解。该研究表明eSpCas9 对需要高水平特异性的基因组编辑应用可能广泛有用[14]。
(7)Amyris Inc 阿米瑞斯公司 Paddon 团队在Nature发表题为“High-level semi-synthetic production of the potent antimalarial artemisinin”的文章,使用合成生物学来开发酿酒酵母菌株(面包师酵母)用于高产生物生产青蒿酸(青蒿素的前体)。开发了一种实用、高效且可扩展的化学方法,可使用单线态氧的化学来源将青蒿酸转化为青蒿素,从而避免了使用专门的光化学设备的麻烦。该研究描述的菌株和工艺构成了生产半合成青蒿素的可行工业工艺的基础,可稳定青蒿素的供应,使其衍生成活性药物成分(如青蒿琥酯),以纳入基于青蒿素的联合治疗[15]。
(8)麻省理工学院和哈佛大学的博德研究所 Sellers 团队在Nature发表题为“Nextgeneration characterization of the Cancer Cell Line Encyclopedia”的文章,扩充了来自不同血统和种族的 1 072 株癌细胞系的分子特征,包含遗传、RNA 剪切、DNA 甲基化、组蛋白 H3 修饰、microRNA 表达以及反向蛋白阵列数据。通过与功能特征进行整合揭示了肿瘤药物的潜在靶点和相关生物标志物。这一数据库将加速基于肿瘤细胞系模型的癌症研究[16]。
(9)加州大学伯克利分校 Olzmann 团队在Nature发表题为“The CoQ oxidoreductase FSP1 acts parallel to GPX4 to inhibit ferroptosis”的文章,报道了肉豆蔻酰化将 FSP1 募集到质膜,它在其中起氧化还原酶的作用,降低辅酶 Q10 (CoQ)(也称为泛醌-10)活性。其中,CoQ10 可阻止脂质过氧化物的传播。同时发现了 FSP1 的表达与数百种癌细胞系中的铁死亡抵抗正相关,并且 FSP1介导了培养的肺癌细胞和小鼠肿瘤异种移植物中对铁死亡的抵抗。数据确定 FSP1 是非线粒体辅酶 Q 抗氧化剂系统的关键成分,该系统与典型的基于谷胱甘肽的 GPX4 途径平行起作用。这些发现定义了一条铁死亡抑制途径,并表明 FSP1 的药理抑制作用可能提供一种使癌细胞对铁死亡诱导化疗药物敏感的有效策略[17]。
(10)中国科学院深圳先进技术研究院合成生物学研究所的罗小舟研究员和其导师 Keasling院士在Nature发表题为“Complete biosynthesis of cannabinoids and their unnatural analogues in yeast”的文章,通过构建人工酵母菌,引入医用大麻素的相关基因,采用工业化发酵,在几周之内就可以生产大量医用大麻素,为其大规模药用奠定基础。该研究证明所设计的生物系统可由简单的合成化学来补充,从而进一步扩大其可应用领域。同时,为生产天然和非天然大麻素提供了一个平台,使更深度研究这些化合物成为可能,并可用于开发治疗各种人类健康问题的药物[18]。
(11)德克萨斯大学西南医学院 Siegwart 团队在Nature Nanotechnology发表题为“Selective organ targeting (SORT) nanoparticles for tissue-specific mRNA delivery and CRISPR-Cas gene editing”的文章,报道了一种被称为选择性器官靶向(SORT)的策略,其中系统地设计了多种脂质纳米颗粒,通过添加一个补充的 SORT 分子来专门编辑肝外组织。肺、脾和肝的脂质纳米颗粒旨在选择性编辑治疗相关的细胞类型,包括上皮细胞、内皮细胞、B 细胞、T 细胞和肝细胞。SORT 兼容多种基因编辑技术,包括 mRNA、Cas9 mRNA/单导 RNA和 Cas9 核糖核蛋白复合物[19]。
3 合成生物医学专利分析
3.1 技术简介
在医学应用领域,合成生物学以人工设计的基因线路改造人体自身细胞,或改造细菌、病毒等人工生命体,再使其间接作用于人体。这些经人工设计的生命体能够感知疾病特异信号或人工信号、特异性靶向异常细胞和病灶区域、表达报告分子或释放治疗药物,从而实现对人体生理状态的监测,以及对肿瘤、代谢疾病、耐药菌感染等典型疾病的诊断与治疗[4,20-21]。
在 PatSnap 数据库中检索合成生物医学应用领域相关数据,于 116 个国家/地区中,共检索到 1 826 组(5 043 件)简单同组专利(注:每组简单同族一个专利代表)。
专利计量检索式:TAC_ALL: ((“synthetic biology” or “genome editing” or “gene editing”or “CRISPR” or “synthetic genome” or “synthetic chromosome” or “gene assembly” or “DNA assembly” or “synthetic genomics” or “synthetic life” or “chromosome biology” or “genome engineering” or “DNA-based data storage” or “DNA computation” or “unnatural nucleotide” or “unnatural amino acid” or “de novo protein” or “directed evolution protein” or “genetic circuit” or “genetic logic gate” or “biosynthetic pathway” or “protocell”or “artificial cell” or “reconstitut cell” or “metabolic engineering” or “synthetic microbiome” or“synthetic microbiota” or “synthetic microbial communities” or “synthetic microbial consortia”or “microbiome engineering”) and (“medicine” or“therapy”))[22]。
3.2 全球专利态势分析
3.2.1 历年申请趋势分析
从计量分析可见(图 3),合成生物学医学领域专利数量逐年增加,专利申请增长趋势与论文增长趋势大体一致。自 2014 年起,随着全球合成生物学科研及产业布局加速,合成生物医学相关专利呈现爆发式增长(2020 年专利由于延迟数据公开不全,统计数据截至 2021 年 3 月 15 日)。在各国高度重视合成生物学医学学科发展的同时,各界也非常关注合成生物医学领域科技成果转化与产业应用,高度重视对知识产权的保护。
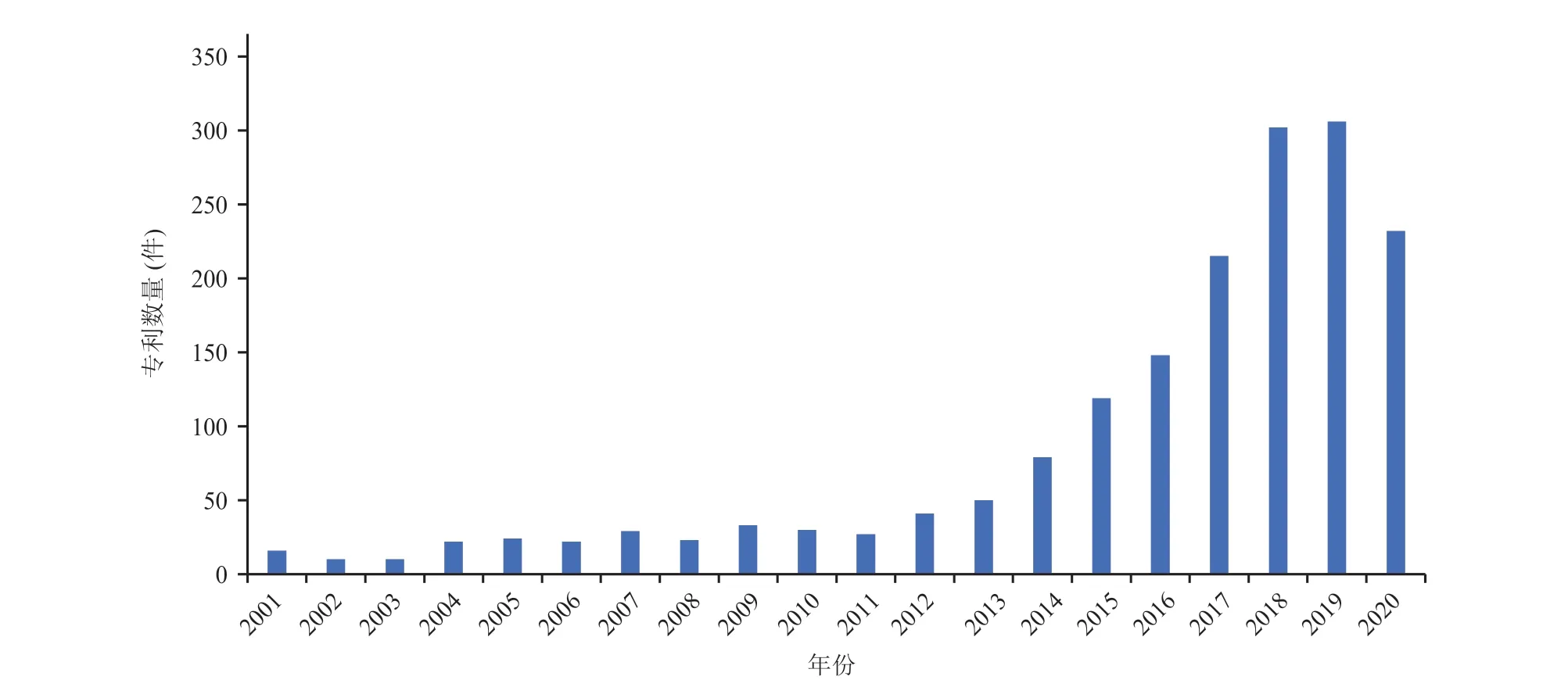
图3 合成生物医学领域专利申请趋势Fig. 3 Patenting trends in the field of synthetic biomedicine
3.2.2 技术来源趋势分析
美国在合成生物医学应用相关领域专利申请数量位于第一位(图 4),遥遥领先领先于其他国家,中国紧随其后,位列第二。从历年数据来看,美国在合成生物医学应用相关领域专利布局都远多于其他国家(图 5)。
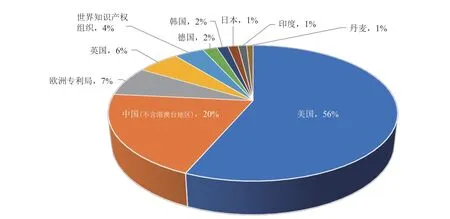
图4 合成生物医学领域专利来源分布(前 10,2001—2020)Fig. 4 Distribution of patents in the field of synthetic biomedicine (Top 10, 2001—2020)

图5 合成生物医学领域专利来源历年变化趋势Fig. 5 Trends of patents in the field of synthetic biomedicine
3.2.3 目标市场趋势分析
从合成生物医学领域专利目标市场来看(图 6~7),除了保护本国专利权之外,各国也非常重视在世界其他区域的专利保护。尤其值得关注的是,大部分专利保护关注中国市场。
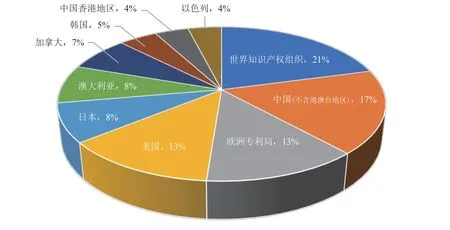
图6 合成生物医学领域专利目标市场分布(前 10,2001—2020)Fig. 6 Target market distribution of patents in the field of synthetic biomedicine (Top 10, 2001—2020)
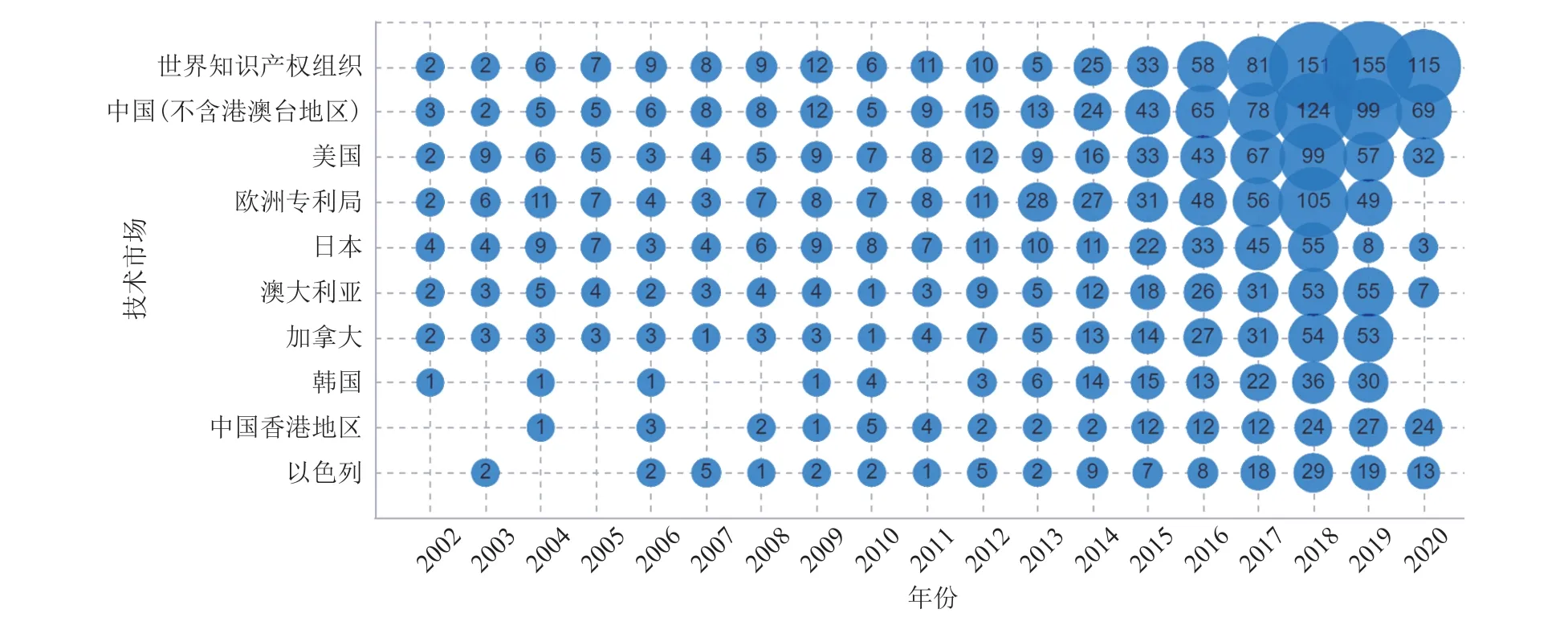
图7 合成生物医学领域专利目标市场历年变化趋势Fig. 7 Trend of target market of patents in the field of synthetic biomedicine
3.3 中国专利态势分析
随着合成生物学在中国的迅猛发展,许多高校与科研机构都有实际举措密切跟进,其中最为突出的是上海、天津和深圳的机构。从中国各省份/直辖市在合成生物学领域专利分布可以看出(图 8~9),相关专利主要集中在北京、江苏、上海与广东四个地区。

图8 中国各省/直辖市在合成生物医学领域的专利分布(前 10)Fig. 8 Distribution of patents in the field of synthetic biomedicine in China (Top 10)
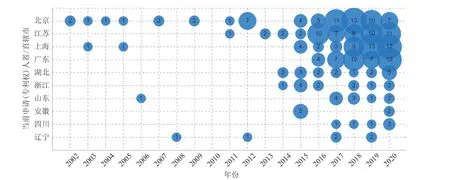
图9 中国各省/直辖市在合成生物医学领域历年专利申请趋势Fig. 9 Trend of patens application in the field of synthetic biomedicine in China
3.4 专利申请人技术流向分析
在合成生物医学领域,中国的专利申请目的地主要集中在中国,美国在全球多个国家/国际组织全面布局保护,说明其更加重视全球市场(表 4)。
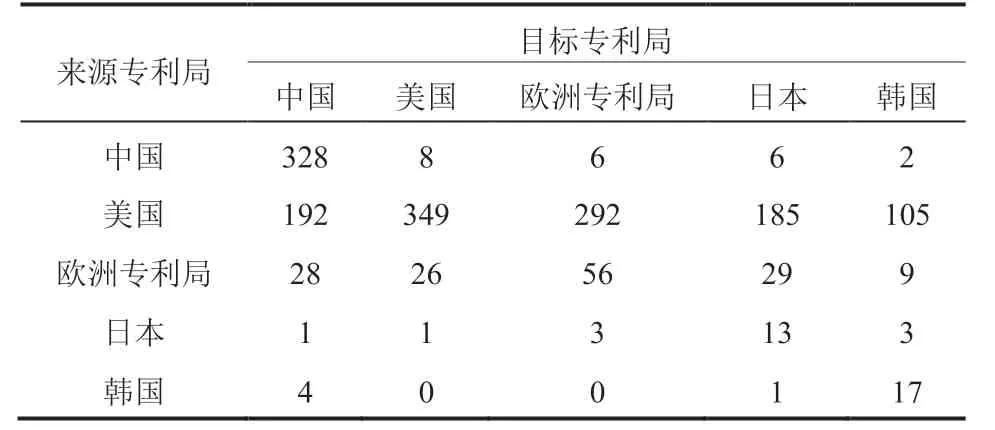
表4 合成生物医学领域重要国家技术流向(单位:件)Table 4 Key technological flows in the field of synthetic biomedicine (unit: piece)
3.5 主要国际专利分类
从国际专利分类号(International Patent Classification,IPC)的角度来看(表 5),合成生物医学领域专利主要集中在 C12N(微生物或酶;变异或遗传工程)、A61K(医用、牙科用或梳妆用的配制品)、A61P(化合物或药物制剂的特定治疗活性)、C07K(肽)、C12Q(包含酶、核酸或微生物的测定或检验方法)、G01N(借助于测定材料的化学或物理性质来测试或分析材料)、C07D(杂环化合物)、A01K(畜牧业;禽类、鱼类、昆虫的管理;捕鱼)、C07H(糖类;及其衍生物;核苷;核苷酸;核酸)、C12P(发酵或使用酶的方法合成目标化合物或组合物或从外消旋混合物中分离旋光异构体)。
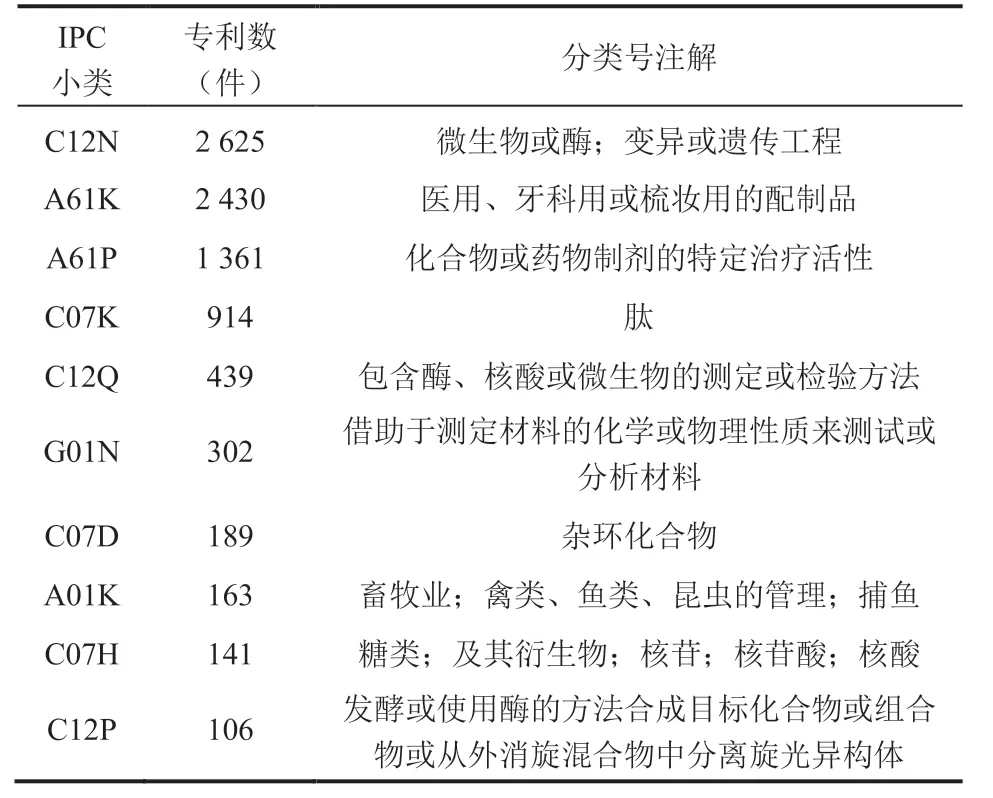
表5 合成生物医学领域专利国际分类分布Table 5 IPC distribution of patents in the field of synthetic biomedicine
3.6 重要专利申请人分析
从合成生物医学领域重要申请人分布来看(表 6),专利申请量排名前 15 的机构,仍主要分布在美国,占 12 席,其他国家 3 席。而在各机构中,当前以高校和研究所居多(9 席),企业迎头赶上(5 席)。美国各主要机构在合成生物医学领域研发上占据明显主导优势。值得一提的是,从 2018 年开始,中国人民解放军军事科学院军事医学研究院在合成生物医学应用方面具有不可小觑的发展趋势,2018—2020 年共申请 26件相关专利。
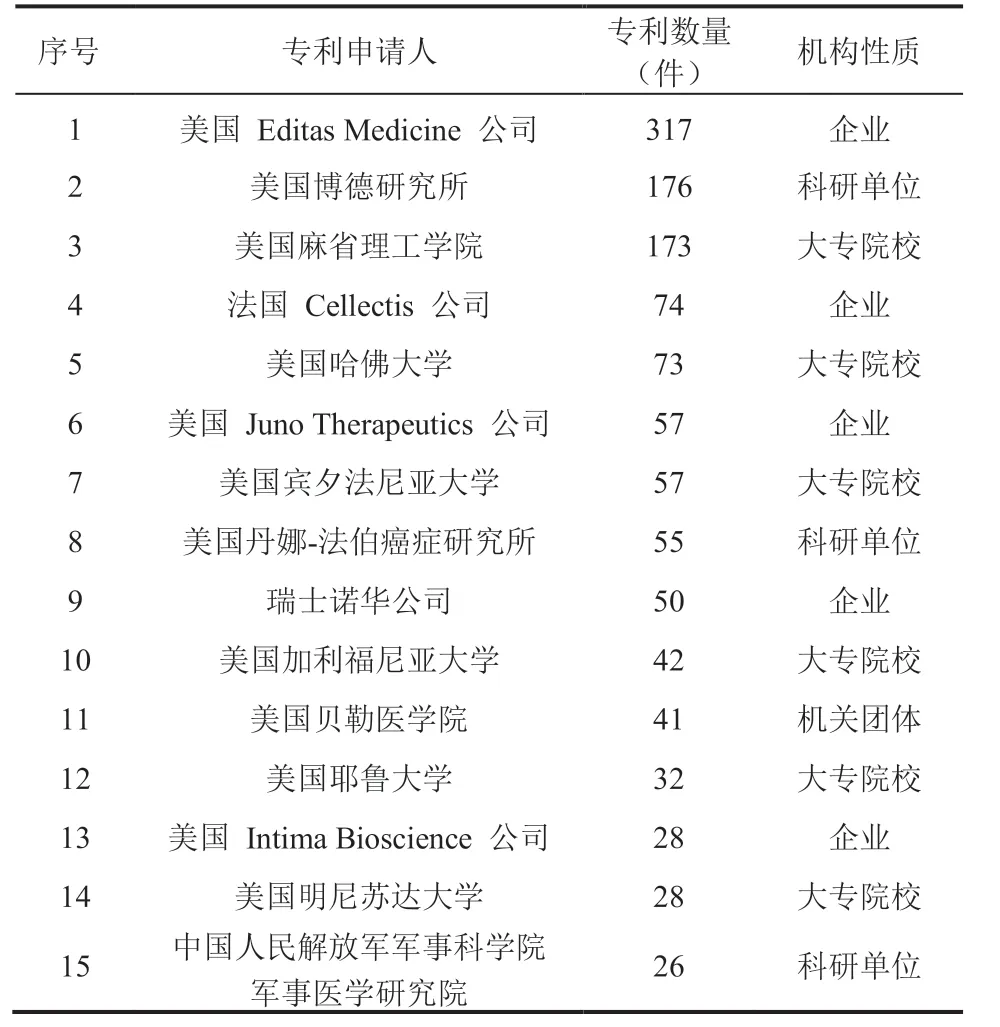
表6 合成生物医学领域重要专利申请人分布Table 6 Distribution of important patent applicants in the field of synthetic biomedicine
从重要专利申请人技术解析来看(表 7),在合成生物医学领域,美国重要专利申请人在全球多个国家/地区/国际组织全面布局保护,说明美国更加重视全球市场,与专利申请人技术流分析趋势一致。主要包含的范围部分,又主要集中在C12N(微生物或酶;变异或遗传工程)、A61K(医用、牙科用或梳妆用的配制品)等领域。
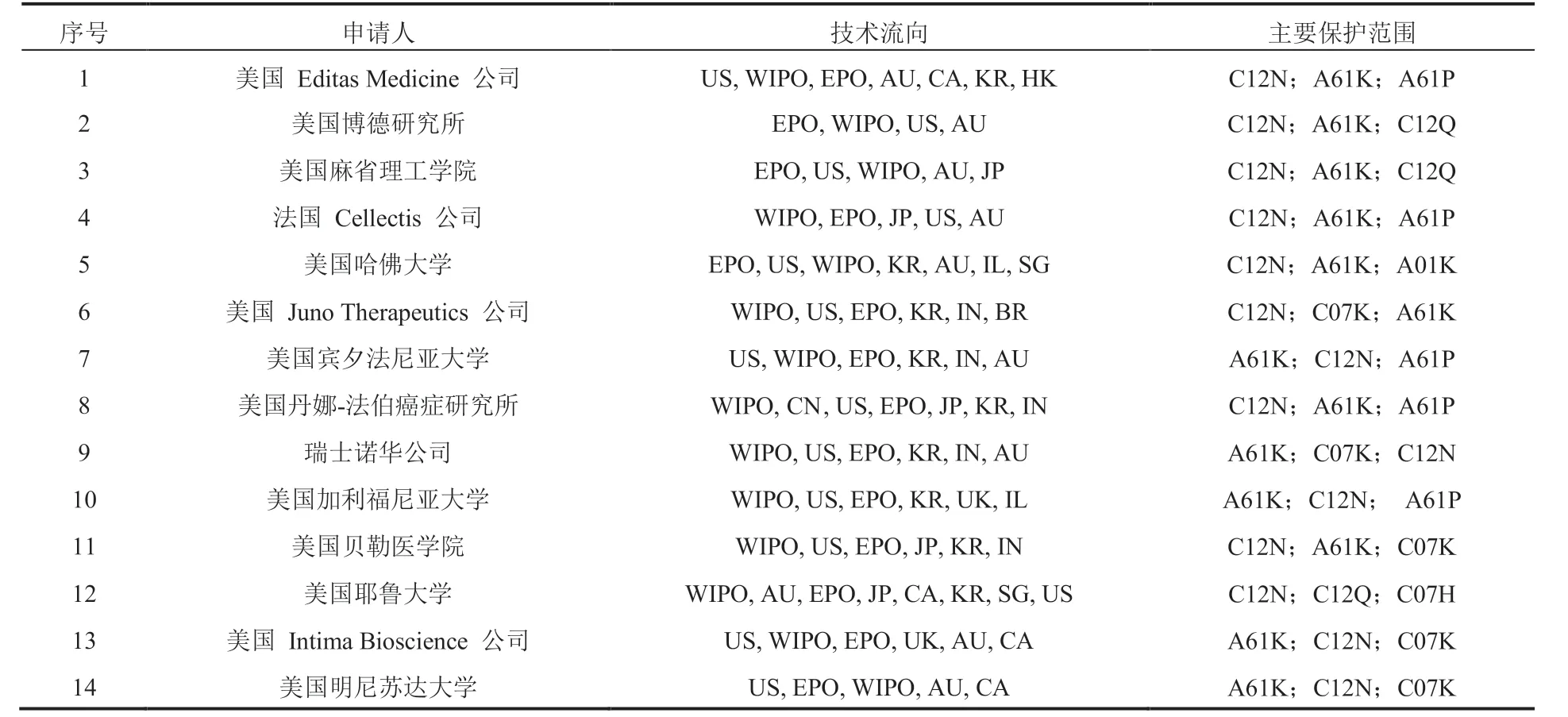
表7 合成生物医学领域重要专利申请人技术解析Table 7 Technical analysis of important patent applicants in the field of synthetic biomedicine
3.7 代表性专利
根据估值情况,列举前 10 项代表性专利(表 8)。从表 8 可以看出,代表性专利申请人以美国高校与企业居多。在合成生物医学应用领域,美国起步早,且已在产业应用方面进行全面布局。

表8 合成生物医学领域代表性专利Table 8 Representative patents in the field of synthetic biomedical science
4 总结与展望
2020 年,当 COVID-19 新冠病毒大流行席卷全球时,合成生物学界成为制定有效诊断措施以及研发药物和疫苗的主要力量之一,凭借他们手中的先进技术迅速应对这一巨大挑战[23]。
计量分析可见,随着全球各科技强国在合成生物学领域的战略布局与系列政策的制定,合成生物医学领域的论文与专利逐年增长。自 2014年起,随着全球合成生物学科研及产业布局加速,合成生物医学领域论文与专利呈现爆发式增长。从论文发表量来看,美国(占 44.5%)遥遥领先于其他各国。近年来,我国在合成生物学方向投入持续增大,科研领域蓬勃发展,但较美国仍有一定差距,发文量紧随其后(占 21.9%),中美两国的发文量总计占全球 2/3 以上。从机构分析来看,美国各机构发文数量仍处于领先地位,中国科学院在合成生物医学领域发文 555 篇,位居全球第三。
从专利布局来看,美国在合成生物医学领域专利申请量上的优势体现了其在该领域的技术主导地位。自 2014 年后,我国在合成生物医学领域的专利数量也明显增长,成为该领域专利数量排名第二的专利来源国家。从专利技术流向来看,美国更加重视全球市场,而我国则主要集中于国内;从专利主要保护范围来看,各机构对微生物或酶工程、基因工程或者医用配置品等方面的保护比较重视。
未来十年,合成生物等前沿生物技术或将彻底变革医疗领域,我国合成生物医学领域的发展突飞猛进,尤其 2019 新冠肺炎疫情防控中合成生物技术在诊断、疗法以及疫苗研发方面表现突出,但较美国仍存在一定差距。因此,为推动我国合成生物医学领域发展,提出以下三点建议:
第一,保持基础研究投入,强化原创成果产出。近两年,我国对合成生物学方向投入持续加大,科研领域蓬勃发展,但较美国仍有一定差距。为避免在生物领域重蹈信息领域“卡脖子”覆辙,亟需加强我国合成生物学战略布局和发展路线凝练。新冠疫情的爆发,人民对生命健康的关注达到前所未有的高度,加强合成生物医学领域技术攻关,强化重大原创成果产出,将进一步提升我国在全球合成生物医学领域的国际影响力与话语权。
第二,注重科技转化,加强专利布局。在已有科学研究基础上,积极培育高价值专利,加强全球市场专利布局。在现有科技成果转化政策基础上,特别关注并完善合成生物等前沿生物科技成果产业转化体制机制。同时,加强合成生物等前沿生物技术知识产权专业服务机构,建立前沿生物技术知识产权保护绿色通道,构建知识产权快速协同保护体系,打造科技金融和科技成果转化平台、知识产权和科技信息服务平台。
第三,审慎而科学地规制与监管。合成生物在应用领域具有无法估量的价值,合成生物技术作为典型的两用性技术,与其他两用生物技术一样,也存在生物安全风险。在针对合成生物技术潜在风险的具体监管制度构建方面,应采用谨慎的、科学的理念和机制。建议为合成生物学,尤其在合成生物医学方面的相关研究与开发建立注册登记系统,制定分类风险评估标准与计划,由独立的专家小组逐一评估每一类合成生物技术与产品。加快出台具有针对性、可操作性的合成生物医药品或诊疗方式市场准入规范及政府监管政策。
