吸波材料辅助的初始非饱和物料微波冷冻干燥
2021-07-19唐宇佳姬艺佳张大为
唐宇佳, 王 维, 张 朔, 姬艺佳, 张大为
吸波材料辅助的初始非饱和物料微波冷冻干燥
唐宇佳, 王 维, 张 朔, 姬艺佳, 张大为
(大连理工大学 化工学院, 辽宁 大连 116024)
为了强化冷冻干燥过程,制备咖啡溶液的初始饱和与非饱和2种冷冻样品,分别使用石英与碳化硅底盘进行常规和微波冷冻干燥实验,同时采用电阻法测定溶液的共晶温度。结果表明,在温度为25℃、压力为22 Pa时采用石英底盘,初始非饱和物料冷冻干燥时间比饱和物料缩短了14.9%,适当提高操作温度可以强化冷冻干燥过程。在25℃、22 Pa时施加功率为1 W的微波,饱和与非饱和物料干燥时间分别缩短了19.1%和12.5%;当温度提高至35℃时,非饱和物料可避免崩塌,微波冷冻干燥时间比非饱和与饱和物料常规冷冻干燥(0 W)分别缩短了20.6% 和30.8%。在35℃、22 Pa、1 W下采用碳化硅底盘,非饱和物料微波冷冻干燥时间比非饱和与饱和物料常规冷冻干燥分别缩短了32.4% 和42.5%。吸波材料辅助的初始非饱和物料微波冷冻干燥实现了过程传质传热的同时强化。
吸波材料;饱和度;冷冻干燥;微波加热;传质传热
1 前 言
速溶咖啡食用便捷、品质稳定、便于运输和储存,是当今流行的饮品[1]。在咖啡生产干燥工艺中,冷冻干燥可以避免高温对有效成分的破坏,产品口感好、品质佳[2-4]。但是,冷冻干燥时间长、能耗高,增加了生产成本[5-6]。冷冻干燥是一个典型的质、热耦合传递过程。强化冷冻干燥过程必须从传质和传热2个方面入手。Searles[7]和Pikal[8]均认为,冷冻干燥的主要传递阻力来自水蒸气在干燥层的迁移。冷冻阶段决定了物料内部孔隙(或冰晶)的大小、形状和连通性。因此,优化冷冻阶段是强化传质的有效手段,包括控制冷冻速率、调节冰晶成核和退火处理[9-12]。这些方法的共同点是通过增大冰晶尺寸降低升华干燥阻力。但是,冰晶尺寸增大会导致物料内部比表面积减小,解吸干燥阻力增大[13-14],强化效果并不明显。直接冷冻方法制备的冷冻物料内部没有初始孔隙,不能从根本上为升华/解吸的气体提供便捷的传质通道。Wang等[15]采用“软冰”冷冻技术将待干料液制备成具有初始孔隙的“非饱和”物料,再进行冷冻干燥。物料的初始孔隙可以减小水蒸气迁移阻力,较大的内部比表面积也有利于束缚水分解吸,从而大幅度强化了传质过程,提高了冷冻干燥速率[16-17]。但是,物料孔隙率的增大会降低干燥层的有效导热系数从而增大传热阻力,干燥过程的速率控制因素由传质转变为传热[18]。强化传热最简单而直接的方法是提高操作温度。但是操作温度不能高于物料的共晶或玻璃化转变温度[19]。Hua等[20]认为冷冻干燥过程的主要传热方式是导热和辐射,物料与加热板间的不良接触是传热的外部阻力。Degrazio等[21]指出,为了将热量从物料表面传递到内部,必须减小干燥层的传热阻力。微波加热可以实现物料整体加热,从而避免内部传热阻力[22-23]。但是,微波加热具有选择性,取决于物料的损耗因子。由于冰的损耗因子很小,几乎不吸收微波,微波加热效果取决于物料中固体基质的吸波能力。如果固体基质不易吸收微波,微波加热将不起作用。Wang等[24]在微波冷冻干燥过程中使用具有较大损耗因子的吸波材料碳化硅(SiC)来辅助微波加热。SiC首先吸收微波并转换为热能传递给物料,从而显著强化了传热过程[25-26]。但是,在较大微波功率下升华的气体不能及时迁移到外部,物料出现局部过热、甚至塌陷现象[26],表明传质又成为过程的速率控制因素。
Liapis和Bruttini[19]指出,冷冻干燥的内部传递阻力是过程的主要速率控制因素。结果表明,只有寻求传质传热的同时强化,才能从根本上解决冷冻干燥时间长、能耗高的问题。本研究在课题组以前研究的基础上,以咖啡为溶质,用初始非饱和冷冻物料强化传质,同时用吸波材料SiC辅助微波加热强化传热。本研究采用电阻法测定咖啡溶液的共晶温度,以此为依据确定物料的冷冻温度;然后制备初始饱和与非饱和的2种冷冻物料,使用石英和SiC 2种底盘,进行常规和微波冷冻干燥实验,考察初始非饱和物料和吸波材料辅助微波加热对冷冻干燥过程的影响;同时基于扫描电子显微镜(SEM)表征,分析干燥产品的多孔固体骨架结构对干燥过程的强化机理和崩塌现象的内在原因。本研究旨在同时强化冷冻干燥过程的传质和传热,以期建立更加合理高效的冷冻干燥方法,为冷冻干燥过程的工业应用提供指导。
2 实验材料与装置
2.1 材料与仪器
本实验以咖啡(质量分数为100%,雀巢,中国)为溶质,去离子水(大连理工大学)为溶剂。液氮购自大连化学物理研究所(中国)。
实验主要仪器包括磁力搅拌器(Wiggens,WB2000-D,德国)、电子天平(Mettler,ME403E,±0.6 mg,瑞士)、电热风干燥箱(一恒,DHG-9070A,RT(10±1)~(300±1) ℃,中国)、水分测定仪(Mettler,HR83-P,±0.001%,瑞士)、冷冻干燥机(Christ,Alpha 1-4 LSCplus,德国)、扫描电镜(SEM,Scanning Electronic Microscope,FEI,Quanta450,美国)。
2.2 共晶点测试装置
为了确定合适的冷冻温度,本研究采用电阻法测定咖啡溶液的共晶温度。冷冻温度以物料的共晶或者玻璃化转变温度为依据,若冷冻温度较高,则会导致部分水分不能完全冻结,使得物料在干燥过程中发生收缩和表面硬化;若冷冻温度过低,则会增加能耗和生产成本[27]。因此,确定物料的共晶温度,对冷冻干燥过程优化具有重要意义。电阻法测量共晶点的原理是基于物料冻结过程中物理化学行为的变化。因电阻法对材料结构的变化具有较高的灵敏度,被广泛应用于结晶过程的研究[28]。
本实验是在Christ冷冻干燥机的共晶点测试系统(Lyo control measuring system)上进行的。该系统主要包括冷冻干燥机冷阱、无线加热隔板(WST,122576,德国)、共晶点测试探头(LyoRx,125130,德国)和数据处理软件(LyoLogplus,125025,德国),如图1所示。

图1 共晶点测试装置流程图
2.3 冷冻干燥实验装置
本文实验在一套自行设计和组装的多功能微波冷冻干燥装置上进行,如图2所示。该装置包括5个子系统:真空系统、控温系统、数据采集系统、冷冻系统和微波加热系统。

图2 冷冻干燥实验装置流程图
1. freezer 2. cool trap 3. vacuum pump 4. pressure sensor 5. regulating valve 6. heat exchanger 7. ring blower 8. Circulator 9. heating cabinet 10. coaxial-to-waveguide transducer 11. microwave drying chamber 12. infrared sensor 13. date acquisition card 14. microwave solid-state source 15. PC 16. three-way valve 17. sample mold 18. load cell
真空系统包括微波干燥室、真空泵和冷阱。控温系统包括换热器、环形风机、恒温循环槽和热风循环室,用于控制干燥室的表面温度。数据采集系统包括数据采集卡、计算机和3个传感器。传感器产生的模拟信号经LabVIEW程序数字化处理后,在计算机上实时显示和存储。冷冻系统为一台深冷冰柜。有关4个子系统的详细描述参见文献[29]。微波加热系统包括同轴波导转换器和固态微波源(Wattsine,WPS-2450-300,中国)。有关固态微波源的选取和微波干燥室的设计参见文献[30]。
3 实验方法
3.1 物料的共晶温度测量
首先制备咖啡水溶液:将一定量的咖啡与去离子水混合,放置在磁力搅拌器上搅拌,配制成水质量分数为60%的咖啡溶液。共晶点测量步骤如下:
1) 开启冷冻干燥机,运行预冻程序,使冷阱温度降至-50 ℃左右;
2) 用滴管取8 mL咖啡溶液移入西林瓶,将西林瓶置于冷冻干燥机的冷阱中;
3) 将共晶点测试探头端置于样品溶液中,连接线端口插入冷冻干燥机无线加热隔板的温度和电阻传感器接口内,观察冷冻干燥机操作面板上的样品温度和相对电阻率读数是否正常;
4) 打开数据处理软件,调至数据采集界面,记录样品温度和电阻率随时间的变化;
5) 待样品的电阻率趋于稳定并达到最大值时,认为样品达到共晶状态,共晶点测量实验结束。依次关闭数据采集系统和冷冻干燥机。
6) 处理数据。
咖啡溶液的共晶温度测量结果如图3所示。图中2条曲线分别为样品温度s和样品相对电阻率随时间的变化。从图中可以看出,在<1 800 s时,样品温度从室温开始不断降低。在≈1 500 s时,样品温度达到水的冰点,而样品仍未冻结;温度继续降低,在=1 800 s时达到-8 ℃,这个阶段称为过冷阶段。由于样品过冷度较高,当>1 800 s时,冰晶开始成核并生长,释放出结晶热,样品温度快速上升,在=2 100 s时样品温度升高到-4 ℃,在温升时冰晶停止生长,这个阶段称为一次成核阶段。在这2个阶段中,有较多带电离子可以自由移动,溶液的导电性良好,电阻率缓慢上升[31]。在>2 100 s时,由于冷阱不断提供冷量,样品温度又开始下降,冰晶持续生长,这个阶段称为二次成核阶段。在这一阶段,更多液态水转化为冰,自由电荷被束缚,电阻率开始快速升高。随着溶液被进一步浓缩,离子强度逐渐增强,溶液最终形成共晶或因黏度过高而转变成无晶型固体[15,32]。此时电阻率达到最大值,对应的温度为共晶温度[33]。从图3中可以看出,最大电阻率对应的咖啡溶液共晶温度为-17.5 ˚C。
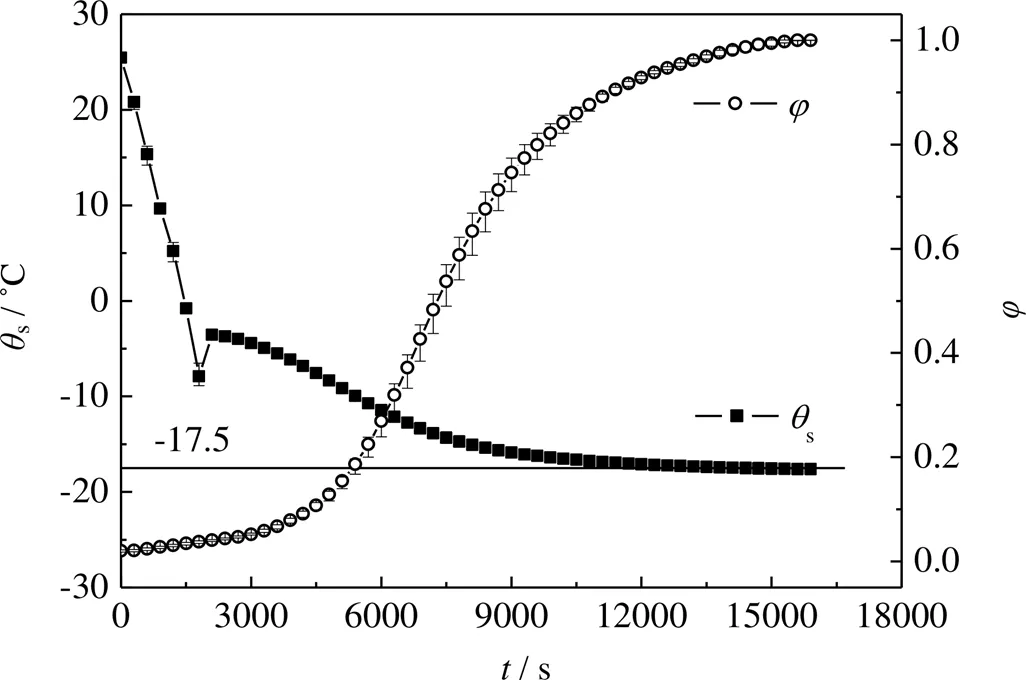
图3 冷冻过程中样品温度和相对电阻率的变化
3.2 微波冷冻干燥实验
3.2.1 不同初始饱和度样品制备
咖啡溶液的制备方法与共晶点测试实验中使用的方法相同。饱和物料的制备是将溶液直接注入模具,与底盘一起在冰柜中冷冻成型。该方法制备的冷冻样品不含初始孔隙。非饱和物料的制备采用软冰(soft ice)冷冻技术[34]。将待干料液置于保温桶内,边搅拌边缓慢加入液氮,使得料液发泡膨化。随着温度降低,溶液逐渐形成冰激凌状的多孔结构,然后再装入模具塑形,放入冰柜中进一步冷冻。如此制备的冷冻样品含有一定的初始孔隙。需要指出,非饱和物料制备过程中不加入任何添加剂[15,30,32]。为了保证物料的完全冻结,冷冻温度通常低于物料共晶温度或玻璃化转变温度10~20℃[27,33]。由于需要将本实验的样品从冰柜中移入干燥室内,这一过程又将产生约10℃的温升。综合以上考虑,本实验最终选取冷冻温度为-48 ℃,冷冻时间为6 h。
非饱和物料制备过程的详细步骤,以及冷冻物料样品的初始饱和度0和初始孔隙率的计算方法见文献[29]。饱和物料(0=1.0)和非饱和物料(0=0.2)初始水质量分数均为60%,初始质量均为2.5 g,样品直径均为19 mm,饱和样品高度为16 mm,非饱和样品高度为39 mm。需要特别指出,非饱和物料的初始饱和度为0.2,是水质量分数为60% 的咖啡溶液发泡膨化体积最大时饱和度。若采用较大的初始饱和度,料液的膨化体积较小,冷冻物料内部的初始孔隙较小,不能充分体现非饱和物料的优越性;若采用更小的初始饱和度(需要加入添加剂),冷冻物料固体骨架的刚度将会降低,干燥过程中极易发生崩塌。实验使用了石英和SiC这 2种材质的底盘,其中SiC底盘仅在4.4节中使用。2种底盘的直径均为30 mm,厚度均为6 mm。
3.2.2 实验步骤
本实验采用辐射加热和组合加热(辐射+微波) 2种加热模式。典型操作条件为:干燥室辐射温度=25 ℃,干燥室压力=22 Pa。微波源发射功率设定为5 W,显示反射微波功率为4 W,故样品吸收和无效损耗功率合计为1 W。操作步骤简述如下:
1) 开启风机(图2中7,下同)和循环水浴(8)预热干燥室(11)至设定温度;向冷阱(2)中加入液氮,调节三通阀(16)使干燥室与真空系统连通;开启真空泵(3),调节阀门(5)使干燥室达到设定压力。
2) 预热完成后,调节三通阀使干燥室与真空系统暂时隔离,将样品组件(17)从深冷冰柜(1)中取出,快速地放入干燥室,调节三通阀使干燥室与真空系统再次连通。
3) 开启固态微波源(14),调节输出功率至预设值。如果选择辐射加热模式,忽略此步骤。
4) 运行计算机(15)上的LabVIEW数据采集程序,自动记录压力传感器(4)、温度传感器(12)和质量传感器(18)读数随时间的变化。
5) 当样品质量没有明显变化时,干燥过程结束。停止运行数据采集程序,关闭固态微波源(如需要)。
6) 从干燥室中取出样品,测定干燥产品的水质量分数,进行SEM表征。
本实验使用电热风干燥箱和水分测定仪确定干燥产品的水质量分数,取两者平均值作为产品最终的水质量分数。操作步骤如下:首先将一次实验的干燥产品一分为二,当使用电热风干燥箱时,在(80±1)℃的温度下烘干约2 h直至样品质量不再变化;当使用水分测定仪测定时,设定温度上限为80℃,在50 s内失重小于1 mg时测试结束。2种方法测定结果十分接近,仅在千分位上有差异。为了考察多孔固体骨架的孔隙结构和连通性,本研究对冷冻干燥产品进行了SEM表征。SEM操作步骤如下:首先将干燥的样品切割成要求的尺寸,用导电胶黏附样品于模具上,使用氮气进行吹扫;然后使用喷金仪(Quorum,Q150T,英国)喷涂黄金薄层于样品表面,使得样品具有一定的导电性,避免出现扫描故障和图像伪影等问题;再将喷涂后的样品放在模具固定架上,缓缓移入扫描电镜室中进行扫描和成像。
4 结果与讨论
4.1 初始非饱和物料对冷冻干燥过程的影响
在典型操作条件(25℃,22 Pa)下,采用石英底盘,实验测试了2种不同饱和度样品的冷冻干燥过程,结果如图4所示。从图中可以看出,饱和样品(0=1.0)与非饱和样品(0=0.2)的干燥时间分别为23 500与20 000 s,非饱和物料比饱和物料干燥时间缩短了14.9%。初始非饱和物料能够有效强化冷冻干燥过程。这一结论与本课题组以前的实验研究结果相一致[15,17,32]。干燥时间的缩短意味着设备运行时间的缩短和能耗的降低。对于饱和物料,随着升华界面的缓慢退却,内部冰晶得以升华。但是,由于冰晶升华后的孔道较小,使得传质阻力较大。而对于非饱和物料,其内部存在的初始孔隙可为水蒸气的迁移提供便捷的通道,在一定程度上增大了多孔介质有效扩散系数,减小了传质阻力,促进了传质过程。此外,实验考察了2种物料干燥产品的水质量分数。初始非饱和物料产品中水的质量分数为1.45%,远小于饱和物料的4.66%。干燥产品具有较低的水质量分数有利于产品长期保存。需要特别指出,无论是观察干燥曲线还是干燥产品外观,干燥过程中都没有出现物料崩塌现象。还需要说明,文中所有实验均做了重复实验,结果显示重复性非常好,验证了结果的可靠性和准确性。

图4 不同初始饱和度样品的冷冻干燥曲线
为了分析具有预制孔隙冷冻物料对干燥过程的强化机理,本研究对2种干燥产品进行了SEM形貌表征。如图5所示,其中图5(a)~(c)分别为500、1 000和5 000倍数下的饱和物料产品,图5(d)~(f)为相应倍数下的非饱和物料产品。从图5(a)和(d)可以看出,饱和物料的孔隙结构紧密排列错乱,形状不规则。这是由于在常规条件下冷冻,液体物料内部存在温度梯度,导致不同位置的结晶速度不同,形成的冰晶尺寸也不同。相比于饱和物料,非饱和物料呈现出均匀的球状结构。这是因为物料在搅拌过程中加入液氮预冷冻,减小了物料内部的温度梯度,冰晶基本在相同的温度条件下成核,形成的冰晶尺寸一致,分布均匀。同时液体物料发泡膨胀,使得冰晶并没有充满全部的孔隙空间,整体骨架结构蓬松多孔。这些预制的孔隙空间为水蒸气的迁移提供了便捷的通道,减小了传质阻力。

图5 饱和与非饱和物料常规冷冻干燥产品SEM图
从图5(b)和(e)中可知,饱和物料的孔隙较小,孔径在15 μm左右;非饱和物料的孔隙较大,孔径在80 μm左右,远大于饱和物料。并且饱和物料的孔与孔之间无空隙,相邻孔隙之间由固体基质隔开,水蒸气在孔隙间迁移时需通过厚实的固体基质层,增大了传质阻力。而非饱和物料的孔壁之间是连通的,水蒸气不仅可以通过孔隙迁移,还可以通过孔壁的空隙和孔与孔之间的空间来迁移,传质效率得到了显著的提高。对比图5(c)和(f)可知,相比于饱和物料,非饱和物料的孔壁更加纤薄,这有利于吸附水的脱附,干燥产品的水质量分数能够达到更低。因此,非饱和物料的孔隙结构不仅加快了升华干燥阶段自由水的迁移过程,也提高了解吸干燥阶段吸附水的脱附速率,从根本上强化了过程传质。
4.2 操作温度对冷冻干燥过程的影响
从4.1节的实验研究结果和分析可知,具有预制孔隙的初始非饱和物料确实能够强化冷冻干燥的过程传质,提高干燥速率。但是随着干燥过程的进行,由于初始非饱和物料具有较大的孔隙空间,有效导热系数逐渐变小,在降低了传质阻力后,传热成为了过程速率的控制因素。提高操作温度是强化传热最简单而有效的方法。为了考察温度对2种物料冷冻干燥过程的影响,在操作压力(22 Pa)不变的情况下,将操作温度从25℃提高至35℃进行冷冻干燥实验,底盘材质仍然是石英,结果如图6所示。从图6中可以看出,随着温度的提高,2种物料的干燥时间均有缩短。对于饱和物料,干燥时间从23 500降至19 500 s,缩短了17.0%;对于非饱和物料,干燥时间从20 000缩短至17 000 s,缩短了15.0%。温度的升高会增大干燥室表面的热辐射功率,提高升华与解吸速率。因此,适当地提高干燥室表面辐射温度可以在一定程度上强化冷冻干燥过程传热,但过高的温度会使物料崩塌。对比35 ℃下2种物料的干燥时间可以看出,非饱和物料的干燥时间仍要少于饱和物料,这进一步证明了非饱和物料对于传质过程有着强化作用。

图6 操作温度对饱和与非饱和物料干燥过程的影响
4.3 微波加热对冷冻干燥过程的影响
冷冻干燥过程的操作温度要始终低于物料的崩塌温度,因此提高温度仅能在有限的范围内强化过程传热。微波加热具有独特的内加热特点,可以有效降低干燥层产生的传热阻力。咖啡已被证明具有较高的损耗因子,能够吸收一定的微波[35]。因此,本研究考察了微波加热对咖啡溶液冷冻干燥过程的影响。在25 ˚C、22 Pa和功率为1 W的微波条件下,仍然采用石英底盘,对饱和与非饱和的物料样品进行了微波冷冻干燥实验,结果如图7所示。与无微波(0 W)时相比,在1 W条件下,饱和与非饱和物料的干燥时间分别缩短了19.1% 和12.5%,说明微波能够利用物料本身的吸波性完成由电磁能向热能的转变。相比于其他加热方式,微波加热为内源加热,可直接穿透干燥层到达物料内部,传热效率更高[36-37]。在维生素C水溶液的微波冷冻干燥过程中,由于维生素C的损耗因子极小,难以吸收微波,常规的微波加热不能将微波能量有效地施加于待干物料上,微波加热不起作用[30]。因此,准确地说在微波冷冻干燥过程中,微波加热的效果取决于冷冻物料中固体基质的损耗因子。比较图7与6,1 W时2种样品的干燥时间与无微波加热35 ℃下的干燥时间基本持平,证明在本实验条件下极小的微波功率输入就能够达到操作温度提高10 ℃所产生的加热效果。当微波功率提高至2.5 W时,2种样品都能够保持其原有的结构,但干燥时间比1 W时都缩短不多,强化幅度有限。咖啡虽然能够吸收一定量的微波,但由于冰的损耗因子不够大,物料整体的吸波能力有限,使得一部分微波能被浪费。因此,在本实验条件下2.5 W的微波功率没有太大的意义。
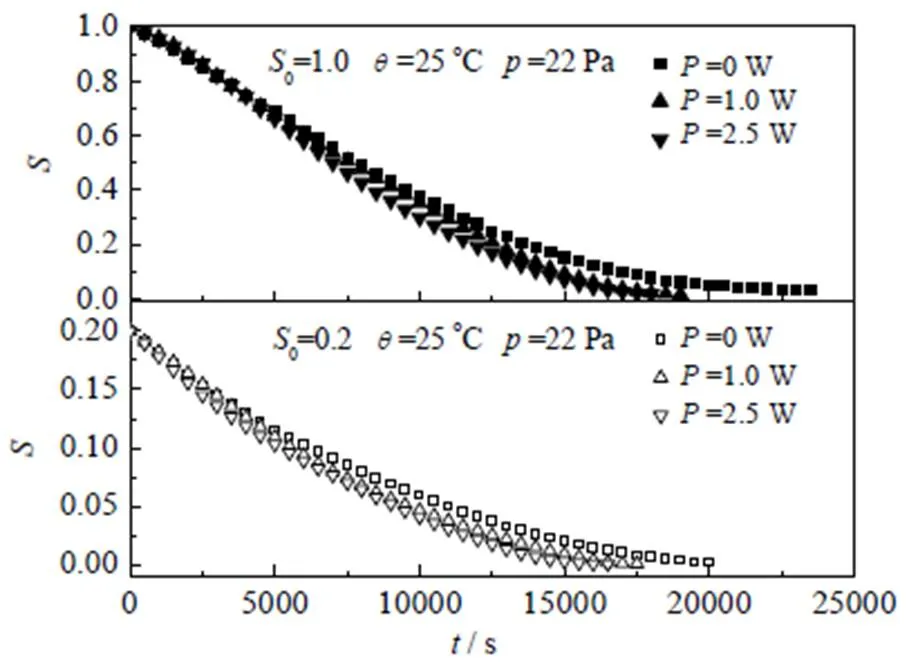
图7 25 ˚C下微波加热对饱和与非饱和物料干燥过程的影响
在保持22 Pa和1 W的条件下,将操作温度提高至35℃进行冷冻干燥实验。实验中发现,饱和物料在该条件下发生了崩塌,产品的实物图和SEM图如图8所示。从图8(a)饱和物料干燥产品的实物图中可以看出,崩塌位置在样品的内部。这是由于常规冷冻物料内部是饱和的,干燥过程中升华界面逐渐从样品表面向内部移动。微波的内源加热作用使得样品内部温度升高,水蒸气无法通过致密的干燥层及时向外迁移。当局部温度超过样品的共晶或者玻璃化转变温度时,物料会融化或者黏度降低,水蒸气会冲破外部的固体骨架,导致样品的结构崩塌[38]。观察图8(b)样品的SEM形貌发现,崩塌后的样品出现了典型的片状无晶型结构[39],物料内部几乎失去了所有传质通道,如此会使一部分水分存留在塌陷的样品内部,导致干燥过程无法进行,水分脱除不彻底、产品质量不佳[40]。

图8 饱和样品微波冷冻干燥产品的实物图和SEM图
与饱和物料不同,非饱和物料在该实验条件下没有发生崩塌,产品的实物图和SEM图如图9所示。从图9(a)中可以看出,干燥产品的品相完好。图9(b)与图5(d)和(e)的结构相同,证明微波加热没有改变非饱和物料的初始预制孔隙结构。同时表明非饱和物料所具有的初始孔隙能够有效地避免局部过热现象,均匀而有序的骨架结构在干燥过程中具有更好的稳定性和更宽泛的温度适应范围。35℃下非饱和样品的微波冷冻干燥曲线如图10所示。在1 W条件下,干燥时间比无微波加热时缩短了20.6%,这与图7中35℃条件下的实验结果相类似。35℃和1 W条件下非饱和物料的干燥时间比35℃和0 W条件下(图6)饱和物料缩短了30.8%。在采用微波加热强化传热过程的基础上,采用非饱和物料能够进一步强化传质过程,从而实现传热传质的同时强化。

图9 非饱和样品微波冷冻干燥产品的实物图和SEM图

图10 35 ˚C下微波加热对非饱和物料干燥过程的影响

图11 不同温度下非饱和物料碳化硅辅助微波加热的干燥曲线
4.4 吸波材料辅助微波加热对冷冻干燥过程的影响
为了进一步强化传热、提高能量利用率,本实验采用具有较大损耗因子的吸波材料SiC底盘代替石英底盘进行冷冻干燥实验,结果如图11所示。在温度分别为25和35℃条件下(22 Pa),采用SiC底盘的微波冷冻干燥(1 W)时间分别为14 000和11 500 s。与石英底盘的微波冷冻干燥(1 W)相比,干燥时间分别缩短了20.0%和14.8%。这是由于SiC材料介电损耗因子较大、吸波能力较强,而且导热系数较高[41]。在实验过程中,SiC底盘能够有效地将电磁能转换为热能,并通过热传导的方式将热量传递给物料,进而提高了能量利用率。
从图11中可知,相比于2种温度下的常规冷冻干燥(0 W),采用SiC底盘的微波冷冻干燥时间均缩短了30% 以上。本研究采用的方法能够利用微波内源加热的特点减小传热阻力,结合吸波材料SiC辅助加热的特点充分吸收微波,从2个方面强化了过程传热。对比图6中25和35 ˚C下饱和物料的常规冷冻干燥(0 W),SiC辅助的非饱和物料微波冷冻干燥时间分别缩短了40.4% 和42.5%。与饱和物料相比,初始非饱和物料具有更大的孔隙空间,较大的有效扩散系数和较小的气体扩散阻力,能够使物料内部的水蒸气得以快速迁移,大幅度强化过程传质;吸波材料辅助的微波加热是让物料底盘首先吸收微波并转化为热能,然后以热传导的方式传递给物料,同时固体基质也吸收一定量的微波成为内热源,能够使物料充分吸收微波能,大幅度强化过程传热。因此,本研究采用的吸波材料辅助的初始非饱和物料微波冷冻干燥可同时强化过程的传质传热,显著缩短干燥时间、提高能量利用率。该方法为解决冷冻干燥过程能耗大、时间长的问题提供了新的解决方案。
5 结 论
采用软冰冷冻技术制备了咖啡溶液的初始非饱和冷冻物料,在吸波材料SiC辅助下进行微波冷冻干燥实验,旨在强化过程的传质传热。具体结论如下:
(1) 初始非饱和物料能够强化过程传质。非饱和物料具有疏松的球状孔隙结构,显著降低过程传质阻力,干燥产品具有较低的水质量分数。适当提高干燥室表面辐射温度,饱和与非饱和物料的干燥时间均有所缩短。
(2) 微波加热能够强化过程传热,饱和与非饱和物料的微波冷冻干燥时间均明显缩短。提高辐射温度,饱和物料发生了崩塌,非饱和物料具有较好的温度耐受性。初始非饱和物料的微波冷冻干燥实现了过程传质传热的同时强化。
(3) 吸波材料辅助的微波加热能够进一步强化过程传热,非饱和物料的干燥时间进一步缩短。吸波材料辅助的初始非饱和物料微波冷冻干燥实现了过程的终极强化。
[1] HUMBERT S, LOERINCIK Y, ROSSI V,. Life cycle assessment of spray dried soluble coffee and comparison with alternatives (drip filter and capsule espresso) [J]. Journal of Cleaner Production, 2009, 17(15): 1351-1358.
[2] BALLESTEROS L F, RAMIREZ M J, ORREGO C E,. Encapsulation of antioxidant phenolic compounds extracted from spent coffee grounds by freeze-drying and spray-drying using different coating materials [J]. Food Chemistry, 2017, 237(24): 623-631.
[3] KESHANI S, WAN R W, NOUROUZI M M,. Spray drying: An overview on wall deposition, process and modeling [J]. Journal of Food Engineering, 2015, 146(3):152-162.
[4] PADMA I S, ANANDHARAMAKRISHNAN C. Spray-Freeze-Drying approach for soluble coffee processing and its effect on quality characteristics [J]. Journal of Food Engineering, 2015, 149(6): 171-180.
[5] NAIL S L, JIANG S, CHONGPRASERT S,. Fundamentals of freeze-drying [M]. New York: Kluwer Academic & Plenum Publishers, 2002: 281-361.
[6] WANG W, CHEN G H. Physical interpretation of solid drying: an overview on mathematical modeling research [J]. Drying Technology, 2007, 25(4): 659-668.
[7] SEARLES J A. Freezing and annealing phenomena in lyophilization [M]. New York: CRC Press. 2010: 52-81.
[8] PIKAL M J. Freeze drying [M]. New York: Informa Healthcare, 2007: 1807-1833.
[9] CAPOZZI L C, PISANO R. Looking inside the ‘black box’: Freezing engineering to ensure the quality of freeze-dried biopharmaceuticals [J]. European Journal of Pharmaceutics and Biopharmaceutics, 2018, 129(6): 58-65.
[10] GOSHIMA H, DO G, NAKAGAWA K. Impact of ice morphology on design space of pharmaceutical freeze-drying [J]. Journal of Pharmaceutical Sciences, 2016, 105(6): 1920-1933.
[11] SACLIER M, PECZALSKI R, ANDRIEU J. Effect of ultrasonically induced nucleation on ice crystals' size and shape during freezing in vials [J]. Chemical Engineering Science, 2010, 65(10): 3064-3071.
[12] SEARLES J A, CARPENTER J F, RANDOLPH T W. Annealing to optimize the primary drying rate, reduce freezing-induced drying rate heterogeneity, and determine T'g in pharmaceutical lyophilization [J]. Journal of Pharmaceutical Sciences, 2001, 90(7): 872-887.
[13] ODDONE I, PISANO R, BULLICH R,. Vacuum-induced nucleation as a method for freeze-drying cycle optimization [J]. Industrial & Engineering Chemistry Research, 2014, 53(47): 18236-18244.
[14] ODDONE I, BARRESI A A, PISANO R. Influence of controlled ice nucleation on the freeze-drying of pharmaceutical products: the secondary drying step [J]. International Journal of Pharmaceutics, 2017, 524(1/2): 134-140.
[15] WANG W, HU D P, PAN Y Q,. Freeze-drying of aqueous solution frozen with prebuilt pores [J]. AIChE Journal, 2015, 61(6): 2048-2057.
[16] 牛利娇, 王维, 潘思麒, 等. 具有预制孔隙多孔介质冷冻干燥的多相传递模型 [J]. 化工学报, 2017, 68(5): 1833-1844.
NIU L J, WANG W, PAN S Q,. Multiphase transport model for freeze-drying of porous media with prefabricated porosity [J]. CIESC Journal, 2017, 68(5): 1833-1844.
[17] 李恒乐, 王维, 李强强, 等. 具有预制孔隙多孔物料的冷冻干燥 [J]. 化工学报, 2016, 67(7): 2857-2863.
LI H L, WANG W, LI Q Q,. Freeze-drying of porous frozen material with prefabricated porosity [J]. CIESC Journal, 2016, 67(7): 2857-2863.
[18] WANG W, HU D P, PAN Y Q,. Numerical investigation on freeze-drying of aqueous material frozen with pre-built pores [J]. Chinese Journal of Chemical Engineering, 2016, 24(1): 116-125.
[19] LIAPIS A I, BRUTTINI R. Freeze drying [M]. New York: CRC Press, 2015: 259-282.
[20] HUA T C, LIU B L, ZHANG H. Freeze-drying of pharmaceutical and food products [M] Cambridge: Woodhead Publishing Limited, 2010: 18-67.
[21] DEGRAZIO F L. Closure and container considerations in lyophilization [M]. New York: CRC Press. 2010: 396-412.
[22] CHANDRASEKARAN S, RAMANATHAN S, BASAK T. Microwave food processing-a review [J]. Food Research International, 2013, 52(1): 243-261.
[23] OZCELIK M, AMBROS S, HEIGL A,. Impact of hydrocolloid addition and microwave processing condition on drying behavior of foamed raspberry puree [J]. Journal of Food Engineering, 2019, 240(1): 83-91.
[24] WANG W, CHEN G H. Numerical investigation on dielectric material assisted microwave freeze-drying of aqueous mannitol solution [J]. Drying Technology, 2003, 21(6): 995-1017.
[25] WANG W, CHEN G H. Heat and mass transfer model of dielectric-material-assisted microwave freeze-drying of skim milk with hygroscopic effect [J]. Chemical Engineering Science, 2005, 60(23): 6542-6550.
[26] WANG W, CHEN G H. Freeze drying with dielectric-material-assisted microwave heating [J]. AIChE Journal, 2007, 53(12): 3077-3088.
[27] MA Y, WU X, ZHANG Q,. Key composition optimization of meat processed protein source by vacuum freeze-drying technology [J]. Saudi Journal of Biological Sciences, 2018, 25(4): 724-732.
[28] WANG Y P, LU K. Accurate electrical resistance measurement of the crystallization kinetics of amorphous alloys [J]. Science in China, 2001, 44(1): 33-41.
[29] 于凯, 王维, 潘艳秋, 等. 初始非饱和多孔物料对冷冻干燥过程的影响 [J]. 化工学报, 2013, 64(9): 3110-3116.
YU K, WANG W, PAN Y Q,. Effect of initially unsaturated porous frozen material on freeze-drying [J]. CIESC Journal, 2013, 64(9): 3110-3116.
[30] 张朔, 王维, 李强强, 等. 具有预制孔隙的维生素C水溶液微波冷冻干燥 [J]. 化工学报, 2019, 70(6): 2129-2138.
ZHANG S, WANG W, LI Q Q,. Microwave freeze-drying of vitamin C solution frozen with preformed pores [J]. CIESC Journal, 2019, 70(6): 2129-2138.
[31] SEARLES J A, CARPENTER J F, RANDOLPH T W. The ice nucleation temperature determines the primary drying rate of lyophilization for samples frozen on a temperature-controlled shelf [J]. Journal of Pharmaceutical Sciences, 2001, 90(7): 860-871.
[32] WANG W, WANG S H, PAN Y Q,. Porous frozen material approach to freeze-drying of instant coffee [J]. Drying Technology, 2019, 37(16): 2126-2136.
[33] 崔清亮, 郭玉明, 程正伟. 冷冻干燥物料共晶点和共熔点的电阻法测量 [J]. 农业机械学报, 2008, 39(5): 65-69.
CUI Q L, GUO Y M, CHENG Z W. Measurement of the eutectic point and melting point of the freeze-dried materials based on electric resistance method [J]. Transactions of the Chinese Society for Agricultural Machinery, 2008, 39(5): 65-69.
[34] HARTEL R W. Ice crystallization during the manufacture of ice cream [J]. Trends in Food Science & Technology, 1996, 7(10): 315-321.
[35] ISSA A A, ALDEGS Y S, MASHAL K,. Fast activation of natural biomasses by microwave heating [J]. Journal of Industrial and Engineering Chemistry, 2015, 21(1): 230-238.
[36] AMBROS S, FOERST P, KULOZIK U. Temperature-controlled microwave-vacuum drying of lactic acid bacteria: impact of drying conditions on process and product characteristics [J]. Journal of Food Engineering, 2018, 224(9): 80-87.
[37] ZIELINSKA M, ROPELEWSKA E, XIAO H W,. Review of recent applications and research progress in hybrid and combined microwave-assisted drying of food products: quality properties [J]. Critical Reviews in Food Science and Nutrition, 2020, 60(1): 1-53.
[38] MILTON N, PIKAL M J, ROY M L,. Evaluation of manometric temperature measurement as a method of monitoring product temperature during lyophilization [J]. PDA Journal of Pharmaceutical Science and Technology, 1997, 51(1): 7-16.
[39] JIANG S, NAIL S L. Effect of process conditions on recovery of protein activity after freezing and freeze-drying [J]. European Journal of Pharmaceutics and Biopharmaceutics, 1998, 45(3): 249-257.
[40] PIKAL M J, SHAH S. The collapse temperature in freeze drying: Dependence on measurement methodology and rate of water removal from the glassy phase [J]. International Journal of Pharmaceutics, 1990, 62(2/3): 165-186.
[41] DONG S, ZHANG X, ZHANG D,. Strong effect of atmosphere on the microstructure and microwave absorption properties of porous SiC ceramics [J]. Journal of the European Ceramic Society, 2018, 38(1): 29-39.
Wave-absorbing material assisted microwave freeze-drying of initially unsaturated materials
TANG Yu-jia, WANG Wei, ZHANG Shuo, JI Yi-jia, ZHANG Da-wei
(School of Chemical Engineering, Dalian University of Technology, Dalian 116024, China)
The conventional and microwave freeze-drying experiments were carried out using initial saturated and unsaturated samples frozen from coffee solution on quartz and silicon carbide chassis respectively, and the eutectic temperature of coffee solution was determined by resistance method. The experiment results showed that the freeze-drying time of the initial unsaturated sample on quartz chassis was 14.9% shorter than that of the saturated one at radiation temperature 25 ℃and chamber pressure 22 Pa, and that increasing operating temperature could improve the freeze-drying process properly. The freeze-drying time of initial saturated and unsaturated samples under 25 ℃, 22 Pa and 1 W microwave power input was reduced by 19.1% and 12.5% respectively. When temperature was increased to 35 ℃, the unsaturated sample was more stable to avoid collapse, and the microwave freeze-drying time of the unsaturated sample was 20.6% and 30.8% shorter than the conventional freeze-drying (0 W input) time of unsaturated and saturated samples respectively. Under 35 ℃, 22 Pa and 1 W, the microwave freeze-drying time of the unsaturated sample on silicon carbide chassis was shortened by 32.4% and 42.5% compared with the conventional freeze-drying time of unsaturated and saturated samples respectively. This means that wave-absorbing materials assisted microwave freeze-drying of initial unsaturated materials has an enhanced effect on mass and heat transfer.
wave-absorbing materials; saturation; freeze-drying; microwave heating; mass and heat transfer
TQ 028.5;TQ 026.6;TQ 025.1
A
10.3969/j.issn.1003-9015.2021.03.006
1003-9015(2021)03-0430-10
2020-05-12;
2020-07-27。
国家自然科学基金项目(21676042);辽宁省自然科学基金(201602167)。
唐宇佳(1996-),男,辽宁辽阳人,大连理工大学硕士生。
王维,E-mail:dwwang@dlut.edu.cn
