替比培南匹酯在犬体内的相对生物利用度研究
2021-07-17罗玉莹周艺佳崔佳丽张培培赵高琼梅晶刘红斌王京昆
罗玉莹 周艺佳 崔佳丽 张培培 赵高琼 梅晶 刘红斌 王京昆*
(1.大理大学 云南大理 671000;2.云南省药物研究所;3.云南省中药和民族药新药创制企业重点实验室;4.昆明卫生职业学院药学院)
1 前言
替比培南匹酯(Tebipenem pivoxil)化学名为(4R,5S,6S)-6-[(1R)-1-羟基乙基]-4-甲基-7氧代-3{[1-(2-噻唑啉-2-基)-3-氮杂环丁烷基]硫}-1-氮杂双环[3,2,0]庚-2-烯-2-甲酸(2,2-二甲基-1-氧代丙氧基)甲酯[1],是替比培南的酯型前体药物,抗菌谱广、活性强,对大多数临床分离的菌株均表现出比青霉素及头孢类抗生素更强的抗菌活性[2]。它是世界上首类可以口服的碳青霉烯类抗生素,最早由美国辉瑞公司开发,日本明治制药株式会社研制的替比培南酯颗粒剂于2009年4月在日本上市,适用于治疗对青霉素敏感或耐药肺炎链球菌和流感嗜血杆菌所致感染,尤其是儿童耳鼻喉感染、上呼吸道感染、中耳炎和细菌性肺炎抗细菌感染[3-6]。
本试验采用HPLC-MS/MS方法,测定云南白药集团创新研发中心提供的替比培南匹酯片在禁食与进食2种状态下Beagle犬体内的药动学过程,计算主要药动学参数,并与日本明治公司生产的替比培南匹酯颗粒比较,进行相对生物利用度研究,为药品注册和临床用药提供依据。
2 材料
2.1 仪器
Agilent1200 SL液相色谱系统(美国Agilent公司);API 3200 Q-Trap三重四级杆质谱仪系统(美国AB公司);Allegra 64R高速冷冻台式离心机(美国Backman公司);DV215CD电子天平(OHAUS);XW-80A涡旋混合器(上海精科实业有限公司);Research移液器(德国Eppendorf公司)。
2.2 药品与试剂
替比培南匹酯片(125 mg/片,云南白药集团创新研发中心化学制药研究室提供,批号:FM20150503);替比培南匹酯颗粒(50 mg/袋,日本明治公司制造,批号:ORPEM2101);替比培南对照品(100 mg/管,云南白药集团创新研发中心化学制药研究室提供,纯度99%,批号:20151105);对乙酰氨基酚标准品(1 000 mg/瓶,中国药品生物制品检定所,,纯度98%,批号:100018-200408);甲醇、乙酸铵为色谱纯,3-N-吗啉基丙磺酸(MOPS)、氨水为分析纯,水为超纯水。
2.3 动物
普通级健康成年Beagle犬雌雄各4只,10~11月龄,体重范围为雌犬14.2~15.7 kg、雄犬15.4~18.2 kg,雌雄犬总体平均体重约为16 kg,购自广州医药研究总院有限公司,生产许可证号:SCXK(粤)2013-0007,经云南省药物研究所实验动物伦理委员会批准使用。
3 方法与结果
3.1 溶液配制
对照品储备液:精密称取替比培南对照品5.28 mg,用pH7.0的0.1 mol/L 3-N-吗啉基丙磺酸(MOPS)配制得浓度为0.211 mg/ml的替比培南对照品储备液,备用。
内标溶液:精密称取对乙酰氨基酚对照品8.21 mg,用甲醇溶解并稀释得浓度为0.328 mg/ml的对乙酰氨基酚标准储备液,进一步用甲醇稀释得浓度为2.46μg/ml的对乙酰氨基酚内标工作液。
3.2 分析检测方法
3.2.1色谱条件
色谱柱:Agilent poroshell EC-C18柱(50 mm×4.6 mm,2.7μm);流动相:见表1;柱温:25℃;进样量:10μl。
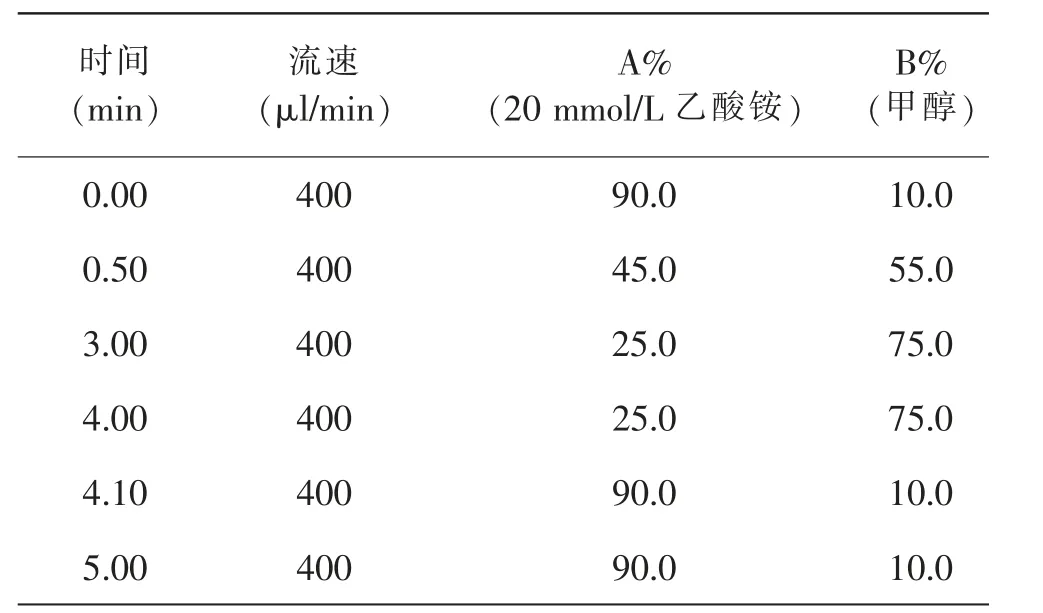
表1 流动相组成表
3.2.2质谱条件
采用电喷雾离子源(ESI),多反应监测模式(MRM)扫描,正离子方式检测;用于定量分析的离子对分别为m/z 384.1→298.0(替比培南,DP电压45 V,CE电压21 V);m/z 152.1→110.1(对乙酰氨基酚,DP电压42V,CE电压22V);离子源电压(IS):5500.00V;离子源温度(TEM):550.00℃;气帘气(CUR)压力30.00psi;雾化气(Gas1)压力:60.00psi;辅助气(Gas2)压力:60.00 psi;碰撞气(CAD)压力:Medium。
3.3 血浆样品处理
取50μl血浆样品,加入10μl内标工作液及100 μl pH7.0 1mol/LMOPS,涡旋混匀,加入200μl乙腈,涡旋30 s,4℃条件下15 000 r/min离心10 min,取出待恢复至室温后,取上清液50μl,加pH7.0 0.1 mol/L MOPS溶液400μl,涡旋混匀后,4℃条件下15000r/min离心10 min,取上清液进样测定。
3.4 方法学考察
3.4.1专属性
以6个来源不同的空白血浆、质控血浆(31.6 μg/ml)和Beagle犬口服替比培南匹酯片后1 h血浆样品,评价方法的专属性。结果如图1所示,表明空白血浆中没有干扰测定的物质。

图1 典型提取离子流图
3.4.2标准曲线与定量范围
制备浓度分别为26.00、7 8.00、234.0、700.0、2 100、6 320 ng/ml的血浆样品,按“2.3”项下方法处理后进样分析。以替比培南峰面积和内标峰面积的比值为纵坐标Y,待测物浓度值为横坐标X,采用加权最小二乘法拟合(W=1/X2),求其回归方程为Y=0.0018X-0.00493,r2=0.9956。表明在26.00 ng/ml~6320ng/ml范围内线性关系良好。定量下限为26.00 ng·ml-1。
3.4.3精密度和准确度
制备浓度分别为74.6、674和6040 ng/ml的低、中、高质控血浆样品,各6份,按“2.3”项下方法处理后进样分析。连续测定3 d,根据当日的标准曲线计算得低、中、高浓度血样的测定浓度,并计算本法的精密度与准确度。结果见表2。

表2 精密度和准确度试验结果
3.4.4提取回收率和基质效应
制备低、中、高浓度质控血样,各6份,按“2.3”项下方法处理后进样,测得峰面积(A1)。另取50μl空白犬血浆,按“2.3”项下方法处理得到空白血浆基质后,再加入低、中、高浓度的质控标准溶液和内标各10μl,使其与各浓度水平质控血样浓度保持一致,各6份,进样测得峰面积(A2),以水代替血浆,制备同理论浓度的纯溶液样本,各6份,进样测得峰面积(B)。提取回收率%=A1/A2×100%,基质效应%=A2/B×100%。计算得低、中、高浓度样品的平均提取回收率分别为107.62%、107.50%和105.35%;内标的平均提取回收率为117.40%、117.14%和111.01%。低、中、高浓度样品溶液的基质效应分别为100.44%、100.37%和99.50%,内标的基质效应为85.18%、87.99%和90.59%,表明血浆无明显基质效应。
3.4.5稳定性考察
分别考察未处理的血样于室温存放6 h、2~8℃存放至约6 h和24 h、约-20℃冻-融循环4次、约-20℃存放1 d、7 d、27 d的稳定性,以及按照“2.3”项下处理后质控血样室温存放24 h稳定性。结果表明替比培南含量无明显变化,RSD均小于15%。说明在上述条件下血浆样品均稳定。
3.5 相对生物利用度试验
3.5.1试验设计与血样采集
试验分为禁食给药试验和进食给药试验,均采用自身双交叉试验设计,2个周期间的洗净期为一周。选用健康Beagle犬8只,雌雄各半,分为2组,每组4只,参比制剂给药前用0.5%羧甲基纤维素钠配制,使两制剂给药剂量均为125 mg/只[7]。
禁食组给药前自由饮水并禁食约12h,给药后2 h统一喂饲;分别于给药前(0 h)和给药后0.17、0.33、0.67、1.0、1.5、2.0、3.0、5.0和7.0 h,于前肢隐静脉取血2 ml置肝素钠采血管中,3 000 r/min离心15min,分离血浆后,取血浆400μl分装,加入800μl pH7.0 1 mol/LMOPS溶液,混合均匀后,-20℃保存,备用。进食组禁食12 h并于给药前1 h禁水,给药前30 min统一喂食150 g/只+100 ml水/只,分别于给药前(0 h)和给药后0.17、0.33、0.67、1.0、1.5、2.0、3.0、5.0和7.0 h,于前肢隐静脉取血2ml置肝素钠采血管中,同上处理后备用。
3.5.2平均血药-浓度时间曲线
8只Beagle犬分别在禁食与进食情况下口服受试和参比受试和参比制剂后的平均药-时曲线见图2。
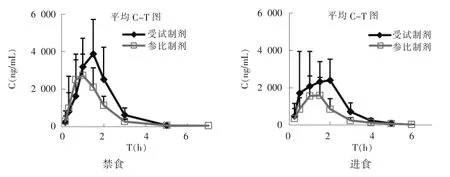
图2 两种状态下平均血药浓度-时间(C-T)曲线图
3.5.3药代动力学参数
用DAS 2.0计算Beagle犬给药后的主要药动学参数,结果见表3。
表3 Beagle犬口服受试和参比制剂后的药动学参数(±s,n=8)

表3 Beagle犬口服受试和参比制剂后的药动学参数(±s,n=8)
禁食 进食受试制剂 参比制剂 受试制剂 参比制剂AUC(0-t)/ng·h·ml-1 6893±2942 4628±1780 5655±1351 2881±1484 AUC(0-∞)/ng·h·ml-1 6939±2948 4653±1777 5757±1370 2940±1473 cmax/ng·ml-1 4269±1847 3031±1115 3834±1321 2009±1179 tmax/h 1.29±0.38 0.94±0.28 1.44±0.68 1.19±0.37药动学参数
3.5.4相对生物利用度分析
相对生物利用度F%=受试制剂AUC(0-t)/参比制剂AUC(0-t)×100%,所以禁食状态2种制剂的相对生物利用度F%=6893/4628×100%=149%,进食状态下2种制剂的相对生物利用度F%=5655/2881×100%=196%。
禁食状态下2种制剂8只犬的AUC(0-t)和cmax经自然对数转化后用SPSS进行方差分析,均没有显著性差异(P>0.05),进食状态下2种制剂8只犬的AUC(0-t)和cmax经自然对数转化后用SPSS进行方差分析,发现有显著性差异(P<0.05),因为2种制剂均为常规制剂,未对tmax进行非参数检验。
4 讨论
本研究首次建立了适用于测定Beagle犬血浆中替比培南浓度的HPLC-MS/MS方法,并对方法学进行了完整的验证,相对于其他方法,本法更简单、快速、准确,适用于替比培南在Beagle犬体内相对生物利用度的研究。本实验采用乙腈蛋白沉淀法,与其他方法相比,操作简单,应用范围广,且不受物种和免疫原性限制[8]。
本试验中,Beagle犬于两种状态下给予受试制剂或参比制剂,均出现不同程度的呕吐,此现象与本药具有一定的胃肠道刺激性有关,由于Beagle犬的胃肠及其消化系统反应通常较为敏感,致使犬随着交叉实验给药次数的增加出现较明显的呕吐症状,且呕吐的时间具有随机性,均以参比制剂的影响稍明显,而该情况与参比制剂给予动物后血药浓度稍低于受试制剂的结果基本吻合。因此认为试验所获血药浓度-时间曲线与理想状态曲线的较大偏移可能主要与犬给药后的呕吐现象相关,与是否进食关系较小,直接影响了相对生物利用度结果的准确性。故仅从本次试验结果来看,2种制剂的相对生物利用度不一致。
