抑郁症患者精神焦虑与多导睡眠图参数相关性研究
2021-07-16丁秀珊徐彩霞徐国洪
丁秀珊 徐彩霞 徐国洪
广东省佛山市第三人民医院功能检查科,广东佛山 528000
抑郁症是心理学上常见的情感障碍之一,以持续性的情绪低落、悲观沮丧、消极应对为主要特征。随着社会节奏的不断加快,学习压力、工作压力、生活压力加大,抑郁症发病率呈现显著上升趋势,文献报道我国自然人口中抑郁患病率超过4.0%[1]。抑郁症除了已知的影响情绪功能、中枢神经系统功能、消化系统功能外,还可导致不同程度的入睡困难、失眠、睡眠觉醒等睡眠障碍。睡眠障碍又将加重抑郁症状,甚至诱发精神疾病、自杀倾向[2-3]。多导睡眠图(multiple sleep map,PSG)是评估睡眠障碍的重要方法,其通过监测睡眠过程中的脑电波参数变化,客观反应患者睡眠质量。本文分析了伴精神焦虑的抑郁症患者与不伴精神焦虑的抑郁患者PSG的结构参数差异,旨在了解抑郁患者睡眠结构参数与精神焦虑的相关性,为今后PSG监测抑郁症患者焦虑状况及改善睡眠质量提供指导。
1 资料与方法
1.1 一般资料
选取2018年6月至2020年5月于佛山市第三人民医院功能检查科接收的为抑郁症患者68例作为研究对象。按汉密尔顿抑郁24项(Hamilton depressive 24,HAMD 24)量表[4]中第 10项(HAMD-10)评分作为分组依据(0分=问及时诉述,1分=自发地表达,2分=表情及言谈流露出明显忧虑,3分=明显惊恐),以HAMD-10≥1分为伴精神焦虑(研究组,n=42),HAMD-10<1分为不伴精神焦虑(对照组,n=26)。两组患者的年龄、性别、婚姻状况、受教育年限、抑郁家族史、基础疾病比较,差异无统计学意义(P>0.05),具有可比性,见表1。本研究经医院医学伦理委员会批准,患者知情知悉并同意。
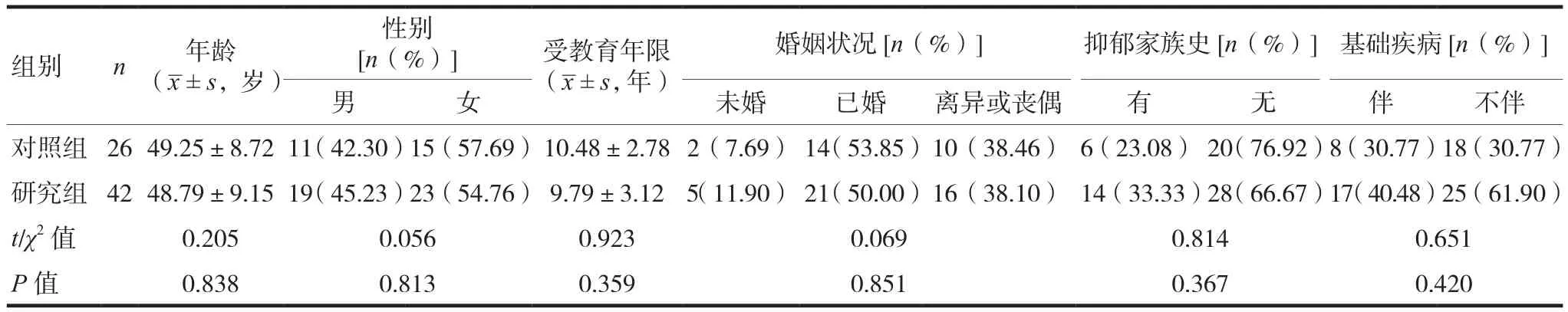
表1 两组患者基线资料比较
1.2 纳入与排除标准
纳入标准:①年龄>18周岁;②均经汉HAMD 24项版评分≥20分;③均为首次接受PSG监测。排除标准:①严重心、肝、肾脏器官病变;②肿瘤、自身免疫性疾病、心血管疾病、内分泌疾病、癫痫等;③妊娠或哺乳期妇女;④其他影响认知功能、躯体功能疾病;⑤合作性差,无法完成HAMD抑郁量表评测或PSG检测者。
1.3 方法
1.3.1 抑郁症 采用HAMD 24项版本[4],包含焦虑/躯体化、体重、认知障碍、日夜变化、阻滞、睡眠障碍、绝望感7个维度,共24个评价条目。正常:HAMD<8分,轻或中等抑郁症:20分< HAMD≤35分;重度抑郁症>35分[5]。
1.3.2 PSG监测 PSG监测采用德国施曼诺提供的PSG分析系统,嘱受试者检查当天不吃刺激性食物,不饮酒、浓茶、咖啡等饮料。多导睡眠环境:无干扰、相对舒适、房间隔音效果好,可遮挡光线的睡眠监测室内实施,室内环境温度为21~28℃,湿度调整为45%~65%。于当日8:30 pm安装PSG电极,取患者平卧位后侧卧位,在自然状态下入眠,分别在患者耳屏正前方、颧弓根凹陷处和左右耳前点置放脑电电极,于颏肌和胫骨前肌置放肌电电极,在眼外眦上、下方 0.8~1.2 cm置放眼电电极,在右锁骨下窝外1/3及左侧的锁骨中线4~5肋置放心电电极,时间参数设置为0.3 s,肌电参数为0.03 s,电压为40 μV。监测时间为当晚9:30pm至次日6:30am,监测时间为9 h,嘱咐患者依据作息时间睡眠。依据美国睡眠医学研究会睡眠及相关事件判读标准标准,判读睡眠分期,监测参数睡眠进程指标[总睡眠时间(total sleep times,TST)、睡眠效率(sleep efficiency,SE)、睡眠潜伏期(sleep latency,SL)、醒 觉 次 数(awakening,times,NW)、醒觉时间(awakening time,AT)],快速眼动相睡眠(rapid eye movement sleep,REMS)指标[REM活动度(REM activity,RA)、REM 强 度(REM intensity,RI)],非快速眼动相睡眠(non rapid eye movement sleep,NREMS)指标[非快动眼睡眠第1期(nonrapid eye movement sleep phase 1,N1)、非快动眼睡眠第2 期(non-rapid eye movement sleep phase 1,N2)、非快动眼睡眠第3期(non-rapid eye movement sleep phase 3,N3)]。多导睡眠图分析均由我院多导睡眠操作图分析经验>3年的医师实施,记录上述数据。
1.4 统计学处理
数据处理采用SPSS 18.0统计学软件;计数资料采用χ2检验;计量资料符合正态分布采用()表示,采用t检验;模型1将HAMD-10评分作为自变量,PSG参数作为应变量行单因素方差分析(One-Way ANOVA);模型2将HAMD校正分作为中心协变量,采用协方差分析精神焦虑与PSG参数是否受到抑郁症严重程度评分影响。HAMD校正分为HAMD 24项总分删除睡眠(第4、5、6条目)及精神焦虑(第10条目)的分数,P<0.05为差异有统计学意义。
2 结果
2.1 两组患者的PSG参数比较
研究组的TST、SE、N3低于对照组,差异有统计学意义(P<0.05);研究组的SL、NW、AT高于对照组,差异有统计学意义(P<0.05)。见表2。
表2 两组患者的PSG参数比较()
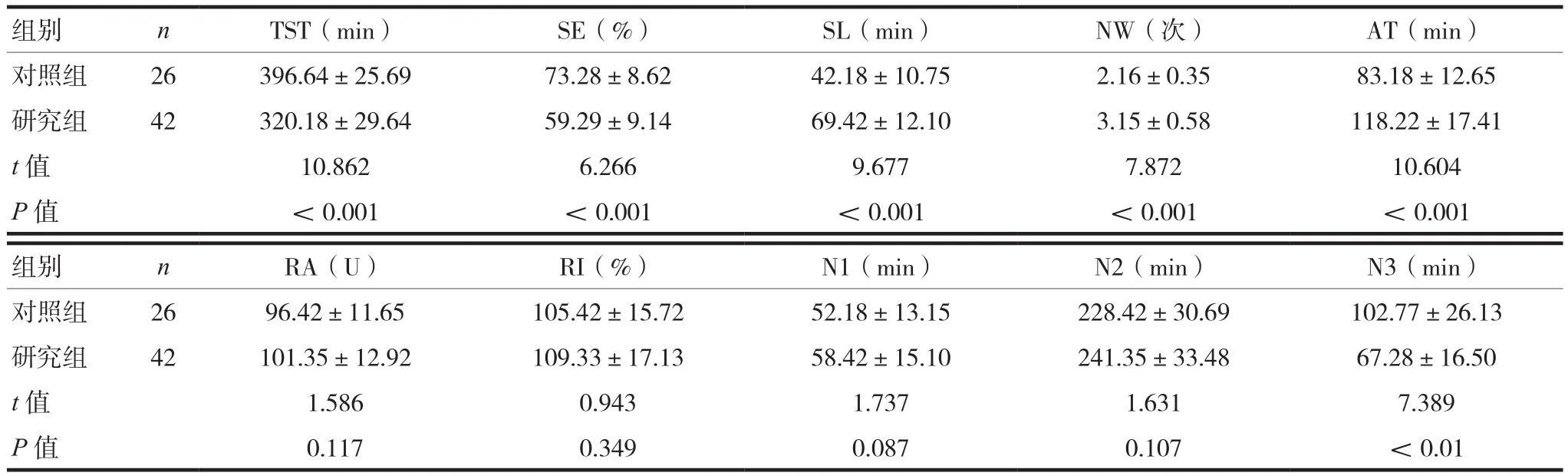
表2 两组患者的PSG参数比较()
组别 n TST(min) SE(%) SL(min) NW(次) AT(min)对照组 26 396.64±25.69 73.28±8.62 42.18±10.75 2.16±0.35 83.18±12.65研究组 42 320.18±29.64 59.29±9.14 69.42±12.10 3.15±0.58 118.22±17.41 t值 10.862 6.266 9.677 7.872 10.604 P值 <0.001 <0.001 <0.001 <0.001 <0.001组别 n RA(U) RI(%) N1(min) N2(min) N3(min)对照组 26 96.42±11.65 105.42±15.72 52.18±13.15 228.42±30.69 102.77±26.13研究组 42 101.35±12.92 109.33±17.13 58.42±15.10 241.35±33.48 67.28±16.50 t值 1.586 0.943 1.737 1.631 7.389 P值 0.117 0.349 0.087 0.107 <0.01
2.2 两组患者的PSG参数与精神焦虑的关联
模型1显示,抑郁症患者的精神焦虑与SL、NW、AT及N3有关;模型2显示,抑郁症患者的精神焦虑与AT及N3有关,差异有统计学意义(P< 0.05)。见表3。
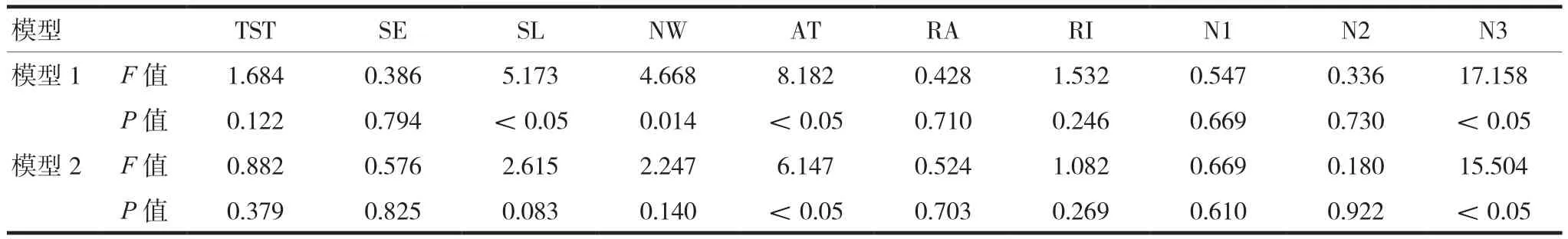
表3 抑郁症患者精神焦虑与PSG参数的方差分析
3 讨论
睡眠障碍以失眠症及睡眠结构改变为主要表现,睡眠障碍在西方发病率约35.2%,我国发病率约为40.0%[6],抑郁症患者约70.0%~90.0%伴有不同程度的睡眠障碍[7],表现为失眠、易醒、多梦。睡眠障碍将加剧抑郁、焦虑情绪,形成恶性循环[8-9]。PSG通过检测、记录睡眠中的生物电信号,实现对个体睡眠定量分析,可评估睡眠质量,发现早期睡眠异常。有研究[10]对伴精神焦虑与不伴精神焦虑患者行PSG监测,结果发现伴精神焦虑的TST、SE、SL、N3均低于不伴精神焦虑受试者,NW、AT均高于不伴精神焦虑受试者。本研究对象均为抑郁症患者,以是否伴精神焦虑实施分组,结果显示,伴精神焦虑的抑郁患者N1、N2有所延长,N3显著缩短,提示精神焦虑的抑郁症患者存在明显的睡眠效率低下及睡眠质量欠佳等问题。因此,在治疗抑郁症患者时,应重视睡眠质量的改善,阻断睡眠障碍对抑郁程度的恶性循环影响。
模型1显示,抑郁症患者的精神焦虑与SL、NW、AT及N3有关;模型2显示,抑郁症患者的精神焦虑与AT及N3有关,差异有统计学意义(P<0.05),提示PSG参数AT及N3与抑郁症患者精神焦虑密切相关,且相关性程度并不会受到抑郁严重程度的影响,可作为抑郁症患者精神焦虑的独立预测指标。笔者推测上述指标与抑郁症患者精神焦虑的关联原因可能为:①AT。失眠是精神焦虑的常见症状,也是精神焦虑的前驱症状,抑郁症患者伴精神焦虑均有不同程度睡眠障碍,其中以觉醒频繁及觉醒后入睡困难为常见表现。有研究[11-12]发现,精神焦虑的抑郁症患者普遍存在5-羟色胺(5-HT)、多巴胺(dopamine,DA)低表达。Wang等[13]研究发现,5-HT及DA的长期低表达,将加重焦虑症状。刘文娟等[14]通过睡眠剥夺诱导大鼠焦虑样行为,并测定血中5-HT水平,分析5-HT水平与焦虑量化行为的相关性,结果发现,5-HT低表达可导致焦虑量化行为明显增多。Bhatt等[15]通过对大鼠的睡眠多导图与5-HT关联分析发现,5-HT水平下降的大鼠焦虑评分更高,PSG表现为NW、AT上升,N3下降,其推测5-HT可能是引起焦虑的重要神经递质,并可导致醒觉次数增加、醒觉时间延长。5-HT若长期低表达,可导致神经元细胞兴奋性电冲动传导频率受到抑制,引起焦虑[16-17];5-HT的低表达还可抑制HPA轴神经传导功能[18-19],造成睡眠调节紊乱,引起睡眠剥夺,导致AT增加。②N3。N3期亦称为熟睡期,该时期肌肉完全放松、心跳缓慢、血压下降,N3期是评价睡眠质量的重要指标,研究[20]发现,N3时间或N3占NREM时间比例可作为抑郁、自杀倾向的独立影响因子。调查[21]发现,精神焦虑患者高达2/3存在入睡困难及睡眠维持困难,且在睡眠期可出现惊恐发作;惊恐发作后可引起心动过速、心悸、呼吸困难、窒息感,导致N3下降;惊恐发作后还将给患者留下的心理阴影将继续影响入睡速度、深度睡眠维持时间,造成睡眠剥夺。
本研究局限性在于研究样本数量较少,可能对研究结果产生偏倚,今后将加大样本数量进一步论证;另外由于汉密尔顿抑郁量表评分有HAMD 17、HAMD 21、HAMD 24项版本,本研究中采用的是HAMD 24项版本,在不同版本中由于评价条目数的差异可能会对研究结果产生影响,今后该类研究中应加以关注;由于关于伴精神焦虑的抑郁患者多导睡眠相关研究较少,缺乏文献横向比较,期待后续更多的相关研究涌现。
综上,伴精神焦虑的抑郁症患者存在更严重的睡眠障碍,PSG参数表现为SL、NW、AT下降,TST、SE、N3延长;AT及N3多导参数可能用于抑郁症患者精神焦虑的评估,关于AT及N3作为抑郁症患者伴精神焦虑的原因仍值得加以论证。
