不同处理态的高速列车用TP2铜导体腐蚀行为研究①
2021-07-12崔志国鲁海洋于海然薛学栋刘赛男蔡圳阳肖来荣
崔志国,鲁海洋,于海然,陈 曦,薛学栋,刘赛男,蔡圳阳,肖来荣
(1.中车青岛四方机车车辆股份有限公司,山东 青岛 266111;2.中南大学 资源加工与生物工程学院,湖南 长沙 410083;3.中南大学材料科学与工程学院,湖南 长沙 410083;4.有色金属材料科学与工程教育部重点实验室,湖南 长沙 410083)
车顶铜导体是高速列车输送电能的关键部件,由于常年在露天环境下工作且无备用设施,对其安全可靠性和使用寿命均有较高要求。目前常采用TP2铜(Cu含量不低于99.90%,P含量在0.015%~0.040%之间)作为高速列车车顶铜导体材料,其具备导电性高、导热性好和机械强度适中等优点。然而在实际服役过程中,铜导体裸露部分在服役一段时间后易出现表面变色甚至局部区域发生点蚀现象,这种腐蚀坑可能会导致后续服役过程中发生失效断裂[1],给高速列车的安全运行带来极大安全隐患。
前期研究表明,在含有工业气体的大气环境、酸雨环境或含有Cl-、SO42-离子的环境,铜及铜合金会出现明显的腐蚀现象[2-5]。例如在含SO2等工业废气的大气环境下铜表面会生成碱式硫酸铜导致腐蚀失效[6];文献[7]进一步指出,铜表面会形成Cu2O内层和Cu4SO4(OH)6外层两层腐蚀产物;在NO2气氛中Cu2O有被碱式硝酸铜代替的倾向[8];SO2和O3共同作用在铜的表面形成强腐蚀性的硫酸,SO2和O3的协同效应要大于SO2和NO2的协同效应[9];而在含Cl-的环境往往也会出现铜材腐蚀失效现象[10-11],主要腐蚀形式为蚁巢腐蚀[12],Cl-对铜合金的腐蚀与钝化金属在含Cl-的溶液中孔蚀机理一样[13],是通过Cl-对铜表面膜的局部破坏造成的[14-15],由于表面膜上的Cl-吸附和迁移不可能完全均匀,因此腐蚀往往从局部腐蚀点开始并逐渐扩大[16]。虽然Cl-和SO42-是铜及铜合金腐蚀失效的主要原因[17],但不同铜合金在不同腐蚀环境下的腐蚀过程、腐蚀速率和腐蚀行为均不尽相同[18],需要开展针对性研究。车顶铜导体服役环境为大气环境且易受到雨水浸蚀,其服役环境不排除Cl-、SO42-离子存在,目前SO42-和Cl-对TP2铜腐蚀行为的研究以及不同处理态TP2铜耐腐蚀性能差异的研究较少,因此有待于开展深入研究,剖析其腐蚀行为。
本文采用浓度均为10%的盐酸溶液和硫酸溶液加速模拟了高速列车车顶TP2铜导体的腐蚀行为,比较了TP 2铜对Cl-和SO42-的腐蚀敏感性,对比了硬态、半硬态两种不同处理态的TP2铜导体腐蚀性能,为进一步强化TP2铜导体的腐蚀防护与提高服役寿命提供基础数据。
1 实验方法
研究所用材料为硬态和半硬态的TP2铜管,其性能如表1所示。由表1可知,TP2铜管性能符合国标GB/T 1527—2006[19]要求。通过线切割手段将铜管切割为10 mm×10 mm×3 mm的样品,经过机械研磨、抛光后,在无水乙醇中超声振动清洗后备用。样品按照不同处理态(硬态、半硬态)分别置于10%盐酸溶液和10%硫酸溶液中腐蚀15 d(大气环境,平均温度约15℃),此后一起取出观察腐蚀后样品表面形貌、分析样品腐蚀产物,研究不同处理态下的TP2铜在不同腐蚀溶液中的腐蚀行为。

表1 实验用硬态和半硬态TP2铜管性能
使用D/max 2550型X射线衍射仪(XRD)分析表面腐蚀产物的相组成(Cu靶,40 kV,250 mA);采用MIRA3 TESCAN型场发射扫描电镜(SEM)观察腐蚀产物表面的微观形貌,并使用能谱仪分析TP2铜表面腐蚀产物元素分布情况。
2 实验结果与讨论
2.1 腐蚀形貌
对经10%盐酸溶液腐蚀15 d后的不同处理态的样品表面进行观察,其SEM形貌如图1所示。从图1可以看出,腐蚀产物呈颗粒状分布在样品表面,且已经将样品表面完全覆盖,说明此时样品表面已经被完全腐蚀。硬态样品的腐蚀产物多为多边形颗粒状,尺寸相对粗大,多为2~5μm;半硬态样品的腐蚀产物同样为不规则形状,尺寸相对细小,多为1~2μm。硬态和半硬态样品的Cl-腐蚀产物颗粒与颗粒之间存在缝隙、孔洞等微缺陷,半硬态样品腐蚀产物颗粒间的缝隙与孔洞密度相对于硬态样品更高,因此,在Cl-存在的环境下,半硬态样品更容易被腐蚀。

图1 盐酸溶液腐蚀后样品表面微观形貌
使用SEM对经10%硫酸溶液腐蚀15 d后的不同处理态的TP2铜样品表面进行观察,其形貌如图2所示。硬态和半硬态样品的腐蚀产物形貌存在明显差异,对于硬态样品,其腐蚀产物为阶梯层簇状,在腐蚀产物聚集区域有明显的片状或块状晶体,反应了腐蚀产物不断增殖的过程,在高放大倍数下可以观察到块状晶体之间有明显的缝隙。半硬态样品的腐蚀产物表面有更为明显的块状颗粒,随机分布在铜导体上,颗粒尺寸明显大于硬态样品,高放大倍数下可发现腐蚀产物表面存在明显裂缝,腐蚀产物厚度更厚、腐蚀程度更深。

图2 硫酸溶液腐蚀后样品表面微观形貌
2.2 腐蚀产物
使用能谱仪分析经10%盐酸腐蚀的TP2铜样品表面成分,结果如图3所示。由图3可知,不同处理态样品的腐蚀产物元素种类相同、元素分布类似,腐蚀产物中主要含有Cu、Cl元素,O元素含量少,这表明样品表面腐蚀产物主要为Cu和Cl化合物。进一步分析Cl元素分布情况可以观察到,硬态和半硬态样品表面均存在不少缝隙与孔洞,硬态样品缝隙尺寸更大,而半硬态样品缝隙与孔洞比例更高。
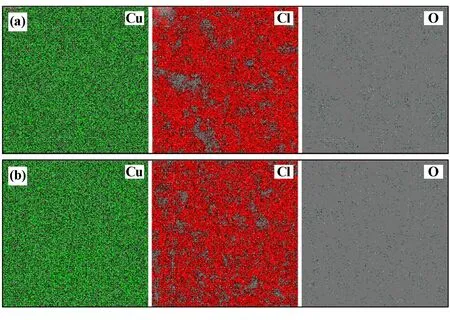
图3 盐酸溶液腐蚀后样品表面元素分布EDS面扫描图
不同处理态样品表面典型区域EDS点分析如图4所示。2种处理态样品表面腐蚀产物能谱结果相差不大,主要元素均为Cu、Cl,两者原子比约为1∶1,表明形成的腐蚀产物主体可能是CuCl;硬态和半硬态样品氧化产物的主要差别在于O元素含量略有不同,半硬态样品氧化产物氧含量1.19%(质量分数),略高于硬态样品的0.51%;相关文献认为O元素的主要存在形式为Cu2O[7,17-18],这是因为在样品表面形成CuCl以后,部分CuCl会水解形成Cu2O[13]:2CuCl+H2O →Cu2O+2HCl;相对于Cu和Cl元素的含量,2种处理态TP2铜氧化产物中O元素含量均很少,与EDS面扫描结果一致。
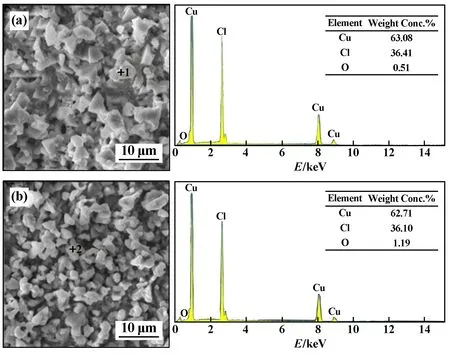
图4 盐酸溶液腐蚀后样品表面局部EDS成分分析
TP2铜在10%盐酸溶液中腐蚀15 d后,其表面产物的XRD分析结果如图5所示。从图5可以看出,腐蚀后2种处理态TP2铜表面的相组成均主要为Cu和CuCl相,由于Cu与CuCl同时存在,表明生成的腐蚀产物不连续或厚度不深,这可能与Cu在Cl-环境中的腐蚀形式主要为点蚀有关。对比硬态和半硬态样品腐蚀表面的XRD图谱,发现硬态较半硬态的Cu峰更高,表明其腐蚀程度更轻。

图5 盐酸溶液腐蚀后样品表面XRD图谱
使用能谱仪对经10%硫酸腐蚀15 d后的样品表面进行成分面扫描分析,样品表面元素分布图如图6所示。从图6可以看出,S元素与O元素在样品表面部分区域聚集,这是因为SO42-对TP2铜材料的腐蚀以点蚀为主。半硬态腐蚀样品表面大部分区域均分布有S和O元素,表明这些区域均已被腐蚀,而硬态样品还只有小部分区域被腐蚀,说明半硬态样品的腐蚀程度更深。
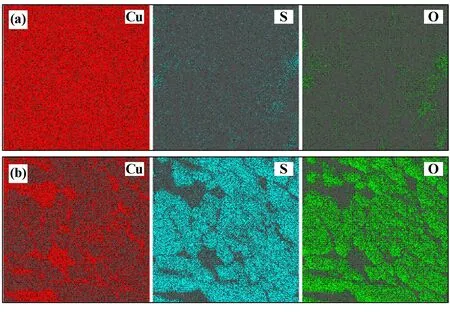
图6 硫酸溶液腐蚀后样品表面元素分布EDS面扫描图
对不同处理态的TP2铜样品表面部分区域进行EDS点分析,结果如图7所示。硬态样品表面元素仍以Cu为主,S和O元素含量很低,结合样品表面元素分布图来看,硬态样品只有部分区域被腐蚀,样品表面大部分仍然为Cu。而半硬态样品表面存在大量块状颗粒,该区域S和O元素含量大幅上升,说明块状颗粒为腐蚀产物,在腐蚀产物中间的缝隙区域仍然以Cu为主,含有少量的S和O元素。
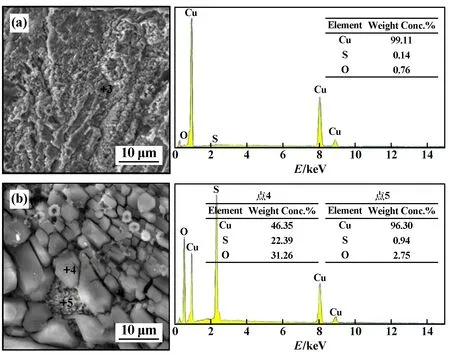
图7 硫酸溶液腐蚀后样品表面局部EDS成分分析
TP2铜在10%硫酸溶液中腐蚀15 d后,其表面产物的XRD分析结果如图8所示。在硬态TP2腐蚀样品的XRD图谱中仅检测到Cu,没有观测到腐蚀产物衍射峰,这可能与测试区域腐蚀产物含量偏低有关;而半硬态腐蚀样品表面的XRD图谱中出现了Cu与CuSO4(H2O)5的衍射峰,表明其腐蚀产物为CuSO4(H2O)5,不过CuSO4(H2O)5衍射峰峰强并不强,表明其腐蚀程度不深。
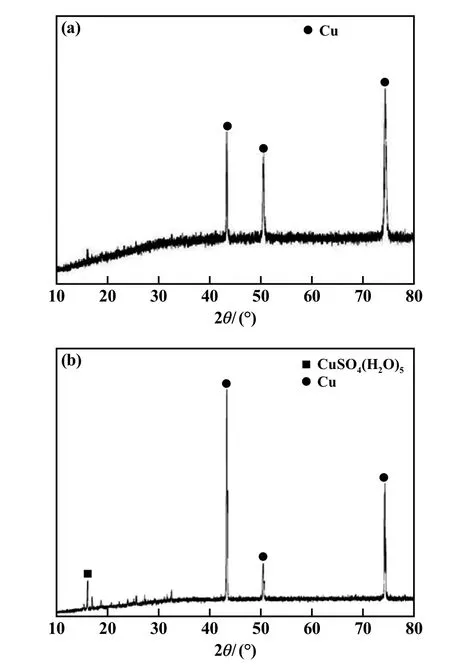
图8 硫酸溶液腐蚀后样品表面XRD图谱
综合对比TP2铜在10%盐酸溶液和硫酸溶液中的腐蚀行为,发现TP2铜抗Cl-腐蚀性能比抗SO42-腐蚀性能差,在盐酸溶液中形成的腐蚀产物已经完全覆盖样品表面,且腐蚀程度更深;在硫酸溶液中腐蚀相同时间后,TP2样品表面没有全面腐蚀,腐蚀仍仅限于局部区域。Cl-、SO42-对TP2铜的腐蚀均以点蚀为主,再逐渐发展为全面腐蚀。硬态和半硬态TP2铜材对Cl-和SO42-的耐蚀性不同,半硬态TP2铜材耐Cl-离子和SO42-离子腐蚀能力均弱于硬态TP2铜材。因此,基于耐腐蚀角度考虑,高速列车用TP2铜导体建议使用硬态TP2铜材;如使用半硬态TP2铜材则应在其表面制备均匀的耐腐蚀涂层以提升其耐腐蚀性能。
3 结 论
1)高速列车车顶TP2铜导体材料在10%盐酸溶液和10%硫酸溶液腐蚀15 d后的主要腐蚀产物分别为CuCl和CuSO4(H2O)5。
2)TP2铜在Cl-和SO42-溶液的腐蚀行为均以点蚀为主,再逐渐发展为全面腐蚀;TP2铜对2种离子表现出不同耐蚀性,对Cl-离子腐蚀更敏感,腐蚀更严重。
3)硬态和半硬态TP2铜在Cl-和SO42-溶液中的腐蚀产物基本相同,但腐蚀程度与腐蚀形貌不同,半硬态样品腐蚀程度更深,耐Cl-和SO42-腐蚀性能更弱。
