特发性门脉高压1例
2021-07-07张先姚李梦梦王姣张国梁
张先姚,李梦梦,王姣,张国梁
特发性门脉高压(idiopathic portal hypertension,IPH)是一种临床上很罕见的门脉高压,IPH的临床表现主要是一系列由门脉高压引起的症状和体征,但却尚未发现肝脏硬化的情况。我国临床上比较少见,现将1例特发性门脉高压病人的临床资料报告如下。
1 病例摘要
男,14岁,学生,汉族。因“反复肝功能异常1年”于2019年8月1日入院。病人1年前于安徽中医药大学第一附属医院骨科行右侧胫腓骨骨折后内固定取出术,完善术前检查时发现肝功能异常,生化提示丙氨酸氨基转移酶(ALT)116 U/L,天冬氨酸氨基转移酶(AST)67 U/L,尿酸(UA)594 umol/L,免疫组合(-),肝胆胰脾彩超未见明显异常,遵医嘱予以水飞蓟宾、复方甘草酸苷降酶治疗复查肝功能正常后停药。后定期门诊复查肝功能,2019年3月复查肝功能:ALT 73 U/L,AST 48 U/L,予以甘草酸二胺肠溶胶囊口服后复查肝功能恢复正常。7月26日查肝功能:ALT 102 U/L,AST 68 U/L,为求进一步诊治入住我科。病人既往身体健康,否认肝炎病史,否认家族遗传病史,无个人不良生活史。查体:神志清楚,精神可,正常面容。皮肤弹性好,全身皮肤黏膜及巩膜未见黄染,皮肤黏膜无皮疹,未见出血点及蜘蛛痣,浅表淋巴结无肿大,双手肝掌(-)。心肺听诊(-),腹部平坦,对称,压痛及反跳痛(-),肝区叩击痛(-)。肝肋下未触及,脾肋下未触及,腹部移动性浊音(-),双下肢未见水肿。辅助检查:血常规:白细胞计数4.29×10/L,红细胞计数4.69×10/L,血红蛋白142 g/L,血小板计数104×10/L;凝血常规:凝血酶原时间10.5 s;铜蓝蛋白0.165 g/L;优生优育系列、自身免疫性肝病抗体阴性;心电图:窦性心动过缓;肝胆胰脾彩超未见明显异常。
2 结果
入院完善相关检查后在超声引导下行肝组织穿刺活检术,组织病理学报告回示:肝细胞轻度水肿,小液内点灶状坏死,部分汇管区轻度扩大见纤维组织轻度增生,相当于Scheuer分级:G0-1S0-1,(见图1)。由于我院病理诊断水平有限,为进一步明确诊断我院病理科制作8张病理切片(未染色)送至北京地坛医院病理科会诊,结果显示:肝小叶结构存在,肝板排列基本整齐。局灶肝细胞疏松肿胀及气球样变,中央静脉周围肝窦扩张,肝板结构轻度紊乱。汇管区未见纤维化及炎症,但可见结构改建及明显门静脉扩张,汇管区纤维化并不明显,未见桥接坏死及纤维间隔形成。汇管区内小胆管未见破坏。特染结果:D-PAS(-),Masson(+),网织染色(+),铜染色-罗丹宁(-)。最终病理诊断为肝脏特发性门脉高压(IPH)(见图2,3)。
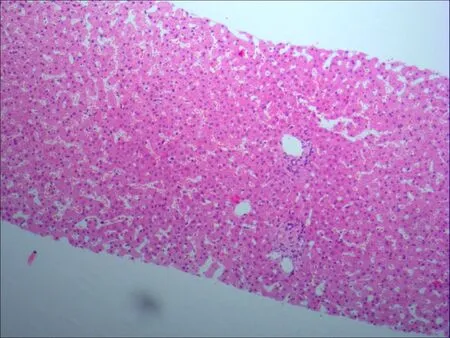
图1 安徽中医药大学第一附属医院肝组织病理学表现(HE×100)
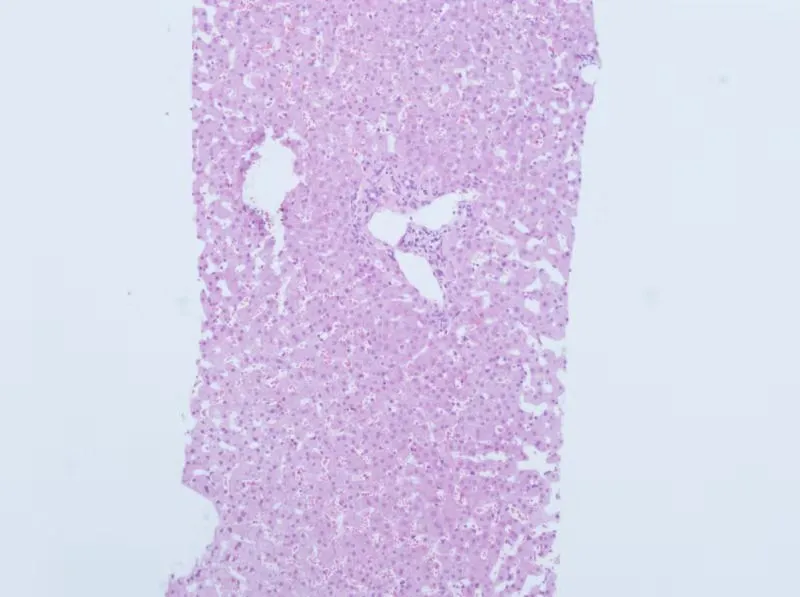
图2 北京地坛医院肝组织病理学表现(HE×100)
3 讨论

图3 北京地坛医院肝组织病理学表现(特殊染色×100)
IPH是由肝内门静脉和窦内皮细胞损伤引起阻力增加而导致的一种以长期的肝内窦前性门脉压增高为特征性表现的综合征,也称为特发性门静脉高压征或班替(Banti)综合征。本病在我国临床较少见,主要发生在日本及印度,其次西方国家。目前研究发现IPH的发病原因主要与感染、毒物或药物、血栓形成倾向、免疫异常、基因异常、淋巴循环异常、营养状态等致病因素有关,具体的发病机制尚不明确。IPH呈隐匿性发展,门脉高压的症状和体征是其初始表现,尤其是脾大(有或无脾功能亢进)和食管静脉曲张,因此在临床诊断中很容易误诊为肝硬化。IPH的实验室检查主要体现在肝功能正常或轻度异常;在血三系检查中可能会出现因食管静脉曲张破裂出血和脾功能亢进引起的贫血、血小板减少或白细胞减少;同时研究发现约80%的IPH病人有凝血功能异常的表现。本例病人临床表现及实验室、影像学检查并无门脉高压的表现,仅仅表现为肝功能反复异常,这对诊断IPH有很大的难度。病理诊断对于确诊IPH具有重要意义,主要表现为偶见肝脏萎缩,肝包膜下肝实质缺失。肝板排列基本正常,肝内周围门静脉分支破坏和狭窄、分支闭塞、异常侧支静脉形成,可见血栓形成,可见门静脉纤细纤维化,可见门静脉纤维性扩张。可见肝细胞增生,偶见结节性增生,但无周围性纤维化。
目前对于IPH的诊断尚无统一的标准,属于排除性诊断。2015年EASL肝脏血管疾病临床实践指南中提出IPH的诊断标准:(1)具有门静脉高压临床表现;(2)肝组织活检排除肝硬化;(3)排除已知原因导致肝硬化或非肝硬化门静脉高压的慢性肝病(包括慢性乙型/丙型肝炎、酒精性脂肪性肝炎/非酒精性脂肪性肝炎、自身免疫性肝炎、遗传性血色素沉着症、Wilson氏病、原发性胆汁性胆管炎);(4)排除目前诊断明确导致非肝硬化性门静脉高压的疾病(如结节病、血吸虫病、遗传性肝纤维化);(5)多普勒超声或CT证实门静脉及肝静脉通畅。本例病人反复肝功能异常,血小板提示减少,肝胆胰脾彩超未见明显异常,免疫组合检查排除了乙、丙型肝炎,优生优育系列、铜蓝蛋白、自身免疫性肝病抗体检查均未见明显异常,因此排除了病毒性肝炎、肝外病毒感染、自身免疫性肝病及代谢性肝病等疾病;同时病人否认有饮酒史和服药史,排除了酒精性及药物性肝病。最终通过肝穿刺送检病理,结果病理诊断提示IPH,符合诊断标准。该病人目前虽尚无IPH的特征性临床表现,考虑病人年纪轻,病情发现比较早,后期仍需定期复查随访。
IPH的治疗主要是控制和预防门脉高压的并发症。IPH病人因无肝硬化表现,肝脏的组织病理学改变与肝硬化不同,其远期预后较肝硬化门脉高压来说,大多数病人具有一定的生存优势。食管胃底静脉曲张破裂出血是IPH病人的最大危险,因此对于食管胃底静脉曲张破裂出血的控制和预防是重中之重。IPH在临床上较罕见,而对于IPH引起食管胃底静脉曲张破裂出血的预防及治疗的研究较少,尚无统一的方案。临床上推荐按照肝硬化并食管胃底静脉曲张破裂出血相关指南建议进行预防及治疗,主要治疗方案包括内镜下治疗、非选择性β受体阻滞剂、手术治疗等。对于急性出血病人的治疗采取内镜下硬化治疗和套扎术,同时联用血管活性药物是目前临床上常见且高效的治疗方案。非选择性β受体阻滞剂在预防肝硬化门脉高压致食管胃底静脉曲张出血的风险中具有一定的优势,但对于IPH的临床研究较少,需要进一步的探索。而对于应用药物、内镜治疗出血失败且Child-PughA、B级的病人优先考虑经颈静脉肝内门体分流术(TIPS),在没有进行TIPS治疗条件时再考虑外科分流术。对于脾功能亢进的病人可以优先采取脾切除术。当肝功能较差或者出现肝衰竭时应考虑行肝移植。另外,有学者研究提出抗凝治疗以减少疾病的进展。然而,在临床上对于有些病人来说,口服抗凝药物来平衡出血和血栓形成的风险是非常困难的。因此,抗凝仅适用于明确的潜在血栓形成前状态或发生门静脉血栓形成的病人。
综上所述,目前IPH病因仍不明确,其临床表现易被误诊为肝硬化。因此,在临床上高度怀疑此病需及时行肝脏穿刺明确病理诊断,早发现,早预防,早治疗。
