UPLC-TQ-MS同时测定金红片中12个成分
2021-06-24刘苓娴李海波石丹枫王振中姚新生
刘苓娴,李海波,石丹枫,王振中,姚新生,肖 伟*,于 洋*
1.暨南大学中药及天然药物研究所,广东 广州 510632
2.江苏康缘药业股份有限公司 中药制药过程新技术国家重点实验室,江苏 连云港 222001
金红片(Jinhong Tablets)是原中药3 类新药,源于金元四大家之首刘完素的《素问·病机气宜保命集》中的金铃子散(川楝子、延胡索)化裁而来的中药复方创新药物。由川楝子、延胡索(醋制)、川木香及红花八角叶4 味中药组成,具有疏肝解郁、理气活血、和胃止痛的功效[1-3]。方中以川楝子为君药,延胡索为臣药,红花八角叶与木香为佐使,川楝子用以清肝火,延胡索用以理气,川木香用以行气止痛,红花八角叶用以散瘀行气,组方精炼,诸药合用共奏疏肝解郁、利气活血、和中止痛之功。现代药理学研究表明,金红片可以使胃液分泌量和总酸排出量降低,抑制胃蛋白酶的分泌、延缓胃排空;还具有镇痛、解痉、抗炎以及抗胃溃疡、促进溃疡愈合等药效[3]。临床上在治疗慢性浅表性胃炎的同时还可改善患者情绪状态、通畅血脉、消散瘀滞,标本兼治。
金红片临床应用广泛,但其在质量控制方面,仅对莽草酸进行限量以及对延胡索乙素进行含量测定,未建立其与功效相关联的多指标成分的整体质量控制方法。有文献报道,川楝子、延胡索、木香和红花八角叶的主要有效成分分别为楝烷型三萜类化合物[4]、生物碱类化合物[5]、倍半萜类化合物[6]以及黄酮类化合物[7-9]。另由于方中君药川楝子具肝毒性[10]、致肌无力[11]、呼吸抑制[12]、妊娠毒性[13]。因此,需对其功效成分同时也是毒性成分川楝素进行限量,提升产品的科学内涵和安全性。本研究采用UPLC-TQ-MS 技术,选取覆盖组方4 个单味药的特征性成分以及活性成分(莽草酸、绿原酸、异绿原酸B、异绿原酸C、普洛托品、别隐品碱、延胡索乙素、紫堇碱、巴马汀、槲皮素、异川楝素和川楝素)为指标成分,建立与功效相关联的多指标成分含量测定方法,并对毒性成分川楝素进行限量,为金红片质量标准的提升奠定一定的基础。
1 仪器与试剂
超高效液相色谱三重四极杆质谱联用(UPLCTQ-XS-MS)系统,包括Waters AcquityTMI-Class超高效液相色谱仪(含二元梯度泵–自动进样器–柱温箱)、Waters Xevo TQ-XS Triple Quadrupole Mass Spectrometry 三重四极杆质谱,Waters 公司;KQ-250D 型数控超声波清洗器,昆山市超声波仪器有限公司;XS205 型十万分之一天平,Mettler Toledo公司;Sigma 台式高速冷冻离心机3K-15,德国Sigma 公司;QL-861 涡旋仪,海门市其林贝尔仪器有限公司。
质谱级乙腈及质谱级甲醇,美国赛默飞世尔科技公司;质谱级甲酸,美国西格玛奥德里奇公司;质谱用水,北京屈臣氏蒸馏水有限公司。
对照品:莽草酸(批号PRF10080721,质量分数98%)、绿原酸(批号PRF20051641,质量分数98%)、普洛托品(批号PRF10051621,质量分数98%)、别隐品碱(批号PRF20030227,质量分数98%)、延胡索乙素(批号PRF10031241,质量分数98%)、紫堇碱(批号PRF10022126,质量分数98%)、巴马汀(批号PRF10030643,质量分数97%)、异川楝素(批号PRF10120625,质量分数98%)、川楝素(批号PRF10062524,质量分数98%)均购于成都普瑞法科技开发有限公司;异绿原酸B(批号ST06590120,质量分数98%)购于上海诗丹德标准技术服务有限公司;异绿原酸 C(批号111894-201102,质量分数94.1%)购于中国食品药品检定研究院;槲皮素(批号170813,质量分数99%)购于上海融禾医药科技发展有限公司。
15 批金红片,规格0.45 g/片,批号分别为180502、190304、190305、190306、190401、190402、190403、190404、190405、190406、190407、200701、200702、201101、201102,均由江苏康缘药业股份有限公司提供。
2 方法与结果
2.1 UPLC 分析条件
色谱柱为Acquity UPLC BEH C18柱(100 mm×2.1 mm,1.7 µm);柱温35 ℃,体积流量0.3 mL/min;流动相为0.1%甲酸水溶液(A)-0.1%甲酸乙腈溶液(B),洗脱梯度:0~1.5 min,2%~20% B;1.5~6.0 min,20%~22% B;6.0~10.0 min,22%~30%B;10.0~13.0 min,30%~60% B;13.0~14.0 min,60%~100% B;14.0~15.0 min,100% B;15.0~16.0 min,100%~2% B;16.0~17.0 min,2% B;进样量2 μL。
2.2 质谱条件
电喷雾离子化电离源(ESI),毛细管电压为2.5 kV(正/负离子模式)。离子源温度150 ℃,脱溶剂气温度550 ℃,反吹气体积流量50 L/h,脱溶剂气体积流量1000 L/h,碰撞气为氩气。数据采集模式为多反应监测(MRM)模式,数据采集模式为棒状图(centriod)。各定量成分的参数设定见表1。12个化合物的MRM 叠加色谱图见图1。
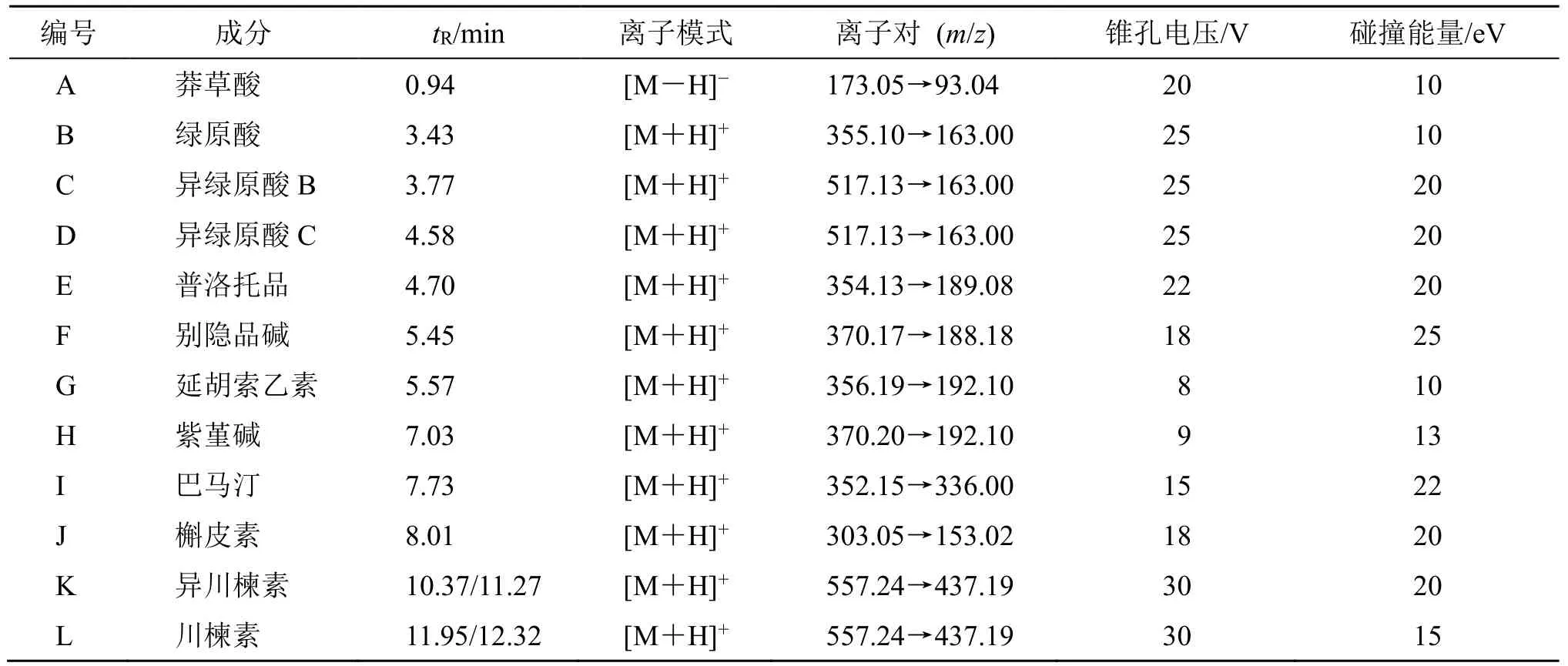
表1 12 个化合物的多反应监测模式信息Table 1 MRM information of 12 analytes
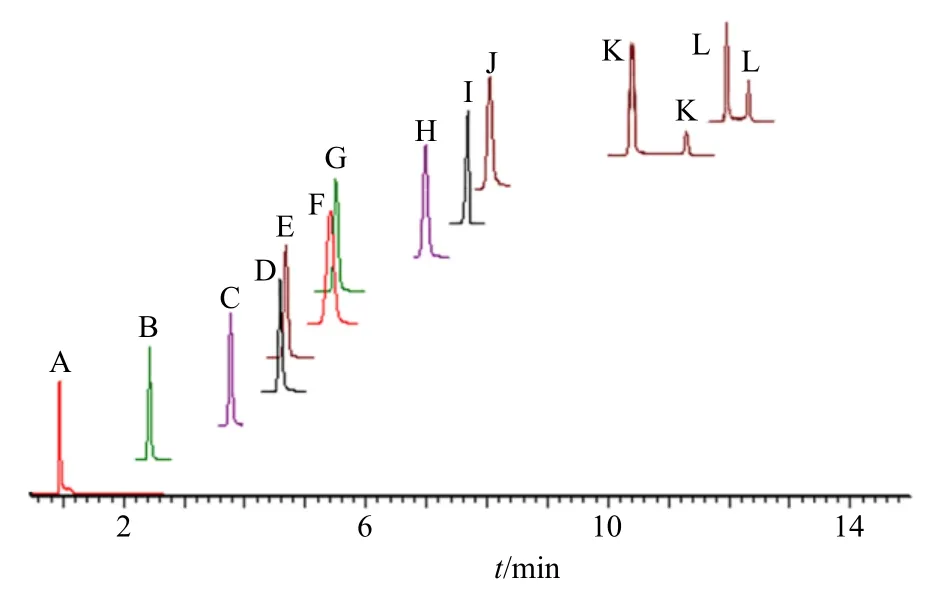
图1 12 个化合物(A~L)的MRM 色谱图Fig.1 MRM chromatograms of 12 analytes(A—L)
2.3 溶液的制备
2.3.1 供试品溶液的制备 取金红片(去除包衣,研磨,过50 目筛)约1.0 g,精密称定,置具塞锥形瓶中,加入80%甲醇10 mL,超声处理30 min,取出,放冷,用80%甲醇补足减失的质量,摇匀,稀释质量浓度至100 μg/mL,15 521×g离心10 min,取上清液即为供试品溶液。
2.3.2 对照品储备液的制备 分别精密称取12 个对照品适量,以甲醇稀释溶解,分别得到质量浓度为莽草酸(A1)160 μg/mL、绿原酸(B1)146 μg/mL、异绿原酸B(C1)131 μg/mL、异绿原酸C(D1)100 μg/mL、普洛托品(E1)145 μg/mL、别隐品碱(F1)120 μg/mL、延胡索乙素(G1)120 μg/mL、紫堇碱(H1)125 μg/mL、巴马汀(I1)100 μg/mL、槲皮素(J1)100 μg/mL、异川楝素(K1)93 μg/mL以及川楝素(L1)139 μg/mL 的对照品储备液,精密量取绿原酸、异绿原酸B、异绿原酸C、普洛托品、别隐品碱、紫堇碱、巴马汀、异川楝素以及川楝素的对照品储备液各500 μL 分别置于5 mL 量瓶中,加80%甲醇至刻度线,摇匀,得到分别稀释了10 倍的对照品(B2、C2、D2、E2、F2、H2、I2、K2、L2)储备液,对照品溶液均置于4 ℃冰箱放置,备用。
2.3.3 混合对照品储备液的制备 精密移取各对照品储备液莽草酸(A1)400 μL、绿原酸(B2)200 μL、异绿原酸B(C2)80 μL、异绿原酸C(D2)200 μL、普洛托品(E2)80 μL、别隐品碱(F2)100 μL、延胡索乙素(G1)100 μL、紫堇碱(H2)300 μL、巴马汀(I2)160 μL、槲皮素(J1)400 μL、异川楝素(K2)130 μL 及川楝素(L2)130 μL,置于10 mL量瓶中,加80%甲醇至刻度线,摇匀,得到S1 混合对照品溶液。以80%甲醇依次倍半稀释得S2~S8混合对照品溶液。
2.4 方法学考察
2.4.1 专属性考察 分别取金红片供试品溶液(批号190401)、混合对照品溶液(S5)以及空白溶液(80%甲醇),按“2.1”和“2.2”项下分析测试条件分别进行检测,色谱图见图2。实验结果表明,空白溶剂在MRM 分析窗口对供试品溶液的测试不存在干扰,表明所建立的液质方法专属性良好。
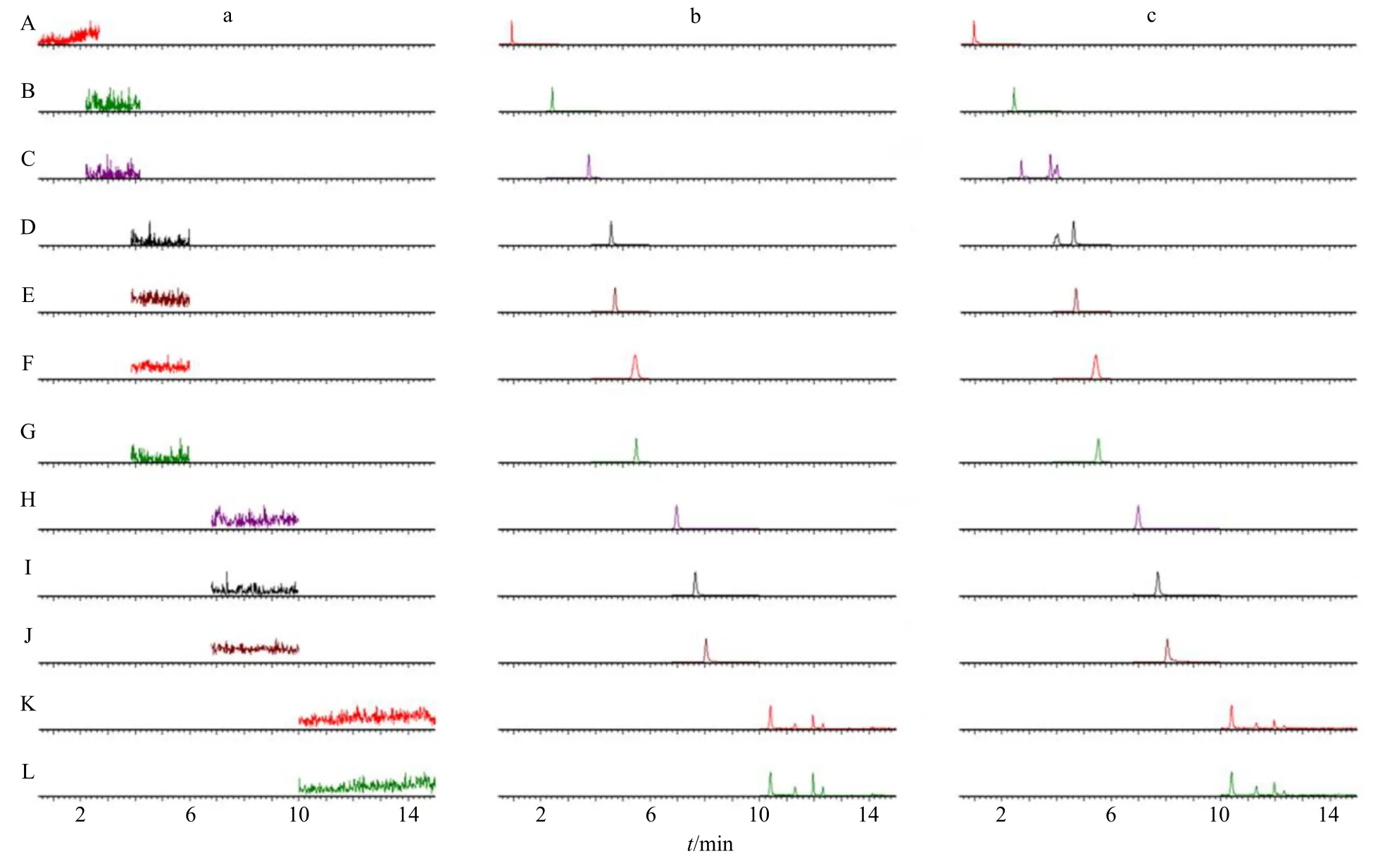
图2 空白溶剂(a)、12 个成分混合对照品(b)及金红片样品(c)的MRM 色谱图Fig.2 MRM chromatograms of blank sample(a),mixed reference substances of 12 components(b)and JHT sample(c)
2.4.2 线性范围及定量下限考察 取“2.3.3”项下方法配制的系列不同质量分数的混合对照品溶液,平行3 份,按照“2.1”和“2.2”项下UPLC-TQ-MS条件分别进样分析并记录上述12 个定量成分的峰面积,以各对照品质量浓度为横坐标(x),峰面积为纵坐标(y),对定量成分进行线性回归计算。结果表明12 个定量成分在线性范围内线性良好(表2),符合分析测试要求。
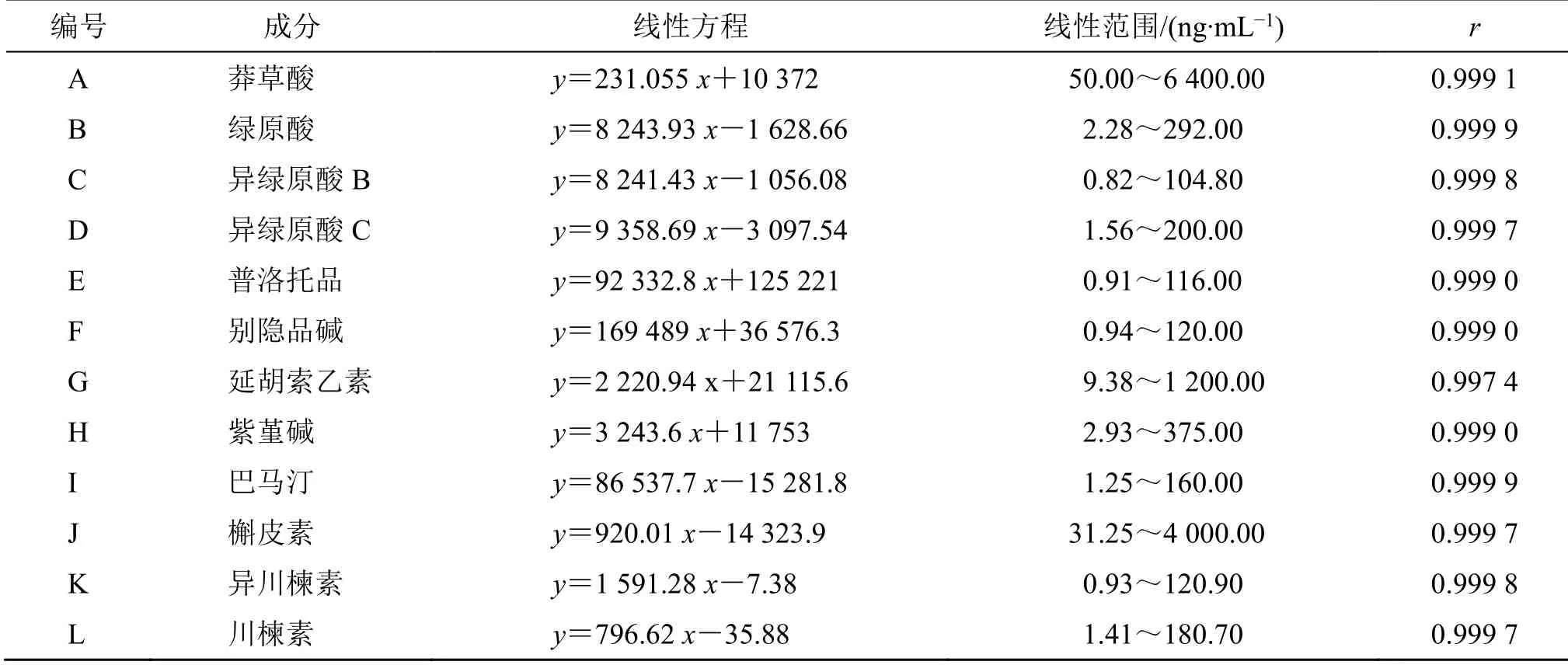
表2 12 个化合物的线性范围考察结果Table 2 Results of liner regression of 12 components
2.4.3 重复性考察 按“2.3.1”项下方法平行制备6 份金红片供试品溶液(批号190401),并按照“2.1”和“2.2”项下分析条件依次进行测定,随行当日标准曲线,记录统计12 个定量成分的含量,平均质量分数及RSD 值,作为方法重复性结果。结果显示,12 个定量成分质量分数分别为15.00、0.30、0.12、0.18、0.13、0.13、2.39、0.41、0.12、2.09、0.05、0.04 mg/g,RSD 值分别为0.7%、0.9%、1.8%、1.1%、1.2%、0.9%、1.0%、1.5%、1.2%、1.6%、1.1%、2.5%。结果表明,各定量成分的重复性良好,满足分析测定要求。
2.4.4 精密度考察 取同一批金红片样品(批号190401),按“2.3.1”项下方法制备供试品溶液,平行3 份,并按照“2.1”和“2.2”项下分析测试条件进行测定,随行当日标准曲线,记录统计12 个定量成分的峰面积并计算其RSD 值,所得结果作为日内精密度考察结果。连续操作3 d,计算定量成分的峰面积及其RSD 值,作为方法日间精密度结果。各定量成分日内精密度RSD 分别为1.0%、1.1%、0.9%、0.9%、1.2%、1.2%、0.4%、2.0%、0.8%、1.2%、1.1%、0.0%;日间精密度RSD 分别为1.1%、1.4%、1.4%、3.0%、1.0%、0.8%、1.5%、1.5%、1.9%、1.7%、1.9%、1.8%。12 个定量成分日内及日间精密度的RSD 分别小于2.0%、3.0%,结果表明该方法日内、日间精密度良好。
2.4.5 加样回收率考察 取同一批金红片样品(批号190401,去除包衣,研磨,过50 目筛)约1.0 g,精密称定,平行6 份。采用“2.3.2”项下所得各对照品溶液配制混合对照品溶液,使加入后的各成分含量分别为金红片中相应成分的含量。
供试品溶液并按照“2.1”和“2.2”项下定量测试条件进样分析,利用当日随行的标准曲线计算各定量成分的含量,12 个定量成分的平均回收率分别为101.9%、101.2%、97.9%、96.8%、100.8%、100.1%、108.7%、100.0%、99.2%、102.0%、99.0%、103.2%,RSD 值分别为2.9%、2.4%、3.1%、3.8%、1.1%、1.9%、1.6%、3.0%、0.9%、2.4%、3.8%、2.6%。结果显示,12 个化合物的加样回收率为96.8%~108.7%,RSD 值不大于3.8%,表明该方法准确度满足测试要求。
2.4.6 稳定性考察 按“2.3.1”项下供试品溶液制备方法制备金红片供试品溶液(批号190401)作为稳定性考察样品,在15 ℃存放0、2、4、8、12、24 h 后按照“2.1”和“2.2”项下测试条件依次进行测定,记录统计12 个分析物的峰面积变化情况,以峰面积RSD 表示。结果显示,12 个定量成分峰面积的RSD 分别为3.2%、2.7%、2.6%、3.4%、2.2%、2.0%、3.7%、3.3%、1.6%、1.9%、2.8%、3.0%,表明供试品溶液在24 h 内稳定性良好。
2.5 样品定量测定
取批号为180502、190304、190305、190306、190401、190402、190403、190404、190405、190406、190407、200701、200702、201101、201102 的金红片,按照“2.3.1”项下方法制备供试品溶液,按照“2.1”和“2.2”项下UPLC-TQ-MS 分析测试条件依次进行测定,随行当日标准曲线,测定15 个批次金红片12 个定量成分的质量分数分别为10.11~22.72 mg/g、0.16~0.43 mg/g、0.06~0.23 mg/g、0.13~0.42 mg/g、0.08~0.26 mg/g、0.08~0.25 mg/g、1.94~2.59 mg/g、0.20~0.96 mg/g、0.07~0.30 mg/g、1.72~2.14 mg/g、0.03~0.06 mg/g、0.03~0.06 mg/g。结果见表3。
3 讨论
3.1 检测方法的选择
川楝子为金红片中的君药,而川楝素被认为是川楝子的主要药效物质基础,但也可能是其主要毒性成分[4]。川楝素具有肝毒性[10,14-16]及生殖毒性[17],小鼠口服急性毒性实验显示,异川楝素的毒性远高于川楝素[18]。《中国药典》2020年版一部[19],川楝子的含量测定项下以川楝素为质控指标成分,采用了LC-MS 方法进行定量分析。为提高金红片产品质量标准,需对其中的毒性成分进行含量限定,而HPLC 难以对微量成分进行准确定量。目前,UPLCTQ-MS 技术的高灵敏、高选择性、MRM 等特性在中药质量控制中具有广阔的应用前景[20],故采用UPLC-TQ-MS 对复方进行含量分析方法的建立。
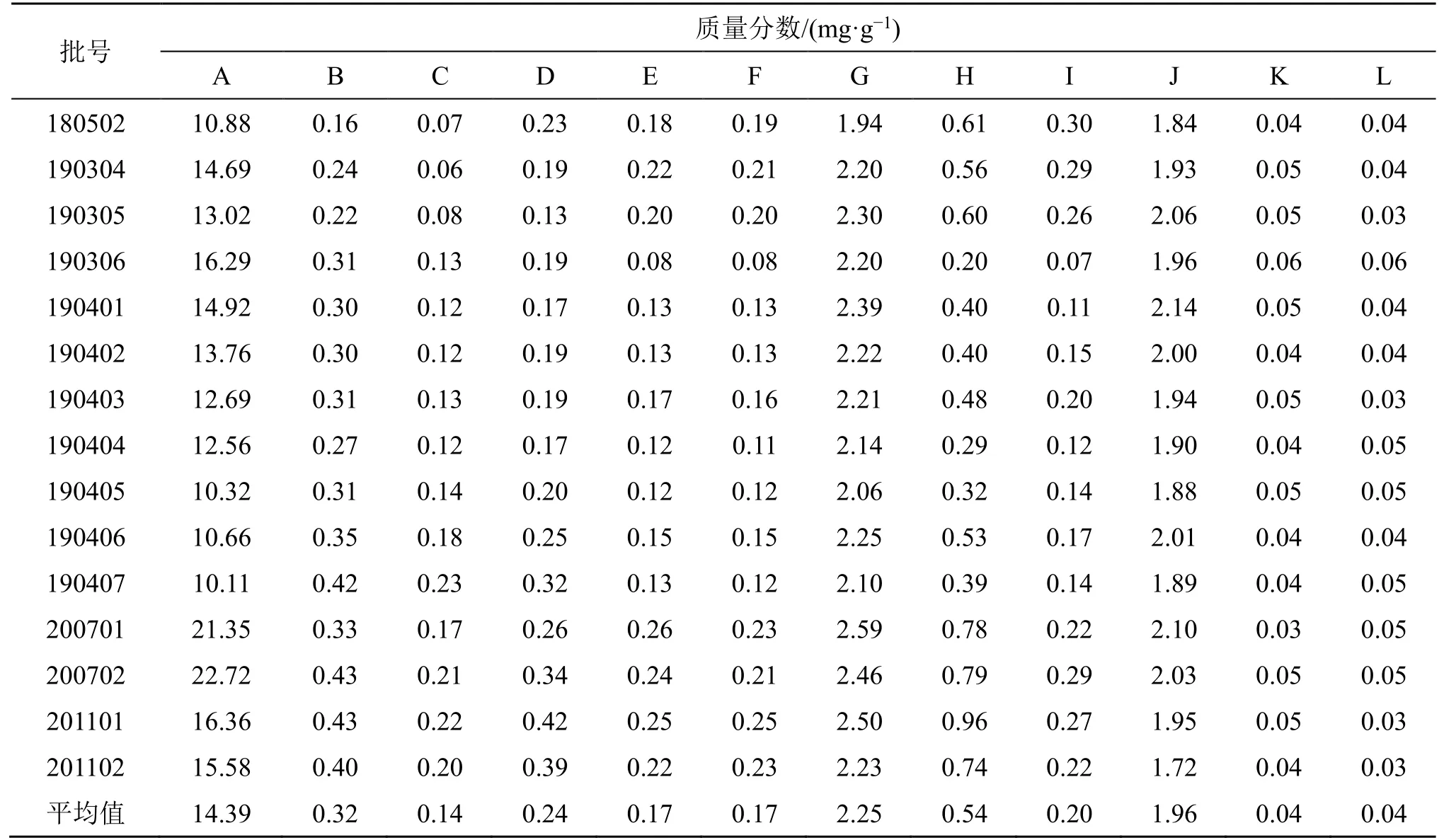
表4 15 批次金红片样品中12 个成分的含量测定结果Table 4 Contents of 12 analytes in 15 batches of JHT
3.2 前处理方法及分析条件优化
实验过程中对样品前处理方法进行了考察,考察了多种提取溶剂(纯水、30%甲醇、60%甲醇、80%甲醇和纯甲醇)以及不同超声时间(15、30、45 min)对金红片中12 个定量成分的影响。根据在不同条件下的各色谱峰的分离度及峰面积比较,最终选择以80%甲醇作为提取溶剂,超声提取30 min,做为金红片样品前处理条件。此外,本实验前期采用了正、负离子扫描模式对单个标准品的质谱响应进行初步探索,以选择最佳离子监测模式。结果显示,莽草酸在负离子模式下灵敏度高,其他各成分在正离子模式下灵敏度高。最终按照各化合物在不同条件下的质谱响应结果,选择了最佳的离子扫描模式以及最佳离子对,以使各目标化合物均具有最好的质谱响应,确保能够满足准确、快速的定性定量要求。
3.3 指标性成分的选择
中药复方化学成分复杂,是由多成分共同作用于多靶点、多途径而产生药效[21],故而对其产品进行质量控制不能局限于单一指标成分。作为一个有机的整体,其质量控制方法的建立应选择多指标成分且与功效成分或毒性成分相关联。
在金红片前期物质基础的研究中,采用UPLCQ/TOF-MS 技术及MassLynx V4.1、MetabolynxTM数据处理软件对金红片全方及ig 给药大鼠后生物样本中的体内外源物进行检识分析,表征金红片的体外化学轮廓及体内代谢轮廓,共检识得到96 个化学成分以及163 个大鼠体内外源物[22]。而后构建了金红片治疗慢性浅表性胃炎的精细的药理学网络,预测潜在活性成分,研究发现发挥药效活性的成分主要为生物碱类、有机酸类和黄酮类[23]。
基于以上研究结果,定量成分的选择主要依据以下原则:①金红片化学成分研究中主含成分且涵盖4 个组方药味代表性结构类型的成分(川楝素、延胡索乙素和槲皮素);②金红片体内代谢研究中吸收入血的原型成分,且其代谢产物较丰富的成分(普洛托品、别隐品碱、延胡索乙素、紫堇碱和巴马汀);③金红片网络药理学研究中预测具有治疗慢性浅表性胃炎的潜在活性成分(绿原酸、异绿原酸B 和异绿原酸C);④《中国药典》2020年版[14]规定各单味药质控指标性成分、文献报道具有相关活性的成分及毒性成分(川楝素、异川楝素、延胡索乙素和莽草酸)。综上,选择12 个成分作为指标成分,建立多指标成分含量测定研究方法,同时进一步考察这些成分在多批次产品中的含量变化,为建立现代化金红片产品质量标准提供科学依据。
3.4 定量测定结果分析
依据现行《中国药典》2020年版[19]对于川楝子所含毒性成分川楝素的规定(0.06%~0.20%),川楝子的用法与用量(5~10 g/d)以及金红的日用量(1 次5 片,3 次/d)。据此,金红片所含川楝素(C30H38O11)不超过2.96 mg/g 时处于安全剂量水平。定量分析所测定15 批次的金红片每片所含川楝素平均值为40 μg/g,均不超过0.06 mg/g(批号190306),结果显示多批次川楝素的含量均处于所规定的安全剂量范围。
根据国家食品药品监督管理局–国家药品标准颁布件CXZB0500279 苏中的规定,本品每片含红花八角叶以莽草酸(C7H10O5)计,不得超过50.00 mg,本次实验所测定15 批次的金红片每片所含莽草酸平均值为6.48 mg,所含莽草酸含量最高的批次为200702,该批次金红片每片所含莽草酸为10.22 mg。CXZB0500279 苏中的规定显示,金红片每片含延胡索以延胡索乙素(C21H25NO4)计,不得少于0.20 mg。本次实验所测定15 批次的金红片每片所含延胡索乙素平均值为1.01 mg,所含延胡索乙素最低含量为0.87 mg(批号180502)。依据本次实验测量数据对各批次金红片所含莽草酸以及延胡索乙素含量分析显示,所测定的15 批次金红片含莽草酸均不超过50 mg,含延胡索均不少于0.20 mg,均符合CXZB0500279 苏下对金红片的质量控制规定。
3.5 小结
本实验首次采用UPLC-TQ-MS 技术对不同批次金红片质量进行了深入探索。综合考虑组方药味的主含特征成分及活性、毒性成分,建立了包含莽草酸、延胡索乙素等12 个代表性成分的同时定量方法,对15 批市售制剂进行质量评价。上述建立的UPLC-TQ-MS 定性定量方法为进一步提升制剂整体质量标准提供了重要证据,为金红片进一步的药效评价,药物代谢动力学研究以及质量标准提升奠定了一定的基础。
利益冲突所有作者均声明不存在利益冲突
