AhR/CYP1B1介导香烟烟雾诱导人永生化支气管上皮细胞损伤的机制
2021-06-15王进覃丽蓉贾蓓蓓陈涛李建祥
王进,覃丽蓉,贾蓓蓓,陈涛,李建祥
苏州大学医学部公共卫生学院毒理学系,江苏 苏州 215123
吸烟是导致肺癌的最主要危险因素,本课题组前期研究表明,长期香烟烟雾(cigarette smoke,CS)暴露能够诱导人永生化支气管上皮细胞(BEAS-2B)恶性转化[1]。香烟烟雾主要由二噁英、卤化和非卤化多环芳烃(polycyclic aromatic hydrocarbons,PAHs)和促氧化剂组成,这些物质能够损坏细胞结构并诱导细胞凋亡[2]。PAHs 和2,3,7,8-四氯二苯并-p-二噁英(tetrachlorodibenzo-p-dioxin,TCDD)通过配体依赖性转录因子芳香烃受体(aryl hydrocarbon receptor,AhR)起作用[3]。一些研究表明AhR的激活能够促进细胞凋亡,而另一些研究表明它能够抑制细胞凋亡[3-4]。AhR在肺部高度表达,它能够与香烟烟雾中的多个配体结合。AhR与配体结合后,能够激活一系列下游基因以启动细胞功能。细胞色素P450(cytochrome P450,CYP)家族1中的成员A1和B1(CYP1A1和CYP1B1)是AhR的两个主要靶基因[5]。经AhR 配体刺激后,细胞中AhR 蛋白水平的下降以及CYP1A1 和CYP1B1 表达的增加通常表明AhR 被激活。另外多项研究表明,CYP1A1 主要起着药物排毒系统的作用,体外研究表明其具有预防癌症的作用[6]。相反地,CYP1B1 能够激活几种人类促突变原和致癌原[7],并且其在肾脏、乳腺、脑和肺的恶性细胞中过表达[8]。以往的许多研究依赖于用TCDD外源性地激活AhR,而不是香烟烟雾中发现的复杂化学物质。本研究采用模拟人吸烟的场景将BEAS-2B 细胞直接暴露于香烟烟雾中,观察CYP1B1 表达变化和加入AhR 拮抗剂CH223191(CH22)后AhR 在香烟烟雾诱导BEAS-2B细胞损伤中的作用。
1 材料与方法
1.1 材料
市售某品牌香烟(每支烟焦油含量11 mg,烟雾烟碱量0.8 mg);BEAS-2B 细胞购自美国菌种保藏中心;DMEM 高糖培养基购自美国Gibco 公司;FBS 购自美国HyClone 公司;AhR 拮抗剂CH223191(CH22)购自MedChemExpress 公司;胰蛋白酶、BCA 试剂盒、活性氧(ROS)检测试剂盒、BeyoClick™ EdU-555 细胞增殖检测试剂盒和Annexin V-FITC 细胞凋亡检测试剂盒购自中国碧云天生物科技公司;逆转录聚合酶链反应(reverse transcription-polymerase chain reaction,RT-PCR)试剂盒、荧光定量PCR 试剂盒购自瑞士Roche公司;CYP1B1 抗体购自美国Proteintec公司。
1.2 基因表达和蛋白组学数据库分析
从基因表达数据库(gene expression omnibus,GEO)获得基因芯片数据集GSE994,共有75 个肺内气道上皮细胞样本资料,其中包含34 名目前吸烟者、23 名从不吸烟者和18 名戒烟者;GSE17913 数据集也被用于本研究,其中包含39 名当前吸烟者和40名从不吸烟者的口腔上皮细胞样本数据;另一个吸烟肺癌患者数据集GSE10072 也被用于本研究,其中包含49 例非肿瘤组织样本信息。此外,临床蛋白质组学肿瘤分析协会(Clinical Proteomic Tumor Analysis Consortium,CPTAC)数据库中的99 例肺癌患者正常肺组织数据也被用于蛋白表达量分析。
1.3 细胞培养和香烟烟雾染毒
BEAS-2B细胞用含有10% FBS 的DMEM高糖培养基常规培养在细胞培养箱(37℃、5% CO2),利用3孔HOPE-MED8170B型体外细胞烟雾动式染毒装置(天津合普,中国),采用Transwell多孔膜,对BEAS-2B细胞进行培养(37℃、5% CO2),细胞接种浓度为1×105个·孔-1,采用自动点烟和动式烟雾染毒控制装置进行Transwell膜上细胞染毒,染烟时间设置为10 min。为了探究AhR 在其中的作用,用AhR 拮抗剂CH22(10 µmol·L-1)预处理BEAS-2B细胞1 h后再进行染毒。依据本课题组前期研究结果[9],共设置了使得细胞存活率介于60%和100%之间的3 个香烟烟雾水平,体积分数分别为0%(CS0)、20%(CS20)和40%(CS40),仪器通过传感器检测烟雾浓度并根据实际香烟烟雾浓度调整,使进入染毒腔的烟雾浓度稳定在设定值。同时,以正常未处理细胞作为空白对照组。
1.4 mRNA表达检测
采用TRIzol(Ambion,美国)法提取各处理组细胞总RNA,利用逆转录试剂盒合成cDNA。CYP1B1正向引物:5’-TGAGTGCCGTGTGTTTCGG-3’;反向引物:5’-GTTGCTGAAGTTGCGGTTGAG-3’。采用SYBR Green PCR Master Mix进行实时定量RT-PCR 扩增,以GAPDH作为内参(正向引物:5’-ACAACTTTGGTATCGTGGAAGG-3’;反向引物:5’-GCCATCACGCCACAGTTTC-3’),采用2-ΔΔCt进行相对表达量分析。
1.5 蛋白表达检测
用RIPA 裂解液(碧云天,中国)提取各组细胞总蛋白,BCA 法进行蛋白定量后加入上样缓冲液,沸水浴使蛋白样本变性。将样本进行SDS-PAGE分离后转移到PVDF膜上,室温封闭2 h后在4℃孵育CYP1B1抗体(稀释比为1:1 000)过夜。次日采用TBST 洗膜并进行二抗孵育,再次洗膜后滴加ECL发光液进行显影拍照。
1.6 ROS的测定
利用ROS 检测试剂盒(碧云天,中国)中的荧光探针DCFH-DA 进行ROS 检测。将各处理组细胞与10 µmol·L-1DCFH-DA在37℃孵育30 min。然后用无血清培养基洗涤细胞3次,以完全除去细胞外的DCFH-DA。洗涤后,立即用荧光显微镜(型号IX73,Olympus)测定ROS 水平。
1.7 细胞凋亡检测
利用Annexin V-FITC 细胞凋亡检测试剂盒(碧云天,中国)进行细胞凋亡检测。收集每个染毒时间点的细胞(至少1×105个),分别加入195 µL 结合液以及5 µL Annexin V-FITC和10 µL PI染色液,避光孵育20 min。立即用流式细胞仪上机检测。从每个样本收集至少10 000个细胞的数据,采用FlowJoV 10 进行分析。
1.8 EdU细胞增殖检测
根据试剂盒说明书在细胞培养基中加入10 µmol·L-1EdU,37℃孵育2 h,随后加入反应液并且进行核复染,最后在荧光倒置显微镜下进行观察拍照,采用ImageJ 1.8.0进行计数。
1.9 统计学分析
试验数据用均值±标准差表示,应用SPSS 20.0 软件对试验数据进行单因素方差分析,两组间比较使用SNK 检验。检验水准α=0.05。
2 结果
2.1 CYP1B1表达水平在吸烟患者肺组织中上调
在肺内气道上皮细胞样本数据集GSE994 中,目前吸烟人群中CYP1B1mRNA 的表达量高于从未吸烟人群(P< 0.001),而已戒烟人群中CYP1B1表达量较目前吸烟人群明显下调(P=0.007),但仍高于从不吸烟人群(P=0.036)(图1A)。在口腔上皮细胞样本数据集GSE17913 中,目前吸烟人群中CYP1B1mRNA 的表达量也高于从不吸烟人群(P< 0.001)(图1B)。在肺癌患者数据集GSE10072 的正常肺组织中,CYP1B1mRNA在不同吸烟史人群中的变化与GSE994 相似,目前吸烟和戒烟人群肺组织中CYP1B1表达均高于从未吸烟人群(P< 0.001 和P=0.004),而戒烟人群肺组织中的表达量低于目前吸烟人群(P< 0.001)(图1C)。此外,在CPTAC 数据库中,也发现目前吸烟肺癌患者正常组织中的CYP1B1 蛋白表达水平高于从不吸烟患者(P=0.005),而戒烟患者正常肺组织中的表达水平与从未吸烟患者差异无统计学意义,但低于目前吸烟患者(P=0.022)(图1D)。

图1 CYP1B1在吸烟人群肺组织中表达变化Figure 1 Changes of CYP1B1 expression in lung tissues of smokers
2.2 香烟烟雾暴露通过AhR上调CYP1B1
与未经处理的空白组相比,CS0 组CYP1B1 mRNA和蛋白表达水平无明显变化,而20%和40%香烟烟雾暴露组CYP1B1 表达水平上调(均P< 0.05)。加入AhR拮抗剂(CH22)后,CS0组CYP1B1表达下调(P< 0.05),CS20和CS40组的CYP1B1表达较未加CH22组下调(均P< 0.05),但仍高于对照组(均P< 0.05)。见图2。

图2 香烟烟雾通过AhR调控CYP1B1 的mRNA(A)和蛋白(B、C)表达Figure 2 Cigarette smoke regulates the mRNA (A) and protein (B and C) expressions of CYP1B1 through AhR
2.3 ROS改变
与未经处理的空白组相比,CS0 组ROS 水平无明显变化,而20%和40%香烟烟雾暴露组ROS 水平上调(均P< 0.05)。加入AhR 拮抗剂CH22 之后,CS0 组ROS水平明显下调(P< 0.05),并且CS20 和CS40 组的ROS水平较未加CH22 组均下调(均P< 0.05),但仍高于对照组(均P< 0.05)。见图3。

图3 流式细胞术检测不同处理组ROS水平的变化Figure 3 Changes of ROS levels in different treatment groups by flow cytometry
2.4 细胞凋亡率改变
与未经处理的空白组相比,CS0 组细胞凋亡比例无明显变化,而20%和40%香烟烟雾暴露组凋亡细胞比例上调(均P< 0.05)。加入AhR 拮抗剂CH22,CS0 组凋亡细胞比例无明显变化(P> 0.05),而CS20 和CS40组的凋亡细胞比例较未加CH22 均下调(均P< 0.05),但仍高于对照组(均P< 0.05)。见图4。

图4 流式细胞术检测不同处理组凋亡水平的变化Figure 4 Changes of apoptotic levels in different treatment groups by flow cytometry
2.5 细胞增殖能力变化
与空白组相比,CS0 组细胞增殖能力无明显变化,而20%和40%香烟烟雾暴露组细胞增殖比例下调(均P< 0.05)。加入AhR 拮抗剂(CH22)后CS0 组细胞增殖比例无明显变化(P> 0.05),而CS20 和CS40 组的细胞增殖比例较未加CH22 均上调(均P< 0.05),但仍低于对照组(均P< 0.05)。见图5。
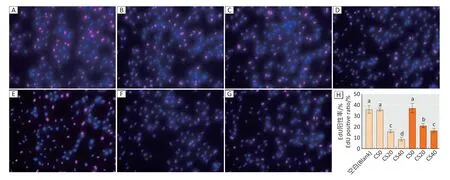
图5 EdU实验检测不同处理组细胞增殖能力Figure 5 Cell proliferation ability in different treatment groups by EdU assay
3 讨论
香烟烟雾是一种复杂的混合物,包含近5 000 种化学物质,包括致癌物、ROS 和其他化学物质,以及AhR 配体(例如二噁英和二噁英类化学物质等)。而研究也发现香烟烟雾中二噁英和单个种类PAH 的含量较低,不能解释香烟烟雾引起的毒性反应[10]。因此研究香烟烟雾混合物对肺部细胞的损伤机制非常重要。很多研究已经证实AhR 在许多类型的人类肺细胞中广泛表达,包括内皮、血管平滑肌、支气管上皮、肺泡囊上皮和基质细胞[11]。本研究采用香烟烟雾直接染毒细胞的动式染毒方式,更接近人实际吸烟过程,尤其是烟雾产生的物质更接近于真实情况;同时,结合人肺组织来源的数据库分析吸烟相关影响的基因,通过体外单一烟雾实验加以验证。通过分析吸烟相关GEO 和CPTAC 数据库分析吸烟相关基因,并以体外细胞烟雾动式染毒装置对人永生化支气管上皮细胞(BEAS-2B)进行染毒,探究烟暴露后AhR 信号通路中CYP1B1 变化及其发挥的作用。
CYP1B1受AhR 信号通路的转录调控,能够催化内源性和外源性亲脂性化合物的氧化。CYP 催化循环偶联不良会诱导ROS 的产生,如超氧阴离子等[12]。香烟烟雾激活AhR 可能通过上调CYP 家族蛋白的表达和/或活性来产生ROS。AhR 介导的CYP1A1 和CYP1B1 活化将PAHs 转化为致癌的环氧代谢物。CYP1B1 和AhR都是化学预防的潜在目标。本研究中,本研究分析了GEO 数据库中的三个吸烟相关数据集,均发现与从未吸烟人群相比,CYP1B1 在吸烟人群上呼吸道组织中明显上调,并且戒烟人群肺组织中的表达量明显低于吸烟人群,表明香烟烟雾在上呼吸道中能够诱导CYP1B1 的表达。为了进一步验证香烟烟雾诱导的CYP1B1高表达是由AhR激活导致的,本研究在BEAS-2B细胞培养基中加入AhR 拮抗剂CH22 抑制AhR 活性之后再进行染毒。结果表明,CH22 能够下调CYP1B1 的表达,并且CH22 预处理能够拮抗香烟烟雾暴露引起的CYP1B1 表达上调。同时,CH22 预处理能够拮抗香烟烟雾暴露诱导的BEAS-2B 细胞中ROS 的上升、细胞凋亡率的增加和细胞增殖能力的降低。结果表明香烟烟雾诱导的BEAS-2B 细胞CYP1B1 表达上调和损伤作用是由AhR信号通路介导的。
另外,本课题组前期的研究已经发现长期香烟烟雾暴露能够诱导BEAS-2B 细胞恶性转化,具有成瘤能力[1]。虽然香烟烟雾中的二噁英被归类为人类致癌物,已被证实通过AhR 起作用,然而AhR 在癌症发展中的作用仍存在争议。AhR 的基因变异也被报道与吸烟者的肺癌易感性有关,这种变异可能会影响AhR 蛋白的表达和/或活性[13]。此外,在癌细胞和癌症微环境细胞中经常观察到CYP1B1 表达水平的增加[6]。关于AhR/CYP1B1 在香烟烟雾诱导BEAS-2B 恶性转化过程中的作用还有待进一步探讨。
综上,本研究通过数据库分析发现CYP1B1在吸烟人群肺组织中上调,通过体外实验发现香烟烟雾诱导的BEAS-2B细胞损伤作用是由AhR/CYP1B1信号通路激活引起的,其中的机制还有待进一步研究。
