吉西他滨联合奈达铂治疗肺癌患者的临床效果
2021-05-31吕慧
吕 慧
(抚顺市第四医院,辽宁 抚顺 113123)
目前国内对肺癌的早期筛查的不完善导致许多肺癌患者初诊时已经处于中晚期而错失了最佳的治疗时机。吉西他滨(gemcitabine,GEM)能够通过抑制DNA合成限速酶RNA的作用对肺癌患者起到良好的治疗效果。实践发现GEM能够与铂类药物发挥协同效应,GEM联合顺铂(cisplatin,DDP)的全身化疗是临床治疗肺癌患者的常用方法。但相关报道指出在药品不良反应(ADR)涉及的抗肿瘤药物8大类中,DDP的ADR居首位[1]。这是因为DDP具有较强的毒性,治疗过程中需要水化而造成依从性低、患者耐受度不高。据报道,病情严重的患者常常会因为严重的不良反应而终止化疗[2]。为了给肺癌患者提供合理用药方案,本研究探讨了GEM联合奈达铂(nidaplatin,NDP)治疗肺癌患者的临床效果,报道如下。
1 资料与方法
1.1 一般资料 选择2016年8月至2018年4月我院收治的70例肺癌患者作为研究样本。将患者随机分为GEM+DDP(GD)组和GEM+NDP(GN)组,每组患者各35例进行对比评价。GD组:男19例,女16例;年龄40~76岁,平均年龄(60.32±9.12)岁;病理类型为腺癌者18例、鳞癌者14例、其他类型者3例;临床分期为Ⅲa期者12例、Ⅲb期13例、Ⅳ期10例。GN组:男18例,女17例;年龄39~75岁,平均年龄(60.35±9.15)岁;病理类型为腺癌者17例、鳞癌者15例、其他类型者3例;临床分期为Ⅲa期者10例、Ⅲb期14例、Ⅳ期11例。两组患者的一般资料经检验,P>0.05,无明显差异。
1.2 纳入标准 ①经病理、影像学、实验室检查等明确诊断为肺癌患者。②入院后患者卡氏(Karnofsky,KPS)功能状态评分≥60分(60分为生活能够大部分自理,偶尔需要别人帮助,随着分值增加,患者的功能状态越好)。③可测量的肿瘤指标≥1个。④治疗前生化、血常规检查指标未见明显异常。⑤预计生存期>3个月。⑥距离上次化疗开始时间>21 d。⑦依从性良好,对研究知情同意者。
1.3 排除标准 ①患者一般情况差,如存在严重血液病、肝肾病,病情已经处于终末期。②患者影像学资料缺失,无法判断疾病分期及进行效果评价。③合并其他恶性肿瘤者。④化疗不足2周期退出者。
1.4 方法 依据美国国立综合癌症网络(National Comprehensive Cancer Network,NCCN)的肺癌临床实践指南制订两组患者给药方案与剂量[3]。GD组:依据体表面积给药,第1、8天静脉滴注GEM(山东新时代药业有限公司;国药准字H20163144)1 mg/m2,每日1次。DDP(云南生物谷药业股份有限公司;国药准字H20043888)总剂量100 mg/m2,第1~3天连续3 d静脉滴注,每日1次。1个化疗周期为21 d。GN组:依据体表面积给药,第1、8天静脉滴注GEM 1 mg/m2,每日1次。NDP(江苏奥赛康药业有限公司;国药准字H20064295)总剂量为80~100 mg/m2,第1~3天连续3 d静脉滴注,每日1次。1个化疗周期为21 d。
1.5 评价指标
1.5.1 临床疗效 依据新版实体瘤疗效评价标准RECIST指南(1.1版)评估患者临床疗效[4]。将患者临床疗效分为完全缓解(CR)、部分缓解(PR)、病情稳定(SD)、病情进展(PD)。相较于WHO的评价标准,RECIST标准强调了测量的易追踪性和重复性,目前其已经被许多重要国际组织与机构广泛采用等。
CR:目标病灶消失,病理性淋巴结短轴值<10 mm。PR:参照临界半径总和,所有目标半径的综合减少≥30%。SD:参照目标病灶半径总和最小值,介于缓解与恶化之间的患者。PD:目标半径总和最小值为参照,所有目标病灶半径的总和增长≥20%。判断指标包括有效率和疾病控制率,计算公式分别为有效率=(CR例数+PR例数)/总例数×100%。疾病控制率=(CR例数+PR例数+SD例数)/总例数×100%。
1.5.2 不良反应 依据美国卫生及公共服务部国立卫生研究院、国家癌症研究所制定的CTCAE 4.0(常见不良反应评价标准)进行评价[5]。排除其他药物、疾病等因素导致的症状,确定全部不良反应均为化疗方案引起。
血液毒性:评价指标为化疗后血红蛋白(hemoglobin,HGB)、血小板计数(Platelet count,PLT)、白细胞计数(white blood cell count,WBC)、中性粒细胞计数(neutrophil count,NEUT)。标准为HGB男性<130 g/L,HGB女性<115 g/L,WBC<3.5×109/L,PLT<100×109/L,NEUT<2.0×109/L。
肝脏毒性:化疗后丙氨酸转氨酶(alanine aminotransferase,ALT)和(或)天冬氨酸转氨酶(aspartate aminotransferase,AST)水平异常升高。
胃肠道反应:化疗后出现恶心、呕吐、腹泻症状>2 d,伴发血性腹泻。
肾脏毒性:肌酐异常值。
1.6 统计学方法 应用SPSS22.0软件统计分析数据,计数资料用率(%)表示,行χ2检验,计量资料用()表示,行t检验,P<0.05表示差异具有统计学意义。
2 结果
2.1 两组患者临床疗效对比 GN组患者的治疗有效率和控制率高于GD组,P<0.05,差异具有统计学意义。见表1。
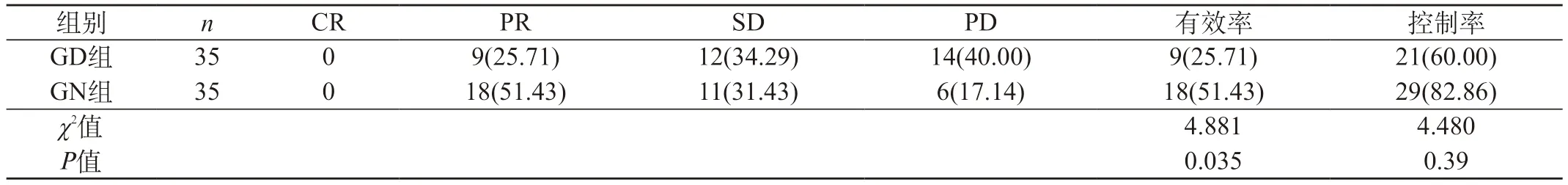
表1 两组患者临床疗效对比[n(%)]
2.2 两组患者不良反应对比 两组患者的不良反应表现在肝脏、肾脏毒性及血液毒性相关指标异常方面对比差异均不具有统计学意义(P>0.05)。但GD组的胃肠道不良反应发生率明显高于GN组,对比χ2=5.710,P<0.05,差异具有统计学意义。见表2。

表2 两组患者不良反应对比[n(%)]
3 讨 论
医学资料显示,我国肺癌的发病率和病死率居于恶性肿瘤榜首,并且仍然存在着逐渐攀升的趋势[6]。依据数据预测,到2025年国内肺癌患者将达到100万例。巨大的肺癌基数和高病死率的危害背景与国内对肺癌的医疗对策尚未完善形成鲜明对比。肺癌的临床治疗方面相关实践指南指出,大多数肺癌患者可以从含有DDP的联合化疗中获益,预期1年生存率为30%~40%。
NDP是第二类铂类抗癌药物,具有毒性较低、无交叉耐药等优势,且研究指出其抗癌效果与DDP相近,可作为替代方案,并且如今已被临床广泛应用[7]。NDP的抗肿瘤机制从本质上来说与DDP相似,均为细胞周期非特异性药物可通过与DNA形成交叉键的方式破坏细胞的DNA结构从而抑制肿瘤细胞分裂。联合GEM能够进一步强化铂类药物与DNA之间的嵌合稳定性。联合两种药物还能够通过抑制DNA的修复而产生更强的破坏力。有关报道指出,GEM联合DDP能够显著增强患者的临床疗效[8]。本研究结果显示,当GEM与DDP或NDP联用时在临床疗效和疾病控制率比较,GEM与NDP组患者的治疗有效率和疾病控制率更优。这反映出GEM联合NDP治疗肺癌疗效更佳。许多医学报道称,顺铂为基础的联合化疗方案有利于改善患者的生存质量,延长患者生存时间。但同时指出了化疗方案存在许多不良反应,如骨髓抑制、肝肾毒性、胃肠道反应等。本次研究中发现两组患者的不良反应集中在肝脏、肾脏毒性、血液毒性、胃肠道反应方面。在发生率发面两组患者在肝脏、肾脏毒性、血液毒性方面相近。而GD组患者的恶心、呕吐、腹泻等胃肠道不良反应发生率为31.43%,明显高于GN组(8.57%),对比P<0.05,差异具有统计学意义。这一结果与有关资料报道的结论相一致[9]。DDP的主要限制性毒性为累积性和计量相关性肾毒性,由于药物诱导肾小管上皮细胞凋亡而产生大量自由基损害肾脏。其发生率为25%~35%。肺癌患者需要多个周期化疗,药物蓄积导致毒性增加进一步降低患者的耐受性与依从性,从而限制了DDP的临床应用。而NDP的主要限制性毒性为骨髓抑制造成的PLT减少。另外,医学研究指出,虽然DDP和NDP都会增加人胚肾细胞293T活性氧自由基、丙二醛水平,降低超氧化物歧酶水平,但NDP造成的细胞氧化损伤明显比DDP轻,且毒性表现程度也小于DDP。本研究中两组患者在肾毒性发生率方面没有表现出明显的差异,推测原因与GD组接受了水化治疗有关。水化治疗在用药第1天、第2天补液3 000~4 000 mL,第3天补液2 000~3 000 mL,还应酌情应用甘露醇或速尿进行利尿,从而保持患者化疗期间24 h尿量>3 000 mL。水化治疗对年龄较大、心肺储备功能较差的患者会造成不利影响[10]。而GN组患者可减少补液量,具有明显优势。从结果可以看出,GN组在HGB减少、PLT下降、NEUT减少方面略高于GD组,这是因为NDP具有较强的血液毒性,通常这些不良反应在对症治疗或化疗结束后会逐渐恢复。GEM联合NDP无须水化治疗,胃肠道反应较轻,能够极大减轻患者负担与压力。临床在选择化疗方案时可依据患者病情与药物作用特点综合考虑有效性和安全性指标进行合理选择。由于本研究纳入的样本数量有限,故进一步结论仍需要大样本多中心研究。
综上所述,吉西他滨联合奈达铂治疗肺癌患者疗效确切,安全性佳,无须水化治疗且胃肠道反应更轻,有利于患者接受。
