中医药干预铁死亡机制的研究进展
2021-05-27林鹏展田菲张林林方圆韩佳彤吴圆圆
林鹏展 田菲 张林 林方圆 韩佳彤 吴圆圆
〔摘要〕 铁死亡是近年来发现的一种全新的细胞死亡方式,与正常细胞凋亡和坏死不同,铁死亡具有铁离子的依赖性。铁死亡的发生与细胞内脂质活性氧(reactive oxygen species, ROS)的平衡失调息息相关,其通过介导脂质过氧化(lipid peroxidation, LPO),调节谷胱甘肽(glutathione, GSH)和谷胱甘肽过氧化物酶4(glutathione peroxidase 4, GPX4),依赖细胞内铁、ROS和氧化还原稳态失衡,根据Fe-ROS或者GSH-GPX4-ROS信号通路介导细胞死亡。中药具有多靶点、多通路的优势,干预铁死亡具有一定的疗效和价值,本文总结了铁死亡的相关机制,汇总了近年来中医药领域通过GSH-GPX4-ROS通路介导铁死亡的实验研究成果,以期为疾病铁死亡的靶点治疗提供参考。
〔关键词〕 铁死亡;铁代谢;脂质过氧化;氧化应激;中医药
〔中图分类号〕R28 〔文献标志码〕A 〔文章编号〕doi:10.3969/j.issn.1674-070X.2021.02.029
〔Abstract〕 Ferroptosis is a new way of cell death discovered in recent years, which is different from normal cell apoptosis and necrosis. Ferroptosis is iron dependent. Ferroptosis is closely related to the imbalance of intracellular reactive oxygen species (ROS), which mediates lipid peroxidation (LPO) and regulates glutathione (GSH) and glutathione peroxidase 4 (GPX4), relies on the imbalance of intracellular iron, ROS and redox homeostasis, and mediates cell death according to the Fe-ROS or GSH-GPX4-ROS signaling pathway. Traditional Chinese medicine has the advantages of multi-target and multi-channel, intervention of ferroptosis has certain curative effect and value. This paper summarized the related mechanisms of ferroptosis, summarized the experimental research results of ferroptosis mediated by GSH-GPX4-ROS pathway in the field of traditional Chinese medicine in recent years, in order to provide reference for the target treatment of ferroptosis.
〔Keywords〕 ferroptosis; iron metabolism; lipid peroxidation; oxidative stress; traditional Chinese medicine
细胞死亡是维持机体完整性的重要过程之一,在人体的生长发育、细胞衰老、细胞稳态、免疫应答和应激反应中扮演者重要的角色[1]。不同类型的细胞死亡方式有着不同表现的形态特征和应答机制,常见的细胞死亡类型包括细胞坏死及细胞凋亡,凋亡是细胞的编程死亡,包括细胞自噬、坏死性凋亡、胀亡、细胞焦亡和铁死亡等。铁死亡于2012年首次被Dixon等[2]提出,认为铁死亡是一种铁依赖性的非细胞凋亡,由于脂质过氧化(lipid Peroxidation, LPO)而发生的一种可调节性细胞死亡方式。作为一种新型的细胞死亡方式,铁死亡发生于细胞内,通过破坏细胞内的线粒体、核酸与内质网等介导细胞死亡[3]。研究发现多种疾病中均存在铁死亡,铁死亡也已经成为近年来研究靶点干预细胞死亡的热点。传统中药具有多靶点、多通路等优势,相关学者研究通过临床研究发现中药干预铁死亡具有一定的疗效和价值[4],挖掘中药通过铁死亡机制干预疾病的靶点,可为其研究探索疾病新疗法提供理论依据。
1 铁死亡
在人体正常生理情况下,细胞内的铁含量会处于稳态。过量的铁离子会导致细胞内“铁浓化”,介导活性氧(reactive oxygen species, ROS)过度积累,谷胱甘肽过氧化物酶4(glutathione peroxidase 4, GPX4)的抗氧化清除作用衰减,ROS生成与降解的紊乱,从而诱导细胞死亡[5]。铁在细胞内的过度负载以及脂质的过氧化在介导铁死亡的过程中起着至关重要的作用。参与铁代谢和脂质过氧化的各种调控分子都是调节铁死亡的机制。
1.1 铁死亡的机制
铁代谢与脂质过氧化被认为是铁死亡的主要介质,铁是人体必需的微量元素,不仅参与血红素的合成,同时也作为一些酶的辅基在细胞增殖、氧气运输和DNA合成等人体内的生理病理过程中,扮演者重要角色,正常情况下机体通过食物吸收及循环铁来保持铁含量的稳定,一旦吸收过多亦或铁循环失衡则易导致铁过量,过量的铁将产生毒性[6]。循环铁以三价铁的形式通过与转铁蛋白相结合的形式存在。三价铁通过膜蛋白转铁蛋白受体1(transferrin receptor 1,TFR1)进入细胞。铁还原酶可以将三价铁还原成二价铁,二价铁由二价金属转运蛋白1(divalent metal transporter 1, DMT1)介导进入细胞质不稳定的鐵库中。由于二价铁到三价的氧化还原需要电子的转移,故铁经常参与底物之间的电子迁徙[7],二价铁可以与过氧化氢通过芬顿样反应产生具有更强氧化能力的羟基自由基,增加细胞内的ROS水平[8],这是铁诱导产生氧化应激的机制。此外,ROS可以通过机体负反馈调控铁稳态基因的表达,参与人体二价铁浓度的调控[9]。研究[10]表明,在铁死亡期间细胞内铁离子水平明显增高,铁离子在铁死亡过程中明显负载,因此提出铁过量是铁死亡的重要标志,这可能与氧化及抗氧化失衡有关。此外,在铁螯合剂的干预下,铁死亡会明显受到抑制,这充分说明了铁过度负载是铁死亡的重要机制[11]。
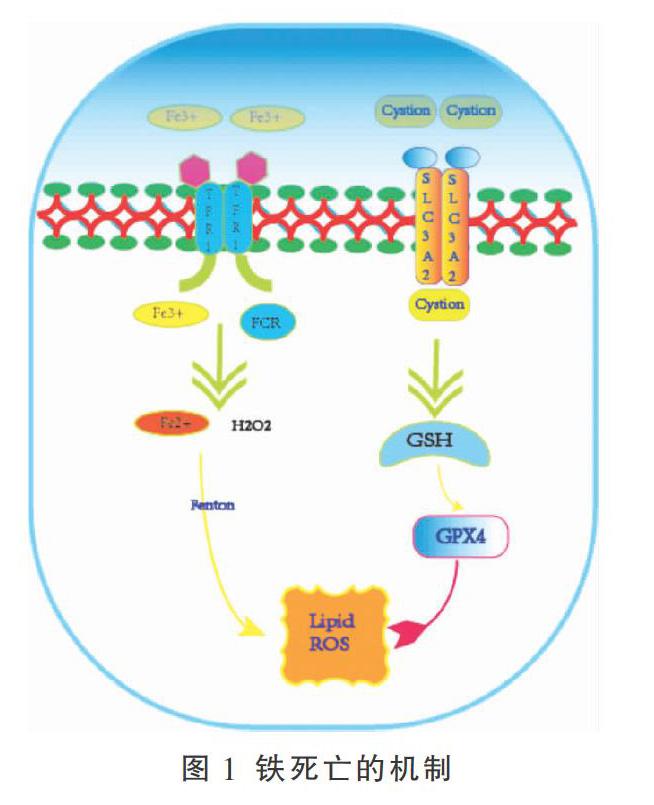
半胱氨酸(cysteine, Cys)是谷胱甘肽(glutathione, GSH)的合成需要的原料,细胞对Cys的摄取有4种途径,半胱氨酸转运体(the cystine/glutamate antiporter system, systemXc-)是其中很重要的一条[12]。GSH具有抗氧化应激的作用,并以此维持细胞的完整和稳态。研究者以14C标记Cys,并以铁死亡诱导剂erastin处理细胞,发现其可增加铁死亡的表达,降低细胞摄取Cys的能力和GSH的合成[13],这充分证明了systemXc-参与了诱导剂erastin介导的铁死亡,且systemXc-的表达与铁死亡呈负相关。GSH作为辅酶参与GPX4分解过氧化氢的过程,所以通过抑制GSH和GPX4细胞内活性可以提高细胞内的脂质ROS水平,最终介导铁死亡,细胞铁死亡的相关机制如图1。
1.2 铁死亡的检测
依据铁死亡的发生发展机制,针对脂质过氧化,铁含量,GPX4可以检测铁死亡。(1)在脂质过氧化的检测中,传感器C11-BODIPY和Liperfluo是亲脂性的,可以用来监测脂质过氧化[2],对于特定的脂质过氧化,可以通过液相色谱/质谱(Liquid chromatography/mass spectrometry, LC/MS)来检测[14];(2)铁含量可以通过电感耦合等离子体质谱法(inductively coupled plasma-mass spectrometry, ICP-MS)检测;(3)GXP4的检测可以使用细胞内磷脂酰胆碱氢过氧化物还原法[15]。
2 中医药通过GSH-GPX4-ROS通路干预铁死亡
2.1 对肿瘤相关疾病干预作用
青蒿素是菊科植物黄花蒿干燥茎叶的有效成分,属于倍半萜类化合物,也是青蒿发挥药理作用的基础物质[16],青蒿素最早是由中国中医科学院屠呦呦团队发现。青蒿素和其衍生物能够通过诱导肿瘤细胞的铁依赖性死亡发挥抗肿瘤效应[17]。在人类肝癌细胞HepG2的实验中[18],双氢青蒿素的抗肿瘤机制为通过芬顿样反应增加癌细胞内的ROS,并减少GSH和GPX4的表达而诱导癌细胞铁死亡,且外源性铁可以加速双氢青蒿素的芬顿样反应,加速癌细胞裂解。Yang等[19]发现青蒿琥酯有激活溶酶体的功能,并增加铁蛋白水解,升高铁浓度,通过铁依赖性诱导铁死亡。不仅是在抗肿瘤方面,双氢青蒿素抗疟机制中的一个重要通路就有诱导恶性疟原虫铁死亡[20]。
黄芩素,别名黄芩苷元、黄芩黄素,是唇形科植物黄芩的干燥根的有效成分,属于黄酮类化合物。Xie Y等[21]发现黄芩素是一种天然的铁死亡抑制剂,可抑制胰腺癌细胞中麦角菌素诱导的铁死亡。黄芩素还可以抑制铁死亡诱导剂erastin诱导的GPX4降解,保护细胞免受脂质过氧化。Probst L等[22]发现黄芩素可以降低脂质过氧化和ROS的产生,保护RSL3诱导的急性淋巴细胞白血病细胞的铁死亡。
荜茇酰胺是胡椒科植物荜茇的干燥根的有效成分,属于生物碱类化合物。在胰腺癌中,荜茇酰胺通过升高ROS的表达水平,以诱导铁死亡的方式杀伤癌细胞[23],其杀伤效果可以被抗氧化剂N-乙酰半胱氨酸、铁死亡抑制剂和铁螯合剂抑制,但是凋亡抑制剂不能抑制其杀伤活性,这说明荜茇酰胺的抗癌机制与铁死亡有关。在大肠癌细胞HT29和SW620中,荜茇酰胺调节可以调节ROS水平,控制GSH和Nrf2表达水平诱导铁死亡,发挥杀伤癌细胞的作用[24]。
2.2 对神经系统相关疾病干预作用
在缺氧的条件下,大脑的活动发生障碍,当氧化还原信号出现问题时,此时大脑对氧化应激就会敏感[25],氧化应激参与了铁死亡,所以大脑的生理病理与铁死亡密切相关。脑组织中的铁水平在衰老和神经系统退行性疾病发病过程中会升高,这可能会介导细胞铁死亡。GPX4缺失的成年小鼠可以导致海马神经元与星形胶质细胞减少,这与帕金森患者的病理改变一致[26]。
艾灸能调节GPX4的表达,对右黑质定向注射6-羟基多巴胺诱导的帕金森大鼠,艾灸百会穴和四神聪穴艾灸20 min,每周6次,持续6周,右黑质中的GPX4和铁蛋白重链1显著表达,大鼠帕金森症状缓解,这可能和艾灸抑制铁死亡有关[27]。李全等[28]认为Xc-/GPX4通路是电针夹脊穴促进脊髓损伤的机制之一。
丹参酮ⅡA是双子叶植物唇形科鼠尾草属丹参的干燥根的有效成分之一。丹参酮具有祛瘀生新、活血调经等效用,为妇科要药,此外亦可以治疗神经性衰弱、失眠、关节痛和肾孟肾炎等[29-30]。丹参酮ⅡA可能通过抑制小鼠海马细胞内ROS、过氧化脂质活性和铁含量,抑制铁死亡的发生保护海马细胞[31]。
花椒是芸香科花椒属植物,是传统的调味品及中药材,临床可以用于治疗腹痛、腹泻和牙痛等疾病。花椒具有广泛的抗癌、抗炎和治疗糖尿病等广泛生物活性[32-33]。在erastin诱导的小鼠海马神经元细胞中,花椒中的异丁基酰胺化合物可以抑制铁死亡,说明花椒保护小鼠海马神经元细胞的机制与抑制铁死亡有关[34]。
2.3 对泌尿系统相关疾病干预作用
急性肾损伤、肾单位的死亡和急性肾小管坏死是铁蛋白下调和坏死的主要病理生理作用[35]。王俊巖等[36]在小鼠慢性心力衰竭模型中发现,益气温阳活血利水法除了可以改善心衰,还可以改善肾脏损伤,减少肾脏纤维化,其机制可能是通过调控JNK/p53,进一步调节SLC7A11/GPX4/GSH信号通路,降低ROS减少细胞铁死亡有关。在诊断为原发性肾小球疾病的患者中,槐杞黄可以通过调节氧化应激、钙流入和线粒体ATP来调节免疫功能,可能以此参与与调控细胞凋亡、自噬和铁死亡等死亡方式,以减少肾损伤[37]。
3 中医药干预铁死亡的展望
中医药干预铁死亡的机制尚处于初步探索阶段。在针刺研究中,针刺-改善铁代谢-清除氧自由基-抗氧化的相关研究很多,但是针刺-抗氧化-铁死亡机制的相关研究较少。石学敏的醒脑开窍针刺法联合阿替普酶在治疗急性脑梗死患者时,可以减轻大脑中脂质过氧化的表达[38],针灸链脲佐菌素诱导的糖尿病大鼠,可以减轻脂质过氧化损伤[39]。针药并用时,针刺联合人參可以缓解大鼠慢性疲劳,其中GSH、谷胱甘肽过氧化物酶(glutathione peroxidase,GSH-Px)、超氧化物歧化酶(superoxide dismutase,SOD)活性提高,相比较于单独使用针刺或者汤药,加强了抗氧化能力[40]。
在中药的临床或动物实验中,中药抗氧化机制和脂质过氧化的相关研究很多,但是深入挖掘中药-脂质过氧化-铁死亡机制的研究较少,而脂质过氧化恰恰是铁死亡的重要介质。大鼠的黄药子肝损伤研究发现,黄药子可以破坏抗氧化系统及线粒体,导致细胞膜损伤和氧化-抗氧化系统失衡[41]。桦褐孔菌多糖可以通过降低高脂血症大鼠总胆固醇、甘油三酯、低密度脂蛋白水平,提升高密度脂蛋白水平,GSH-Px酶活升高发挥抗氧化机制[42]。山楂总黄酮可以通过提高SOD和谷胱甘肽S来转移酶活力,延缓或阻止非酒精性脂肪性肝病肝细胞抗氧化作用。
上述针刺和中药研究虽然探索了ROS、GSH等对抗氧化机制的调节作用,但是并没有深入挖掘与铁死亡相关的内容,这些都是拓展中医药研究的机遇。
4 小结
铁死亡从概念的提出到现在已接近8年,尽管对于铁死亡很多研究有了开创性的发现。铁死亡虽可消除病理状态的细胞,维持体内的稳态,但也可以损害正常细胞,导致机体功能和结构异常,运用好这把双刃剑需先掌握其机制。目前,对铁死亡的机制尚不清楚,可以认为铁死亡与脂质过氧化、铁负载及铁过量有关。在Fe/GPX4/GSH/ROS氧化机制中,中医药可以通过其中的一个靶点发挥抗氧化疗效的研究很多,但是深入挖掘中医药-脂质过氧化-铁死亡的相关研究很少。目前,已经报道的对铁死亡具有调节作用的中药及其活性成分虽然与经典铁死亡诱导剂相比,具有多靶点、多通路的特点,但是因其对铁死亡的相关研究很少,起步也晚,中医药干预铁死亡的机制有待进一步发掘,以期更好地运用到临床疾病诊治中来。
参考文献
[1] KAZAN K, KALAIPANDIAN S. Ferroptosis: yet another way to Die[J]. Trends in Plant Science, 2019, 24(6): 479-481.
[2] DIXON S J, LEMBERG K M, LAMPRECHT M R, et al. Ferroptosis: an iron-dependent form of nonapoptotic cell death[J]. Cell, 2012, 149(5): 1060-1072.
[3] 李瑶琪,杨 敏,李晓天.铁死亡的生化过程及对肿瘤的影响[J].中国生物化学与分子生物学报,2018,34(8):838-843.
[4] 徐文慧,李沧海,姜廷良.铁死亡通路与中药干预机制研究进展[J].中国中药杂志,2018,43(20):4019-4026.
[5] XIE Y, HOU W, SONG X, et al. Ferroptosis:process and function[J]. Cell Death & Differentiation, 2016, 23(3): 369-379.
[6] 张 宇,孙文爽,赵建宁,等.铁死亡与氧化应激的关系及其在运动系统疾病中的研究进展[J].医学研究生学报,2020,33(4):438-442.
[7] BENNETT B D, GRALNICK J A. Mechanisms of toxicity by and resistance to ferrous iron in anaerobic systems[J]. Free Radical Biology and Medicine, 2019, 140: 167-171.
[8] ZENG B L, ZHANG P F, ZHENG M Q, et al. Detection and identification of the oxidizing species generated from the physiologically important Fenton-like reaction of iron(II)-citrate with hydrogen peroxide[J]. Archives of Biochemistry and Biophysics, 2019, 668: 39-45.
[9] TOTSUKA K, UETA T, UCHIDA T, et al. Oxidative stress induces ferroptotic cell death in retinal pigment epithelial cells[J]. Experimental Eye Research, 2019, 181: 316-324.
[10] HAMBRIGHT W S, FONSECA R S, CHEN L J, et al. Ablation of ferroptosis regulator glutathione peroxidase 4 in forebrain neurons promotes cognitive impairment and neurodegeneration[J]. Redox Biology, 2017, 12: 8-17.
[11] BROWN RIKKI A M, RICHARDSON K L, KABIR T D, et al. Altered Iron Metabolism and Impact in Cancer Biology[J]. Metastasis and Immunology, 2020, 10:476.
[12] JAN L, J H S, YING H, et al. The cystine/glutamate antiporter system x(c)(-) in health and disease: from molecular mechanisms to novel therapeutic opportunities[J]. Antioxidants & redox signaling, 2013, 18(5): 522-555.
[13] YU H T, GUO P Y, XIE X Z, et al. Ferroptosis, a new form of cell death, and its relationships with tumourous diseases[J]. Journal of Cellular and Molecular Medicine, 2017, 21(4): 648-657.
[14] KAGAN V E, MAO G W, QU F, et al. Oxidized arachidonic and adrenic PEs navigate cells to ferroptosis[J]. Nature Chemical Biology, 2017, 13(1): 81-90.
[15] SPANGLER B, MORGAN C W, FONTAINE S D, et al. A reactivity-based probe of the intracellular labile ferrous iron pool[J]. Nature Chemical Biology, 2016, 12(9): 680-685.
[16] 于 然,金琳博,魏 強,等.双氢青蒿素抗肿瘤的分子机制研究进展[J].中国免疫学杂志,2020,36(19):2425-2428.
[17] OOKO E, SAEED M E M, KADIOGLU O, et al. Artemisinin derivatives induce iron-dependent cell death (ferroptosis) in tumor cells[J]. Phytomedicine, 2015, 22(11): 1045-1054.
[18] 费伟东,叶轶青,陈 玥,等.双氢青蒿素诱导肿瘤细胞铁死亡及其机制研究[J].中草药,2020,51(13):3473-3481.
[19] LIN R Y, ZHANG Z H, CHEN L F, et al. Dihydroartemisinin (DHA) induces ferroptosis and causes cell cycle arrest in head and neck carcinoma cells[J]. Cancer Letters, 2016, 381(1): 165-175.
[20] 徐文慧.双氢青蒿素抗疟机制:铁死亡的作用研究[D].北京:中国中医科学院,2019.
[21] XIE Y C, SONG X X, SUN X F, et al. Identification of baicalein as a ferroptosis inhibitor by natural product library screening[J]. Biochemical and Biophysical Research Communications, 2016, 473(4): 775-780.
[22] PROBST L, D?CHERT J, SCHENK B, et al. Lipoxygenase inhibitors protect acute lymphoblastic leukemia cells from ferroptotic cell death[J]. Biochemical Pharmacology, 2017, 140: 41-52.
[23] YAMAGUCHI Y, KASUKABE T, KUMAKURA S. Piperlongumine rapidly induces the death of human pancreatic cancer cells mainly through the induction of ferroptosis[J]. International Journal of Oncology, 2018, 52(3): 1011-1022.
[24] BASAK D, PUNGANURU S R, SRIVENUGOPAL K S. Piperlongumine exerts cytotoxic effects against cancer cells with mutant p53 proteins at least in part by restoring the biological functions of the tumor suppressor[J]. International Journal of Oncology, 2016, 48(4): 1426-1436.
[25] COBLEY J N, FIORELLO M L, BAILEY D M. 13 reasons why the brain is susceptible to oxidative stress[J]. Redox Biology, 2018, 15: 490-503.
[26] 李博文,王志维.铁死亡是一种新的调节性细胞死亡形式[J].基础医学与临床,2019,39(2):247-251.
[27] LU J, LIU X L, TIAN Y, et al. Moxibustion exerts a neuroprotective effect through antiferroptosis in Parkinson's disease[J]. Evidence-Based Complementary and Alternative Medicine, 2019, 2019: 2735492.
[28] 李 全,栾逸先,朱荟一,等.基于铁死亡Xc-/GPX4通路探究夹脊电针促进脊髓损伤修复机制[J].针灸临床杂志,2020,36(6):6-10.
[29] 孙环宇,许 晴,张燕欣,等.丹参类制剂及丹参活性成分改善脑循环作用机制的研究进展[J].药物评价研究,2020,43(8):1496-1500.
[30] 王云龙,房 岐,郑 超.丹参化学成分、药理作用及质量控制研究进展[J].中国药业,2020,29(15):6-10.
[31] 许 璐,汤其强.丹参酮ⅡA抑制HT22海马神经元发生铁死亡的机制研究[J].安徽医科大学学报,2019,54(6):833-839.
[32] 马丽梅,杨军丽.花椒属植物抗肿瘤活性成分研究进展[J].天然产物研究与开发,2020,32(2):334-340,357.
[33] 游玉明,任 亭,张世奇,等.花椒麻味物质对糖尿病大鼠肠道微生态的影响[J].营养学报,2017,39(2):170-176.
[34] 张凯峰,贺鹏杨,何达海.花椒中的异丁基酰胺化合物及其对HT22海马神经元铁死亡的抑制作用研究[J].天然产物研究与开发,2020,
32(1):18-22,56.
[35] BELAVGENI A, MEYER C, STUMPF J, et al. Ferroptosis and necroptosis in the kidney[J]. Cell Chemical Biology, 2020, 27(4): 448-462.
[36] 王俊岩,王陵军,梁碧容,等.基于“水火相济”理论探讨慢性心力衰竭对肾功能和肾脏纤维的影响及益气温阳活血利水法的干预研究[J].中华中医药学刊,2020,38(8):162-166,277-278.
[37] DUAN S B, PAN P, XU Q, et al. Preliminary study of Huai Qi Huang granules delay the development of primary glomerular diseases in human[J]. Renal Failure, 2014, 36(9): 1407-1410.
[38] 張 琦,田朝霞.醒脑开窍针刺法联合阿替普酶对急性脑梗死患者神经功能缺损、脂质过氧化及脑血管储备功能的影响[J].上海针灸杂志,2020,39(1):25-30.
[39] 庄 严,王 威,盖茹霜.针刺抗实验性糖尿病大鼠脂质过氧化损伤的研究[J].中国中医药信息杂志,2002,9(4):27-28.
[40] 张天仁.针刺结合人参煎剂对慢性疲劳模型大鼠抗氧化的实验研究[D].沈阳:辽宁中医药大学,2015.
[41] 梁玉琼,时 乐,徐 立.黄药子水煎液致肝损伤的早期作用机制研究[J].中药药理与临床,2013,29(3):117-119.
[42] 崔敬爱,王思霁,刘 畅,等.桦褐孔菌多糖对高脂饮食诱导的高脂血症大鼠血脂和肝脏的保护作用及机制[J].食品科学,2020,41(19):185-190.
