基于代谢组学的补阴药药性研究
2021-05-27许振鹏康立欣杨炳友匡海学
杨 靖,许振鹏,刘 艳,康立欣,杨炳友,匡海学
黑龙江中医药大学 教育部北药基础与应用研究重点实验室,黑龙江 哈尔滨 150040
中药药性理论中的“四气”即四性,是指中药的寒、热、温、凉4种基本特性,是中药药性理论的核心内容之一[1]。然而,阐明中药四性的科学内涵仍然是中药药性理论研究的难点和重点领域。代谢组学作为系统生物学研究的重要组成部分,其研究思想与中医药研究思想的整体观相似[2]。近年来,代谢组学技术在中医药现代研究中应用越来越广泛,可通过研究外源性物质对体内代谢所产生的影响,从整体上系统考察药物对机体的调控作用[3]。同时,代谢物作为基因表达的下游产物,能够更直接、更准确反映生物体的病理生理状态[4]。因此,运用代谢组学技术对更好地理解机体代谢状态与药物刺激后的代谢变化有重要的价值与意义。
百合为百合科植物卷丹Lilium lancifoliumThunb.、百合L.browniiF.E.Brownvar.viridulumBaker或细叶百合L.pumilumDC.的干燥肉质鳞叶,天冬为百合科植物天冬Asparagus cochinchinensis(Lour.) Merr.的干燥块根,麦冬为百合科植物麦冬Ophiopogon japonicus(L.f) Ker-Gawl.的干燥块根。3者味甘、苦(微苦),性寒(微寒),均为百合科植物,均具有养阴润肺之功效[5]。目前对这3种补阴药的研究主要集中在化学成分[6-8]、药理作用[9-11]、质量控制[12-14]等方面,对3者的药性研究鲜有报道。因此,本研究从代谢组学角度阐释了补阴药寒热药性的科学内涵,为中药药性的相关研究提供依据。
1 材料
1.1 动物
SPF级SD雄性大鼠36只,6~8周龄,体质量(200±20)g,购自辽宁长生生物技术有限公司,动物许可证号SCXK(辽)2020-0001。动物饲养于温度18~22 ℃、湿度40%~60%、黑暗/光亮周期为12 h的清洁级动物房,自由进食饮水。动物实验经黑龙江中医药大学伦理委员会批准(批准号2019121101)。
1.2 药材
百合饮片(批号20041207,产于浙江)、天冬饮片(批号20010702,产于贵州)、麦冬饮片(批号20030101,产于四川)购自同仁堂中药饮片有限责任公司,经黑龙江中医药大学樊锐锋副教授鉴定分别为百合科植物卷丹L.lancifoliumThunb.的干燥肉质鳞叶、百合科植物天冬A.cochinchinensis(Lour.) Merr.的干燥块根、百合科植物麦冬O.japonicus(L.f) Ker-Gawl.的干燥块根。
1.3 药品与试剂
对照品4-丙酮酸(批号B24354,质量分数≥98%)、5-甲基胞嘧啶(批号B21826,质量分数≥98%)、苯乙酮(批号B65459,质量分数为99%)、D-生物素(批号B21899,质量分数≥98%)、咖啡酸(批号B20660,质量分数≥98%)、α-拉帕醌(批号B21974,质量分数≥98%)、N-乙酰神经酰胺(批号B50728,质量分数≥98%)、盐酸吡哆胺(批号B27245,质量分数≥98%)、穿心莲内酯(批号B20207,质量分数≥98%)购自上海源叶生物科技有限公司;对照品反式-2-羟基肉桂酸(批号H113425,质量分数为97%)、3-羟基-3-甲基戊二酸(批号H137616,质量分数≥93%)、十二烷二酸(批号D109484,质量分数为99%)购自上海阿拉丁生化科技股份有限公司;斑蝥素对照品(批号CDAA-281387,质量分数为99.5%)购自北京中科质检生物技术有限公司;丙酮酸脱氢酶(pyruvate dehydrogenase,PDH)ELISA试剂盒(批号MM-20844R2)、丙酮酸激酶(pyruvate kinase,PK)ELISA试剂盒(批号MM-70147R2)、葡萄糖激酶(glucokinase,GCK)ELISA试剂盒(批号MM-20489R2)、乳酸脱氢酶(lactate dehydrogenase,LDH)ELISA试剂盒(批号MM-0605R2)、果糖磷酸激酶(phosphofructokinase,PFK)ELISA试剂盒(批号MM-70551R2)、琥珀酸脱氢酶(succinate dehydrogenase,SDH)ELISA试剂盒(批号MM-20910R2)、乙酰辅酶A(acetyl coenzyme A,Ac-CoA)ELISA试剂盒(批号MM-70207R20)、脂肪甘油三酯酶(adipose triglyceride lipase,ATGL)ELISA试剂盒(批号MM-70549R2)、Na+,K+-三磷酸腺苷(adenosine triphosphate,ATP)ELISA试剂盒(批号MM-43903R2)购自江苏酶免实业有限公司;色谱级甲醇、乙腈、甲酸购自美国Thermo Fisher Scientific公司;超纯水由美国Milli-Q system制备;其他试剂均为分析纯。
1.4 仪器
超高效液相色谱与四极杆-静电场轨道阱-线性离子阱三合一组合式质谱仪(UHPLC-Orbitrap-MS,美国Thermo Fisher Scientific公司);低温高速离心机(日本Hitachi公司);CENCO型涡旋仪(荷兰Breda公司);KQ-500DB型超声波清洗仪(昆山市超声仪器公司);大鼠代谢笼(苏州新区枫桥实验动物笼具厂);酶标仪(美国伯腾仪器有限公司);AL204电子天平(梅特勒-托利多仪器有限公司);TH-Mini手持均质仪器(北京兰杰柯科技有限公司)。
1.5 数据库及软件
人类代谢组学数据库(human metabolome database,HMDB,https://www.hmdb.ca);京都基因与基因组百科全书(Kyoto encyclopedia of genes and genomes,KEGG)数据库(https://www.genome.jp/kegg/ligand.html);mzCloud数据库(https://www.mzcloud.org/);MetaboAnalyst 5.0数据库(https://www.metaboanalyst.ca/);Compound Discoverer 3.1软件(美国Thermo Fisher Scientific公司);SIMCA 14.1软件(Umetrics AB);R统计软件包R×64 3.2.4(http://cran.r-project.org);SPSS 24.0软件。
2 方法
2.1 中药水提液的制备
分别称取百合、天冬、麦冬饮片,置圆底烧瓶中,加入10倍量蒸馏水回流提取1 h,连续提取2次,滤过,合并滤液,浓缩至质量浓度为0.52 g/mL的中药水提液(以生药量计)[2,15]。参照文献方法[5,16-18],采用紫外分光光度计和高效液相色谱法(high performance liquid chromatography,HPLC)测得百合水提液中百合多糖、咖啡酸、绿原酸、阿魏酸质量分数分别为25.119 5%、0.003 5%、0.001 4%、0.002 4%,天冬水提液中天冬多糖、原薯蓣皂苷质量分数分别为31.735 6%、0.177 1%,麦冬水提液中麦冬多糖质量分数为23.977 3%。
2.2 分组及给药
动物适应性喂养7 d后,随机分为对照组、百合提取物(5.2 g/kg)组、天冬提取物(5.2 g/kg)组和麦冬提取物(5.2 g/kg)组[2,19-20],每组9只。上午9: 00时各给药组ig相应药物(10 mL/kg),对照组ig等体积蒸馏水,1次/d,连续21 d。
2.3 大鼠样本收集与处理
2.3.1 尿液样本的采集及处理 末次给药后,收集各组大鼠12~24 h的尿液[2],离心,取100 μL上清液,加入200 μL甲醇,涡旋2 min,4 ℃、13 000 r/min离心15 min,取上清液,经0.22 μm滤膜滤过。每个尿样吸取50 μL于同一离心管中,涡旋2 min混合均匀。按照上述尿样样品的处理方法制备质控(quality control,QC)尿样样本,用于UHPLCOrbitrap-MS分析。
2.3.2 肝脏的采集 末次给药24 h后,大鼠脱颈椎处死,采集肝脏,以生理盐水漂洗,用滤纸吸干肝脏组织表面多余的水分,于 −80 ℃冰箱保存备用。
2.4 UHPLC-Orbitrap-MS检测
2.4.1 色谱条件 ACQUITY UPLC®CSHTMC18(100 mm×2.1 mm,1.7 μm)色谱柱,流动相为0.1%甲酸水溶液(A)-乙腈(B),梯度洗脱:0~5 min,2%~17% B;5~11 min,17%~30% B;11~15 min,30%~46% B;15~18 min,46%~79% B;18~22 min,79%~98% B;22~24 min,98% B;体积流量为0.3 mL/min,柱温为40 ℃,进样室温度为4 ℃。为确保系统的稳定性和重复性,在分析序列中,每4~5个样本加入1个QC样本。
2.4.2 质谱条件 应用Orbitrap Fusion Lumos质谱仪,采用加热电喷雾电离(heated electrospray ionization,HESI)方法:正负离子切换采集模式,扫描方式Full Scan/dd-MS2;喷雾电压正负极分别为3500、2500 V;毛细管电压为325 ℃;鞘气体积流量为50 arb;辅助气体积流量为10 arb;分辨率为120 000;高分辨质谱(HRMS)强度阈值为2.0×104;HRMS2扫描高能碰撞解离为20%、35%、50%,分辨率为30 000;碰撞诱导解离为15%、30%、45%,分辨率为30 000;采集范围为m/z100~800;进样量为5 μL。
2.5 数据处理
采用Compound Discoverer 3.1软件进行色谱峰识别、对齐、归一化,得到含有m/z、保留时间(tR)及峰面积的文件。将原始文件引入SIMCA 14.1数据处理软件,采用主成分分析法(principal component analysis,PCA)和正交偏最小二乘-判别分析法(orthogonal partial least squares discriminant analysis,OPLS-DA)对各组大鼠尿液的代谢物进行分析。根据变量投射重要性(variable importance in the project,VIP)>1且P<0.05比较对照组和补阴药组大鼠尿液代谢物,筛选出与寒热药性相关的潜在生物标记物。根据相对分子质量和串联质谱结果,与对照品、mzCloud数据库进行质谱信息匹配,鉴定可能的潜在标志物。
2.6 各组大鼠肝脏组织中糖代谢、能量代谢和脂代谢相关酶活性的检测
称取肝脏组织50 mg,加入1.5 mL预冷的PBS溶液,充分研磨,4 ℃、2000 r/min离心20 min,按ELISA试剂盒说明书检测各组大鼠肝脏组织中PDH、PK、GCK、LDH、PFK、SDH、Ac-CoA、ATGL和Na+,K+-ATP酶活性。
2.7 统计分析
实验数据以±s表示,采用SPSS 24.0软件进行单因素方差分析(ANOVA)。
3 结果
3.1 大鼠尿液代谢组学分析
3.1.1 大鼠尿液样品检测 对照组和各给药组大鼠尿液样品总离子流图见图1,采用PCA研究补阴药对大鼠尿液代谢谱的影响,如图2-A、D所示,与对照组比较,补阴药组大鼠尿液样本发生变化(正离子:R2X=0.685、Q2=0.478;负离子:R2X=0.754、Q2=0.443),二者明显分离。对正、负离子的质谱代谢轮廓进行有监督的OPLS-DA分析,如图2-B、E所示,对照组和补阴药组样本分离更加明显。OPLS-DA模型响应的置换检验如图2-C、F所示,所有排列的R2和Q2低于原始点,且Q2的回归线具有负截距,表明所有原始的OPLS-DA模型均有效。

图1 正离子 (A) 及负离子 (B) 模式下对照组和补阴药组大鼠尿液总离子流图Fig.1 Urine total ion maps of rats in control group and yin-tonifying herbs in positive ion mode (A),urine total ion maps of rats in control group and yin-tonifying herbs in negative ion mode (B)

图2 对照组和补阴药组大鼠尿液样本正离子模式下的PCA得分图 (A)、OPLS-DA得分图 (B) 和permutation检验图 (C)及负离子模式下的PCA得分图 (D)、OPLS-DA得分图 (E) 和permutation检验图 (F)Fig.2 PCA score (A),OPLS-DA score (B),and permutation test (C) of control group and yin-tonifying herbs in positive ion mode and PCA score (D),OPLS-DA score (E) and permutation test (F) of control group and yin-tonifying herbs in negative ion mode
3.1.2 标志物筛选 对照组和补阴药组大鼠尿液样品S-Plot图见图3,根据各组间各离子点量的变化趋势,筛选出P<0.05且VIP>1的代谢物;利用对照品和mzCloud数据库鉴定代谢物结构见表1,鉴定出3种补阴药共有差异代谢物26个。通过层次聚类分析见图4,发现补阴药可显著下调大鼠机体内15个生物标志物,提示这些潜在生物标志物对阐释中药的寒热药性具有重要的生物功能。
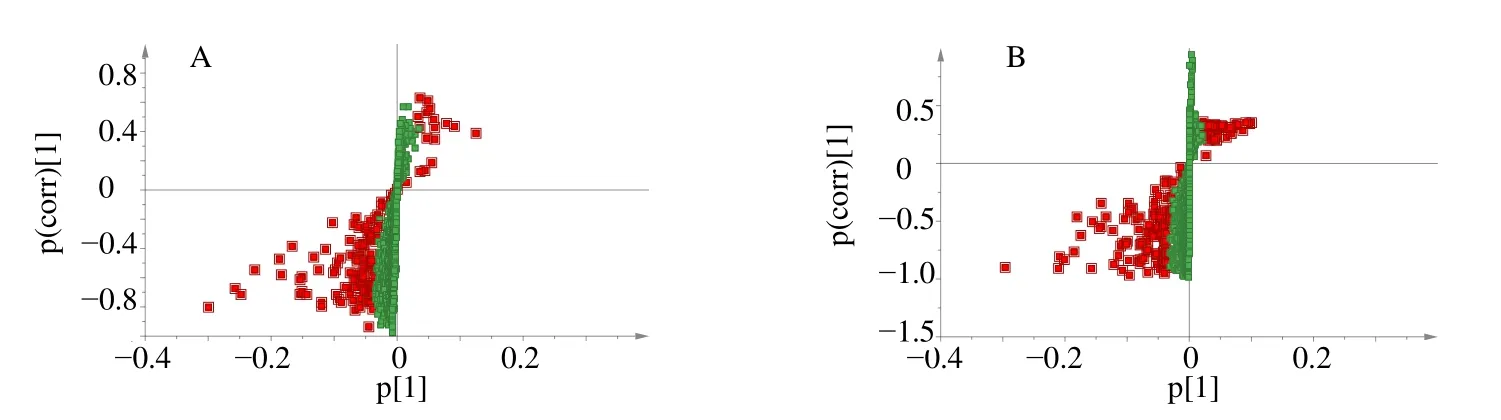
图3 正离子 (A) 和负离子 (B) 下对照组与补阴药组S-Plot图Fig.3 S-Plot of control and yin-tonifying herbs group in positive ion mode (A) and negative ion mode (B)

表1 补阴药组与对照组的差异代谢物Table 1 Different metabolites between yin-tonifying herbs and control group

图4 显著差异代谢物的层次聚类分析热图Fig.4 Hierarchical cluster analysis heat map of metabolites with significant differences
3.1.3 代谢途径的富集分析 通过KEGG、MetaboAnalyst 5.0对补阴药影响的代谢途径进行富集分析,结果如图5和表2所示,这些代谢物与D-甘油醛-3-磷酸参与的糖酵解、磷酸肌醇代谢、果糖和甘露糖代谢、糖异生、磷酸戊糖途径、N-乙酰神经氨酸参与的氨基糖和核苷酸糖代谢、2-羟基肉桂酸参与的苯丙氨酸代谢、茉莉酸参与的α-亚麻酸代谢、5-甲基胞嘧啶参与的嘧啶代谢、4-丙酮酸参与的维生素B6代谢、生物素参与的生物素代谢11条能量代谢通路相关。其中,与物质代谢、能量代谢密切相关的糖代谢、氨基酸代谢、脂代谢对生物代谢具有一定的影响。

图5 代谢通路分析Fig.5 Metabolic pathway analysis

表2 相关代谢通路分析的主要信息Table 2 Main information of related metabolic pathway analysis
3.2 补阴药对大鼠肝组织中糖代谢、能量代谢和脂代谢相关酶活性的影响
PK、GCK、PFK、PDH、Ac-CoA、SDH参与葡萄糖有氧氧化的3个阶段,即葡萄糖氧化生成丙酮酸、丙酮酸氧化脱羧生成Ac-CoA、三羧酸循环过程[21]。糖的有氧氧化是机体获得能量的重要方式[22]。LDH是一种糖酵解酶,其活性直接影响机体的能量代谢[23]。如图6所示,与对照组比较,百合组大鼠肝脏中PK、GCK、PFK、PDH、Ac-CoA、SDH、LDH活性均显著降低(P<0.05、0.01),天冬组大鼠肝脏中PK、GCK、PFK、PDH、SDH活性显著降低(P<0.05、0.01),麦冬组大鼠肝脏中GCK、PFK、PDH、Ac-CoA活性显著降低(P<0.05、0.01),表明百合、天冬、麦冬可以通过下调葡萄糖代谢相关酶的活性,从而抑制糖代谢。
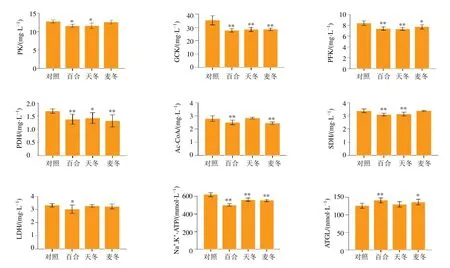
图6 补阴药对大鼠肝组织中糖代谢、能量代谢和脂代谢相关酶活性的影响 (±s ,n=9)Fig.6 Effect of yin-tonifying drugs on activities of enzymes related to carbohydrate metabolism,energy metabolismand lipid metabolism in liver tissues of rats (±s,n=9)
Na+,K+-ATP酶是与能量代谢相关的酶[24],是位于膜脂质双分子层中的一种蛋白质分子,可催化ATP水解供能,驱动位于细胞膜两侧Na+和K+交换,维持膜电位,调节渗透压,为物质吸收提供动力[25-26]。与对照组比较,各给药组大鼠肝脏Na+,K+-ATP酶活性显著降低(P<0.01),表明百合、天冬、麦冬能抑制能量代谢。ATGL是细胞内脂解过程中三酰甘油释放脂肪酸的关键酶[27-28]。与对照组比较,百合、麦冬组大鼠肝脏ATGL活性显著升高(P<0.05、0.01),表明百合、麦冬能够通过抑制脂代谢从而抑制能量代谢。
4 讨论
基于匡海学教授提出的新假说,即“药性(气)是药物通过不同途径,以主要影响机体的能量代谢、物质代谢为特征、与治疗作用有关或无关,但均可影响药物疗效发挥或与不良反应发生有关的一类生物学效应,促进机体能量、物质代谢的中药具有热性或温性,抑制机体能量、物质代谢的中药具有寒性或凉性”,课题组已经完成了基于代谢组学典型清热药(黄连、黄芩、黄柏)和温里药(附子、干姜、肉桂)的寒热药性研究,为后期研究其他功效中药,寻找能代表寒热药性相关的标志物提供了方法学平台。尿液和血清是代谢组学研究中使用最为广泛的生物样本。尿液中含有大量代谢终产物,具有丰富的代谢信息,同时具有非破坏性、重复性采集等优点[20];血清中内源性代谢物成分稳定,但存在连续采集困难且采集过程具有破坏性等弊端。因此,本研究基于尿液代谢组学,首次对补阴药的寒热药性进行了研究,并对代谢组学的研究结果进行验证。
能量代谢系统是需氧生物体内分布于线粒体的普遍代谢途径,是糖、脂肪、蛋白质三大物质的最终代谢通路,又是糖类、脂类、氨基酸代谢联系的枢纽。本研究发现,补阴药(百合、天冬、麦冬)能够下调与糖代谢相关的代谢物D-甘油醛-3-磷酸及N-乙酰神经氨酸、与脂代谢相关的代谢物茉莉酸、与氨基酸代谢相关的代谢物2-羟基肉桂酸、与核苷酸代谢相关的代谢物5-甲基胞嘧啶水平,从而发挥抑制物质代谢、能量代谢的作用。
PK、GCK、PFK、PDH、Ac-CoA、SDH参与糖有氧氧化的3个阶段,此过程为绝大部分细胞获得能量的主要方式,因此以上酶在机体内的低表达抑制能量产生[29];LDH在糖酵解过程中能够催化丙酮酸还原成乳酸,其活性的降低抑制糖酵解的第二阶段,使ATP水平减少;能量代谢相关酶Na+,K+-ATP酶活性降低可下调ATP水平,从而供能减少;脂代谢相关酶ATGL活性的升高可促进脂肪酸合成,进而消耗ATP[30]。本研究结果显示,补阴药组大鼠肝脏组织PK、GCK、PFK、PDH、Ac-CoA、SDH、LDH、Na+,K+-ATP活性降低,ATGL活性升高,与代谢组学结果一致,进一步证实补阴药(百合、天冬、麦冬)能够抑制物质代谢、能量代谢。
四气又称四性,指药物具有的寒、热、温、凉4种特性,反映药物影响人体阴阳盛衰和寒热变化的作用特点。药性的确定是以用药反应为依据,能够减轻或消除热证的药物,一般属于寒性或凉性,反之,能够减轻或消除寒证的药物,一般属于热性或温性。百合、天冬、麦冬具有养阴润肺、清心安神的功效,为寒(微寒)性药,常用于治疗阴虚燥咳、骨蒸潮热、内热消渴、热病津伤、咽干口渴、心阴不足之心悸易惊及热病后期热伤津液等热证[5]。热证是人体机能活动亢进所表现出来的证候,能够促进机体物质代谢、能量代谢[4,29,31-32]。本研究结果表明,百合、天冬、麦冬具有抑制物质代谢、能量代谢的功能,可以纠正热证所导致的物质代谢、能量代谢偏盛,从代谢组学角度阐释了补阴药大多为寒性或凉性的科学内涵,与中医临床用药“寒者热之、热者寒之”的原则相契合。
综上所述,本研究从补阴药中找到了15个符合寒药作用表达规律的共有差异代谢物,其表达趋势均为下调,对其相关代谢通路的影响与课题组前期通过代谢组学方法发现寒药/热药主要抑制/促进糖代谢(糖异生、磷酸戊糖途径)、花生四烯酸代谢、三羧酸循环、氨基酸代谢结果一致[2]。本研究基于代谢组学,拓展了所研究中药的功效范围,进一步验证了中药性味科学内涵新假说的客观性。
利益冲突所有作者均声明不存在利益冲突
