同一射野角度不同优化方式对中央型肺癌调强适形放射治疗计划的影响
2021-05-27刘凌湘陈照辉黄贤海易兰
刘凌湘 陈照辉 黄贤海 易兰
广州市番禺区中心医院肿瘤科 511400
放疗是肺癌治疗的常见手段,其中,调强适形放射治疗(intensity modulated radiotherapy,IMRT)是目前常用的一种放疗技术,其采用一系列不同射野从不同方向照射靶区,通过调整射野内强度分布,使高剂量区适形于靶区,并在一定程度上避开靶区周围的正常组织。对于中央型肺癌,由于其主要发生在段支气管至主支气管[1],靶区趋近纵隔而使周围正常组织如脊髓、食管、心脏等不可避免地受到照射,进行IMRT 计划设计时,需要选择合适的射野方向和射野数目,其中射野方向的选择是关键。目前,临床上普遍仍采用物理师根据经验给出的射野方向,射野大小也普遍采用铅门自动跟随适形于整个靶区。这样对部分中央型肺癌来说,可能某一个或某几个射野有部分位置需穿过较多的正常肺组织才能到达靶区,增加了正常肺组织的照射剂量。为了达到更好地保护正常肺组织的目的,我们在参考相关文献[2~5]的基础上,选取6 例中央型肺癌患者,根据靶区分布情况和靶区边缘到皮肤表面的距离,遵循射野以最短路径到达靶区(即穿过肺部最小)的原则,采用锁铅门[2-3]和添加虚拟“Block”[4-5]的方法对所给定的射野方向进行一定的优化处理,探讨给定射野方向进一步优化对肿瘤靶区和危及器官剂量分布的影响。
1 资料与方法
1.1 一般资料
回顾性分析2017 年11 月至2019 年10 月在广州市番禺区中心医院接受IMRT 的6 例中央型肺癌患者的临床资料,其中,男性5 例、女性1 例,中位年龄64(53~73)岁。6 例患者中,小细胞肺癌1 例(局限期)、非小细胞肺癌5 例(鳞癌3 例:2 例Ⅲb 期、1 例Ⅳ期;腺癌2 例:均为Ⅳ期)。纳入标准:①靶区分布处于居中偏右位置;②可顺利完成整个放疗计划。排除标准:①靶区分布处于居中偏左或其他位置;②由于各种原因未能完成放疗计划。所有患者治疗前均签署了知情同意书。本研究符合《赫尔辛基宣言》的原则。
1.2 靶区和危及器官的勾画
患者取仰卧位,手臂上举抱头,用真空袋固定,采用荷兰Philips 公司Brillance Big Bore CT 于平静呼吸状态下行CT 平扫与增强扫描,扫描层厚、层间距均为5 mm,范围从环状软骨至肾上腺水平。扫描后的图像传至美国Varian 公司Eclipse 10.0 三维治疗计划系统。由主治及副主任职称的放疗医师在CT 图像上勾画靶区和危及器官,其中,大体肿瘤体积(gross tumor volume,GTV)为影像学可见肺部病灶和纵隔肿大淋巴结;临床靶体积(clinical target volume,CTV)为GTV 外一定范围和区域的淋巴结,包括肿瘤潜在侵犯的范围;计划靶体积(planning target volume,PTV)包括计划大体肿瘤体积(planning gross target volume,PGTV)和计划临床靶体积(planning clinical target volume,PCTV),PGTV 基于GTV 向各方向均匀外扩5 mm,PCTV 则基于CTV 向各方向均匀外扩5 mm;危及器官包括肺、脊髓、心脏、食管。
1.3 治疗计划的设计
采用Eclipse 10.0 三维治疗计划系统进行IMRT计划设计。采用9 野均分、去掉穿健侧肺(左肺)的2 个射野的布野方法(射野方向为200°、240°、280°、320°、0°、40°、160°),对所给定的射野方向,部分射野根据靶区分布和靶区边缘到皮肤表面的距离,遵循穿过肺部最小的原则分别进行锁铅门设计(F-plan)和添加虚拟的“Block” (B-plan)设计(图1),其余射野铅门自动跟随适形于整个靶区。其中,F-plan 主要进行240°、280°、40° 3 个角度的锁铅门设计,图1A 为40°射野方向的锁铅门设计,该处靶区分布倾向于右侧,与右侧相比,靶区边缘距左侧皮肤表面距离较远,该射野在此处如果采用铅门自动跟随,则入射路径长,需穿过左肺才能到达靶区,因此设计时对该部分采用了锁铅门设计,缩回Y1 方向处的部分铅门。同理,240°和280°射野方向也是如此设计,在靶区上半段缩回Y2 方向处的部分铅门,这样,靶区上半段参与照射的射野方向包括200°、320°、0°、40°、160°,下半段参与照射的射野方向包括200°、240°、280°、320°、0°、160°。B-plan 所添加虚拟的“Block”的射野方向与F-plan 相同,在接近皮肤表面射野入射路径处添加虚拟的“Block” (图1B)。肿瘤靶区和危及器官剂量优化的优先顺序依次为靶区、脊髓、肺、食管、心脏;B-plan 中所添加虚拟的“Block”的优化权重仅次于靶区,限量“Block”≤5~10 Gy。
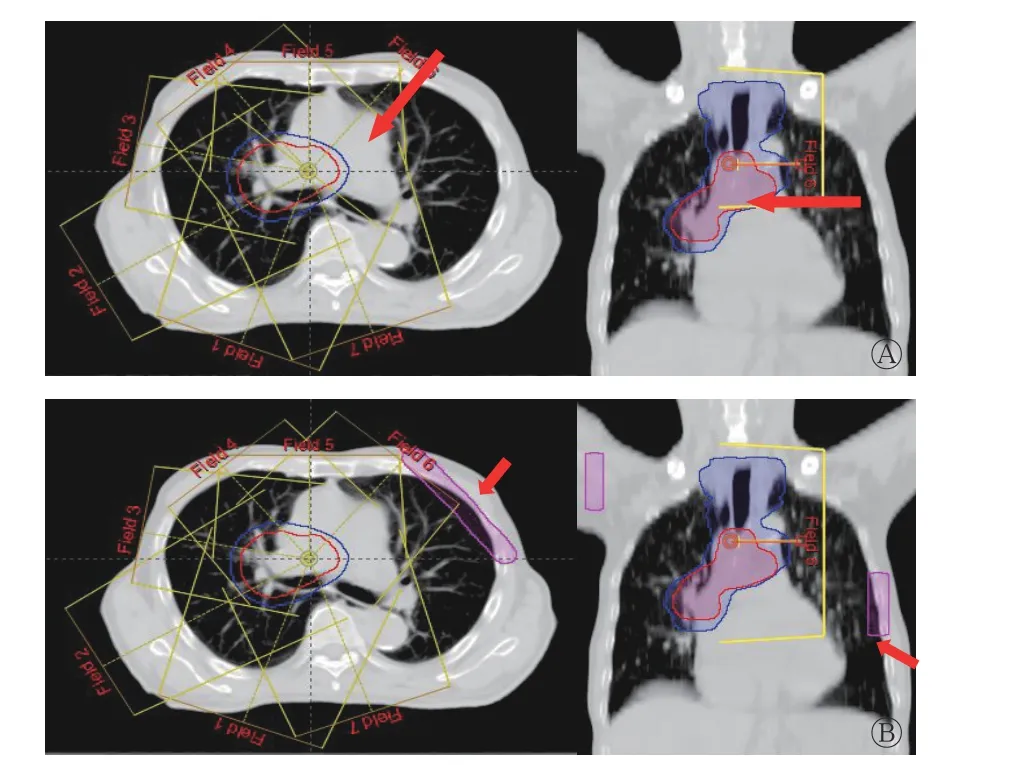
1.4 处方剂量的要求
PGTV 的处方剂量为6020 cGy /28 次(215 cGy/次),PCTV 的处方剂量为5040 cGy /28 次(180 cGy/次)。要求至少95%的PTV 接受处方剂量以上的剂量,PTV 内大于处方剂量110%的体积不超过1%。危及器官的剂量约束条件:双肺的V5≤60%~65%、V10≤50%、V20≤25%~35%、V30≤20%、双肺的肺平均剂量(mean lung dose,MLD)≤20 Gy(其中,Vx指接受x Gy 剂量照射的体积占总体积的百分比);脊髓的最大剂量(maximum dose,Dmax)<45 Gy;食管的Dmax<60 Gy;心脏的V30≤40%、V40≤30%。
1.5 计划评估
观察剂量-体积直方图(dose-volume histogram,DVH)和CT 各层面的剂量分布可直观地得出靶区和危及器官的剂量体积分布情况。靶区的评估参数包括V95%、V100%、V105%(Vx%指接受x%处方剂量照射的体积占总体积的百分比)、D50、D95(Dx指x%的靶区体积所接受的照射剂量)、平均剂量(mean dose,Dmean)、靶区均匀性指数(homogeneity index,HI)、适形度指数(conformity index,CI)[6]和总的机器跳数。HI=(D2−D98)/D处方,其中D2指DVH 上2%的靶区体积所接受的照射剂量,近似于“最大剂量”;D98指DVH 上98%的靶区体积所接受的照射剂量,近似于“最小剂量”。HI 越小,剂量均匀性越好。CI=(VT,ref/VT)×(VT,ref/Vref),其中,VT为靶体积;VT,ref为参考等剂量线所包绕的靶体积;Vref为参考等剂量线所包绕的所有区域体积。CI 范围为0~1(数值越接近1,表示适形度越好)。
危及器官的评估参数包括双肺的V5、V10、V13、V15、V20、V25、V30、V40和MLD;心脏的V30、V40;脊髓的Dmax;正常组织(指靶区所在层面、外轮廓减去靶区外扩1 mm的所有正常组织)的V5、V10、V20、V30、V40、Dmean。食管由于严格限制其Dmax<60 Gy 或V60≤1%,这里不作评估。
1.6 统计学方法
采用SPSS20.0 软件进行统计学分析。经Shapiro-Wilk 检验,符合正态分布的数据以±s表示,经Levene's 方差齐性检验,方差齐的条件下,2 种治疗计划之间的剂量学差异比较采用配对t检验。P<0.05 为差异具有统计学意义。
2 结果
2.1 2 种治疗计划的靶区剂量比较
6 例患者的PGTV 和PCTV 分别为(241.84±148.21) cm3和(581.79±233.47) cm3。图2、3 为其中1 例患者的靶区剂量分布图和DVH。结合图3 和表1 可知,2 种治疗计划的靶区覆盖率基本符合临床要求(V95%均>99%,V100%均在95%左右),且均具有较好的靶区适形度和剂量均匀性(CI 接近0.78,HI 接近0.09)。由表1 可知,2 种治疗计划的PGTV 和PCTV 的各参数的差异均无统计学意义(均P>0.05),但B-plan的PGTV 的高剂量区(D2、D50)略低于F-plan,低剂量区(D95、D98)略高于F-plan;另外,2 种治疗计划的总的机器跳数相近,差异无统计学意义(P>0.05)。
2.2 2 种治疗计划的危及器官受照剂量比较
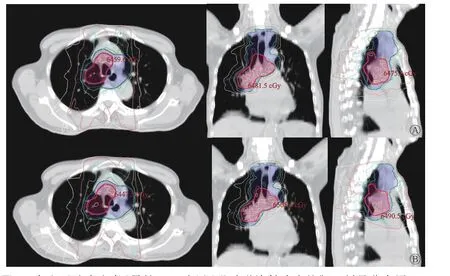
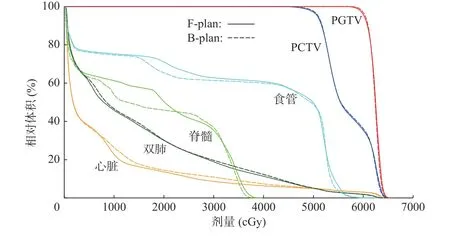
表 1 中央型肺癌调强适形放射治疗中2 种治疗计划的靶区覆盖结果的比较(n=6, ±s)Table 1 Comparison of target coverage between the two plan types of intensity modulated radiotherapy in central lung cancer(n=6, ±s)
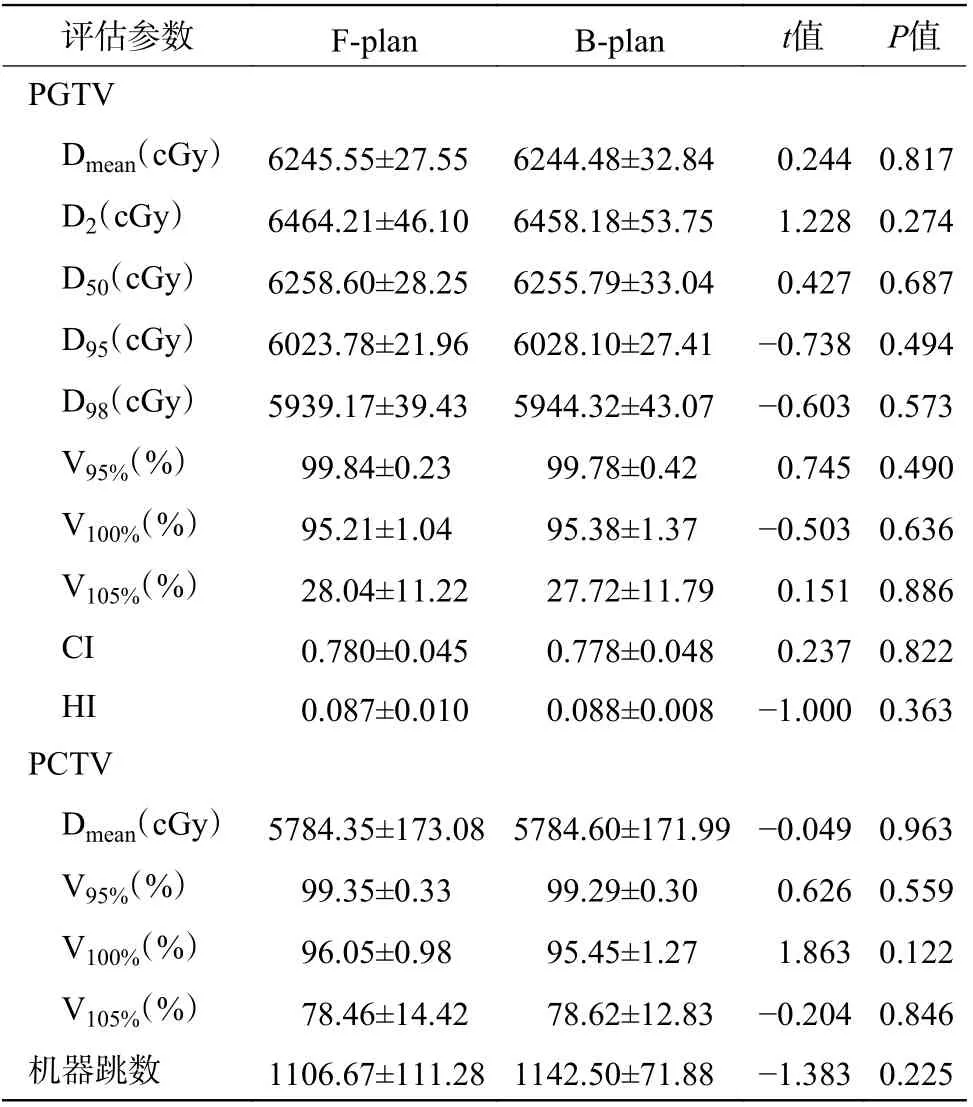
表 1 中央型肺癌调强适形放射治疗中2 种治疗计划的靶区覆盖结果的比较(n=6, ±s)Table 1 Comparison of target coverage between the two plan types of intensity modulated radiotherapy in central lung cancer(n=6, ±s)
注:F-plan 为锁铅门设计;B-plan 为添加虚拟的“Block”设计;PGTV 为计划大体肿瘤体积;Dmean 为平均剂量;Dx 为x%的靶区体积所接受的照射剂量;Vx%为接受x%处方剂量照射的体积占总体积的百分比;CI 为适形度指数;HI 为均匀性指数;PCTV 为计划临床靶体积
评估参数 F-plan B-plan t值 P值PGTV Dmean(cGy) 6245.55±27.55 6244.48±32.84 0.244 0.817 D2(cGy) 6464.21±46.10 6458.18±53.75 1.228 0.274 D50(cGy) 6258.60±28.25 6255.79±33.04 0.427 0.687 D95(cGy) 6023.78±21.96 6028.10±27.41 −0.738 0.494 D98(cGy) 5939.17±39.43 5944.32±43.07 −0.603 0.573 V95%(%) 99.84±0.23 99.78±0.42 0.745 0.490 V100%(%) 95.21±1.04 95.38±1.37 −0.503 0.636 V105%(%) 28.04±11.22 27.72±11.79 0.151 0.886 CI 0.780±0.045 0.778±0.048 0.237 0.822 HI 0.087±0.010 0.088±0.008 −1.000 0.363 PCTV Dmean(cGy) 5784.35±173.08 5784.60±171.99 −0.049 0.963 V95%(%) 99.35±0.33 99.29±0.30 0.626 0.559 V100%(%) 96.05±0.98 95.45±1.27 1.863 0.122 V105%(%) 78.46±14.42 78.62±12.83 −0.204 0.846机器跳数 1106.67±111.28 1142.50±71.88 −1.383 0.225
6 例患者双肺的体积为(3374.70±990.20)cm3、脊髓在三维方向上距靶区的最近距离为(1.45±0.61)cm。由表2 可知,2 种治疗计划的危及器官受照剂量基本满足临床的限量要求,其中,B-plan的双肺的MLD、V5、V25、V30、V40和正常组织的Dmean、V5、V40普遍高于F-plan,且差异均有统计学意义(均P<0.05);对于心脏和脊髓的受照剂量,2 种治疗计划的差异均无统计学意义(均P>0.05),但B-plan 的心脏受照剂量(V30、V40)高于F-plan,脊髓的受照剂量(Dmax)却低于F-plan。
3 讨论
在肺癌的放疗中,限制剂量的正常组织包括肺、脊髓、食管和心脏。其中,放射性肺损伤是肺癌患者放疗时最主要的剂量限制因素[7],发生功能性肺损伤的概率取决于所受到照射的体积。现有研究结果显示,全肺V20为放射性肺损伤最佳的独立预测因子[7-11]、V30为独立预测因子[7];全肺低剂量受照体积(V5、V10、V13)[8,11-12]、全肺MLD[10]和全肺体积[13]是有效预测因子。其次,脊髓是仅次于肺的主要危及器官,是肺癌患者放疗时主要的剂量限制因素,放疗后不良反应主要与患者接受的最大剂量有关,常规照射时脊髓受照剂量不应>45 Gy。食管、心脏位于身体中线附近,对于中央型肺癌,在给定射野方向时很难将它们完全避开,因此,放射性食管损伤[14]和心脏损伤[1]同样是其放疗的并发症之一。其中,放射性食管损伤的发生概率与最大受照剂量的关系密切,最大受照剂量(≥60 Gy)及最大受照剂量体积所处的解剖位置对食管3~5级毒性反应具有较大的预测价值[14]。而放射性心脏损伤的发生率及程度则与受照总剂量、受照体积相关[1,15]:受照总剂量<30 Gy 时,极少引起心脏损伤,受照总剂量>40 Gy 时,随受照剂量的增加,放射性心脏损伤的发生率增高;同时,受照心脏体积越大,放射性心脏损伤的发生率越高,>65%的心脏体积受照时,放射性心脏损伤的发生率明显升高。
表 2 中央型肺癌调强适形放射治疗中2 种治疗计划的危及器官受照剂量的比较(n=6, ±s)Table 2 Dosimetric comparison of organs at risk between the two treatment plans types of intensity modulated radiotherapy in central lung cancer (n=6, ±s)
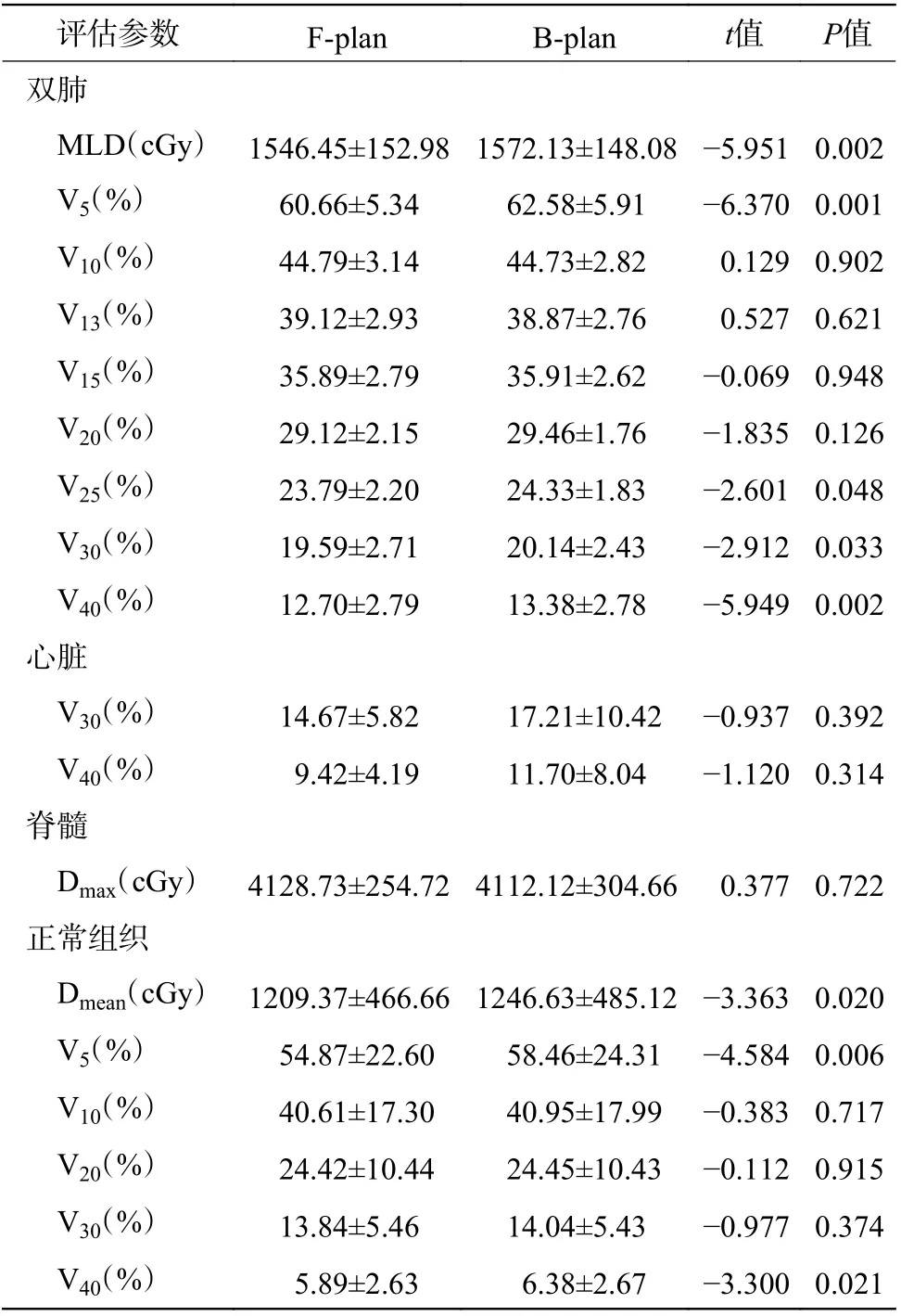
表 2 中央型肺癌调强适形放射治疗中2 种治疗计划的危及器官受照剂量的比较(n=6, ±s)Table 2 Dosimetric comparison of organs at risk between the two treatment plans types of intensity modulated radiotherapy in central lung cancer (n=6, ±s)
注:F-plan 为锁铅门设计;B-plan 为添加虚拟的“Block”设计;MLD 为肺平均剂量;Vx 为接受x Gy 剂量照射的体积占总体积的百分比;Dmax 为最大剂量;Dmean 为平均剂量
评估参数 F-plan B-plan t值 P值双肺MLD(cGy) 1546.45±152.98 1572.13±148.08 −5.951 0.002 V5(%) 60.66±5.34 62.58±5.91 −6.370 0.001 V10(%) 44.79±3.14 44.73±2.82 0.129 0.902 V13(%) 39.12±2.93 38.87±2.76 0.527 0.621 V15(%) 35.89±2.79 35.91±2.62 −0.069 0.948 V20(%) 29.12±2.15 29.46±1.76 −1.835 0.126 V25(%) 23.79±2.20 24.33±1.83 −2.601 0.048 V30(%) 19.59±2.71 20.14±2.43 −2.912 0.033 V40(%) 12.70±2.79 13.38±2.78 −5.949 0.002心脏V30(%) 14.67±5.82 17.21±10.42 −0.937 0.392 V40(%) 9.42±4.19 11.70±8.04 −1.120 0.314脊髓Dmax(cGy) 4128.73±254.72 4112.12±304.66 0.377 0.722正常组织Dmean(cGy) 1209.37±466.66 1246.63±485.12 −3.363 0.020 V5(%) 54.87±22.60 58.46±24.31 −4.584 0.006 V10(%) 40.61±17.30 40.95±17.99 −0.383 0.717 V20(%) 24.42±10.44 24.45±10.43 −0.112 0.915 V30(%) 13.84±5.46 14.04±5.43 −0.977 0.374 V40(%) 5.89±2.63 6.38±2.67 −3.300 0.021
综上,设计中央型肺癌的IMRT 计划时,不仅需要考虑肺和脊髓的受量,还必须兼顾食管和心脏的受量[8]。目前临床上常用的布野方法倾向于射野集中于前后方向,强调双肺的受量,忽略靶区的适形度和均匀性及其他危及器官的受量。喻冰琪等[16]提出了平衡参数控制下的IMRT 的概念,既强调靶区剂量和靶区剂量适形度,又平衡了各主要危及器官的受照剂量,在这种情况下,可以考虑增加一个斜野(近似水平野)[17]来分担中央型肺癌前后方向射野的调制压力。射野方向和射野数目作为IMRT计划的主要参数,二者相辅相成,郝龙英等[18]比较了5 野、7 野、9 野动态调强的肺癌剂量分布,得出5 野就可以满足临床剂量要求,但对于脊髓、食管、心脏的保护而言,7 野或9 野更有优势。本研究选取的6 例中央型肺癌患者,依据上述布野原则,在给定射野的基础上,部分射野经过锁铅门或添加虚拟的“Block”设计优化处理后,靶区同一部位至少有5 个方向的射野进行照射,保证了靶区的适形度,改善了脊髓和心脏的受照剂量。2 种治疗计划所得到的靶区剂量覆盖率高、适形度好(CI接近0.78),同时由于各射野方向间距较大,靶区剂量均匀性好(HI 接近0.09)。在保证双肺限量符合临床要求的情况下,脊髓Dmax均控制在<45 Gy,心脏受量也远低于临床限量要求。这样就很好地达到了“平衡参数控制下的IMRT 的概念”的要求。本研究中2 种治疗计划下所得到的靶区剂量分布大同小异,HI、CI 和总的机器跳数相近,各参数的差异无统计学意义,但B-plan 的PGTV 的高剂量区(D2、D50)略低于F-plan,低剂量区(D95、D98)略高于F-plan。这可能是因为B-plan 靶区每一部位参与照射的射野数多于F-plan,增加了计划的调控能力。2 种治疗计划下双肺的V5、V30基本符合临床要求,MLD、V10、V20完全符合临床要求,但B-plan 的MLD、V5、V25、V30、V40普遍高于F-plan,且差异有统计学意义。这可能是因为尽管B-plan 进行了“Block”的剂量限制,但所有射野仍穿过肺部照射至靶区,同一部位参与照射的射野数多于F-plan,导致低剂量区分布广、高剂量区向靶区集中。同时B-plan 有更多的射野穿过心脏,在限制肺和脊髓受量的情况下,照射剂量向纵隔前后方向集中,导致心脏受照剂量高于F-plan;脊髓则由于有更多的射野分担照射,极易达到临床高剂量限量要求,2 种治疗计划下的脊髓Dmax均<45 Gy。
锁铅门和添加虚拟的“Block”的方法是放射治疗计划设计时的一种辅助手段,在降低正常肺组织受照剂量特别是低剂量方面具有很大优势[2-5]。本研究从射野方向的确定出发,采用锁铅门和添加虚拟“Block”的2 种优化处理方法来探讨部分射野方向优化对中央型肺癌IMRT 剂量学分布的影响,发现二者均能获得较好地靶区剂量学分布,在危及器官保护方面二者各有优缺点;在实际临床应用中可以根据个体差异、靶区分布有选择地使用这2 种优化方法,对于分布不太明显的靶区,可以二者结合使用。
利益冲突本研究由署名作者按以下贡献声明独立开展,不涉及任何利益冲突。
作者贡献声明刘凌湘负责研究方案的设计、部分调强计划的设计、数据的统计、论文的撰写与修订;陈照辉、黄贤海、易兰负责部分调强计划的设计、数据的采集。
