应用超声骨刀行后路经关节突关节环形减压术治疗钙化型胸腰段椎间盘突出症的疗效分析
2021-05-25金开基郭昭庆陈仲强
金开基 郭昭庆 陈仲强
(北京大学国际医院骨科,北京 102206)
胸腰段椎间盘突出症(thoracolumbar disc herniation,TLDH)是指发生于胸腰段结合处,即T10-L2 的椎间盘突出,是一种导致胸脊髓病的相对少见的疾病。与下段腰椎间盘突出相比,TLDH 的治疗效果较差,其原因在于TLDH 通常压迫程度较重,椎管侵占率高,此外胸腰段为脊髓圆锥区域,相较于下腰段马尾神经更为脆弱[1]。TLDH 根据突出的椎间盘性质可分为软突出和钙化型突出(calcified thoracolumbar disc herniation,CTLDH)。与软突出相比,CTLDH 多为巨大突出,椎管侵占率高,神经损害重,手术风险高。
TLDH 的手术入路分为前方入路、侧方入路和后路手术[2-6]。前路或侧路主要包括各种经胸及肋横突入路,优势在于从前侧方可直接到达椎间盘,不需要牵开硬膜囊,对脊髓刺激较小[5,6]。但前路经胸手术技术要求较高,且并发症较多,对于中央型椎间盘突出处理较为困难。后路手术可分为单纯椎板切除术和经关节突关节脊髓环形减压术。后路单纯椎板切除术操作较简单,不切除突出的胸椎间盘,为间接减压,存在术后症状不缓解的风险,多适用于胸椎间盘突出合并黄韧带骨化(ossification of ligamentum flavum,OLF),以OLF为主要致压物的情况。
近年来,多个研究报道了后路经关节突关节脊髓环形减压术治疗胸椎前方致压物,其操作要点为切除后方椎板及双侧关节突关节,经椎间孔区域显露并切除前方致压物,取得了良好的治疗效果。早期手术多采用高速磨钻及骨刀进行椎板、小关节及骨性致压物的切除操作,手术效率较低,且存在较大震动,可导致脊髓损伤。近年来,超声骨刀的临床应用为CTLDH 的治疗技术带来了巨大飞跃。超声骨刀辅助下进行椎板切除的安全性和有效性得到大幅提高[7]。本研究探索应用超声骨刀行后路经关节突关节脊髓环形减压术治疗CTLDH的临床疗效。
1 资料与方法
1.1 一般资料
纳入标准:①年龄>18 岁;②应用超声骨刀行后路关节突关节脊髓环形减压术治疗的单节段CTLDH;③进行性脊髓功能损害,经CT 及MRI 证实为CTLDH;④完成2 年及以上随访。排除标准:①多节段或其他原因导致的胸椎管狭窄患者;②合并颈胸腰椎管狭窄者;③影像学及随访资料不完整者。
根据上述纳入与排除标准,回顾性纳入2015年1月至2018年8月行后路经关节突关节环形减压融合术治疗的单节段CTLDH患者17例。男10例,女7例;年龄22~71岁,平均(46.1±15.2)岁;体重指数(body mass index,BMI)为22.3~38.1 kg2/m,平均(26.1±4.6)kg2/m。合并症:糖尿病4 例,高血压6 例。致病节段:T10/11 2 例,T11-T12 5 例,T12-L1 7 例,L1-L2 3 例。术前症状持续时间为1~84 个月,平均(38.1±21.1)个月。所有患者均表现为进行性脊髓功能损害,其中3例同时存在肋间神经损害,表现为相应肋间区域疼痛或麻木。2 例患者曾行下腰椎水平的椎板切除术,3 例患者同时存在相同椎间盘水平的OLF。
本研究经医院伦理委员会批准通过,所有患者均签署相关知情同意书。
1.2 手术方法
患者采用全身麻醉,取俯卧位,胸腰段后正中切口暴露后部结构,于拟减压节段上下椎体放置椎弓根螺钉后,以超声骨刀采用“揭盖法[8]切除椎管后壁,包括椎板及双侧内侧关节突关节,如合并OLF 一并切除。以超声骨刀沿上下关节突关节根部将其全层切断并取出,此时常遇到节段血管分支及硬膜外静脉丛出血,可采用双极电凝和明胶海绵等[9]进行止血,注意保护出口神经根,在T12-L1水平以下节段尤为重要。既往手术技术需将胸膜或腹膜推开显露椎间盘侧方以增大操作空间[10],在应用超声骨刀技术后此步骤可省略。清理软组织后可显露突出骨性致压物的侧方,此时可见隆起的骨化块顶起硬膜囊。首先切除侧方椎间盘,向前方切除髓核,两侧交替操作直到中线水平完成会师。然后于安全三角区[8]上下缘,以超声骨刀向前楔形切除椎体上下缘部分骨质及椎间盘,然后继续切除中线部位的椎间盘。小心分离骨化块与硬膜囊间的黏连,避免损伤硬膜囊。然后将骨化块向前推挤入椎间隙内即可完全切除。将减压过程中切除的椎板及关节突关节骨质修整成碎骨后置入椎间隙内并压实,椎间隙高度允许时置入1枚椎间融合器,如椎间隙狭窄则直接椎体间加压闭合。
1.3 随访计划及评价指标
围手术期评价指标:手术时间、出血量、住院时间、术后并发症情况。术后3、6、12 个月及术后每年进行门诊随访。神经功能评分采用胸脊髓病改良日本骨科学会评分(modified Japanese Orthopedics Association,mJOA),末次随访时计算mJOA 改善率。改善率=(随访时mJOA 评分-术前mJOA 评分)/(11-术前mJOA 评分)×100%。mJOA 改善率:100%~75%为优,74%~50%为良,49~25%为可,24%~0 为无变化,<0为加重,其中mJOA 改善率≥50%认为治疗效果良好。术后并发症评估包括:切口感染,早期脊髓功能损害,硬膜损伤/脑脊液漏,手术切口感染,再手术及其他并发症。术后2 年随访时进行CT 三维重建确认椎体融合情况。
1.4 统计学方法
采用R 语言(3.61版)进行统计学分析,计量资料以均数值±标准差表示,采用配对t检验进行比较,以P<0.05为差异有统计学意义。
2 结果
17 例全部获得2 年及以上随访,随访时间为24~67个月,平均(41.2±15.5)个月。典型病例见图1。
2.1 围手术期情况
手术时间为100~150 min,平均(124±20)min;失血量为200~1500 ml,平均(410±204)ml;术后住院时间为7~16 d,平均(9.1±4.1)d。术中出血主要来自切除关节突关节及切除钙化椎间盘时的节段血管分支及硬膜外静脉丛出血。
4 例患者出现术后并发症:1 例术后即刻查体双下肢肌力0 级(考虑原因为同时合并相同节段的OLF,且骨化块沿椎管侧方与前方钙化椎间盘相连接,在切除椎管后壁时超声骨刀未能将位于椎管侧壁的骨化块完全切断,在掀起椎管后壁时带起部分钙化椎间盘,对硬膜囊产生较大刺激),术后立即给予甲强龙冲击治疗[11],术后次日患者下肢肌力恢复至术前状态,至末次随访时已完全恢复。2 例出现硬膜损伤、脑脊液漏(其中1 例为合并OLF,在掀起椎管后壁时出现硬膜撕裂,硬膜大片缺损而无法修补;另1 例为分离钙化椎间盘与硬膜囊黏连时损伤,损伤位于硬膜囊腹侧,亦未行修补),均采取术中紧密缝合深筋膜,术后平卧处理,必要时给予头低脚高位,并充分补充含钠液体避免电解质失衡,未出现切口感染或假性脑脊液囊肿。1 例为术后次日出现突发意识障碍,经急诊CT 证实为急性颅内出血,随即由神经外科急诊开颅减压,但术后神经功能依然很差。17 例患者均未出现手术切口感染及肺部相关并发症。
2.2 神经功能评价结果
17 例患者均完成术后3 个月、6 个月、1 年和2 年的门诊随访。术前及术后3 个月、6 个月、1 年、2 年随访时的mJOA 评分分别为(5.6±3.1)分、(9.0±2.6)分、(9.2±3.1)分、(9.2±3.2)分和(9.6±2.5)分(图2)。与术前相比,术后随访的mJOA 均明显提高,差异均有统计学意义(P<0.01),术后2年随访时的mJOA 改善率为74.1%。其中1 例术后并发脑出血,虽经积极康复锻炼,但术后神经功能仍不佳,末次随访时的mJOA仅为2.5 分,mJOA 改善率<0,其余16 例的mJOA 改善率均在优良水平(>50%)。
2.3 融合率
术后2 年随访时的CT 三维重建显示,17 例全部获得椎间融合,融合率为100%,未观察到内植物断裂或移位。
3 讨论
CTLDH 是一种相对少见的疾病,文献报告较少,多与后纵韧带骨化(ossification of posterior longitudinal ligament,OPLL)及椎间盘软突出等合并报告[12-14]。与OPLL 类似,CTLDH 常与硬膜囊黏连,在手术操作过程中容易损伤硬膜囊。早期文献报告多采用前方入路,可直接切除钙化椎间盘,达到直接减压效果,且不损伤后方结构,无需联合融合手术。但前方入路解剖结构复杂,手术难度高,手术并发症多。后入路经关节突关节脊髓环形减压术治疗脊髓前方压迫已广泛开展,主要技术难点在于腹侧致压物切除困难。Qi 等[15]、Liu 等[10]均报道应用环形减压治疗OPLL及CTLDH的良好效果,但上述研究均采用高速磨钻或骨刀等完成,手术时间长、术中出血量多。Liu 等[10]报道环形减压治疗CTLDH 的平均手术时间为185 min,术中平均失血量为895 ml。与之相比,本研究的平均手术时间和术中失血量明显减少。
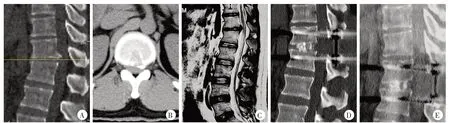
图1 患者,男,35岁,诊断为T12-L1节段CTLDH,行后路经关节突关节脊髓环形减压术
3.1 超声骨刀的技术优势
超声骨刀即“超声骨动力系统”,可实现电能和机械能的转换,通过每秒数十万次的高频率机械振动所产生的加速度破坏骨组织,同时利用刀尖的小振幅保护软组织。在切除骨组织时具有独特的优势,即“吃硬不吃软”,可有效降低在椎管减压操作中对软组织,如脊髓硬膜的损伤。既往胸椎减压手术多采用骨刀和高速磨钻进行切骨操作。骨刀震动较大,脊髓震荡风险高,现已基本不采用;高速磨钻通过磨头的高速旋转达到骨切削效果,切骨效果高,无明显震荡,是胸椎手术最常用的切骨工具,但存在局部温度高,骨碎屑较多,易导致软组织卷刮等缺陷。与之相比,超声骨刀在兼具切骨效率与基本无振动的优势同时,对软组织无卷刮,可紧贴脊髓进行切骨操作,这在进行脊髓前方致压物切除时尤为重要。应用超声骨刀切骨的另一优势即切缘出血少,因刀头工作时局部温度较高[16],可起到边切骨边止血的效果。本研究使用的超声骨刀系统配有即时冷却液喷洒装置,可避免局部温度长时间过高导致的周围组织损伤。
3.2 应用超声骨刀进行经关节胸脊髓环形减压术的技术要点
后路经关节突关节脊髓环形减压术中,超声骨刀主要应用于三处:切除椎管后壁、切除关节突关节及切除钙化椎间盘。椎管后壁切除范围为两侧至关节突关节中线,此处为椎管外侧壁,即使超声骨刀刀头切断全层椎板也不会损伤深处硬膜囊。上下边界为两侧椎弓根钉连线,此处远离椎管狭窄区域,椎管内空间更大,即使刀头深入也有一定的缓冲空间。在进行椎管后壁切除时需避免操作过于粗暴和直接将刀头深入椎管而导致脊髓的物理切割。此外,刀头局部温度过高也可能导致脊髓烧灼。切除剩余关节突时直接于下关节突根部横断后即可完整切除,注意避免刀头过深损伤下方出口神经根。
切除脊髓前方钙化椎间盘是关键操作步骤。胸段脊髓非常脆弱,对于牵拉或震荡等物理刺激的耐受性差,整个操作过程中应避免牵拉脊髓,也应避免使用骨刀敲击,而高速磨钻存在卷刮硬膜囊的风险,因而骨性致压物的切除面临巨大困难。本研究的经验:首先切除侧方椎间盘并向前尽量切除前方椎间盘,扩大前方椎间隙直至两侧贯通。然后在“安全三角区[8]”(被钙化椎间盘顶起的硬膜囊及椎体后缘围成的一个潜在三角形区域)的上下缘以超声骨刀切除钙化椎间盘的上下缘。两侧贯通后,钙化椎间盘已游离,将其轻轻下压至椎间隙深处即可完成切除。但钙化椎间盘常与硬膜囊存在黏连,需仔细分离后下压,绝对避免存在黏连时直接下压椎间盘,以免造成过度脊髓牵拉刺激导致脊髓损害。硬膜囊黏连严重至直接分离困难时,可以采用超声骨刀将其切薄,分块下压至椎间隙后切除,两侧轮流操作,直至完整切除。Chen 等[12]介绍了称为“Ⅳ+Ⅴ+Ⅵ”方法切除脊髓前方致压物告,亦是通过程序方法顺序切断致压物的头尾端并下压至深部椎间隙实现致压物切除。
3.3 并发症分析
本研究中出现1例一过性脊髓功能损害,术中存在较为明显的硬膜囊刺激,考虑为主要原因。Hu等[17]报道行环形减压术治疗OPLL 病例,术后一过性脊髓功能损害发生率为34.6%(9/26)。本研究中出现2 例脑脊液漏,考虑原因包括均为单节段CTLDH,硬膜黏连不重,同时超声骨刀的应用也简化了钙化椎间盘的切除难度。脑脊液漏是胸椎管狭窄减压术最常见的并发症,既往研究的发生率可达30%[18]。本研究中出现1例脑出血,经神经外科急诊开颅减压治疗效果不佳。脑出血非胸椎环形减压术的特异性并发症,患者既往无高血压等脑出血高危因素,术前检查也无异常发现,考虑可能为脑血管畸形,术中血压变化较大所致。
考虑到胸腰段的解剖特点,后方结构及双侧关节突关节均已切除,局部稳定性已破坏,与大多数研究报告一样[19,20],本研究中患者均采取椎间植骨融合,如椎间隙高度正常,则行椎间植入自体碎骨后打入椎间融合器;如椎间隙已很狭窄,则仅植入自体碎骨。术后2 年随访进行CT 三维重建,17 例患者均获得坚固融合。
3.4 本研究的不足之处
本研究的局限:①回顾性研究,可能存在选择性偏倚;②样本量较少,因CTLDH 为相对少见的疾病,故病例选择有限;③未设置对照组,因既往所采用的高速磨钻及骨刀已很少应用,故本研究仅与此前已发表的部分文献进行了比较。有待前瞻性的大样本对照研究进行更为深入的临床研究。
综上,采用超声骨刀行经关节突关节脊髓环形减压术治疗CTLDH 可提高手术效率和安全性,且不增加并发症发生率,值得临床推广。
