髓细胞触发受体2对大鼠颅脑创伤后认知功能障碍的影响
2021-05-18孙中磊刘英富
赵 莉,孙中磊,杨 齐,刘英富,张 赛,3
(1.中国人民武装警察部队特色医学中心,天津,300162;2.山东省枣庄矿业集团中心医院,山东 枣庄,277000; 3.天津市神经创伤修复重点实验室,天津,300162; 4.沧州医学高等专科学校纳米抗体研究所,河北 沧州,061001)
创伤后认知功能障碍是一种进行性和致命性的神经退行性疾病,因其渐进性的记忆丧失、认知困难和思想意识损害,严重影响患者日常活动[1-2]。神经病理学的特征包括细胞内高磷酸化的tau聚集和细胞外β-淀粉样斑块形成,与阿尔茨海默病(AD)先天免疫的激活、突触功能障碍和神经元丢失相一致[3]。髓样细胞2(TREM2)是一种免疫球蛋白(Ig)超家族受体,其表达增加对中枢神经系统(CNS)具有保护作用,主要表现为对小胶质细胞高度特异性,且已经在各种鼠模型中进行了研究[4]。神经元自噬已被证实在神经退行性疾病中有助于清除错误折叠的蛋白和减少炎症细胞因子[5]。目前,关于小胶质细胞自噬作用机制的研究仍较少。研究[6]表明,小胶质细胞自噬有助于β淀粉样蛋白(Aβ)的清除,抑制炎性小体3(NLRP3)的激活,改善认知功能障碍。已有研究[7]表明TREM2影响小鼠的小胶质细胞表型和激活状态,但TREM2相关的小胶质细胞自噬对大鼠颅脑创伤(TBI)后认知功能作用机制尚未阐明。本研究通过建立过表达TREM2大鼠TBI模型,探讨TREM2相关的小胶质细胞自噬作用,以期为TBI后认知功能障碍寻找新的治疗方向,现报告如下。
1 材料与方法
1.1 实验材料
雄性SD大鼠24只,28~32月龄,体质量600~700 g(军事医学科学院)。所有动物实验程序均按照医院批准的动物规程和指南进行。抗体 Aβ1-42、tau、TREM2、LC3-Ⅱ/Ⅰ、P62、β-actin(美国Abcam公司),AAVrh.10 TREM2和AAVrh.10Null(济南思科生物科技有限公司)。SYBR Green实时PCR预混试剂盒购自上海联迈生物工程有限公司。
1.2 实验方法
1.2.1 TBI模型与分组:大鼠TBI模型采用皮质撞击致伤法建立[8],术前8 h禁食禁饮,2%异氟烷吸入麻醉后备皮,沿矢状缝切开皮肤,剥离骨膜,在前囟右后外侧3 mm处行颅钻钻孔(直径约4 mm),显露硬脑膜,俯卧位固定于立体定向仪上,将eCCI打击臂调整至与垂直方向呈20°角,使用3 mm打击帽精确打击大脑皮层。打击参数为(AP为-2.5 mm,R为2.5 mm,H为3 mm),打击速率均为5 m/s,打击最低点持续时间均为200 ms。试验过程中,大鼠均未出现需安乐死的严重并发症。
将24只大鼠随机分为sham组(假手术)、TBI组和TBI并TREM2组(TREM2过表达),每组8只。其中TBI组和TBI并TERM2组采用皮质打击构建大鼠TBI模型,sham组仅开骨窗;TREM2过表达模型采用腺病毒相关病毒(AAVrh.10)AAVrh.10 TREM2脑室注射构建,sham组和TBI组注射等量AAVrh.10衣壳AAVrh.10Null。实验28 d,采用Morris水迷宫实验评估各组大鼠学习记忆功能,取脑组织,采用免疫印迹法(Western blot)评估TREM2和认知相关蛋白表达水平,Western blot法和免疫荧光评估自噬蛋白表达水平。
1.2.2 慢病毒载体治疗:将小鼠麻醉并固定在立体定位框架上,以前囟为坐标原点,将慢病毒载体注射到右侧脑室(立体定位坐标:向外1.7 mm,向后1.2 mm,硬脑膜下方3.0 mm,中线附近1.0 mm,前囟后0.2 mm,颅骨以下3.0 mm),将33号针头的Hamilton 710系列注射器(1~5 μL)固定在立体定向仪的注射泵上,针头缓慢进入目标结构,停留1 min,向双侧脑室分别注射载体(每个部位2 μL,速度0.5 μL/min),注射后,针头停留2 min以减少回流,然后缓慢撤回。注射后,缝合皮肤,观察小鼠麻醉恢复及神经系统并发症情况。
1.2.3 Morris水迷宫实验:实验第24~28天,通过Morris水迷宫实验观察大鼠学习记忆功能。水迷宫直径150 cm,高60 cm,放满水,通过添加脱脂奶粉使其不透明,控制水温25 ℃左右。在第一象限水面下1 cm设置平台。将小鼠分别从水池4个象限放入水池中,开始计时,观察并记录小鼠从不同象限放入后找到平台的时间,即逃避潜伏期时间。
1.2.4 Western blot实验:将左半脑组织破碎后,使用RIPA缓冲液从脑组织中收集蛋白质,BCA法测定蛋白总浓度,使用十二烷基硫酸钠聚丙烯酰胺凝胶电泳后,半干转移至聚偏二氟乙烯膜上。使用5%脱脂牛奶在室温下封闭膜2 h,然后在4 ℃下分别与一抗(TREM2、iNOS、Arg-1、Aβ1-42、tau和β-actin)孵育过夜。用洗膜缓冲液(TBST)洗涤后将膜与山羊抗兔二抗(1∶2 000)在室温下孵育1 h。使用增强的化学发光系统(ECL试剂盒)检测免疫反应性条带,并使用ImageJ 1.42q软件程序分析图像。
1.2.5 免疫荧光检测:采用4%多聚甲醛将右半脑组织固定48 h后,石蜡切片,切片在磷酸盐吐温缓冲液(PBST) (含0.1% Triton X-100/PBS) 中洗涤30 min,用5% 牛血清白蛋白(BSA)和10%正常驴血清阻断60 min。LC3-Ⅱ/DAPI荧光标记染色。切片首先与兔抗LC3-Ⅱ一抗孵育(1∶5 000),4 ℃过夜。随后用PBS冲洗切片并孵育二抗(与红色荧光团结合的驴抗兔IgG)(1∶1 000),室温孵育1 h。DAPI染色后使用hoechest33342染色。所有切片均在共聚焦显微镜下观察。通过计算扫描软件对阳性荧光个数进行量化。
1.3 统计学分析

2 结 果
2.1 TREM2过表达促进TBI大鼠小胶质细胞自噬
与sham组相比,TBI组大鼠脑组织TREM2表达水平升高,自噬标记物(LC3Ⅱ、LC3Ⅱ/LC3Ⅰ)表达水平升高,P62表达水平下降,差异均有统计学意义(P<0.05);与TBI组相比,TBI并TREM2组大鼠脑组织TREM2表达水平升高,自噬标记物(LC3Ⅱ、LC3Ⅱ/LC3Ⅰ)表达水平升高,P62表达水平下降,差异均有统计学意义(P<0.05)。见图1。
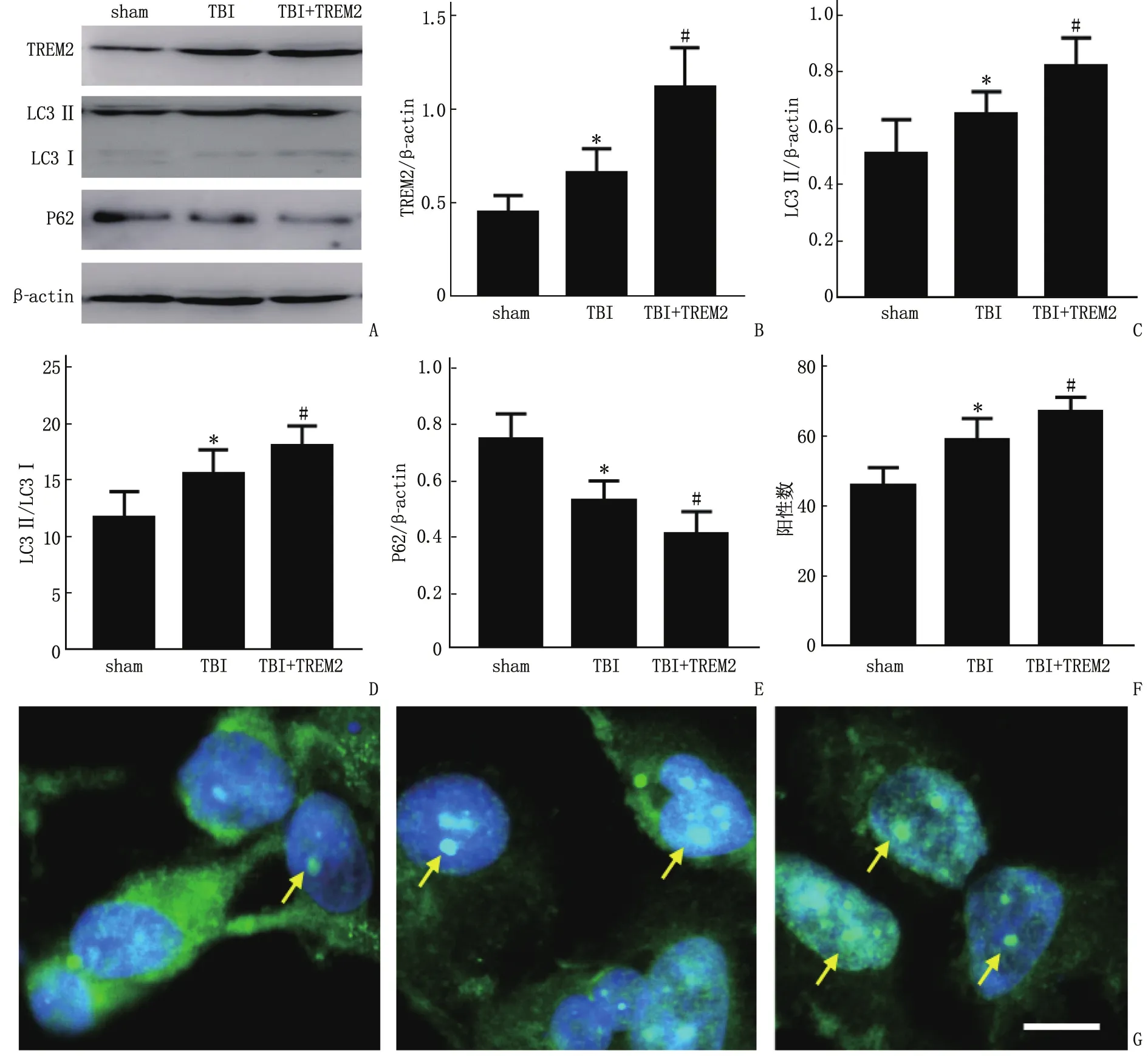
A:TREM2、LC3Ⅱ、LC3Ⅰ、P62免疫印迹条带;B:TREM2表达水平量化;C:LC3Ⅱ表达水平量化;D:LC3Ⅱ/LC3Ⅰ表达水平量化;E:P62表达水平量化;F:LC3Ⅱ免疫荧光阳性点斑数;G:LC3Ⅱ免疫荧光和hoechest33342染色(绿色荧光标记小胶质细胞,蓝色荧光标记细胞核,黄色箭头标记自噬小体阳性点斑,放大倍数50倍)。与sham组比较,*P<0.05;与TBI组比较,#P<0.05。
2.2 TREM2治疗改善了TBI大鼠学习记忆功能
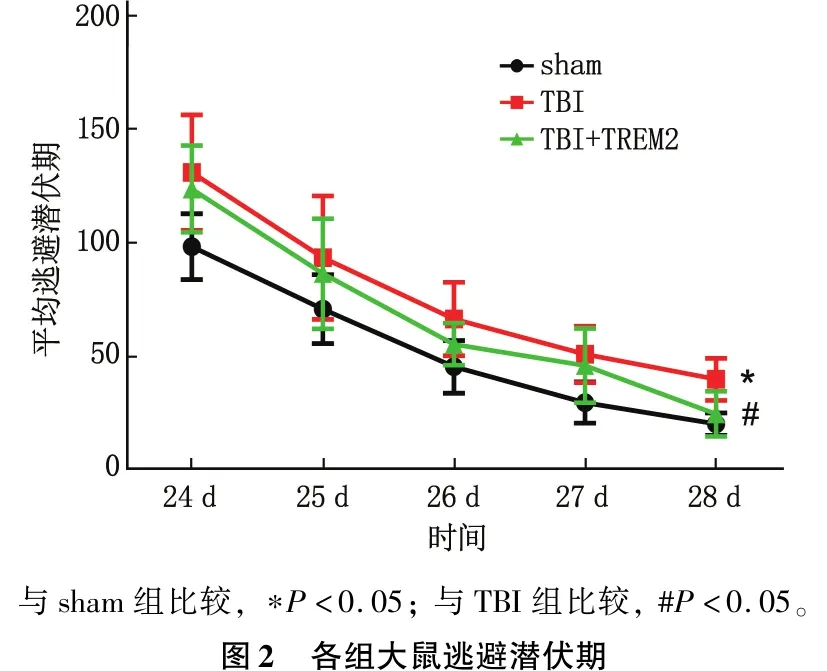
在第28天的定位航行实验中,与sham组相比,TBI组大鼠逃避潜伏期延长,差异有统计学意义(P<0.05);与TBI组相比,TBI并TREM2的逃避潜伏期缩短,差异有统计学意义(P<0.05)。见图2。
2.3 TREM2过表达减少TBI诱导的Aβ1-42、tau蛋白表达
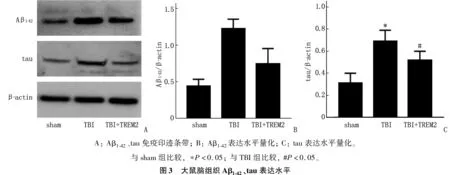
与sham组相比,TBI组Aβ1-42、tau蛋白水平升高,差异有统计学意义(P<0.05);与TBI组比,TBI并TREM2组Aβ1-42、tau蛋白水平下降,差异有统计学意义(P<0.05)。见图3。
3 讨 论
AD的神经免疫情况非常复杂,相关研究[9-10]表明神经胶质细胞(尤其是小胶质细胞)在疾病中起关键作用。AD的疾病风险主要为TREM2突变功能丧失,促进TREM2表达可能是治疗AD的有效方法[4]。研究[11]表明,在骨髓细胞中异位表达TREM2后,将其体内注射可以改善实验性自身免疫性脑脊髓炎。但直接的TREM2治疗会发生毒性作用,因此可增加其表达或蛋白质水平,使更多的TREM2可响应适当的内源性刺激,这可能是治疗AD和TBI后认知功能障碍的方法[12]。本研究结果表明,大鼠TBI后脑组织中TREM2表达增加,体内过表达TREM2 治疗后,TBI介导的tau、Aβ1-42表达显著减少,且认知功能评分显著提高,这说明促进适量的TREM2表达可有益于治疗TBI后认知功能障碍。人类遗传数据表明,TREM2在AD中发挥作用,但并未阐明在临床AD阶段激活TREM2和小胶质细胞是否有益。TREM2可能只在淀粉样蛋白积累的早期或预示着tau病理和神经元丧失的淀粉样蛋白积累早期,可增加小胶质细胞的活性,但一旦变性开始,此做法可能是有害的。因此,本研究选择在TBI后立即干预TREM2表达。
既往研究[4]表明,在TREM2缺陷型AD小鼠中,最一致的表型是明显缺乏小胶质细胞活化。当缺少TREM2时,淀粉样蛋白在AD小鼠模型诱导的小胶质细胞基因表达谱被高度静默[13]。此外,在小鼠脑中,与TREM2完整的小胶质细胞相比,TREM2沉默小胶质细胞,增加淀粉样斑块附近的细胞凋亡[14]。AD小鼠模型和AD患者的一个显著特征是小胶质细胞聚集在斑块周围,在神经元和Aβ之间提供保护性屏障,从而防止神经元营养不良[15]。小胶质细胞可通过TREM2依赖性机制控制淀粉样斑块的结构,并在斑块和相邻的神经纤维之间形成屏障。在小胶质细胞保护的区域,斑块周围营养不良轴突的形成减少了70%,这表明小胶质细胞和TREM2活性可减弱斑块环境的神经毒性[16-17]。
已知自噬与AD相关,沉默Beclin1基因可减少原代神经元自噬,并增加AD模型中的Aβ沉积[18]。雷帕霉素介导的mTOR抑制可导致海马Aβ42水平降低,并能通过增加自噬来改善记忆缺陷[19]。上述研究表明神经元自噬在AD进展中起保护作用。本研究表明,TREM2过表达促进神经细胞自噬,与相关研究结果一致。本研究采用免疫荧光标记小胶质细胞,结果表明TREM2过表达也可促进TBI后小胶质细胞自噬反应。但有研究[7]表明,TREM2在减弱小胶质细胞自噬中发挥作用,TREM2抑制的小胶质细胞含有更多的自噬囊泡。TREM2缺陷型小胶质细胞自噬增加是由于小胶质细胞试图用自噬作为生存机制补偿mTOR缺陷。从TREM2沉默小鼠中发现,小胶质细胞的mTOR信号转导受损,TREM2维持小胶质细胞处于高代谢状态是通过增强mTOR途径激活[20]。研究[21]表明,小胶质细胞通过清除髓鞘和细胞碎片等神经元源性成分来维持大脑稳态,保护神经功能。研究[22]提出,大鼠TBI后,靶向小胶质细胞自噬可能为治疗脑外伤的一种策略。
综上所述,TREM2过表达可能通过调节小胶质细胞自噬来改善TBI后认知功能障碍。
