抗幽门螺杆菌的用药研究进展
2021-05-18周杨朱俊博李向阳
周杨,朱俊博,李向阳,2
(1.青海大学医学院,青海 西宁 810001;2.三江源生态与高原农牧业国家重点实验室,青海 西宁 810016)
幽门螺杆菌(Helicobacterpylori,Hp) 是一种微需氧性、螺旋状的革兰阴性杆菌。1983年,澳大利亚学者Marshall 和Warren首次从人体的胃黏膜活体标本中将其分离出来,是至今被人类发现的唯一的胃部细菌。Hp可以通过黏附素在胃黏膜上黏附与定植,侵入人体的防御系统,利用本身毒素的直接作用以及诱导炎症反应的间接作用从而造成胃炎等消化系统疾病以及缺血性心脑血管疾病、脑出血等非消化系统疾病[1]。更关键的是,Hp感染可触发Correa级联反应,使胃内病变由非萎缩性胃炎发展为萎缩性胃炎、肠上皮化生等,严重者进一步发展为胃癌。由于Hp具有不可自愈性和高危性等特征,所以Hp被国际癌症研究机构认为是 Ⅰ 类致癌原[2]。目前已知主要的传播途径是口-口、粪-口传播,从而呈现出家庭聚集性。虽然在不同地域、不同种族、不同饮食文化的患者的Hp感染情况各异,但是其在世界各国均有发生,而我国有50% 以上的感染人群,人数众多值得关注。与此同时,与我国高感染率格格不入的是,Hp的根除率却在逐年下降,因此进行抗Hp药物的研究则显得尤为重要。
1 抗Hp药物
1.1 抗生素 自从抗生素被发现以来,由于其高效的杀菌抑菌作用,被广泛应用于人类和动物疾病的预防和治疗中。随着医疗的发展,抗Hp的药物根除率却逐年下降,一是由于长期使用,Hp产生了耐药性,且耐药率会随着时间推移而增加[3];二是在胃部的酸性环境下,抗生素易分解破坏,无法达到有效浓度和作用强度。为了减少Hp对单一抗生素耐药性的出现,越来越多的抗生素投入使用,根据目前临床治疗情况,第五次全国幽门螺旋杆菌感染处理共识报告[4]推荐了6种抗生素用来进行抗Hp治疗,具体见表1。
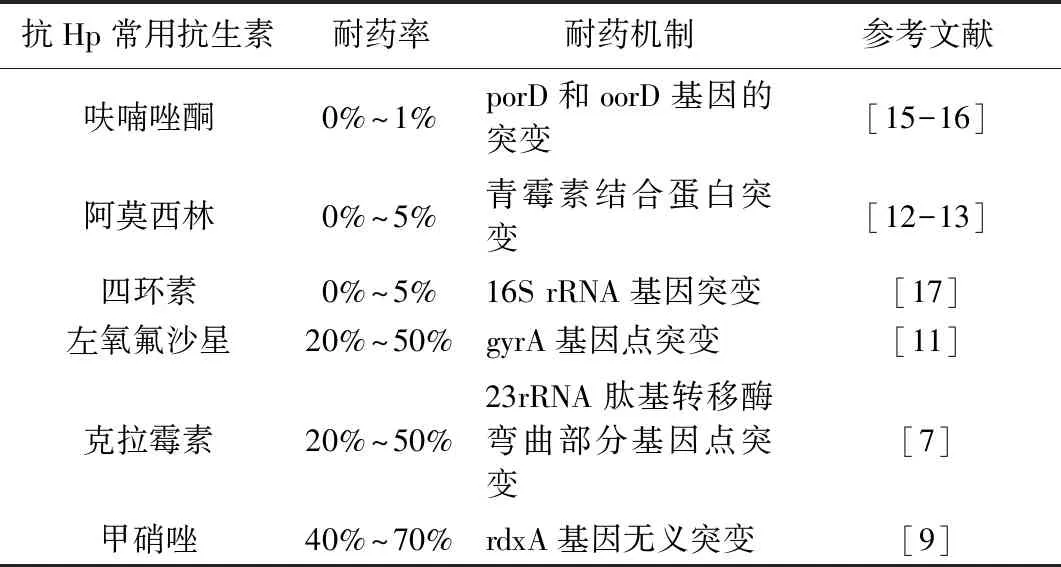
表1 抗Hp常用抗生素及其耐药性差异
1.1.1 高耐药率抗生素 克拉霉素为14 元环大环内酯类抗生素,主要是通过与细菌核糖体50S 亚基进行特异结合,从而使蛋白合成失败,最终达到抑制细菌繁殖的作用。克拉霉素作为红霉素的衍生物,对革兰阳性菌、革兰阴性球菌和厌氧菌均有疗效,其对Hp的抗菌强度是红霉素的8倍[5]。随着克拉霉素的广泛使用,报道出越来越多地区的患者均呈现较高的耐药率[6]。研究发现,克拉霉素耐药是由于Hp的23rRNA肽基转移酶的基因出现点突变,从而阻止克拉霉素与核糖体亚基结合。其中最常见的是A2143G (69.8%),其患病率在53%~95%之间,其次是A2142G (11.7%) 和A2142C (2.6%)[7]。铁丹丹等[8]的研究表明,Hp菌株的点突变位点呈现地区差异性,这极有可能与各地使用大环内酯类抗生素的习惯相关。
甲硝唑是硝基咪唑类抗生素,它通过硝基阴离子的形成破坏细菌DNA从而达到杀菌的目的。研究表明,甲硝唑耐药菌株存在rdxA基因无义突变,导致还原型烟酰胺腺嘌呤二核苷酸磷酸硝基还原酶表达缺失,从而产生耐药[9]。世界各地人群对甲硝唑耐药率差异较大,由于我国常将硝基咪唑抗生素用于各种类型的感染,如妇科、牙科和寄生虫相关的感染,这就导致甲硝唑在我国的耐药率居高不下[10]。
喹诺酮类药物左氧氟沙星是通过抑制细菌DNA复制从而达到杀菌作用,具有抗菌谱广、抗菌作用强、不良反应较轻的特点。虽然大多数幽门螺杆菌分离株最初对氟喹诺酮类药物敏感,但由于点突变的发生,Hp对氟喹诺酮类药物亦会产生不同程度的耐药,且呈现菌株差异性。在Hp中,氟喹诺酮类药物的耐药性主要是由编码氨基酸87、88、91和97的DNA旋转酶基因gyrA的点突变引起的,其中,gyrA基因第87和91密码子的突变最为常见[11]。
1.1.2 低耐药率抗生素 阿莫西林为半合成的广谱青霉素类抗生素,酸性条件下稳定。阿莫西林的抗菌活性主要来源于6-氨基青霉烷酸中的β-内酰胺环,它可专一性地与细菌内膜上靶位点结合,使细菌的细胞壁缺损,从而实现抗Hp的作用。目前大多数研究者认为青霉素结合蛋白(peniciuin binding proteins,PBPs) 突变是导致Hp对阿莫西林耐药的最主要原因,其中 PBP1的突变在Hp对阿莫西林的耐药中所起的作用最为重要[12-13]。Tseng等[14]的研究证实Hp对阿莫西林的高水平耐药与 β-内酰胺酶的合成有关。
呋喃唑酮属于人工合成的硝基呋喃类抗生素,为广谱抗菌药,对常见的革兰阳性菌和阴性菌都有抑制作用。呋喃唑酮可通过干扰细菌体内的氧化还原酶系统,使细菌代谢紊乱而产生抗菌作用。有研究表明,porD和oorD两基因的突变与呋喃唑酮的耐药有关[15-16]。近年来在某些克拉霉素高耐药地区,呋喃唑酮被越来越多地用于 Hp感染的一线治疗,同时也被我国指南推荐用于初次和补救治疗[4]。但与此同时,其不良反应也受到广泛关注。2018年7月国家药品监督管理局发布公告,对呋喃唑酮片说明书进行修改,将其适应证修改为“仅用于难以根除的幽门螺杆菌感染”;2019年2月,国家药品监督管理局再次发布公告,要求停止含呋喃唑酮复方制剂在我国的生产、销售和使用,并撤销药品批准证明文件。尽管呋喃唑酮单药制剂允许应用于幽门螺杆菌感染的治疗,但在临床上的使用却越来越谨慎。
四环素是一种抑菌性药物,主要通过与细菌核糖体30S亚基的16S rRNA相互作用,从而阻碍细菌蛋白质的合成。Hp对四环素耐药的主要机制与16S rRNA基因AGA926-928突变相关[17],且不同地区Hp对四环素耐药有所差异。
1.2 质子泵抑制剂(PPI) 在根除幽门螺杆菌治疗过程中,必须充分抑制胃酸分泌,以增加幽门螺杆菌对抗菌剂的敏感性和抗菌剂的稳定性。相关治疗药物主要包括胃酸中和剂、胃泌素受体拮抗剂、H2受体拮抗剂以及质子泵抑制剂等。PPI作用于胃酸分泌的最后步骤,能阻断各种因素引起的胃酸分泌,效果更稳定,作用也强于其他类型的抑酸剂。有研究表明,PPI疗效呈浓度依赖性,剂量越高,Hp根除率越高[18]。按照PPI竞争的位点不同,又分为K+拮抗型(可逆PPI)和ATP拮抗型(不可逆PPI)两种,具体分类如表2所示。

表2 质子泵抑制剂的分类
1.2.1 不可逆PPI 不可逆PPI主要是以苯并咪唑为母核的脂溶性化合物,经血液转运到胃壁细胞的分泌小管和泡腔内,与H+结合后在局部聚集,转为活性物质次磺酸与次磺酰胺,然后与H+-K+-ATP酶上的巯基结合并使酶失活,从而抑制胃酸分泌。目前全球内上市的不可逆PPI已有9种,而国内常用的一线用药有5种,按照临床使用进展分为第一代 PPI(奥美拉唑、兰索拉唑、泮托拉唑)以及第二代 PPI(埃索美拉唑和雷贝拉唑)。
PPI主要通过肝脏内细胞色素P450代谢的,代谢产物无活性。其中,奥美拉唑为外消旋药物,其左旋和右旋两个异构体的活性相近,但其代谢所需的酶不同,R型异构体主要是由CYP2C19酶代谢,因 CYP2C19表现基因多态性,所以个体用药差异较大。埃索美拉唑是奥美拉唑S型异构体,更多是由 CYP3A4 代谢。因此,埃索美拉唑起效快,生物利用度高,血药浓度持久,在消化道溃疡的治疗中具有较为明显的优势。崔艳玲[19]研究发现,在联合相同的抗生素和铋剂的条件下,以埃索美拉唑为主的四联方案治疗Hp性胃溃疡(GU) 的临床效果优于以奥美拉唑为主的四联方案。曾会等[20]研究得出,埃索美拉唑的四联用药治疗Hp性GU的临床效果优于兰索拉唑的四联用药。雷贝拉唑在肝脏的代谢不再由CYP450降解,而是由烟酰胺嘌呤二核苷酸磷酸(NADP)降解后形成雷贝拉唑硫醚后被排出体内,从而弥补了第一代药物的缺陷,效果稳定。相比于其他PPI而言,雷贝拉唑夜间抑酸作用强,可长时间使胃酸pH 值维持在大于3的状态下,为抗生素根治Hp 提供了一个优越的弱酸环境[21]。与此同时,雷贝拉唑具有较强的抗Hp活性,其能够在几个位点直接对Hp进行攻击,非竞争性且不可逆地抑制Hp的脲酶,从而发挥作用。
1.2.2 可逆PPI 由于不可逆PPI的局限性,具有不同作用机制、药动学性质更好的可逆性PPI(RPPI),即钾离子竞争性酸阻滞剂(potassium-competitive acid blocker,P-CAB)成了新的研究热点。与不可逆PPI相比,RPPI通过可逆性、竞争性地抑制H+-K+-ATP酶的K+结合位点起作用,不需要质子化,起效快,作用持久。目前已上市的沃诺拉赞(Vonoprazan)[22]和瑞伐拉赞(Revaprazan)。沃诺拉赞作为一种新型的钾竞争性酸阻滞剂,CYP2C19基因多态性不影响其药代动力学特征。据报道,含有沃诺拉赞的标准三联疗法可提供高于90% 的根除率,归因于有效的胃酸抑制和维持较高的胃液pH值,而且无论年龄大小都有很高的安全性[23-24]。根据18年的一项荟萃分析表明,在对照试验中,基于沃诺拉赞的疗法和基于不可逆PPI的疗法的根除率没有显著差异,但在克拉霉素耐药菌株中,基于沃诺拉赞的疗法的根除率却是后者的两倍以上[25]。然而,自从沃诺拉赞于2015年在日本开发并推出使用后,仅在部分国家和地区被批准使用,目前使用并不广泛。
1.3 铋剂 铋剂是一种黏膜保护剂,距今为止已经使用了300多年,为了避免早期铋剂所带来的神经毒性,现在使用的是较新形式的铋,主要是枸橼酸铋钾、碱性硝酸铋、次水杨酸铋、雷尼替丁枸橼酸铋和枸橼酸铋钾等。铋剂能抑制Hp所产生的蛋白酶、尿激酶和磷脂酶而起直接作用。酶抑制、铋与热休克和富含组氨酸蛋白的结合以及诱导的反应性氧化应激可能是铋抗Hp的主要分子机制[26]。与此同时,它在酸性环境下产生沉淀,形成弥散性的保护层覆盖于溃疡面上,可以有效地隔断胃蛋白酶、胃酸等对胃黏膜的侵蚀,保护胃黏膜。目前,铋剂在抗Hp上,主要与抗生素药物共用可以达到更好的效果。有学者通过随机双盲实验研究发现,作为三联疗法的一部分,铋剂疗法根除Hp的疗效与吸收无关。因此,应鼓励使用有效但吸收不良的铋制剂进行基于铋的根除治疗。一项研究发现,低浓度的铋剂(<10 μg·mL-1) 对Hp的生长有促进作用,而在较高的药物浓度下,Hp的生长才会收到抑制,当浓度大于40 μg·mL-1时,却又未观察到进一步的抑制作用,原因极有可能是铋剂一定程度上利用了病原菌内的铁转运途径[27]。近日我国一位学者针对铋剂与PPI 联用提出思考,认为其联用支持证据级别较低,缺乏药代及药效动力学数据[28],其于PPI联用所引起的药物相互作用值得进一步探究。
1.4 其他 除了抗生素、PPI和铋剂用于根治Hp之外,为了解决上述药物根治率降低、不良反应较高的现象,一线工作者也尝试更多的方案来达到更佳的疗效。中医主张“清热解毒”来祛除病因,从而抑制和杀灭Hp;利用理气和中、补脾益气等方法实现“治本”,从而促进胃黏膜愈合、止血,修复受损消化道功能,以期望根除疾病。多数实验表明,目前来说,清热解毒为中药主要作用,常用的中草药有大黄、蒲公英、黄连等。郭蒙蒙等[29]通过体外研究发现,草珊瑚浸膏对耐药性Hp菌株有明显的抑制作用,且与克拉霉素等抗生素在抗菌作用上具有协同作用。然而,中药制剂存在的成分复杂、作用不明确的缺点依然存在。其次,如何发掘中药能像西药抗生素那样在各人群、年龄阶段均能应用,亦是下一步亟须攻克的方向。
益生菌是一类对人体有益的活性微生物,常用的益生菌有卫乐舒益生菌、舒克幽益生菌、双歧杆菌等。益生菌能够缓解胃肠道症状,并防止Hp感染及肠道内细菌的过多生长,不仅能够改善消化系统内菌群数量,提高其活性能力,避免Hp堆积在胃黏膜上皮,而且能提高其对抗生素的敏感性,防止Hp造成的细胞凋亡[30]。根据分析报告,联合使用益生菌可显著降低如腹泻和恶心等不良反应,在对于幽门螺杆菌的根除效果上,各类分析均显示益生菌具有不同程度的加强效应[31-32]。但是也有学者发现在铋剂四联的基础上增加益生菌并不能提高治疗Hp的根治率[33],故具体的临床使用仍有待进一步研究。
2 联合用药方案
2.1 二联用药 二联用药,是指一种抑酸剂加一种抗生素,二者合用于治疗幽门螺杆菌感染的用药疗法,具有不良反应小、患者依从性好等优点。二十世纪八十年代使用常规剂量的二联方案根除Hp,但根除率普遍较低,逐渐被三联方案代替。二十一世纪初,二联治疗被重新采用,以用作抗Hp感染的二线、三线甚至四线治疗。最近研究发现高频率、大剂量、长疗程的抗生素和质子泵抑制剂联合用药,具有较高的根除率[23]。
阿莫西林在绝大多数国家耐药率较低,具有较高的应用价值,但是在体内酸性环境下,其抗菌活性会大大降低,故而与PPI联用能发挥更好的疗效。此外,由于PPI除了抑酸作用强之外,其本身还可直接透过黏液层与 Hp表层的尿素酶结合,使尿素酶活性变低,实现抗Hp作用,所以阿莫西林联合PPI的二联方案越来越受到关注,具体见表3。高采平等[34]研究发现大剂量阿莫西林和埃索美拉唑二联给药可作为安全、有效的Hp感染初次治疗方案。毕红燕等[35]通过体外抑菌实验得出,雷贝拉唑和阿莫西林对耐药菌株的联合抗菌作用比奥美拉唑和阿莫西林的联合抗菌作用强。Furuta等[36]发现,沃诺拉赞和阿莫西林二联疗法与沃诺拉赞、阿莫西林和克拉霉素三联疗法根除Hp的疗效相当。由此不难推测,目前与阿莫西林进行二联使用的PPI中,以雷贝拉唑为主的第二代PPI以及沃诺拉赞等可逆PPI均具有较好疗效。然而当患者出现青霉素过敏的情况时,可考虑用其他耐药率低、不良反应少的抗生素代替,如四环素、西他沙星等。
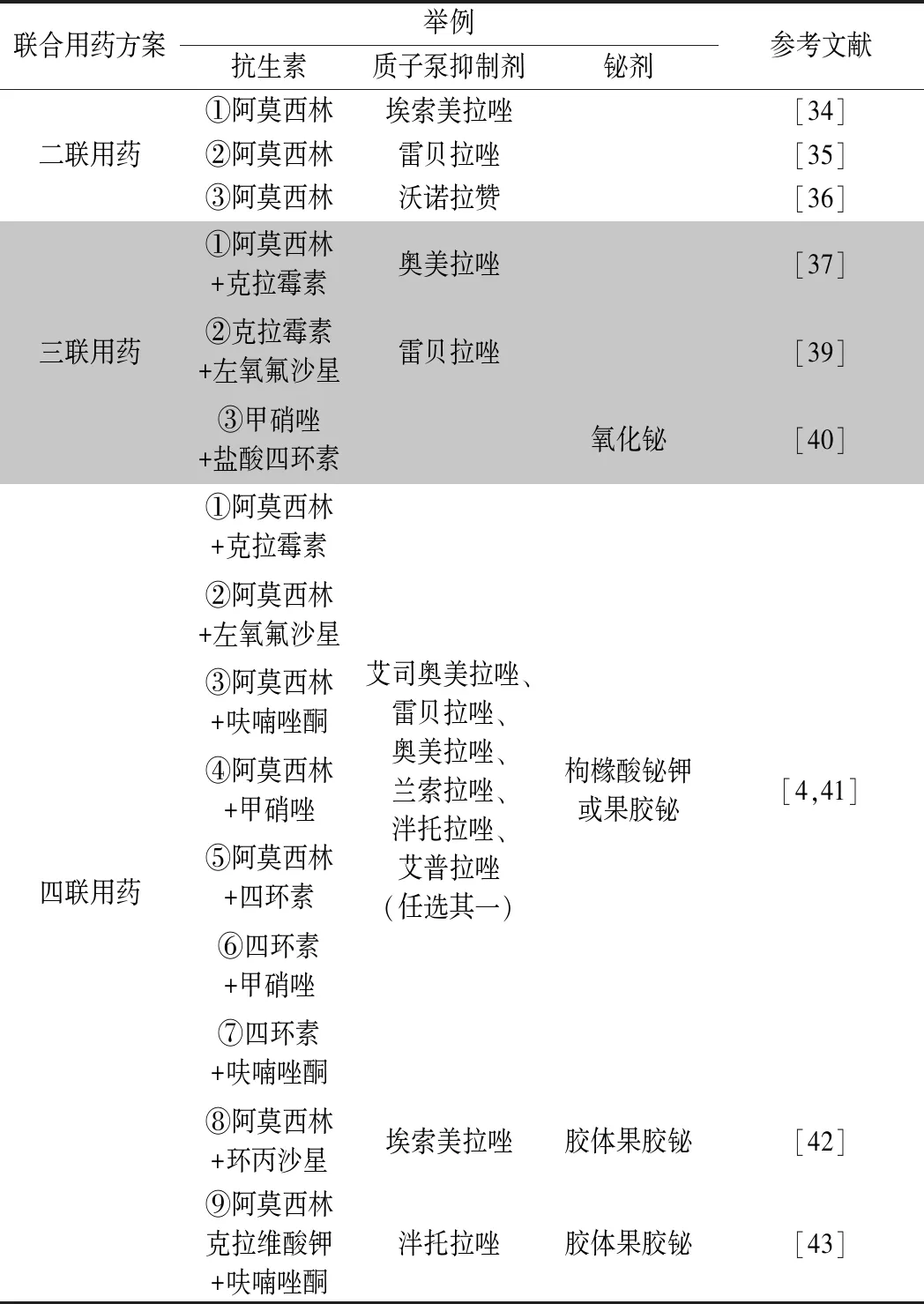
表3 抗Hp联合用药方案
2.2 三联用药 随着Hp对抗生素耐药性的日渐增加,标准二联疗法不能满足一线需要,于是三联疗法应运而生。标准三联疗法,又称质子泵抑制剂三联疗法。目前而言,在克拉霉素耐药性低于15%的地区,标准三联疗法是治疗幽门螺杆菌的标准方案,包括质子泵抑制剂、克拉霉素和甲硝唑或质子泵抑制剂、克拉霉素和阿莫西林。这两种方案的区别在于,当患者出现青霉素皮试过敏时,甲硝唑可替代阿莫西林,其疗效与阿莫西林疗效相当。而在克拉霉素高耐药地区,在未进行敏感性检测之前应摒弃含PPI及克拉霉素的三联疗法。一项临床研究表明[37],在奥美拉唑、阿莫西林联合用药的基础上,增加克拉霉素后,总疗效率从76.60%增大到93.62%,而不良反应率从12.76%降低到6.38%,故而在标准三联法中,一般都会选用克拉霉素。另一项研究显示[38],对于初次治疗的病例,PPI、阿莫西林和甲硝唑的组合在一项研究中表现出比PPI、阿莫西林和克拉霉素的组合明显更高的根除率。对于PPI的选择上,与二联疗法相似,选用雷贝拉唑为代表的二代PPI以及可逆PPI已成为主流。但目前幽门螺旋杆菌的耐药性逐渐增强,根除率逐渐下降。不少临床医生和研究者不再拘泥于标准三联法的使用,而是尝试改进 Hp感染的三联疗法。赵汝峰[39]研究发现,雷贝拉唑、克拉霉素、左氧氟沙星联合治疗 Hp所致相关性胃炎的亦有显著的效果。与此同时,除了以PPI为主的标准三联法之外,含铋剂的三联疗法以及益生菌三联疗法也被提出,复方枸橼酸铋钾片就相当于是一种三联的制剂,它是由甲硝唑125 mg、盐酸四环素125 mg和氧化铋40 mg组成的复方片。一项药动学实验发现[40],食物会导致该制剂生物利用度降低,但是Hp的根除率没有显著变化,这可能与铋剂、甲硝唑和四环素在胃中的滞留时间增加,从而延长了他们在胃黏膜中接触幽门螺杆菌的时间有关。
2.3 四联用药 四联疗法可分为铋剂四联以及非铋剂四联,具体见表3。其中经典铋剂四联是指用铋剂联合PPI及两种抗生素对Hp阳性的患者进行治疗的方案,此疗法的确立早于标准三联疗法,由于早期铋剂不良反应较高,故未广泛应用于临床治疗。近年来随着三联疗法根治率的逐渐降低,铋剂四联疗法重新受到重视。而最近的国际幽门螺杆菌感染管理指南建议,在克拉霉素或甲硝唑耐药较高的地区,铋剂或非铋剂四联疗法作为治疗幽门螺杆菌的一线方案[23]。在难治性消化性溃疡的治疗中,四联疗法抗Hp的显著效果。当然,对于铋剂四联的方案,临床上有较多的选择,经过我国研究拓展,就已经达到7种方案可供参考[4]。黎日杨[41]根据临床研究得出,四联疗法采用埃索美拉唑、阿莫西林、枸橼酸铋钾胶囊、克拉霉素联合治疗难治性消化性溃疡的效果显著,且能减少不良反应,降低复发,值得临床应用推广。顾勇等[42]研究发现以环丙沙星为基础的新四联疗法(埃索美拉唑+胶体果胶铋+阿莫西林+环丙沙星),其疗效均优于标准四联疗法组(埃索美拉唑+胶体果胶铋+阿莫西林+克拉霉素);武绍梅等[43]应用的泮托拉唑、阿莫西林克拉维酸钾、呋喃唑酮和胶体果胶铋组成的四联法,抗Hp有效率达到97%,并且未出现严重的不良反应。虽然含有呋喃唑酮的四联方案具有较高的根治率,但是由于国家对其适应证的修改,临床使用仍处于谨慎的态度。当然,联合用药并不意味着抗生素使用种类越多,根治率越高。一项临床研究显示[44],含铋五联疗法由于其并不优于传统的疗法的疗效以及更高的副作用发生率而不被推荐。
非铋剂四联疗法是由 PPI+阿莫西林+克拉霉素+甲硝唑组成,分为序贯疗法、伴同疗法和混合疗法。这些方案的根除率普遍高于标准三联疗法,随着Hp对克拉霉素、甲硝唑耐药率,尤其是双重耐药率的上升,序贯疗法已被淘汰,混合疗法亦很少被推荐,目前伴同疗法被推荐作为一线方案。有学者研究发现,在克拉霉素高耐药地区,铋剂四联和非铋剂四联在Hp根除率和依从性方面没有差异,但非铋剂四联具有更高的安全性[45]。
3 药物相互作用
目前抗Hp单一用药已经无法满足临床需要,长期和广泛的使用各类联合用药方案则需要我们对其联用药物间的相互作用进行探究,从而为临床合理用药提供理论依据。而在联合用药方案中,无论是三联疗法还是四联疗法,PPI和抗生素总是作为重要角色,故而研究这两类药物与其他合用药物间的相互作用则显得尤为必要,具体见表4。

表4 抗Hp药物间相互作用
3.1 PPI对其他药物的影响 在根除药物中,PPI能抑制胃酸分泌,从而影响其他药物的吸收。比如奥美拉唑作为常用PPI,可产生显著的抑制酸分泌作用,使胃中pH值变高。四环素在碱性环境下,呈难溶性游离型四环素,不易吸收,从而血药浓度下降。有研究表明[46],奥美拉唑通过减少胃酸分泌降低甲硝唑的胃内浓度,增加阿莫西林的胃内浓度。Treiber等[47]通过一个随机安慰剂交叉对照试验,考察了奥美拉唑对铋剂药动学的影响,结果发现,奥美拉唑使铋的AUC增加,提示奥美拉唑可能通过升高胃内pH而增加了铋的吸收,临床应该谨慎合用。Spenard等[48]通过一个随机双交叉对照试验,考察了奥美拉唑对“三合一”胶囊(枸橼酸铋140 mg+甲硝唑125 mg+盐酸四环素125 mg)中铋的生物利用度的影响,得出了相同的结论。除了能够改变胃内pH值而影响其他药物的吸收外,PPI还可以通过药物代谢酶对药物相互作用产生影响。奥美拉唑、兰索拉唑、埃索美拉唑与经 CYP2C19 代谢的药物合用时易发生代谢性相互作用,从而延长联用药物的作用时间、增加疗效,合用需适当调整剂量。Ortiz等[49]研究发现,兰索拉唑降低了克拉霉素的生物利用度,且与幽门螺杆菌状态无关。奥美拉唑与阿莫西林有协同作用,可以提高清除Hp的疗效。但泮托拉唑具有独特的Ⅱ相代谢途径,雷贝拉唑主要通过非酶途径代谢,故而与药物代谢酶竞争少,减少了体内药物相互作用。
3.2 抗生素对其他药物的影响 抗生素对其他药物的相互作用在药物代谢方面表现尤其突出,主要是抗生素对肝药酶的诱导与抑制作用。有些抗生素可增加药酶的合成,如利福平、灰黄霉素等。有些抗生素则具有酶抑制作用,如磺胺药、大环内酯类药物、喹诺酮类、四环素类药物等。而我们特别需要注意的就是克拉霉素,克拉霉素是 CYP3A4、CYP2C19 等代谢酶的抑制剂,并影响这种酶底物的药代动力学,它可以抑制奥美拉唑代谢,升高血药浓度,增加疗效[50-51];影响兰索拉唑经CYP3A4代谢的过程[52];减慢埃索美拉唑的代谢,使其药时曲线下面积加倍[53],但不影响疗效;但对雷贝拉唑及泮托拉唑[51]的药动学无影响。四环素与铋剂间亦存在药物相互作用,水杨酸铋通过抑制胃肠道吸收而降低四环素的水平,故仅适用于两种药物的口服形式。同时,四环素类药物由于能和铋剂结合,生成难吸收的络合物,从而也会降低疗效。
4 展望
自从幽门螺杆菌被发现以来,近四十年内,国内外各个学者和临床医生对其进行大量研究。发现幽门螺杆菌是多种胃和肝胆疾病等胃外疾病的罪魁祸首,因其能通过口-口、粪-口等传播途径,使得全球有极其庞大的患者需要治疗。我国第五次全国幽门螺杆菌感染处理报告指出,对于幽门螺杆菌引起的胃内疾病,建议根除Hp以达到更佳的疗效。然而不尽人意的是,随着近年来人们对抗生素的滥用,像克拉霉素、甲硝唑等都出现了较高的耐药率,使得幽门螺杆菌的根治率逐年下降。寻找疗效更佳、根治率更高的治疗方案成为一线医务工作者的努力目标。于是,应运而生的是高剂量二联用药、三联用药乃至四联用药方案。然而,随着治疗药物的不断增多、剂量的不断增加、疗程的不断延长,Hp根治率依旧会逐年下降。所以,在寻找更加有效的治疗药物的同时,也亟须我们对目前行之有效的治疗方案进行探究与改进。
目前而言,根据我国共识推荐,在克拉霉素耐药率低于15% 的地区,选用标准三联法进行根除治疗,而对于耐药率较高地区,则推荐使用四联方案,以达到更佳的疗效。而我国许多地方均为高耐药地区,因此四联方案的使用在我国更有实际意义。铋剂四联方案经过我国研究拓展,已经达到7种方案,且被 Maastricht-5 共识和多伦多共识推荐。虽然铋剂四联已经在临床上运用成熟,但是仍然存在一些问题没有得到解决:①铋剂与PPI和抗生素联用后,PPI会加重铋剂在体内蓄积,严重时甚至会引发铋剂中毒,针对这种临床现在的解决方案目前尚未制定;②除了我国共识中推荐的枸橼酸铋钾的使用剂量外,其余铋剂,包括胶体次枸橼酸铋、次水杨酸铋、雷尼替丁枸橼酸铋等均缺少更科学准确的数据,且各个铋剂间的抗菌区别也有待更深入的研究;③铋剂的使用虽然作用于局部,能提高Hp的根治率,但是对其他3种药物在胃中的浓度、药效等会不会产生影响,同时,虽然高浓度铋剂入血会造成中毒现象,但是安全剂量的血铋浓度会不会对其他3种药的代谢产生影响犹未可知;④对于常规治疗中,是否加入益生菌证据不足,且争议较大,需要进一步研究阐述。
