石墨炔纳米材料的制备及在电化学能源中的应用
2021-05-17孙全虎黄长水
高 娟,孙全虎,2,黄长水,2
(1.中国科学院青岛生物能源与过程研究所,青岛266101;2.中国科学院大学,材料与光电研究中心,北京100049)
碳是人类接触最早的元素之一,新型碳结构的发现与合成对推动材料科学研究的发展具有重要意义. 尤其是在电化学能源领域方面的应用,碳材料不断受到越来越多的关注[1~5]. 碳的同素异形体,如石墨、碳纳米管、石墨烯及石墨炔(GDY)等,已被用做电极材料广泛应用于电化学能源领域[4,6~14].
与其它由sp2或sp3杂化碳结构组成的碳材料不同,石墨炔是由苯环(sp2碳)和炔键(sp碳)连接构成的二维平面结构材料. 石墨炔于2010年由Li等[15~17]在铜箔表面通过六炔基苯的原位交叉偶联反应首先制备得到. 由于石墨炔平面独特孔道结构和电子性质,金属离子在与石墨炔平面平行和垂直的方向上都能实现很好的扩散迁移[18~21]. 目前许多理论和实验研究已报道石墨炔均表现出优异的锂离子和钠离子储存能力[22~30]. 理论计算表明,石墨炔结构中碳碳三键的存在可以有效地锚定多种金属元素,实现对石墨炔进行掺杂,调节石墨炔的物理化学性质. 同时,制备不同纳米形貌和结构(如纳米墙、纳米片、纳米薄膜等)能够为石墨炔提供独特的分级和多孔结构:(1)组成中大量的大孔、中孔和微孔可以有效提高石墨炔的比表面积,同时提供了大量的活性位点;(2)独特的纳米结构能够有效减短离子传输距离,从而达到较高的功率密度;(3)改善了界面相容性,有利于电解液更好地浸润,降低了过电势,进一步提高材料的循环稳定性. 因此,石墨炔的纳米结构形貌优化可以进一步提高其电化学性能.
1 石墨炔结构
石墨炔结构中可以观察到4种环境结构的碳碳键:(1)苯环的Csp2-Csp2键;(2)相邻碳碳双键和碳碳三键之间的Csp2-Csp键;(3)Csp-Csp碳碳三键;(4)Csp-Csp单键连接相邻的碳碳键. 因为炔基单元和苯环之间的弱共轭,芳香键相对于典型值(约1.54和1.40 Å)(1 Å=0.1 nm)发生了一定的收缩,反映了sp和sp2杂化碳原子的杂化效应[31,32]. 通过分子动力学(MD)计算表明[33],增加一个乙炔键,晶格间距增加约2.66 Å,而从量子水平分析,则增加约2.58 Å. 这些结果表明,延长的乙炔键的加入不会导致较大的结构变化. 碳碳三键的存在导致石墨炔的结构灵活性大于石墨烯,从而提供了进一步形成弯曲结构的机会.
石墨炔材料独有的另一个特点是可以通过化学方法制备,便于调整和优化石墨炔材料的形貌. 目前,石墨炔的典型合成技术主要包括干法化学和湿法化学. 干法化学主要是在各种基底上通过气液固相沉积法等制备;而湿法化学中主要是在溶液中进行,如直接生长在铜片上,或通过液/液、气/液界面法得到. 通过制备方法的选择可以很好地控制石墨炔纳米形貌以及引入到石墨炔纳米结构中的杂原子或杂化结构的位置和数量,使得石墨炔纳米结构的优化成为可能,且更加便利.
石墨炔独特的结构和合成方法,使其可以通过反应条件优化、杂原子掺杂等手段获得不同形貌的石墨炔基纳米材料. 如通过反应条件的优化,制备石墨炔纳米墙[34,35]和石墨炔纳米片[36,37];通过杂原子掺杂,获得异原子掺杂石墨炔纳米颗粒[38,39]和柔性石墨炔纳米薄膜[27,30,40];通过复合杂化结构的构筑,获得石墨炔复合纳米线[41~43]、纳米花[44]和纳米立方体[45]材料等. 本文将重点介绍几种石墨炔基纳米材料的构筑及在电化学能源领域中的应用.
2 石墨炔基纳米结构在电化学能源领域中的应用
2010年,Li等[17]通过六乙基苯原位交叉偶联反应,在铜表面生成面积为3.61 cm2的大面积石墨炔薄膜,测得其电导率为2.516×10-4S/m. 随后,一系列基于石墨炔及石墨炔掺杂或杂化复合结构的不同形貌的纳米材料被广泛制备,并表现出优异的性能.
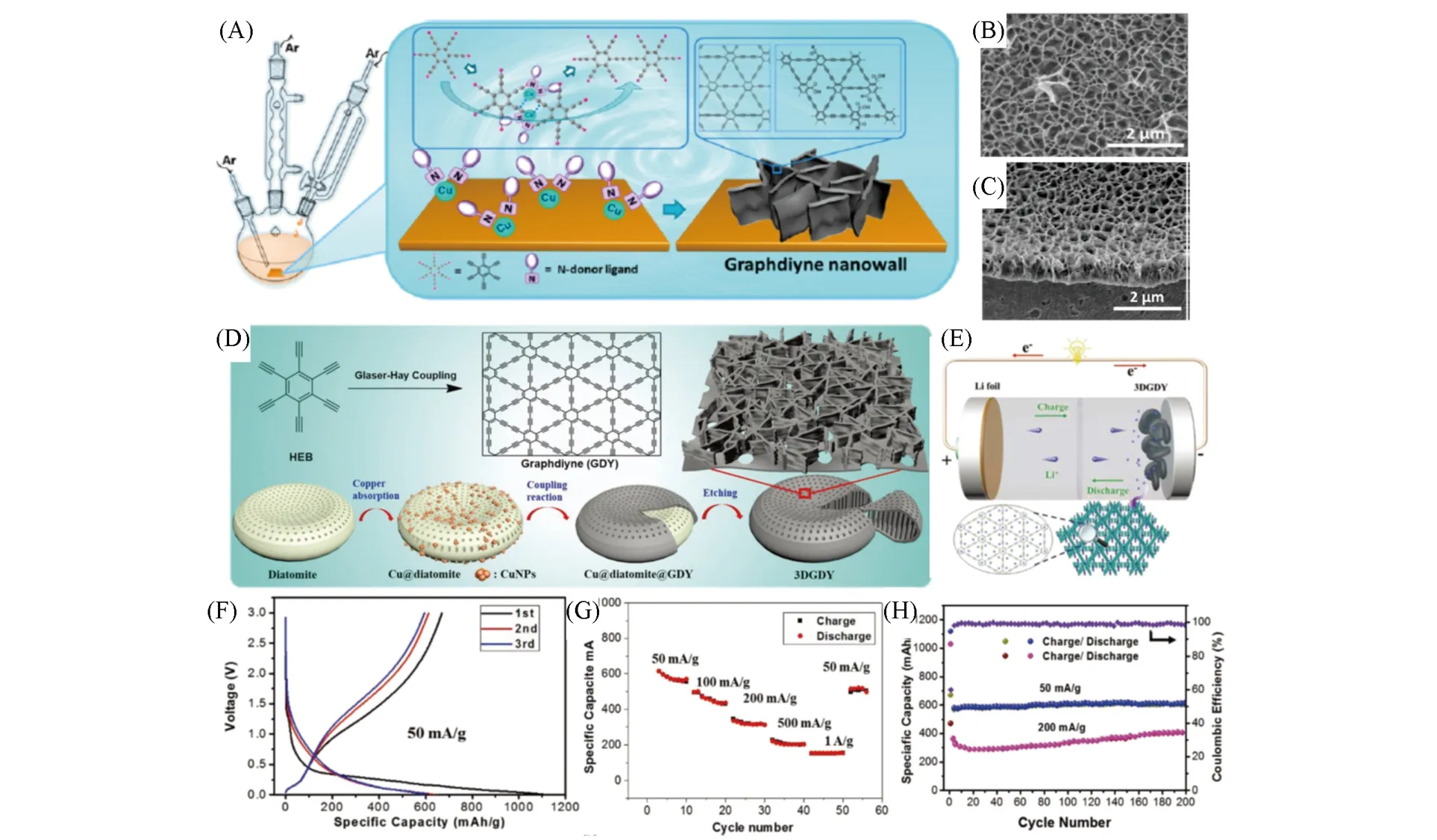
Fig.1 Schematic illustration of the experimental setup(A),top view(B)and cross-sectional view(C)of SEM images of graphdiyne nanowalls on Cu substrate[34],schematic illustration of the synthesis of 3DGDY using diatomite as template(D), schematic representation of an assembled 3DGDY-based LIB(E),charge/discharge profiles(F), rate performance(G) and cycle performance(H) at different current densities of the 3DGDY-based LIBs[35]
2.1 纳米墙
除了石墨炔纳米薄膜之外,Zhou 等[34]调节了Glaser-Hay 耦合反应的反应条件,以吡啶和少量的N,N,N,N-四甲基乙二胺及丙酮为溶液,用铜箔和六炔基苯制备了石墨炔纳米墙结构[图1(A)~(C)],表现出优于石墨烯纳米片的场发射性能,其场发射开启电场为6.6 V/μm,阈值电场为10.7 V/μm. 除铜箔外,Li等[35]还选取硅藻土作为铜离子催化剂的载体[图1(D)],制备出了具有纳米形貌的石墨炔粉体,并用作锂离子电池电极材料,由图1(F)可见,其初始库仑效率为57.4%,说明发生了不可逆反应,即在石墨炔高表面积上会形成大量稳定的固态电解质层(SEI),产生一个较大的不可逆能量损失. 但其特殊的多孔结构,为锂离子提供了储存位点,当电流密度为50 mA/g 时,其可逆容量为605 mA·h·g-1. 即使在1 A/g的高电流密度下,也能保持102 mA·h·g-1的稳定容量. 同时该材料也有着良好的的循环性能,在电流密度为50 mA/g时,200次循环后,其可逆容量依然可达610 mA·h·g-1[图1(E)~(H)]. 由硅藻土为模板合成的三维石墨炔具有独立的结构、高比表面积和电子导电性. 同时,非平面的多孔结构可以使石墨炔薄片避免受强范德华作用力和π-π作用而相互堆叠,同时由于大量孔隙的存在,提供了更多的锂离子储存位点和转移通道,提高了电化学性能.
石墨炔纳米墙结构中的多孔结构和高比表面积,使其能够被直接用作金属离子电池的电极材料,并提供了丰富的存储位点和通道,进而表现出优异的电化学储能性能. Wang 等[46]将生长在铜片基底上的石墨炔纳米墙(GDYNWs)材料直接应用于锂离子电池(LIBs)[图2(A~C)]. 在0.05 A/g的电流密度下,可逆比容量约为908 mA·h·g-1[图2(D)]. 由图2(D)可见,石墨炔纳米墙的初始库仑效率高达56.2%,归因于在第一次放电过程中,在电极表面形成了SEI膜,出现了不可逆能量损失,并在循环中逐渐消失,表明稳定SEI层的形成. 这在很大程度上是由于石墨炔的多孔纳米结构,较高比表面积,形成了大量的SEI 膜. 但同时由于GDY 分子平面上存在的缺陷可以为Li 原子提供额外的存储位点,所以,在1 A/g的电流密度下充放电循环1000次后,比容量仍可保持在526 mA·h·g-1.
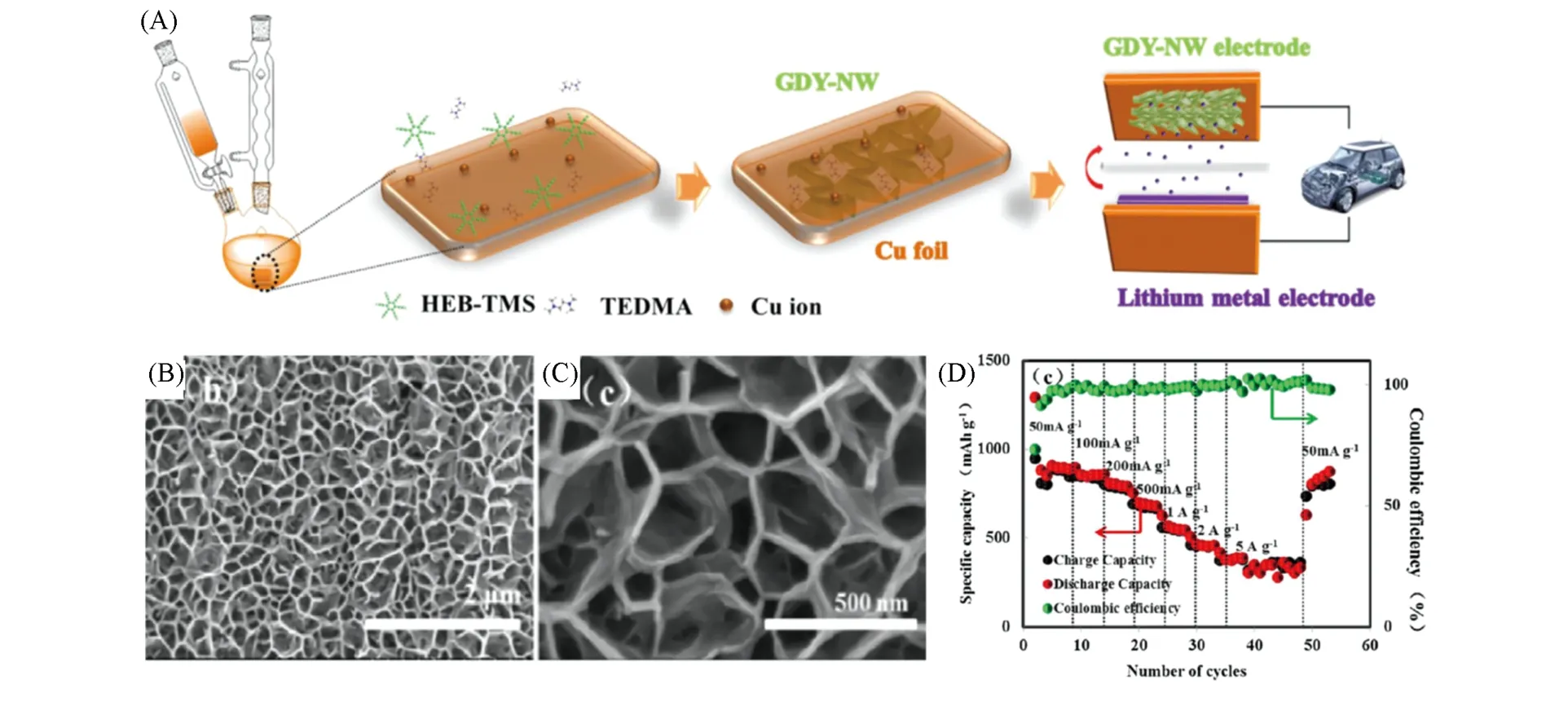
Fig.2 Schematic of synthesis of GDYNWs and LIBs based on GDYNW(A), top view SEM images(B, C) of GDYNW on Cu substrate, the rate performance of the GDYNW based electrodes for LIBs(D)[47]
2.2 纳米片
石墨炔纳米片结构通过调节分子内孔、三维互联孔结构和增加活性位点来促进金属离子快速扩散通道,从而极大地优化电极材料的能量存储能力.
Sakamoto和Nishihara等[47]首次报道了以六乙炔基苯为前体在液/液或气/液界面自下而上合成石墨炔晶体纳米片. 用乙酸铜分散在上层水层中,前驱体溶解于二氯甲烷下层,石墨炔纳米片在这两种液相界面之间逐渐长大. 在气液界面合成过程中,生成了具有单晶特征的规则六边形结构多层石墨炔纳米片,具有大约3 nm的厚度.
2018年,Shang等[36]探索了一种生长石墨炔纳米片的新方法,与铜箔为催化剂和基底不同的是,提出了以铜纳米线为催化剂,大规模制备高质量超薄石墨炔纳米片的方法[图3(A)~(E)]. 铜纳米线表面的晶界非常活泼,可为石墨炔的增长提供更多的反应位点. 通过这种方法制备的石墨炔纳米片的平均厚度为3.75 nm. 石墨炔纳米片结构表现出了1388 mA·h·g-1的高比容量,即使在较高的电流密度下,储锂性能仍然优越(10 A/g 时为870 mA·h·g-1,20 A/g 时为449.8 mA·h·g-1),且具有很强的稳定性[图3(F)~(I)]. 这种可弯曲的超轻石墨炔纳米片在铜晶体边界生长,嵌入的铜纳米粒子进一步增强了超薄层之间的电导率,可作为锂离子电池阳极. 由于其超薄特性,显示出类似石墨烯片的双面锂离子存储模型,展示出了可观的锂离子存储性能.
在此基础上,Shang 等[48]将铜纳米线和硅纳米粒子混合成溶液,在室温条件下原位制备石墨炔纳米片,此方法同时解决了硅阳极在循环过程中的界面接触和体积变化问题,有效提高了硅电极的电化学性能,在0.2 A/g 的电流密度下,电池容量可达4122 mA·h·g-1. 并且在2 A/g 的电流密度下,经过1450次循环仍可获得1503 mA·h·g-1的可逆容量.
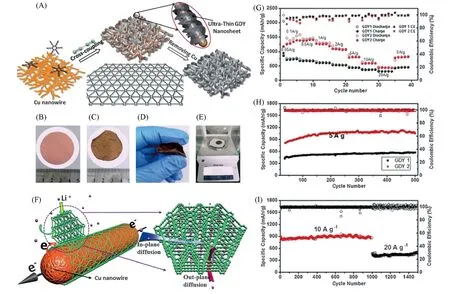
Fig.3 Representation of the synthesis of GDY on CuNW paper(A),photograph of CuNW paper before(B),after(C) growth of GDY, the bendability(D), weight(E) of the Cu@GDY paper, representation of a possible mechanism for the high rate performance(F),electrochemical performance of Cu@GDY paper(G)variations in specific capacity,long-term stability of GDY1 and GDY2 at 5 A/g(H)and GDY2 at 10 and 20 A/g(I)[36]
Wang等[49]在铜片表面制备3D结构石墨炔纳米片作为钠离子电池的阳极材料,同样实现了高功率性能和良好的循环性能. 通过调节分子内孔、三维互联孔结构和增加活性位点来促进钠离子快速扩散通道,从而极大地优化钠的存储能力. 在电流密度为0.05 A/g 时,钠离子电池的稳定可逆容量约为812 mA·h·g-1;在电流密度为1 A/g时,1000次循环后仍可保持超过405 mA·h·g-1的可逆容量.
2.3 纳米花状结构
2019年,Gao等[44]采用原位法成功地合成了石墨炔/二硫化钼杂化纳米花状结构[图4(A)和(B)].GDY与二硫化钼(MoS2)之间通过C—S键紧密接触,不仅有效地防止了结构分离问题,且提供了有效的电子传递途径. 导电GDY层不仅起到电子收集器的作用,还为MoS2提供了体积膨胀空间. 而花样结构中GDY与MoS2较大接触面积可极大缩短锂离子的扩散距离. 该复合材料表现出优异的锂离子存储性能,当电流密度为0.05 A/g 时,其比容量为1463 mA·h·g-1,是相同电流密度下纯MoS2纳米材料的2.5倍[图4(C)和(D)]. 并且有效地解决了二硫化钼的容量衰减问题.
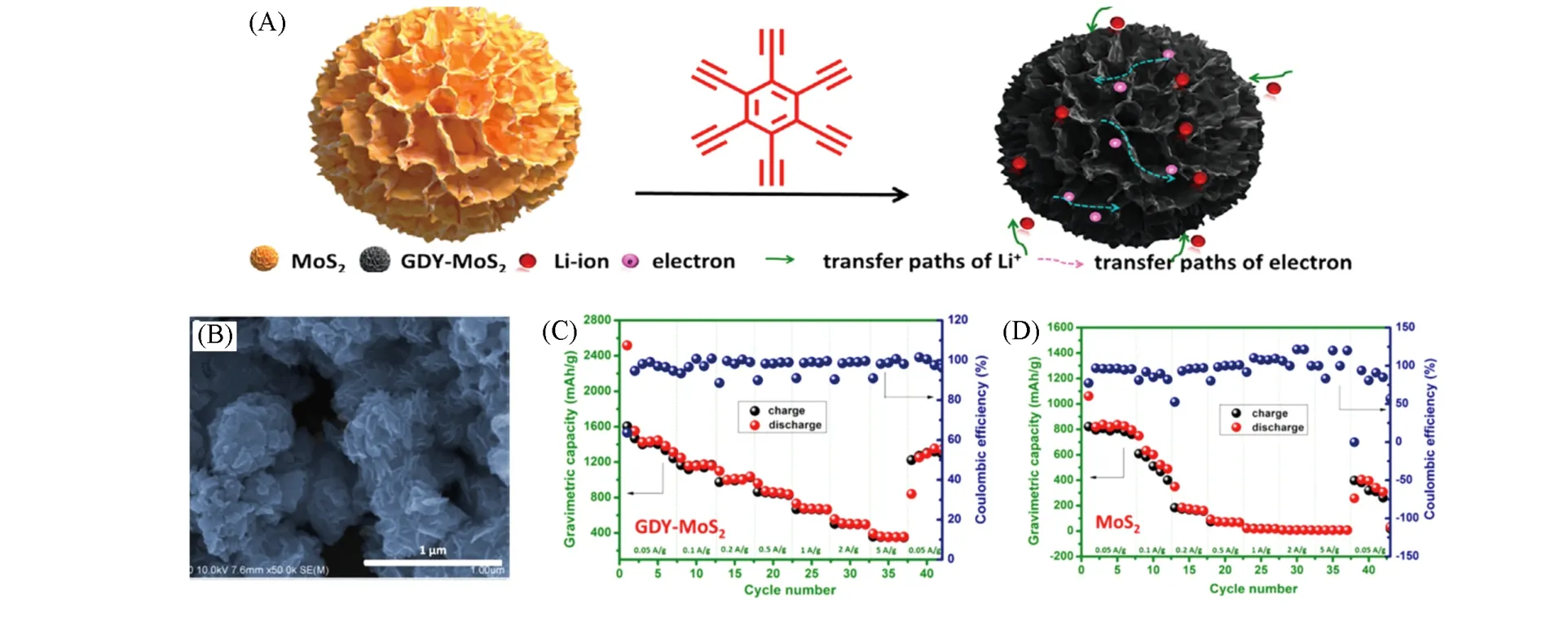
Fig.4 Synthetic procedure of GDY-MoS2 hybrid nanomaterial(A),SEM image of GDY-MoS2(B),rate capabilities of GDY-MoS2(C)and pure MoS2(D)[44]

Fig.5 Schematic illustration of the synthetic route of PyN-GDY(A),SEM image of PyN-GDY(B),RDE polarization curves in O2-saturated 0.1 mol/L KOH solution at a rotating speed of 1600 r/min with a scan rate of 5 mV/s(C)and schematic diagram for the process of ORR on PyN-GDY(D)[39]
2.4 纳米颗粒
纳米石墨炔材料也被用于电催化方面. Lv 等[39]合成了由离域π共轭吡啶氮组成的石墨炔材料(PyN-GDY),吡啶氮是该结构中唯一的含氮重复单位. SEM照片[图5(A)和(B)]表明PyN-GDY是由尺寸相近的纳米颗粒聚集而成,比表面积为689.7 m2/g,氮原子均匀分布在PyN-GDY 的微孔结构中,这有利于提高其在电化学氧还原反应(ORR)中的表面积和传质. 在碱性和酸性介质中均表现出优异的ORR 性能. 特别是在碱性条件下,PyN-GDY 的催化活性高于商业Pt/C,其起始电位(Eonset)、半波电位(E1/2vs. RHE)和极限电流密度(jL)分别为1.0 V,0.84 V和5.5 mA/cm2[图5(C)和(D)]. 密度泛函理论计算表明,吡啶氮是碳材料中提高ORR电催化性能的一种有效的氮掺杂形式. PyN-GDY结构中的氮原子均匀分布在尺寸相近的纳米颗粒的微孔结构中,同时该结构也提供了较高的比表面积,而理论研究亦表明最接近N 原子的乙炔碳原子是PyN-GDY 最可能的活性位点,进而使得该材料表现出优异的ORR性能.
Si 等[38]利用石墨炔中独特的乙炔键,以少量的铁前驱体制备了铁氮共掺杂石墨炔Fe-N-GDY[图6(A)]. 扫描电子显微镜照片[图6(B)~(D)]显示样品中存在大量的纳米颗粒. 通过调控Fe 掺杂量,1.5%Fe-N-GDY复合催化剂具有较好的氧还原催化性能,其相对于标准氢电极(RHE)的起始电位为0.94 V,极限电流密度为5.4 mA/cm2,塔菲尔斜率为89.1 mV/dec[图6(E)和(F)]. 该催化剂中应该有多种活性位点,氮是ORR上碳基催化剂掺杂最普遍、最有效的非金属元素. 在N掺杂的基础上,在催化剂中引入了Fe元素,提供了另一个活性位点Fe-Nx. Fe-N-GDY中另一个可能的活性位点是包裹铁的碳层(Fe@GDY),也可以提高其对ORR的催化活性. 另一方面,铁与GDY的强相互作用使催化剂在反应过程中更加稳定. 进而表现出良好的ORR性能. 此外,其在酸性和碱性电解质中均表现出良好的抗甲醇中毒性和稳定性,可以作为一种有前途的新型非贵金属催化剂取代铂基催化剂.
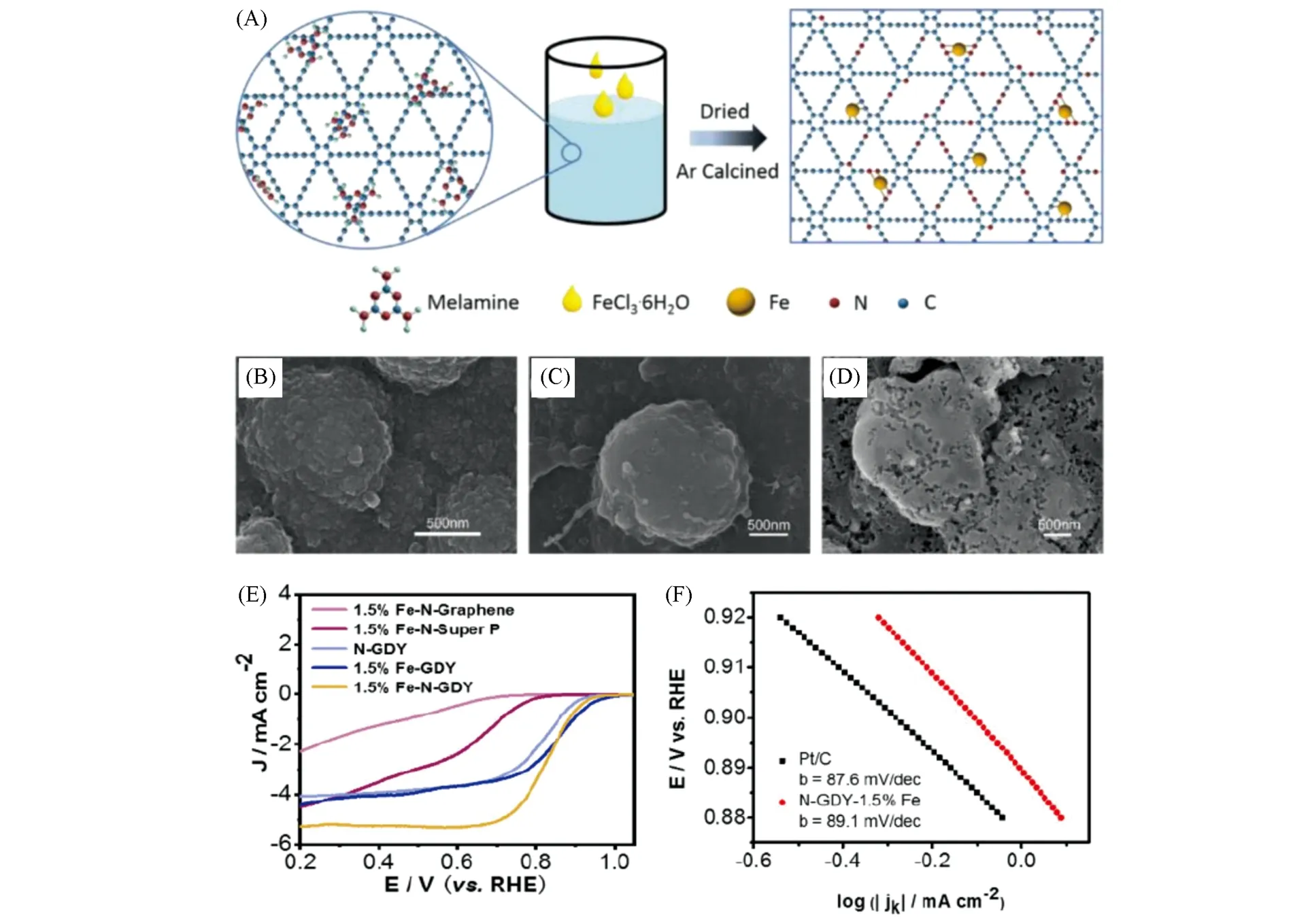
Fig.6 Schematic illustration of synthetic procedure for Fe-N-GDY catalysts(A),SEM images of 0.1%Fe-NGDY(B),1.5%Fe-N-GDY(C)and 2%Fe-N-GDY(D),LSVs of 1.5%Fe-N-Graphene,1.5%Fe-N-Super P,N-GDY,1.5%Fe-GDY and 1.5%Fe-N-GDY in O2-saturated 0.1 mol/L KOH at 1600 r/min(E),the Tafel slopes for Fe-N-GDY and Pt/C(F)[38]
Xue等[50]用石墨炔作为锚定单原子催化剂的强有力的支撑材料. 通过电化学还原Ni2+和Fe3+,将单原子Ni(0)和Fe(0)精确地锚定在石墨炔上[图7(A)~(C)]. 源于单原子Ni/Fe和石墨炔之间的强化学相互作用和电子耦合,使得催化活性位点和载体之间的电荷传输程度很高,在析氢反应(HER)中表现出优越的性能. Fe/GDY 最小的起始电位都仅为9 mV[图7(D)和(E)],Fe/GDY 和Ni/GDY 塔菲尔斜率分别为37.8 和45.8 mV/dec[图7(F)],并表现出高的长期稳定性. Hui等[51]随后对石墨炔纳米片负载单原子催化方面进行了系统研究,零价钼原子分散石墨炔(Mo0/GDY)催化剂中GDY可以使Mo原子牢固地锚定在炔烃环上,在酸性和中性电解液中对N2的电化学还原反应具有良好的催化活性和选择性. 同时,Yu 等[37]研究发现,石墨炔超薄纳米薄片负载零价钯原子催化剂(Pd0/GDY)在非常低的质量负载(0.2%)下只需55 mV,电流密度就能达到10 mA/cm2. 2020年,Yu等[52]成功制备石墨炔负载零价钌催化剂Ru/GDY. 密度泛函理论(DFT)计算表明,钌原子与邻近碳原子之间的强p-d耦合产生了一个本征电子补偿,以保持锚定Ru原子的高氧化活性,这种相关性使得Ru/GDY成为一种具有动态自修改特性的,用于快速可逆氧化还原开关的独特电子介质,酸性条件析氢反应中,电流密度为10 mA/cm2时,过电位仅为44 mV. 同时在酸性溶液中,Ru/GDY对析氧反应(OER)的催化活性和稳定性高于RuO2.
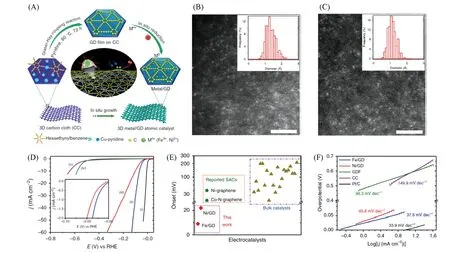
Fig.7 Protocols for the synthesis of Ni/GD and Fe/GD(A), additional HAADF-STEM images of Ni/GD(B)and Fe/GD(C)[inset: size distribution of Ni(B) and Fe(C) atoms counted from HAADF-STEM images, scale bar: 2 nm], HER activities of Ni/GD and Fe/GD: polarization curves of Pt/C(i),Fe/GD(ii), Ni/GD(iii), GDF(iv), and CC(v)(D), onset values of Ni/GD and Fe/GD(red square) along with other catalysts(E),Tafel plots of the presented data(F)[50]
电化学储能电池应用中,Wang等[30]利用自下而上的合成策略制备硼原子取代石墨炔是由sp杂化碳骨架和均匀分布的硼杂原子组成,同时sp碳骨架和缺电子硼中心与金属原子有亲和力,从而提供了额外的结合位点. 扫描电子显微镜图像显示薄膜的表面由大量的纳米颗粒均匀致密排列组成. 实验测得其电导率为1.33×10-2S/m. 其用作钠离子电池的负极材料时,表现出良好的速率性能和长周期可逆容量,在电流密度为5 A/g的情况下,在循环4000次后比容量仍可以保持在180 mA·h·g-1.
2.5 多孔纤维网状结构
多孔纤维网状结构的大比表面积和高孔隙率为离子存储提供了丰富的离子传输通道和活性位点.此外,多孔的纤维网有利于电解质的渗透,提高电导率. 因此,此类材料表现出良好的电化学能量存储和转化性能.
精确定位和共掺杂相结合的方法可以用来实现碳基材料更好的锂存储性能. Lu等[53]通过H和F定位平衡共掺杂战略,当两者均匀共掺杂时,制备了H,F共取代的石墨炔H1F1-GDY[图8(A)],形成了纤维状的网状多孔结构,并产生了良好的电解质浸润和界面稳定性[图8(B)~(E)]. 锂离子电池测试结果表明,在50 mA/g的电流密度下,可达2050 mA·h·g-1的极高容量[图8(F)],在2 A/g时循环超过3200次后,容量维持在828.5 mA·h·g-1(保持率96%)[图8(G)]. 这种结构的大比表面积和高孔隙率为锂存储提供了丰富的离子传输通道和活性位点;粗糙的表面有利于降低表面张力,增强电解质的扩散;多孔的纤维网有利于电解质的渗透,提高电导率. 摩尔比为1∶1下H/F定位共掺杂的协同效应优于其它配比. H1F1-GDY独特的层次化多孔结构非常有利于增强界面相容性,提高作为LIBs电极的碳材料的锂存储稳定性.
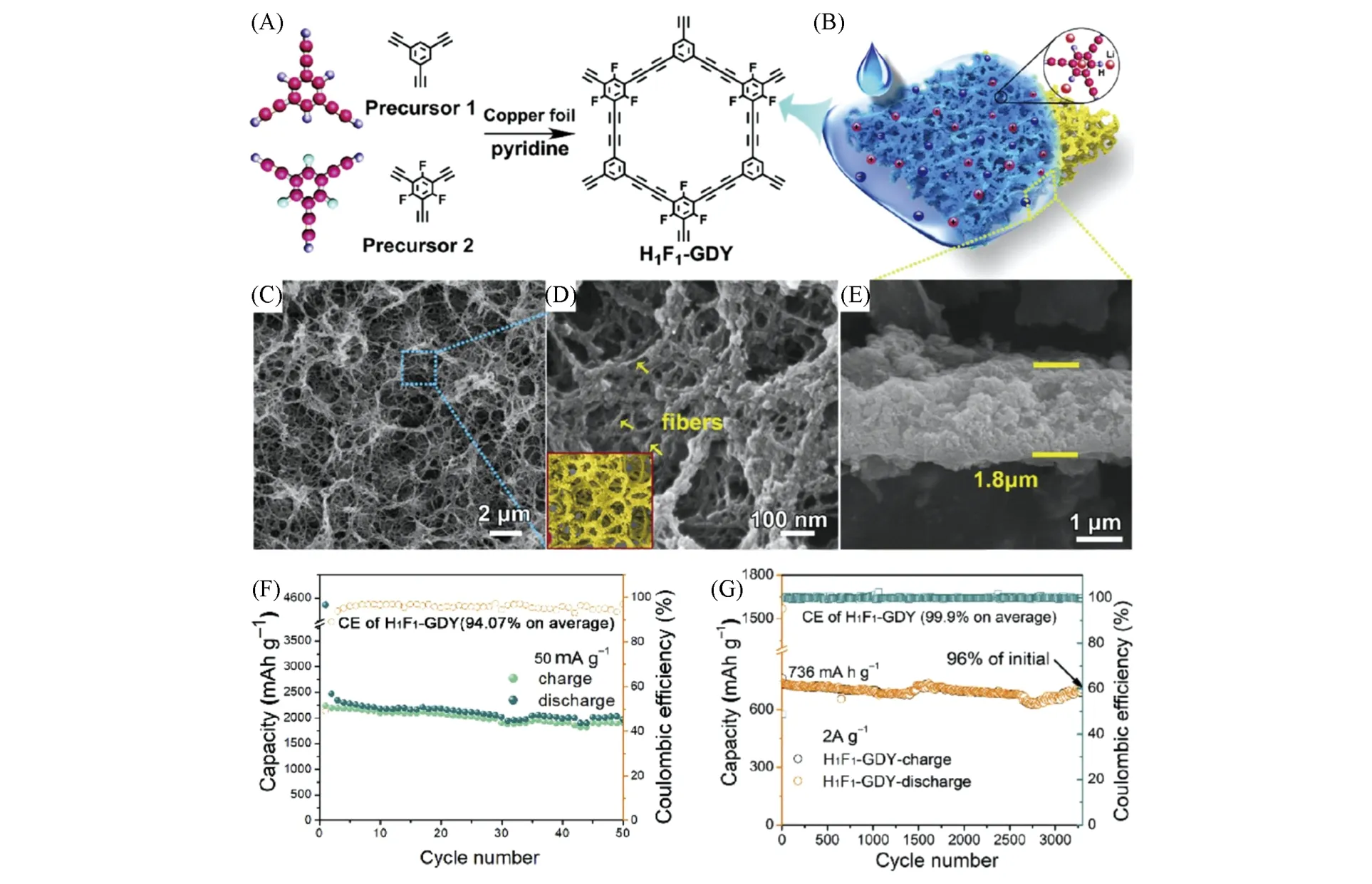
Fig.8 Schematic diagram of preparation for H1F1-GDY and the ball-and-stick model of two precursors(A),structural schematic diagram of H1F1 - GDY and the advantages of H and F doped(B), SEM images(C, D) of H1F1-GDY from top view[inset of (D): the structural model of H1F1-GDY], SEM image of H1F1-GDY from side view(E), the cycle performance at 50 mA/g(F) and the stability at 2 A/g of H1F1-GDY(G)[53]
此外,Li 等[24]通过将甲基引入石墨炔结构,获得一种交织纳米纤维网状结构. 由于甲基的引入,sp3杂化碳具有刚性的三维锥状构象,导致其层间距增大到0.41 nm. 取代石墨炔碳骨架,仍保证了良好的电子传递能力,同时3种碳原子杂化形式的存在提供了更多的储存位点. 同时,平面孔隙中的修饰甲基区分为两个功能区,一部分是从甲基到骨架边缘的位置,在锂离子穿越过程中能量势垒较高,有利于甲基与炔键之间的协同作用储存锂. 另一部分是骨架中心甲基的一部分. 锂离子在此位置与甲基的相互作用较弱,为锂离子的转运提供了通道. 锂离子电池测试结果显示,在50 mA/g的电流密度下,比容量可以达到1020 mA·h·g-1.
在电化学催化方面,氮掺杂是提高ORR性能的有效手段之一,Lv等[43]在高温氨(NH3)气氛中,分别在700,800,900 和1000 ℃下对氢取代石墨炔处理,得到氮掺杂的氢取代石墨炔(N-HsGDY). 高温下掺杂后,N-HsGDY材料几乎都保持了纳米线组成的网状结构. 在碱性条件下,N-HsGDY-900 ℃对氧还原反应表现出优异的催化活性. 氧还原反应起始电位约为1.02 V(vs. RHE),半波电位(E1/2)约为0.85 V(vs. RHE),并且活性高于商业可用的Pt/C(JM,Pt的质量分数20%). 同时此类材料也表现出比商业Pt/C更优的的稳定性和甲醇耐受性.

Fig.9 Schematic illustration and possible reaction pathway for PY-GDY and PM-GDY(A),photographs of a PM-GDY(B),and the bending for the PY-GDY film(C),rate performance of PY-GDY(D)and PMGDY for LIBs(E)[27],the detailed synthetic route of F-GDY(F),the photograph of the F-GDY film(G),contact angles of water and ethylene carbonate/dimethyl carbonate electrolyte with F-GDY(H), the illustration of Li storage mechanism in F-GDY(I), the rate performance of F-GDY electrodes in Li metal half-cell(J)[55]
2.6 柔性纳米薄膜
除了本体石墨炔制备过程中可以在铜箔表面生成大面积薄膜之外,利用自下而上法制备大面积柔性杂原子掺杂石墨炔薄膜材料,也是最近的研究热点. 其中最主要的为氮原子取代石墨炔和卤素取代石墨炔. 这种大面积柔性薄膜的构建,具有较大层间距离和有利于离子扩散的微孔结构. 柔性薄膜电极的高导电性、高比表面积、扩散距离短和大量的金属离子活性存储位点,使其具有较高的功率和能量密度.
氮原子取代石墨炔的研究中,Yang等[27]以三乙炔基吡啶和三乙炔基嘧啶为起始分子分别制备了吡啶-石墨炔(PM-GDY)和嘧啶-石墨炔(PY-GDY),得到了均匀、连续、透明的自支撑薄膜[图9(A)~(C)]. 在100 mA/g 的电流密度下,PM-GDY 和PY-GDY 作为锂离子电池电极材料的比容量分别高达1168 和1165 mA·h·g-1[图9(D)和(E)]. 同时,Yang 等[54]以三乙炔基三嗪为起始分子制备了三嗪石墨炔 (TA-GDY),同样可以得到大面积薄膜结构. 其结构中吡啶型的氮原子均匀地分布在六边形的蜂窝状孔隙中,提供了大量活性的杂原子位点. 在电流密度为50 mA/g 下,锂离子电池比容量可达到1467 mA·h·g-1.
卤代取代石墨炔基碳材料在能源储存器件的应用中也受到广泛关注. He等[55]以1,3,5-三氟苯为起始原料制备了氟取代石墨炔(F-GDY)柔性薄膜[图9(F)和(G)]. 因含氟芳烃对有机电解质有良好的润湿性,测得其水与碳酸乙烯及碳酸二甲酯电解液的接触角分别为84.1°和2.1°[图9(H)]. 在电流密度为50 mA/g 时,其锂离子电池可逆容量高达1700 mA·h·g-1[图9(I)和(J)]. 除了氟取代石墨炔以外,Wang 等[56]合成了氯取代石墨炔(Cl-GDY)薄膜电极材料,由于氯原子具有适当的电负性和尺寸,二维平面中氯原子的加入可以有效地稳定插层中的锂原子. 在电流密度为0.05 A/g时,循环50次后电极的可逆容量仍高达1150 mA·h·g-1.
除了氮取代和卤素取代石墨炔,氢原子取代部分乙炔基获得的氢取代石墨炔(HsGDY)[40]具有较大的分子孔径,更有利于离子的扩散传输,有效地提高了电池的可逆容量. 将此大面积柔性薄膜用作电极材料,电流密度为100 mA/g 时,充放电循环100次后,锂离子电池和钠离子电池的比容量仍分别可达1050和650 mA·h·g-1.

Fig.10 Schematic representation of MGDY preparation(A),SEM image of MGDY on the copper foil(B),the CA of the MGDY NTAs changes with time(C), schematic diagram of the MGDY’s protective effect on metals(D), schematic diagram of MGDY NTAs for oil-water separation(E), schematic diagram of an oil-water separator(F), change in the oil-water separation efficiency with time(G)[57]
2.7 其它结构
石墨炔结构特征决定其形貌的多样性,除了石墨炔纳米墙和纳米片等主要形貌之外,Li等[57]制备了一类新型特殊结构的石墨炔纳米刺阵列,其表现出特殊的应用前景. 通过在石墨炔中引入3个甲基(sp3杂化碳),设计并制备了多孔甲基取代石墨炔纳米刺阵列(MGDY NTAs)[图10(A)和(B)],该材料表现出优异的疏水性(接触角为152°)、长期疏水耐久性(接触角在800 d 内仅下降3.2%)和耐酸/耐碱性能. 由于其耐久性和特殊稳定性的提高,可以使用甲基取代石墨炔纳米刺阵列构建超疏水界面,成功地实现了长期金属腐蚀保护和有效的油水分离[图10(C)~(G)].
Qian等[41]使用ZnO纳米线阵列在硅片上作为衬底,通过气液固相沉积生长过程,得到非常高质量无缺陷石墨炔纳米线. 电性能测试表明电导率为1.9×103S/m,迁移率为7.1×102cm2·V-1·S-1. Xue等[42]以铜为基体的自持核壳纳米线阵列Cu@GDNA/CF. 在0.5 mol/L H2SO4中,其析氢反应起始过电位为52 mV,Tafel斜率为69 mV/dec,研究结果表明,石墨炔纳米线与Cu之间存在的协同作用对电极的催化性能至关重要. 这种优异表现源于掺杂铜的石墨炔杂化结构的形成. 其优异的催化活性和稳定性主要是由于石墨炔的超活性金属物质、高孔隙结构、电导率和化学惰性等.
此外,Yu等[45]在泡沫镍支撑的NiO纳米管上涂覆超薄石墨炔层的自支撑纳米立方体异质结构NiOGDY NC. 石墨炔的引入显著增强了杂化结构之间界面上的电荷转移,并可以显著降低催化的自由能.多孔结构不仅改善了离子的输运且增加了活性位点的数量. 析氢反应中,NiO-GDY NC在电流密度10 mA/cm2时的过电位为58 mV,明显优于商业化Pt/C(85 mV). 同时表现出和RuO2相当的析氧反应活性(电流密度10 mA/cm2时的过电位为278 mV),并具有相当优越的稳定性.
3 总结与展望
重点介绍了几种不同的石墨炔纳米结构在能源存储和转化中应用的研究进展. 作为一种新型的二维碳同素异形体,石墨炔纳米材料的研究不断取得新的进展和突破. 不同形貌的石墨炔材料被成功制备,并已经展示出这类材料巨大的电化学储能与催化应用潜力. 随着电化学器件性能的不断提高,对电极材料的容量、催化效率和稳定性的要求也越来越高,为了达到这些要求,更精细更特殊的石墨炔纳米结构材料的设计制备仍有许多挑战. 石墨炔材料的实际性能和理论性能之间还存在着很大的差距. 因此,高质量的、特定形貌的石墨炔材料的制备很必要,更精密有序形貌的设计与合成是亟需解决的问题.
进一步深入对多种掺杂形式共存的特殊结构石墨炔纳米材料的研究. 通过合理选择调控各杂化组分的组成与比例,力求获得更高能源存储和转化性能的石墨炔材料. 石墨炔纳米材料的宏量制备及其电化学能源器件中的应用问题. 其它特殊形貌结构的设计合成,或者特殊基团材料的引入,进一步拓展石墨炔在生物材料、电磁材料等其它领域的应用.
