均二甲脲合成中间体的提纯工艺优化及结构表征
2021-05-07魏弋寻尹进华
魏弋寻,尹进华
(青岛科技大学化工学院,山东 青岛 266042)
均二甲脲广泛应用于有机化学、医药、农业等领域,将其与其它聚合单体按一定比例制成可溶性絮凝剂,可显著提高净水能力[1]。近年来,制药行业对均二甲脲的需求量大幅增加,均二甲脲已成为可可碱、咖啡因和美卡拉明等镇热止痛药物最有潜力的原料之一[2]。均二甲脲的合成方法主要有甲胺-尿素法、甲胺-二氧化碳法和甲胺-异氰酸甲酯法[3]。其中,甲胺-尿素法在工业生产中最为常用,但由于甲胺和尿素在溶液中反应接触面小,转化率低,得到的均二甲脲杂质较多。甲胺-尿素法最早由BASF公司在合成尿素时发现[4],我国于20世纪90年代引进,为提高生产效率,将甲胺直接通入熔融尿素中反应,冷却合成均二甲脲。由于反应传质条件改变,均二甲脲纯度有所提高;但反应时间过长、反应机理不明确,从而制约了该工艺的发展[5]。
目前,国内外对均二甲脲的合成研究主要是对甲胺-尿素法工艺条件进行优化以提高产品收率[6-7],而关于合成中间体的研究极少。作者通过前期研究发现,甲胺和尿素在反应过程中会产生一种新的中间体,该中间体含量随反应时间延长呈先增加后减少的趋势。这对研究甲胺-尿素法合成均二甲脲具有重要意义,既能从反应机理角度进一步理解反应,也能从工艺角度优化生产。Ludlam等[8]发现,一甲基脲和均二甲脲等小分子尿素衍生物由于极性较强,普通分离手段难以得到单体纯品,导致后续分析误差较大。目前,提纯方法主要有薄层色谱法、柱层析法、醇洗结晶法等。其中,薄层色谱法操作繁复,不适合大量制备提纯[9];醇洗结晶法适合已知性质的尿素衍生物的提纯,如缩二脲的高纯精制[10]。
单因素实验和正交实验优化化合物提纯工艺[11]均有一定的局限性。中心组合设计是近年来除均匀设计外应用较多的实验设计方法[12-13],其结合响应面法对实验结果进行非线性数学模型拟合,构建具有明确表达形式的多项式,得到最佳响应值,具有精度高、预测性好等优点[14]。鉴于此,作者利用薄层色谱对均二甲脲合成中间体进行鉴别,在前期单因素实验的基础上,采用响应面法对柱层析提纯工艺进行优化,并对中间体进行表征。
1 实验
1.1 试剂与仪器
均二甲脲标准品(质量分数99.9%)、一甲基脲标准品(质量分数99.8%)、尿素标准品(质量分数99.9%),国药集团化学试剂有限公司;乙腈(色谱纯)、三乙胺(分析纯)、磷酸(分析纯)、氯仿(分析纯),上海艾比化学试剂有限公司。
岛津2010A型高效液相色谱仪;Nexus 870型傅立叶红外光谱仪;721型分光光度计;Agilent 1200型液相色谱-Finnigan LCQ Advantage型质谱联用仪;YRT-3型药物熔点仪。
1.2 分析方法
采用高效液相色谱法测定均二甲脲、尿素和一甲基脲的含量;参照文献[15]方法测定中间体含量,因无标准品,按峰面积计算其相对含量。
色谱条件:色谱柱ZORBAXSB-Phenyl(4.6 mm×250 mm,5 μm),紫外可见吸收检测器(UVD),流速1.0 mL·min-1,进样量20 μL,柱温33 ℃,检测波长205 nm。流动相:A:1 000 mL 水中加入2 mL三乙胺,用0.1 mol·L-1磷酸调节pH值至3.00±0.05;B:乙腈;A∶B=97∶3(体积比)。
1.3 中间体的提纯
1.3.1 中间体粗品制备
准确称取甲胺和尿素反应10 h(中间体含量为25%)的样品1 kg,粉碎;用5倍量无水甲醇超声提取3次,每次25 min;40 ℃下减压浓缩,得浓缩液;加入700 mL石油醚充分搅拌,减压浓缩,即得中间体粗品。
1.3.2 中间体定性分析
取浓缩液6 μL,点在荧光薄层色谱板上,用氯仿-甲醇(3∶1,体积比,下同)密闭展开50 min,取出晾干。先喷Ehrlich试剂(2.7%对二甲基氨基苯甲醛乙醇溶液与浓盐酸等体积混合)在可见光下显均二甲脲斑点[8],再喷浓硫酸-甲醇(1∶1)在紫外灯下显中间体斑点。
1.3.3 中间体粗品纯化
精密称取中间体粗品2.0 g,用少量甲醇溶解,加入4.0 g硅胶(500~800目),混匀,减压蒸除溶剂,得负载样品的硅胶。称取适量硅胶(500~800目)均匀填满于层析柱内,砂芯板压实,在上面加入负载样品的硅胶,用砂芯板压实,再用法兰封口。将层析柱安装至层析仪上,柱塞泵泵入氯仿洗脱液,以一定体积流量淋洗至平衡,再用一定体积比的氯仿-甲醇洗脱,根据紫外检测器峰位置分段收集,合并含量98%以上的中间体样液,浓缩,得纯化的中间体。
2 结果与讨论
2.1 样品的高效液相色谱分析
采用甲胺-尿素法合成均二甲脲:取一定量尿素,于反应釜中加热至熔融状态;将甲胺气体通入熔融尿素中,并打开搅拌器。通过调节加热套的功率来控制反应温度。采用高效液相色谱法分别对反应3 h、6 h、9 h、12 h、15 h、18 h、21 h、24 h的样品进行连续分析,结果如图1所示。
由图1可知,保留时间为16.4 min的未知峰的强度随反应时间的延长先增强后减弱。对此峰分离物进行液质联用分析,发现其分子量为105,含量先增加后减少直至接近0(图2)。表明该物质参与反应,且转化完全,可以推断该物质为反应过程产生的中间体。
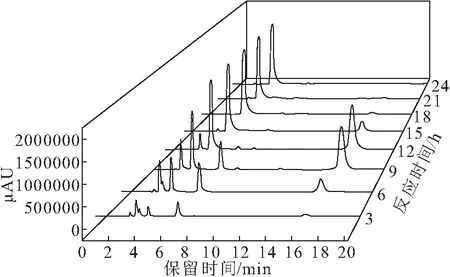
图1 反应不同时间所得样品的高效液相色谱
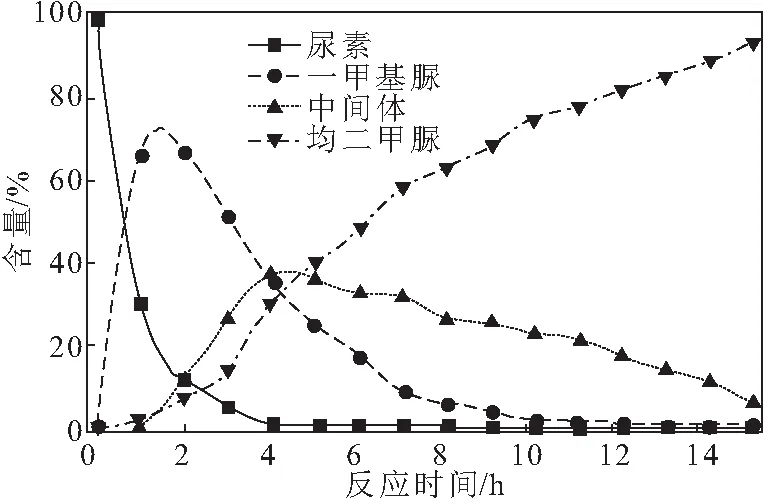
图2 各反应组分含量随反应时间的变化曲线
由图2可知,甲胺-尿素法合成均二甲脲过程中各反应组分含量随反应时间的变化与烷基脲合成反应机理[16-17]相符,即尿素在一定条件下脱氨生成异氰酸,异氰酸与烷基胺生成单取代脲。0~2 h,尿素被大量消耗,一甲基脲含量迅速增加;2~10 h,一甲基脲转化为部分中间体和均二甲脲,特别是在2~4 h,中间体含量迅速达到峰值,说明中间体可能是一甲基脲的转化产物;10 h后,一甲基脲和尿素消耗殆尽,中间体含量减少,均二甲脲含量增加,表明中间体与均二甲脲存在转化关系。中间体的发现为进一步探索甲胺-尿素法合成均二甲脲反应机理和改进工艺奠定了基础。
2.2 响应面实验结果
在前期单因素实验的基础上,选取氯仿体积分数(氯仿占洗脱液氯仿-甲醇的体积分数)、硅胶量、体积流量为考察因素,以中间体产率(纯化后中间体质量占粗品质量的百分数)为评价指标,采用Box-Behnken中心组合设计3因素3水平响应面实验,共17个实验点,其中12个析因点、5个中心点。响应面实验设计及结果见表1。
通过Design-Expert软件对表1数据进行多项式回归拟合分析,得回归模型为:Y=0.24-0.016A+0.027B+0.017C+0.019AB-0.03AC+2.066×10-3BC-0.026A2-0.028B2-0.029C2。
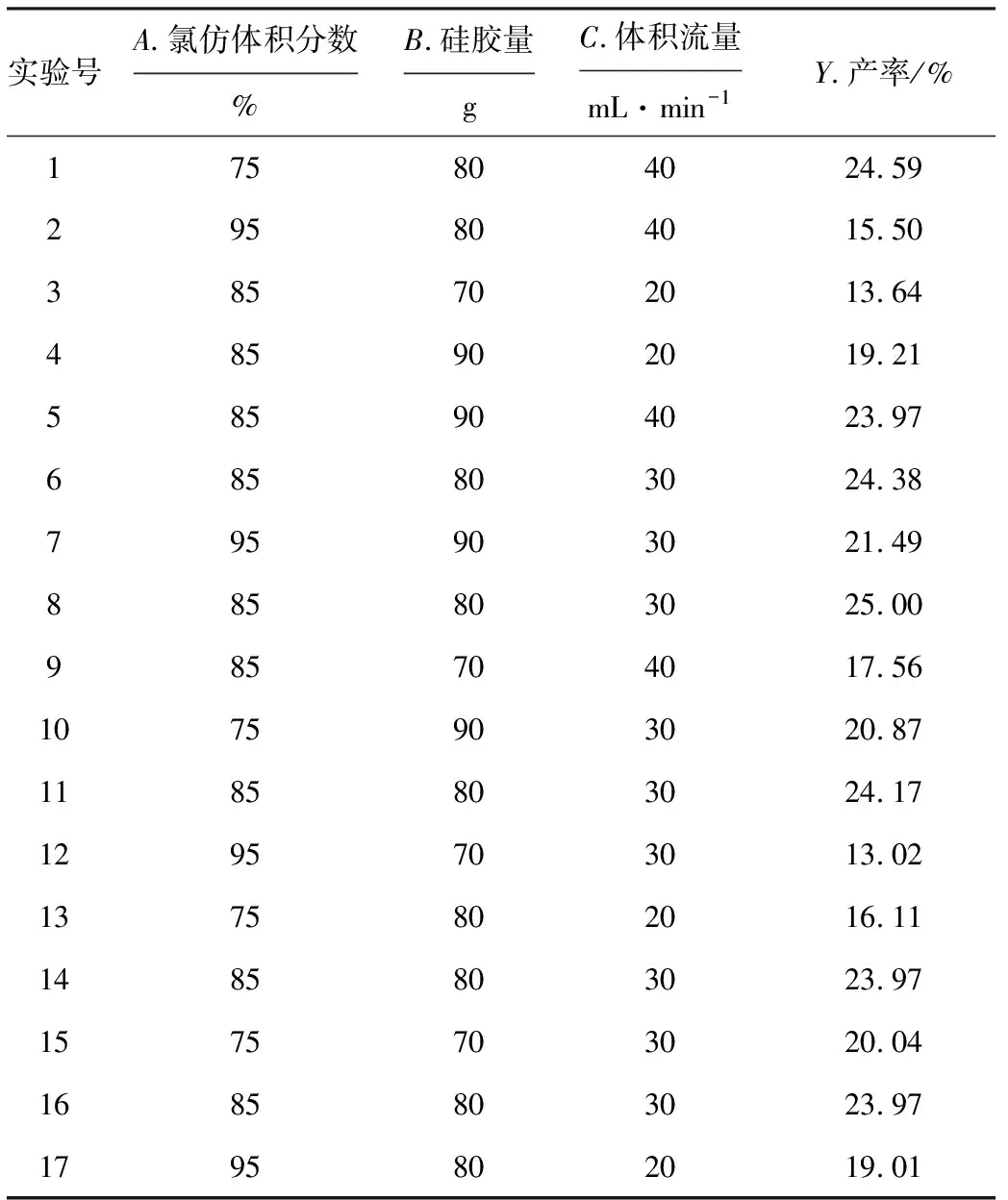
表1 响应面实验设计及结果
对回归模型进行方差分析,结果见表2。
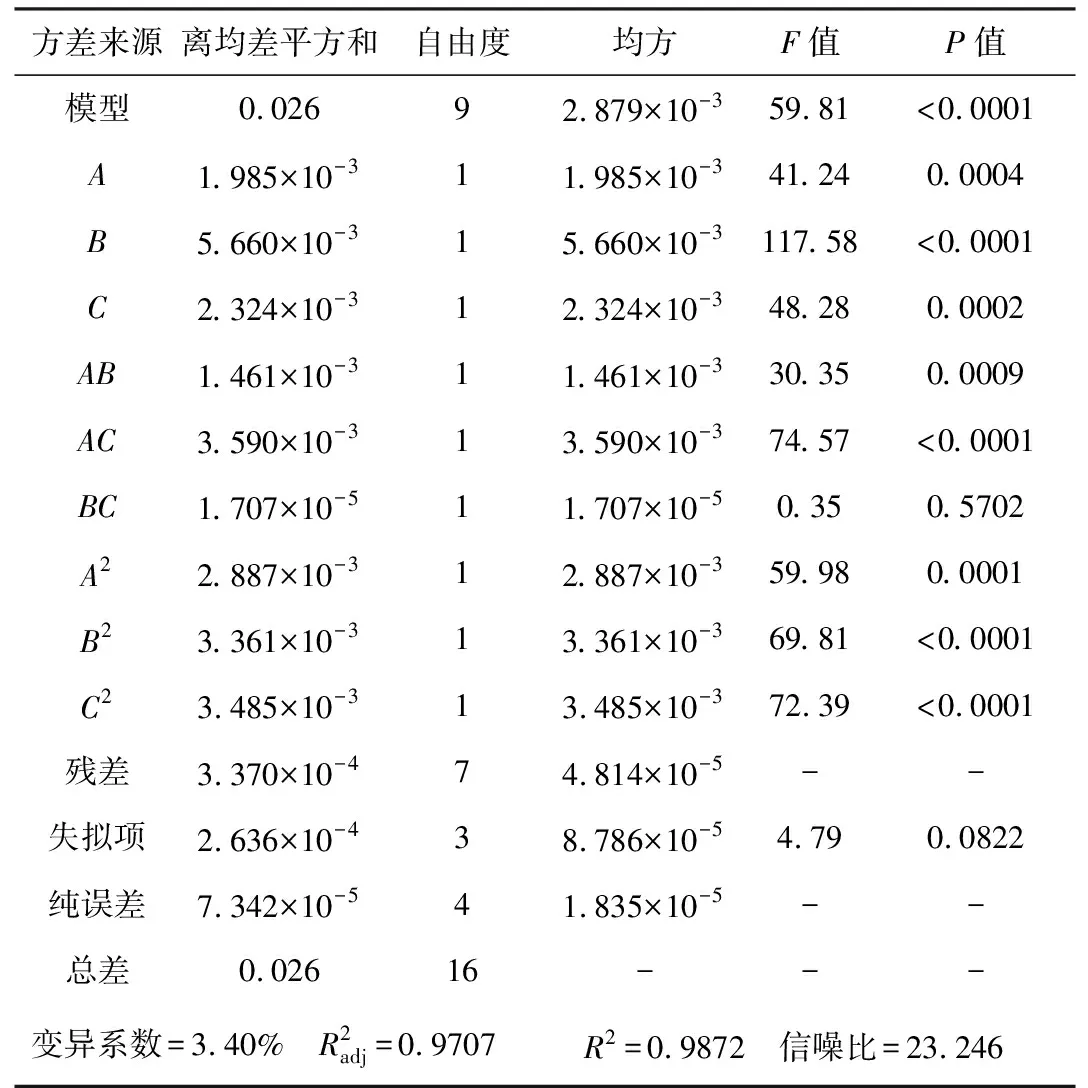
表2 方差分析
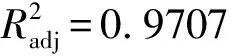
各因素交互作用对中间体产率影响的响应面分析如图3所示。
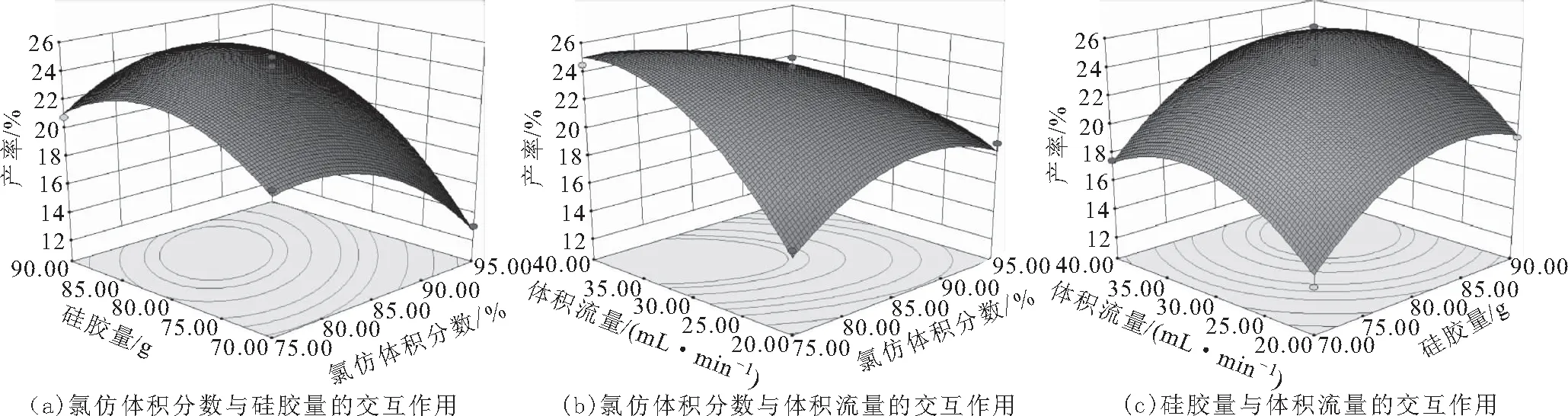
图3 各因素交互作用对中间体产率影响的响应面分析
由图3a可知,当固定体积流量时,氯仿体积分数与硅胶量的交互作用极显著。硅胶量的曲面坡度下降幅度大于氯仿体积分数的,表明硅胶量对中间体产率的影响大于氯仿体积分数。当硅胶量在80 g左右时,中间体产率最高。硅胶量过低时,部分中间体未被吸附即被洗脱液带走,中间体产率下降;硅胶量过高时,中间体被大量吸附,未能完全洗脱导致分离效果下降。
由图3b可知,当固定硅胶量时,氯仿体积分数与体积流量的交互作用极显著。体积流量的曲面坡度下降幅度大于氯仿体积分数的,表明体积流量对中间体产率的影响大于氯仿体积分数。中间体产率随氯仿体积分数的增加而升高;当氯仿体积分数超过85%时,洗脱液极性过强,中间体未被完全洗脱,导致中间体产率降低。
由图3c可知,当固定氯仿体积分数时,硅胶量与体积流量的交互作用不显著。硅胶量的曲面坡度下降幅度大于体积流量的,表明硅胶量对中间体产率的影响大于体积流量。中间体产率随体积流量的增大而升高,当体积流量过大时,中间体被大量洗脱液带走,导致中间体产率下降。
综上可知,各因素对中间体产率影响的大小依次为:硅胶量>体积流量>氯仿体积分数。为进一步确定最佳点,对回归方程取导数求极值得最佳提纯工艺条件为:氯仿体积分数85%、硅胶量80 g、体积流量30 mL·min-1,在此条件下,中间体理论产率可达24.30%。按最佳提纯工艺进行3次验证实验,中间体产率分别为24.23%、24.17%、23.38%。与理论预测值相比,相对误差<2%。因此,采用响应面法优化得到的提纯工艺可靠,对实验室分析和工厂放大提纯都具有实用价值。
2.3 中间体的表征
2.3.1 红外光谱分析
中间体经分离纯化后置于电热鼓风干燥箱中干燥浓缩,进行红外光谱分析,结果见图4。

图4 中间体的红外光谱
由图4可知,2 947.79 cm-1和2 811.57 cm-1处的吸收峰表明该中间体含有C-H键;3 339.08 cm-1处的吸收峰表明该中间体含有N-H键;1 276 cm-1处的吸收峰表明该中间体含有O-H键;1 651.60 cm-1和1 568.62 cm-1处的吸收峰表明该中间体可能存在C=O键;640.65 cm-1处的吸收峰表明该中间体含有C-N键。
2.3.2 熔点与结构分析
经熔点仪测定,中间体的熔程为98~99 ℃,与均二甲脲(101~104 ℃)、一甲基脲(92~93 ℃)熔程接近。可以判断该中间体与均二甲脲、一甲基脲等性质接近。
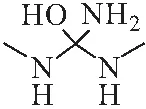
3 结论
在合成均二甲脲的过程中,发现一种未知中间体,该中间体对反应有较大影响,在反应后期,中间体与均二甲脲存在明显的转化关系。这是之前的研究尚未发现的。采用响应面法对该中间体的柱层析提纯工艺进行优化,确定最佳提纯工艺条件为:氯仿体积分数85%、硅胶量80 g、体积流量30 mL·min-1,各因素对中间体产率的影响大小依次为:硅胶量>体积流量>氯仿体积分数,在此条件下,中间体实际产率可达24.23%,验证实验与优化结果相符。该中间体分子量为105,熔程为98~99 ℃;一甲基脲可能与甲胺直接生成中间体,中间体再经脱氨转化为均二甲脲。这与之前的机理路线不同,为后续研究提供了理论依据与方向。
