一种注射用温敏型水凝胶的制备及特征分析
2021-05-06黄永娜宣德春梁荣宋海鑫苗晋锋张金秋
黄永娜 宣德春 梁荣 宋海鑫 苗晋锋 张金秋

摘要:温敏型水凝胶在药物或抗原富集、缓释、控释等方面具有重要的应用价值。为获得一种可用于注射的、在生理温度附近具有良好相变可控性的温敏型水凝胶,试验分析了F127、F68、HPMC等不同组分对成胶行为的影响,通过测定并比较不同配方的凝胶温度、凝胶时间等,筛选到6个符合最优成胶条件的温敏型水凝胶配方,其在室温下为无色透明液体,通针性良好,在温度为37℃时可快速转变为半固体凝胶态,成胶时间约3min。本试验筛选出的温敏型水凝胶配方为后续在疫苗佐剂方面的应用提供了基本试验资料。
关键词:温敏型水凝胶;凝胶温度;凝胶时间;泊洛沙姆
中图分类号:S852.5文献标志码:A
文章编号:1002-1302(2021)04-0120-05
作者简介:黄永娜(1994—),女,山东日照人,硕士,主要从事畜禽疫病防控方向的研究。E-mail:1271794375@qq.com。
通信作者:张金秋,副研究员,主要从事畜禽疫病防控研究。E-mail:jqzh03@126.com。
温敏型水凝胶(temperaturesensitivehydrogel)是目前研究较为广泛的原位水凝胶之一,能够对外界环境温度的变化作出及时响应,实现溶液—凝胶的相转变,在生物医药、组织工程、细胞工程等方面具有重要应用价值[1]。特别是在药物控释方面,温敏型水凝胶的三维网状结构可以将药物包裹在内,形成药物储库,有助于提高药物的载量。随着凝胶在体内的降解或溶蚀,药物缓慢释放,可避免药物的首过效应,延长药物在体内的滞留时间,从而达到持续给药的目的[2]。另外,一些蛋白类药物进入机体后,很容易被酶类物质降解,使药效得不到充分发挥,而利用温敏型水凝胶作为蛋白类药物的载体,可以显著减缓蛋白类药物的降解速度,借助缓释作用提高药物的生物利用度[3]。
温敏型水凝胶的这一特征提示其可以作为优良的抗原载体,即可以用作疫苗佐剂,一方面有利于富集抗原,形成抗原储库,另一方面可以通过缓控释功能,延长抗原在体内的存留时间,增加抗原与机体免疫系统的接触,模拟疫苗多次免疫的效果,持续刺激机体产生高滴度的抗体。因此,本研究选择生物相容性良好的高分子聚合物等作为凝胶基质,筛选不同物质的浓度及配伍比例,旨在制备一种适用于注射的温敏型水凝胶,为后续的疫苗研发提供技术支持。
1材料与方法
1.1主要试剂
泊洛沙姆407(Poloxamer407,F127,SigmaAldrich公司);泊洛沙姆188(Poloxamer188,F68,SigmaAldrich公司);羟丙基甲基纤维素(HPMC,SigmaAldrich公司);其他化学试剂均为分析纯。
1.2主要仪器设备
数显磁力搅拌器,江苏省金坛荣华仪器制造有限公司生产;HPX-9082MBE数显电热培养箱;超声仪,上海声浦超声波设备厂生产;恒温培养箱,德国Binder公司生产;DSC8500差示扫描量热仪,美国PerkinElmer公司生产;流变仪MCR301,奥地利AntonPaar公司生产。
1.3配方的筛选
采用冷法制备温敏型水凝胶[4]。准确称量泊洛沙姆407、泊洛沙姆188、羟丙基甲基纤维素等高分子材料,溶于适量超纯水中,于冰水浴条件下充分混合均匀,4℃冰箱过夜使其充分溶胀。
1.3.1F127对成胶行为的影响选取的F127的浓度为30%,HPMC的浓度为2.5%,调整F127∶HPMC的体积比分别为7∶1、6∶1、5∶2、4∶3、5∶1、4∶1、3∶1,观察其成胶温度的变化,考察F127的含量对凝胶行为的影响。
1.3.2F68对成胶行为的影响选取的F127的浓度为30%,HPMC的浓度为2.5%,F68的浓度为10%,调整F127∶F68∶HPMC的体积比分别为7∶1∶1、6∶1∶1、5∶1∶1、4∶1∶1,考察F68的含量对凝胶行为的影响。
1.3.3HPMC对成胶行为的影响选取的F127的浓度为30%,F68的浓度为10%,HPMC的浓度为2.5%,调整F127∶F68∶HPMC的体积比分别为7∶1∶0.5、7∶1∶1、6∶1∶0.5、6∶1∶1、5∶1∶0.5、5∶1∶1、4∶1∶0.5、4∶1∶1,考察HPMC的含量对凝胶行为的影响。
1.4凝胶时间的测定
采用倒置法,将配制好的温敏性凝胶水溶液放置在培养箱中,自29℃开始升温,控制升温速度在1℃/2min,每隔2min倒置倾斜观察,与水平面夹角成60°,以30s内液体不流动作为成胶判定依据,记录胶凝温度和胶凝时间。试验重复3次,计算平均值。
1.5流变仪测定温敏型水凝胶的玻璃化转变温度及黏弹性
按“1.3”节的方法制备样品后,经流变仪MCR301测定样品玻璃化转变温度(Tg)。设定应变值为10%,角频率Ω为2rad/s,升温范围为10~50℃,升温速度为2℃/min,10℃保温2min,样品测量厚度为0.5mm。观察温敏型水凝胶的储模量G′和失模量G″随温度的模量变化情况,计算损耗因子tanδ的值。
2结果与分析
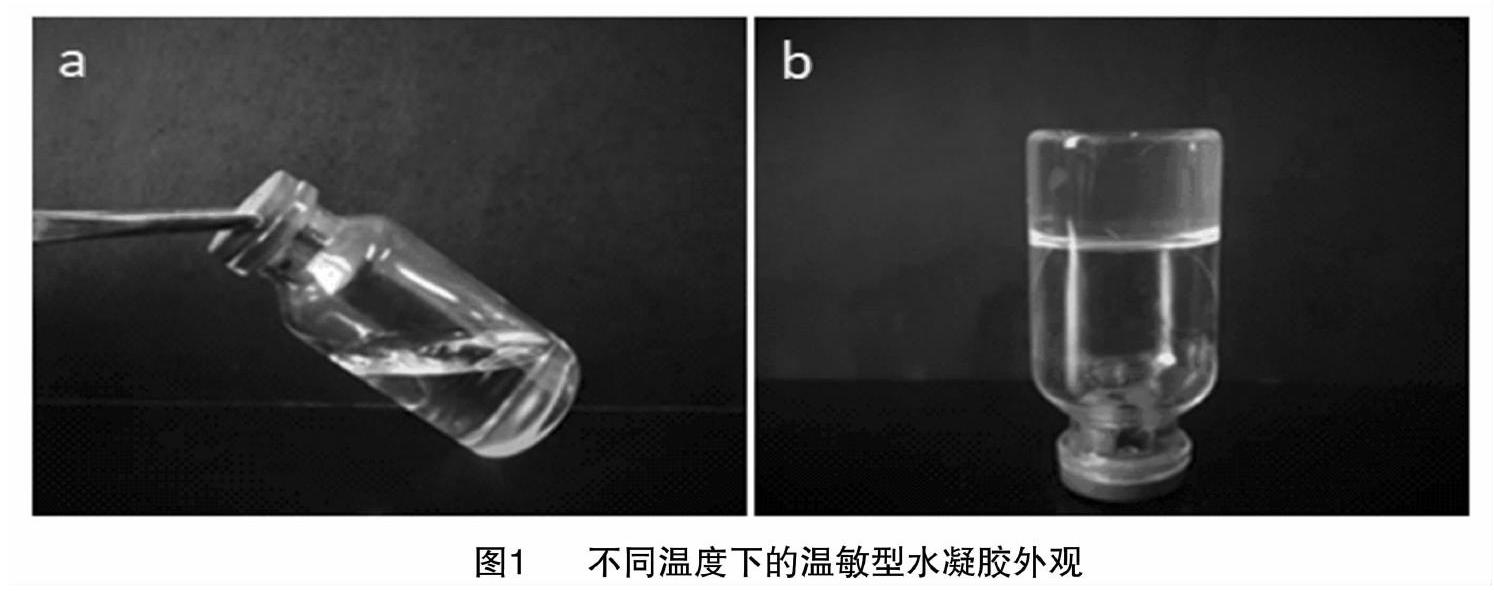
2.1温敏型水凝胶的形态变化
从图1可以看出,在室温下该温敏型水凝胶为具有良好流动性的无色透明液体,且流动性与温度呈反向相关关系,即温度越低,流动性越好,温度为37℃时为不流动的半固体凝胶态。室温下经1mL注射器注射试验,该温敏型水凝胶通针性良好。
[FK(W9][TPHYN1.tif][FK)]
2.2F127对成胶行为的影响
从表1可以看出,温度升至39℃时,体积比为5∶2、4∶3、3∶1的体系仍不能成胶,对应F127的实际浓度为21.43%、17.14%、22.5%。由此筛选出可形成凝胶的试验组别7∶1、6∶1、5∶1和4∶1,用于后续试验。由F127:HPMC組成的体系中,F127的最低成胶浓度为24%,且F127的浓度越大,成胶温度越低。
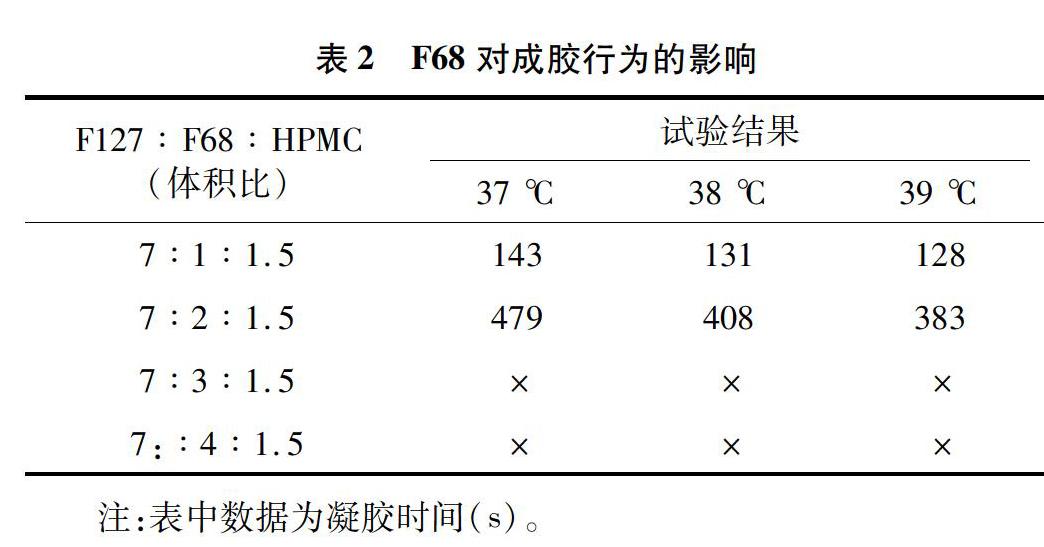
2.3F68对成胶行为的影响
在F127与HPMC体积比不变的情况下,仅改变F68的体积占比,考察成胶时间与成胶温度的关系。从表2可以看出,提高F68的含量,体系的胶凝时间明显增加。当F68的含量进一步增加,即F127∶F68∶HPMC的体积比为7∶3∶1.5、7∶4∶1.5时,体系在39℃以下均不能成胶。
2.4HPMC对成胶行为的影响
从表3可以看出,当固定F127与F68的比例时,增加HPMC的体积比能够提高该温敏型水凝胶的成胶温度。同时,F127的含量越低,体系的成胶温度越高,当F127∶F68∶HPMC的体积比为4∶1∶1时,即使温度升至39℃,体系依然不能成胶。
2.5不同配方的凝胶时间比较
根据上述各因素对胶凝温度和胶凝时间的影响,设计各种高分子物质的比例,比较不同凝胶配方在不同温度的成胶时间。从表4可以看出,上述各组配方在36~38℃的成胶时间均在3min左右,且随着配方中[KG*8]F127[KG*8]和[KG*8]HPMC[KG*8]含量的升高,相同温度下体系的胶凝时间逐渐缩短。
2.6温敏型水凝胶的玻璃化转变温度及黏弹性测定
以F127∶F68∶HPMC(体积比)=7∶1∶1.5的配方为例,通过流变仪测定该配方的玻璃化转变温度及黏弹性。从图2-a可以看出,在10~25℃,样品的储能模量和损耗模量均无明显变化。温度继续升高到25℃以上,储能模量和损耗模量均开始明显增加,但储能模量<损耗模量,体系处于液态或黏性态;温度升高至33℃时,储能模量与损耗模量相当,体系由液态转变为半固体凝胶态,此温度即为该温敏型水凝胶的玻璃化转变温度。当温度继续升高时,储能模量>损耗模量,体系已完全转变为固体凝胶态。该温敏型水凝胶在状态转变的过程中模量变化范围为0~2000Pa。损耗因子tanδ为损耗模量与储能模量的比值,代表了体系的黏弹性。tanδ值越低,体系的黏弹性越大。从图2-b可以看出,在体系处于流动态时,tanδ值较高;当体系成胶后,样品的储能模量大于损耗模量,tanδ值明显下降,凝胶体系的黏弹性增大。
3讨论与结论
温敏型水凝胶良好的生物相容性和相转变的可控性,使其成为医药领域研究的热点。因制备温敏型水凝胶的材料来源不同,凝胶的特性也具有很大差异。如壳聚糖、纤维素、透明质酸等天然物质制备的温敏型水凝胶,生物相容度良好,已在药物控释、组织修复等方面有广泛研究及应用。但壳聚糖溶解性较差,需要溶解在弱酸中,且壳聚糖的脱乙酰度对于体系能否成胶有重要影响[5]。研究表明,壳聚糖的脱乙酰度要达到85%以上,并加入一些物质,如β-甘油磷酸钠等,对化学键进行改性或修饰,才可能形成凝胶体系。这些复杂的操作在很大程度上限制了壳聚糖温敏型水凝胶的应用[6-7]。此外,透明质酸类温敏型水凝胶的机械性能较差,凝胶强度不够,易被酶解,通常需要进行物理或化学交联,以改善凝胶性能。
聚氧乙烯聚氧丙烯嵌段共聚物等高分子合成材料具有良好的水溶性、温度敏感性及生物安全性,近年来已在黏膜给药系统、经皮给药系统中得以应用。本研究所选用的泊洛沙姆407(F127)、泊洛沙姆188(F68)均属于聚氧乙烯聚氧丙烯嵌段共聚物,但聚氧乙烯和聚氧丙烯的比例不同。有文献报道,F127的最佳成胶浓度范围为18%~30%,浓度低于18%,溶液即使升至很高的温度也不能成胶;浓度高于30%时,在室温或更低温度下就可能成胶,并且高浓度的水凝胶在制备过程中会更加困难[8]。因此单独使用F127难以获得在正常体温范围的可用于注射的温敏型凝胶剂。F68单独不能成膠,能在一定程度上起到消泡的作用,常用作稳定剂[9]。本试验发现增加F68的含量,有助于提升F127体系的凝胶温度,同时降低体系浓度。羟丙基甲基纤维素(HPMC)在口服药物中常充当药物赋型剂或辅料,在眼科用药时常被作为润滑剂[10]。HPMC本身的胶凝温度较高,本研究将HPMC加入温敏型水凝胶体系中,可以提高体系的成胶温度,能避免体系在室温下过快胶凝。同时,HPMC也可以作为悬浮剂,使体系更加均一稳定,增加生物黏附性[11]。
流变仪测定法是目前比较常用的衡量温敏型水凝胶玻璃化转变温度的方法。通常情况下,储能模量又称为弹性模量,是指材料在发生形变时,由于弹性形变而储存能量的大小,反映材料弹性大小;损耗模量又称黏性模量,是指材料在发生形变时,由于黏性形变而损耗的能量大小,反映材料黏性大小。当储能模量远大于损耗模量时,材料主要发生弹性形变,所以材料呈固态;当损耗模量远大于储能模量时,材料主要发生黏性形变,所以材料呈液态;当储能模量和损耗模量相当时,材料为半固态。本研究以F127∶F68∶HPMC(体积比)=7∶1∶1.5的配方为例,发现温度约33℃时,体系的储能模量与损耗模量相当,判断在此温度下,体系发生相转变,呈凝胶态。另外,不同的材料表现出的状态转变也有很大差异[12-13]。如Supper等发现,壳聚糖水凝胶的黏弹性变化较为缓和,模量变化范围在0~800Pa之间[14]。而本试验所得的温敏型水凝胶的模量变化范围为0~2000Pa,表明泊洛沙姆及羟丙基甲基纤维素构成的凝胶体系强度更大,推测该类高分子聚合物材料形成的温敏型水凝胶可能具有更致密的凝胶网络结构或类固体性能。研究发现,应用其他辅料可以调节泊洛沙姆类温敏型凝胶的胶凝温度、胶凝时间及凝胶强度[15-16]。如添加甲基纤维素、羟丙基甲基纤维素或具有黏膜黏附性的聚卡泊菲等,能够增加凝胶强度,减缓药物释放速率,这与本试验中观察到的现象相一致。
综上所述,本研究以F127、F68、HPMC为基质,通过分析不同组分对成胶行为的影响,筛选出了在生理温度附近(37℃左右)具有良好相变可控性的温敏型水凝胶的配方。该温敏型水凝胶在室温下流动性良好,通针性佳,为后续进行免疫增强效果评价提供了技术支持。
参考文献:
[1]汤玉峰,杜予民.壳聚糖基可注射型温度敏感性水凝胶[J].化学进展,2008,20(2):239-244.
[2]沈莹.自微乳化胰岛素经鼻给药系统的研究[D].上海:上海医药工业研究院,2005.
[3]王欣欣.姜黄素微丸及囊泡的制备工艺和生物利用度研究[D].青岛:青岛科技大学,2017.
[4]刘玲秀,胡帼颖,刘欣,等.温敏型可注射水凝胶的制备研究[J].中国生物医学工程学报,2010,29(6):901-908.
[5]WangQ,WangM,LiP,etal.TheinteractionofchitosanandBMP-2tunedbydeacetylationdegreeandpHvalue[J].JournalofBiomedicalMaterialsResearchPartA,2019,107(4):769-779.
[6]BaoZ,JiangC,WangZ,etal.Theinfluenceofsolventformulationsonthermosensitivehydroxybutylchitosanhydrogelasapotentialdeliverymatrixforcelltherapy[J].CarbohydratePolymers,2017,170:80-88.
[7]孙斌,刘洪臣.可注射温敏壳聚糖/甘油磷酸钠基水凝胶在医学中应用进展[J].中华老年口腔醫学杂志,2011,9(1):46-49.
[8]候冰娜,郑泽邻,赵梓年,等.可注射海藻酸钠/泊洛沙姆复合水凝胶的制备及药物缓释研究[J].材料工程,2020(12):60-67.
[9]DeyAK,BurkeB,SunY,etal.Useofapolyanioniccarbomer,Carbopol971P,incombinationwithMF59,improvesantibodyresponsestoHIV-1envelopeglycoprotein[J].Vaccine,2012,30(17):2749-2759.
[10]MaheshB,KathyayaniD,NanjundaswamyGS,etal.Miscibility[JP4]studiesofplastic-mimeticpolypeptidewithhydroxypropylmethylcelluloseblendsandgenerationofnon-wovenfabrics[J].CarbohydratePolymers,2019,212:129-141.
[11]CostanzoS,PasquinoR,DonatoR,etal.Effectofpolymerconcentrationandthermalhistoryontheinversethermogelationofhydroxypropylcelluloseaqueoussolutions[J].Polymer,2017,132:157-163.[HJ1.98mm]
[12]Krezovic[DD(-1*2][HT6]'[DD)]BD,Miljkovic[DD(-1*2][HT6]'[DD)]MG,Stojanovic[DD(-1*2][HT6]'[DD)]ST,etal.Structural,thermal,mechanical,swelling,drugrelease,antibacterialandcytotoxicpropertiesofP(HEA/IA)/PVPsemi-IPNhydrogels[J].ChemicalEngineeringResearchandDesign,2017,121:368-380.
[13]Vukovic[DD(-1*2][HT6]'[DD)]JS,Babic[DD(-1*2][HT6]'[DD)]MM,Anti[KG-*5]c[DD(-1*3][HT6]'[DD)]KM,etal.Invitrocytotoxicityassessmentofintelligentacrylatebasedhydrogelswithincorporatedcopperinwoundmanagement[J].MaterialsChemistryandPhysics,2016,175:158-163.
[14]SupperS,AntonN,SeidelN,etal.Rheologicalstudyofchitosan/polyol-phosphatesystems:influenceofthepolyolpartonthethermo-inducedgelationmechanism[J].Langmuir,2013,29(32):10229-10237.
[15]HuangW,ZhangN,HuaH,etal.Preparation,pharmacokineticsandpharmacodynamicsofophthalmicthermosensitiveinsituhydrogelofbetaxololhydrochloride[J].Biomedicine&Pharmacotherapy,2016,83:107-113.
[16]KoffiAA,AgnelyF,PonchelG,etal.Modulationoftherheologicalandmucoadhesivepropertiesofthermosensitivepoloxamer-basedhydrogelsintendedfortherectaladministrationofquinine[J].EuropeanJournalofPharmaceuticalSciences,2006,27(4):328-335.
