脊柱转移瘤病理性骨折的危险因素及影像学预测研究进展
2021-05-06秦思源王奇政张恩龙刘珂陈永晔郎宁
秦思源,王奇政,张恩龙,刘珂,陈永晔,郎宁*
作者单位:1.北京大学第三医院放射科,北京100191;2.北京大学国际医院放射科,北京102206
骨是肿瘤除肝和肺之外最常见的转移部位,脊柱转移瘤约占全部骨转移瘤的50%[1]。随着癌症发病率的增加和生存期的延长,脊柱转移的发生率也在不断增加,而脊柱转移提示癌症已进入晚期,因此如何防止并发症、改善患者的晚期生存质量,是临床医师面临的一大难题。病理性骨折是脊柱转移瘤的严重并发症之一,其中最常见的类型是椎体压缩骨折(vertebral compression fracture,VCF),其特征是椎体前柱骨折而后柱完整,该类型通常相对稳定,并发症少;少数为爆裂骨折,此类型特征是椎体前、中柱骨折并伴随骨折碎片和硬膜外组织侵入椎管,导致硬膜囊受压和脊髓损伤,严重者会导致瘫痪。因而,提前获悉脊柱转移患者病理性骨折的危险因素,进行影像学预测,对高危人群进行合理的预防性治疗,可能会有效降低病理性骨折的发生率。笔者对脊柱转移瘤病理性骨折的危险因素以及影像学预测方法进行了综述。
1 脊柱转移瘤病理性骨折的危险因素
1.1 脊柱因素
脊柱转移瘤病理性骨折最重要的危险因素是脊柱不稳。脊柱不稳目前没有标准的定义,Pope等[2]将脊柱不稳定义为:脊柱对施加载荷的异常响应,即不稳的脊柱容易在正常的载荷下发生反常的活动和位移。既往研究发现,影响脊柱稳定性的因素包括肿瘤大小和位置、载荷及骨矿物质密度(bone mineral density,BMD)等。
肿瘤大小是影响脊柱稳定性最重要的因素之一。Whyne等[3]建立了瘤占比(tumor occupancy,TO)(肿瘤占椎体体积的比例)分别为15%、30%和45%的L1 椎体有限元模型,用椎体膨隆程度(椎体中轴面上前后方向凸出的距离)来描述病理性骨折发生的风险,结果发现在施加相同载荷的情况下,随着肿瘤体积增加,椎体膨隆程度呈指数增加。Hibberd等[4]对72例进行稳定或减压手术的脊柱转移瘤患者的研究中,TO 为25%以下、25%~50%、50%以上的椎体病理性骨折的发生率分别为52%、87%、91%。
肿瘤累及椎骨的范围也是一个关键因素,具体包括肿瘤在椎体中的位置、是否合并皮质、附件及关节的破坏等。Krishnaney 等[5]认为,由于人体的重力作用,轴向平面的溶骨性病变对椎体稳定性的破坏高于矢状面的病变;椎体腹侧的病变比背侧更易导致椎体不稳定,因为椎体后方的韧带、小关节等结构分担了椎体的部分载荷,从而减小了椎体膨隆程度。Tschirhart 等[6]通过有限元分析发现,与完整椎体相比,合并皮质破坏的椎体爆裂骨折的发生率降低了30%,因为当存在皮质破坏时,椎体后壁承受相同张力时的形变也会降低。Taneichi[7]等评估了100 例合并转移瘤的胸腰椎中溶骨性破坏的范围发现,合并肋椎关节破坏是胸椎病理性骨折的危险因素,而合并椎弓根破坏是腰椎病理性骨折的危险因素。
载荷指的是使椎体产生内力或变形的外力或其他因素。Tschirhart 等[8]用有限元模型评估了多种载荷对胸椎骨折风险的影响,结果显示轴向压缩载荷使胸椎爆裂增加的骨折风险高于旋转载荷,该结果对指导患者的日常活动有意义。
BMD 是影响病理性骨折的又一重要因素。在正常骨组织中,成骨细胞与破骨细胞的相互调节使在骨重塑过程中的骨吸收和骨破坏达到相对平衡,而脊柱转移等病理变化可能会导致成骨细胞和破骨细胞异常活动,改变骨骼中矿物质的分布情况,进而影响BMD,增加病理性骨折的风险[9],它与骨质疏松症引起的BMD均匀下降不同。因此,脊柱转移瘤BMD下降的原因包含两个方面,一是转移瘤引起的溶骨性破坏,二是骨质疏松的影响。Dimar等[10]的尸体研究表明,预测胸椎病理性骨折的最佳参数是剩余的完整椎骨横截面积与BMD 的乘积。随着BMD的下降,当剩余椎体横截面积低于51%~96%时,椎体容易发生病理性骨折。此外,也要关注骨质疏松症本身对脊柱转移瘤病理性骨折的影响,因为肿瘤患者的化疗或者激素治疗可能诱发骨质疏松症。Salvatore 等[11]建立了骨质疏松的腰椎转移瘤模型,结果显示,载荷和肿瘤大小一定时,与正常椎体相比,骨质疏松模型椎体膨隆程度和椎体高度下降程度更大。由于肿瘤的化疗或激素治疗可能会引起骨质疏松症,所以在治疗转移瘤本身的同时也需要关注患者BMD 的动态变化,采取相应的预防性治疗措施。
2010 年脊柱肿瘤研究协会(spine oncology study group,SOSG)提出了脊柱不稳定评分(spinal instability neoplastic score,SINS)[12]来评估脊柱的稳定性,包括以下六个方面:受累椎体的位置、有无机械性疼痛、骨破坏的类型、脊柱影像学力线、椎体塌陷的百分比以及椎体后外侧结构受累情况。根据SINS 总分将脊柱稳定性分为3 类:0~6 分为稳定,7~12 分为潜在不稳定,13~18 分为不稳定。Lee 等[13]对SINS 预测VCF 的准确性做了系统综述,结果发现有八项研究报道了SINS 总分及其每个项目预测VCF 的准确性,没有研究认为椎体位置能有效预测VCF,其余项目及SINS 总分也均有研究认为预测VCF 无效。尽管SINS 目前在临床应用广泛,但其中的一些项目(如位置)预测VCF的能力不足,因此未来需要考虑增删SINS的某些项目,使其更加适用于临床实际使用。
1.2 脊柱外因素
脊柱转移瘤病理性骨折的脊柱外因素主要包括年龄、性别、身体质量指数(body mass index,BMI)以及转移瘤的组织学来源等。既往研究表明,高龄(>55 岁或65 岁)可能是脊柱转移瘤病理性骨折的危险因素,可能与脊柱的退行性变、BMD的降低导致的椎体承重能力减弱相关[14-15]。绝经后女性是脊柱转移瘤病理性骨折的另一个危险因素,可能是雌激素降低导致的钙质流失引发BMD 降低[16]。Glogowska-Szelag[17]的研究表明,绝经后女性的BMD 与BMI 呈正相关。而Chen 等[18]认为,肥胖是病理性骨折的保护因素,可能与肥胖者较高的BMD和周围软组织的保护作用相关。但Kaze 等[19]关于BMI 与椎体骨折关系的荟萃分析结果显示,女性BMI 的增加会导致椎体骨折的风险增加,其机制至今仍未清楚,可能是脂肪组织与激素水平变化和椎体的生物力学作用相关。
转移瘤的组织学来源也是可能的危险因素之一,可能与原发肿瘤的恶性程度、生物学行为、骨破坏的类型相关。脊柱转移最常见的来源包括乳腺癌、肺癌、肾细胞癌、前列腺癌等[20]。不同研究分别认为原发血液系统肿瘤、结直肠肿瘤、肺和肝来源肿瘤是病理性骨折的危险因素,前列腺来源肿瘤是病理性骨折的保护因素[21-23]。研究结果不一致的原因可能是转移瘤的组织来源种类广泛、每种组织来源的患者数量较少,后续可进行多中心研究来提高研究结果的准确性。
1.3 治疗因素
脊柱转移瘤治疗方法主要有手术及放疗,其中,放疗与病理性骨折关系最为密切。放疗虽可缓解症状,但同时也可能破坏椎体正常组织结构。传统的放疗方法是姑息性常规外束放射治疗(external beam radiotherapy,EBRT),该疗法使用对正常细胞毒性最低的剂量,实现短期疼痛的缓解和肿瘤的局部控制[24]。近年来,立体定向放射治疗(stereotactic body radiotherapy,SBRT)成为了脊柱寡转移(转移部位≤5)的一种新的放疗方式,其精度更高,肿瘤周围正常组织(如脊髓)受辐射剂量更少,且其生物有效剂量约为EBRT 的2~8 倍[25]。VCF 是SBRT 最常见及最严重的并发症,超过10%的患者在SBRT 后会 发 生VCF[26]。Vargas 等[27]回 顾了各45 例 经EBRT 和SBRT 治疗的脊柱转移瘤患者,发现SBRT 组的VCF 发生率(22.22%)显著高于EBRT组(6.67%)。SBRT造成VCF的原因可能是放射线在杀伤肿瘤细胞的同时诱发椎体坏死,而坏死骨组织导致椎体轴向承载力降低[28]。
影响SBRT后VCF的因素主要包括分割模式和单次放射剂量(dose per fraction)。研究表明,相比于单次大剂量放疗,多次分割治疗的一年疼痛缓解率更低[29],但VCF 发生率也更低[30]。因此,可建议预期生存时间较长的患者可以采取多次分割放疗,而预期生存时长较短的患者可采取单次大剂量放疗以更有效地缓解疼痛。Sahgal等[31]的多中心研究将脊柱转移瘤行SBRT 治疗的患者根据单次放射剂量分为三组:≤20 Gy、20~23 Gy、≥24 Gy,结果发现,三组患者在一年内VCF 的发生率分别为10%、19%、39%,表明单次大剂量放疗可能是诱发VCF的危险因素。
预防性椎体成形术(preventive vertebroplasty,PV)是一种向高危椎体内预防性注入骨水泥或者人工骨以强化椎骨的手术,一些研究[32-34]对大量患者进行危险因素分析发现,先前存在VCF、椎体高度降低>50%、显著溶骨性破坏、脊柱畸形、即将进行单次放射剂量≥20 Gy 的SBRT 的患者可以考虑预防性稳定手术,但术后仍存在发生病理性骨折的风险。骨水泥注入质量是与PV 术后骨折的重要影响因素。Delpla 等[35]回顾了100 例脊柱转移瘤接受PV 治疗的患者,结果显示PV 治疗组骨折发生率(6.5%)远低于未治疗组(20.8%),说明PV 可降低病理性骨折的发生率,研究还发现,PV后仍发生病理性骨折的危险因素包括转移瘤椎体水泥填充<50%以及水泥未与椎体上下终板接触,这都是骨水泥注射质量不好的体现。因而后续还需开发评估并改善骨水泥向椎体内扩散的数量及质量的技术,从而提高PV预防病理性骨折的能力。
2 影像学预测
2.1 X线
X 线是临床应用最广泛、操作最简单、成本最低廉的一种成像方法。X 线可以显示脊柱的整体结构以及是否存在脊柱力线的异常(如后凸、侧弯、椎体移位等),但仅对直径大于1 cm的病灶敏感性较高,并且脊柱解剖结构复杂,在X线片上相互重叠,因而对一些解剖结构复杂部位的肿瘤显示不佳,尤其是累及附件、下颈椎和上胸椎的肿瘤,因此X 线难以用于肿瘤的定量测量。X线还在测量BMD方面具有一定的应用价值。双能X 线吸收法(dual energy X-ray absorptiometry,DXA)是目前测定BMD 的金标准[36],DXA 与骨折风险评估工具(fracture risk assessment tool,FRAX)[37]等相结合可以更加准确地预测骨折。然而DXA 成本较高,多用于骨质疏松症患者的BMD 筛查,不是脊柱转移瘤的常规检查,因此少有研究者使用高成本的DXA来研究BMD与病理性骨折的相关性。DXA在监测脊柱转移瘤治疗后BMD 的动态变化有一定的价值。我们需要开发其他成本低且方便的影像学预测工具。
2.2 计算机断层扫描(computed tomography,CT)
CT是评估脊柱骨性结构的最佳成像技术,分辨率高,可提供大量局部解剖的情况。CT可以较为准确地识别骨破坏的类型(成骨、溶骨、混合性)和肿瘤的边界,可以明确肿瘤在髓腔和周围软组织的浸润范围,还可以进行多种定量测量如肿瘤体积、椎体塌陷的高度等,还能进行图像三维重建、多平面成像,有助于评估皮质骨的破坏情况。
定量CT (quantitative computed tomography,QCT)是一种测量平均体积BMD (g/cm3)的方式。QCT 可以将骨皮质和骨小梁分离开来,提高了BMD 测量的准确度和敏感度。此外,QCT 还可与有限元模型结合,将有限元的弹性模量与CT 图像的灰度值相关联,赋予模型不同的材料特性,从而可以模拟肿瘤的大小和位置、BMD、载荷等对骨折风险的影响。既往研究中有限元模型与尸体实验测定结果显示出良好的一致性[38],体现了其临床应用的价值。与传统的尸体实验相比,该方法具有可重复性高、价格低廉的优势。
CT 参数响应映射(parametric response mapping,PRM)是一种基于体素成像的图像分析技术,可以分析不同时期同一体素平均CT 值的变化情况,近似代表BMD 的动态变化。Hoff等[39]使用了PRM回顾了5例乳腺癌脊柱转移患者,发现发生病理性骨折的椎体6 个月内CT 值增加的体素百分比(12.9%±11.6%)远大于正常对照组(2.3%±2.5%)(AUC=0.918),说明病变椎体局部BMD 快速升高可以预测骨折。该方法的优点是对局部的骨密度变化较为敏感,避免了测量整体骨密度时对局部变化的掩盖,缺点是需要进行两次CT 图像各体素的一一匹配,需要对患者进行长期随访,实际操作较为困难。
2.3 磁共振成像(magnetic resonance imaging,MRI)
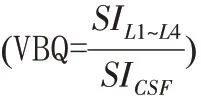
2.4 机器学习
机器学习的目标是研究计算机如何模拟人类学习行为,以获取新的知识和技能,并重新组织已有的知识结构使之不断改善自身,以应用在新数据的做预测的任务。机器学习在影像学中的应用是近年来发展的热点,目前尚无研究用于脊柱转移瘤病理性骨折的预测,但已有研究使用机器学习来预测其他部位或其他类型的骨折。
Muehlematter 等[41]利用机器学习和纹理分析对58 例脊柱机能不全骨折患者的连续两次CT 扫描图像进行评估,结果显示,联合29 个纹理参数特征的支持向量机(support vector machine,SVM)分类器识别出脊柱机能不全的患者的AUC可达到0.97。Oh等[42]纳入了84例接受CT扫描并随访3个月以上的肺癌股骨近端骨转移的患者,提取了16 种临床和影像学特征,将特征标准化后,使用5 种监督学习分类器进行训练,结果发现梯度提升(Gradient boosting,GB)算法预测能力最好,其AUC能达到0.80±0.14。
Wang等[43]收集了1143名骨转移瘤患者的临床和影像学数据,使用机器学习来预测骨骼相关不良事件(skeletal-related events,SREs),发现用使用8个变量的SVM分类器来预测SREs的准确性能达到97.1%,而当使用9个变量的逻辑回归模型预测SREs 的准确性仅为79.2%,这说明机器学习能够用更少的变量更准确地预测SREs。
在医疗大数据时代,机器学习在处理大数据的能力已展现出日益增加的优势。在已发表的文章中,可以看到机器学习在预测骨质疏松性骨折、股骨转移瘤病理性骨折、骨转移瘤SRE 等多因素事件中的预测价值。机器学习在脊柱转移瘤的应用较少的原因可能是脊柱转移发病率偏低、预后差、患者失访率高导致数据量不足。未来可以进行多中心研究,利用机器学习开发脊柱转移瘤病理性骨折的预测模型,识别出需要提前干预的人群。
3 总结与展望
脊柱转移瘤发病率的不断上升和肿瘤患者生存期延长使病理性骨折的发病率越来越高,如何降低此类并发症的发生,改善患者的晚期生存质量,越来越受到现代医学的重视。识别高危患者并对高危患者进行预防性治疗是历年来一直存在的难题。本文回顾了脊柱转移瘤病理性骨折的危险因素及X线、CT、MRI、机器学习等影像学预测方式,但大多影像学预测方式均仅用于科研,未广泛应用于临床。目前需要解决的是成本、对不同人群的普适性、预测的准确性等问题。既往大多数研究都仅仅是“发现”了危险因素,却没有对危险因素进行“量化”,因此对临床医师的价值也有限。现在临床上常用的预测工具是SINS 量表,但部分既往研究发现其中的一些项目准确性不高。因此未来需要发现并量化更有效的危险因素。在多因素事件预测中,机器学习与传统统计学方法相比,能够用更少的变量达到更高的准确性,因此,发现脊柱转移瘤病理性骨折的危险因素及影像学预测因子,并通过机器学习手段构建预测模型,可能会成为未来的研究方向。
作者利益冲突声明:全体作者均声明无利益冲突。
