卡培他滨维持治疗对复发转移性三阴乳腺癌疗效的meta分析
2021-05-04石印青杜立新韩丽炘
黄 玉,石印青,杜立新,韩丽炘
(1.山西大同大学医学院,山西大同 037009;2.大同市第三人民医院普通外科,山西大同 037000)
乳腺癌的发病率居我国女性恶性肿瘤之首,三阴性乳腺癌(triple negative breast cancel,TNBC) 指雌激素受体(ER)、孕激素受体(PR)和人表皮生长因子受体2(Her−2)均为阴性的乳腺癌。具有年轻化、侵袭性强、生存率低、预后差的特点,是乳腺癌研究的热点和难点之一。尽管TNBC占乳腺癌比例不到20%,但与其他病理亚型相比,更易发生转移,尤其是内脏器官的转移,导致TNBC在5年内乳腺癌相关性死亡中所占比重越来越大[1]。对于复发转移性TNBC目前尚无标准治疗方案,给临床医生带来了巨大挑战。卡培他滨(Xeloda/capecitabine,希罗达,简写X)具有给药方便、细胞毒性小、易于吸收、抗肿瘤活性强等优点,近年来国内外学者将其广泛应用于复发转移性乳腺癌维持治疗中。本研究采用Meta分析的方法对国内外研究结果进行二次综合分析,以期为复发转移性三阴乳腺癌患者的治疗和预后干预提供循证医学证据。
1 资料与方法
1.1 文献检索与资料收集
1.1.1 文献检索
采用计算机检索中国知网(CNKI)、维普数据库(VIP)、万方数据库(Wanfang data)、中国生物医学文献数据库(CBM)、Medline、EMbase、National technical in⁃formation service(NTIS),检索时限均为建库至2019年12月,文种限中、英文,查找有关X维持治疗复发转移性三阴乳腺癌的临床研究。中文检索词为三阴乳腺癌、卡培他滨、复发转移、维持治疗;英文检索词为Triple negative breast cancer,Capecitabine,Recurrence and metastasis,Maintenance treatment。
收集资料主要包括:①纳入研究的基本信息,包括第一作者、发表时间、研究类型等;②研究对象的特征,包括样本总数、试验组和对照组例数、患者的年龄、治疗方案、疗效评价、随访时间、结局等。
1.1.2 文献纳入与排除标准
文献纳入标准:①研究设计:复发或转移的TN⁃BC进行X维持治疗的临床随机对照试验(random⁃ized controlled trial,RCT);②研究对象:经病理学或细胞学证实为TNBC的女性患者,年龄≥18岁,卡氏评分(KPS)≥70分,无严重内科疾病,无化疗禁忌症,有可测量或可评价的病灶,治疗过程中不能包括同步的放疗或者内分泌治疗,患者本人及家属同意,剔除研究对象中包括其他癌症的RCT;③干预措施:干预组一线X联合化疗4~8周期后,继续X单药进行维持治疗,至疾病再次进展或不能耐受;对照组一线X联合化疗4~8周期后病情缓解至稳定后停止化疗或支持治疗,定期随访。
文献排除标准:①重复发表;②数据资料有误、不完整或未提供充分原始数据且搜索无果;③样本量<10,或失访率>20%;④综述、病例报告、文摘、讲座、会议摘要,缺乏全文。
1.2 结局指标
(1)近期有效率
根据WHO实体瘤疗效评价标准(RECIST)进行疗效评价,CR(complete response,完全缓解)指所有目标病灶消失;PR(partial response,部分缓解)指基线病灶最大径之和减少至少30%;SD(stable disease,疾病稳定)指基线病灶最大径之和介于PR和PD之间;PR(progresive disease,疾病进展)指基线病灶最大径之和增加至少20%或新发病灶出现。客观缓解率(objec⁃tive response rate,ORR=(CR+PR)/总人数×100%);肿瘤控制率(disease control rate,DCR=(CR+PR+SD)/总人数×100%)。
(2)总生存期(overall survival,OS)
从随机分组开始至(因任何原因)死亡的时间。
(3)无病生存期(disease−free survival,DFS)
从随机分组开始至疾病复发或(因任何原因)死亡之间的时间。
(4)疾病无进展生存期(progression−free survival,PFS)
指从随机分组之日起至疾病进展或死亡的生存时间。
(5)不良反应
主要包括文献中的骨髓抑制、胃肠道反应、肝肾功能损害、手足综合征等。
1.3 文献质量评价
1.3.1 文献提取
由2名独立研究人员对每篇RCT按照纳入和排除标准进行审查和评价,其中包括研究作者、发表时间、病例数、年龄、肿瘤期别、干预措施、生存率、复发率等,确定符合入选标准的文献。如存在分歧可探讨或请第3人协商从而达成共识。
1.3.2 偏倚风险评估
文献质量评价按照Cochrane系统评价手册[2]。对各独立研究从7个方面进行质量评估,以考察各个研究是否存在偏倚及其影响程度:①随机分配方案的产生;②分配方案隐藏;③对患者和医生实施盲法;④对结果评价实施盲法;⑤结果数据的完整性;⑥选择性报告结果;⑦其他偏倚来源。依据评价结果,将纳入文献分为“高风险”、“低风险”和“情况不明”。
1.4 统计学分析
采用RevMan5.3版软件分析,二分类变量数据,ORR、DCR等采用相对危险度(relative risk,RR)及其95%CI为效应分析统计量。首先通过卡方检验进行异质性检验,若P≥0.1和I2 ≤50%具有同质性,选用固定效应模型分析;若P<0.1,I2>50%有异质性,分析原因,可选择随机效应模型;最后对纳入研究数≥10的结局指标采用漏斗图判断及Egger's检验是否存在发表偏倚,即评价漏斗图的对称性,以P=0.05为检验水准。
2 结果
2.1 纳入文献研究的一般特征
文献筛选流程及检索结果初检出相关文献191篇,剔除重复、不完整文献87篇,阅读题目及摘要剔除33篇,阅读全文剔除48篇,最终定性定量综合分析纳入9篇国内外已发表的有关卡培他滨维持治疗的随机对照临床研究[3−11],共计1 491例患者,其中干预756组例,对照组735例,8篇中文发表,1篇英文发表。文献筛选流程及结果见图1。
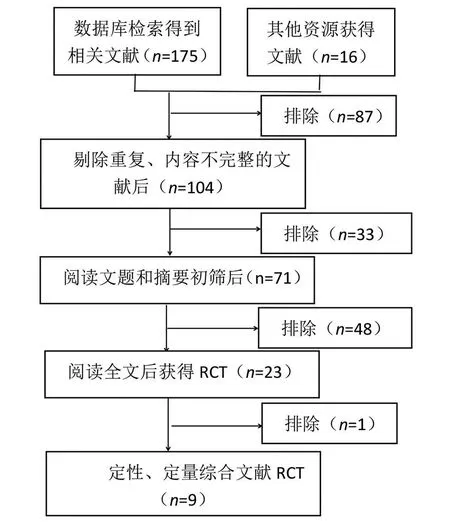
图1 文献筛选过程
2.2 纳入研究质量评估
根据Cochrane协作网推荐的偏倚风险评估方法,纳入的9项研究基线均具有可比性。在随机分组方面,所有纳入研究均提及“随机”,其中5篇采用随机数字表法,判定为“低风险”,余4篇未提及具体随机方法,结合文中信息也未能判定随机的真假,判定为“风险不明”;所有纳入研究均未报道是否实施分配隐藏与盲法,从文中信息也未能得出合理判断,因此判定为“风险不明”;所有纳入研究信息完整,均无选择性报告,判定为“低风险”;所有RCTs均因信息不足而无法判断是否有其他偏倚来源,故均判定为“风险不明”。总体而言,纳入研究整体质量不高,纳入研究偏倚风险结果见图2。
2.3 有效性和安全性指标
2.3.1 ORR
[4−10]、[12]等8项研究报道了患者客观缓解率情况,各研究间存在一定的异质性,采用随机效应模型合并效应量分析,结果显示,X维持治疗组提高患者的客观缓解率(均值差异检验Z检验,P<0.05),见表1。

图2 纳入研究风险偏倚评价
2.3.2 DCR
8项研究报道了肿瘤控制率,各研究间存在统计学异质性,采用随机效应模型合并效应量分析,结果显示,X维持治疗组提高了患者的肿瘤控制率(均值差异检验Z检验,P<0.05),见表2。

表1 客观缓解率的结果
2.3.3 OS
本研究共2篇文献均报告了OS,但只有1篇提供了HR、95%CI和生存曲线,另1篇仅提供了OS所占百分比,无法提取HR和95%CI,只作描述性分析。LLUCH等[10]发现X维持治疗组和对照组的患者5年OS分别为86.2%(95%CI,82.9%~89.4%)和85.9%(95%CI,82.4%~89.3%),无显著统计学差异(P>0.05;HR=0.92;95%CI=0.66~1.28;P=0.623),而容景瑜等[1]认为X维持治疗组和对照组的患者1年OS和2年OS差异是有统计学意义的(P<0.05)。

表2 肿瘤控制率的结果
2.3.4 DFS
有1篇文献报告了DFS,提供了HR、95%CI和生存曲线,仅提供了平均PFS或中位PFS,未提供HR、95%CI和生存曲线,仅作描述性分析。Lluch等发现X维持治疗组和对照组的患者5年DFS分别为79.6%(95%CI=75.8%~83.4%)和76.8%(95%CI=72.7%~80.9%),无显著统计学差异(P>0.05)。
2.3.5 PFS
共8篇文献报告了PFS,仅提供了平均PFS或中位PFS,未提供HR、95%CI和生存曲线,故无法提取HR和95%CI进行meta分析。采用描述性分析,8项研究均认为X维持治疗组能够延长PFS。
2.3.6 不良反应
对纳入的8项[3−5,7−11]研究均报道了毒副反应,但缺乏对照组的毒副反应情况,故无法进行Meta分析。但8项研究结果均表明X维持治疗组的患者主要毒副反应包括骨髓抑制(42.7%)、消化道反应(40.3%)、肝肾功能异常(41.9%)、手足综合征(57.9%),I~Ⅱ级的毒性占的比例比较多,而发生Ⅲ~Ⅳ级的比例极少或没有。其中I~Ⅱ级骨髓抑制占93.6%,I~Ⅱ级消化道反应占95.4%,I~Ⅱ级肝肾功能异常占99.0%,I~Ⅱ级手足综合征占98.3%,均可耐受或经过对症处理后好转,未发生治疗相关的死亡病例。
2.4 敏感性分析与发表偏倚分析
本研究纳入研究的数量有限,数量<10篇,敏感性分析与发表偏倚分析意义有限,故未进行此项分析。
3 讨论
由于对内分泌治疗及抗Her−2治疗不敏感,化疗是TNBC的主要治疗手段,复发转移性TNBC多数已经对蒽环或紫杉类药物耐药。X属于氟尿嘧啶类,在晚期乳腺癌全程治疗中发挥着重要作用,近年来国内外学者将其应用于复发转移性TNBC维持治疗取得了一定的研究成果。绝大多数研究[1,12−13]表明X维持治疗可以提高临床疗效,有效控制病情进展,从而延长患者的生存周期,提高生活质量,本研究结果显示X维持治疗组与对照组比较,ORR和DCR均有统计学差异,可显著提高患者近期疗效,与Chen等研究结果一致。
文献[11]报道了DFS,发现X维持治疗组和对照组5年DFS无统计学意义,与上述结果一致;有两篇文献报道了OS,Lluch等[10]发现X维持治疗组和对照组的患者5年OS无显著统计学差异,而容景瑜等[3]认为X维持治疗组和对照组的患者1年OS和2年OS差异是有统计学意义的(P<0.05)。由此可见,X维持治疗在改善DFS和OS等生存时间方面还存在争议,有待临床进一步研究和探讨。
X在复发转移性TNBC的维持治疗过程中出现不良反应主要有[14]:骨髓抑制、消化道反应、肝肾功能损害、手足综合征,且以I~Ⅱ级的毒性为主。本研究结果与上述结果一致,均表明X维持治疗不良反应小,患者耐受性较好,安全性高。鉴于本研究纳入的关于X维持治疗的原始研究质量普遍偏低;其次,由于X联合化疗方案不统一,且维持治疗的剂量、时间不一致等因素的制约,一定程度上影响了Meta分析的质量。
综上所述,X维持治疗治疗可使复发转移性TN⁃BC临床获益,改善近期疗效,且不良反应可耐受,安全性较高。但由于目前RCTs总体质量较低,尚需更多大样本、多中心的高质量研究对DFS、OS、PFS等远期治疗效果予以验证。
