CyberKnife系统中肝癌计划实施剂量计算及验证的评价研究
2021-04-23
解放军总医院第一医学中心 放射治疗科,北京 100853
引言
肝癌是全球第五大最常见的肿瘤,是癌症相关死亡的第三大原因[1-2]。手术切除是目前最为有效的治疗方法,但满足外科手术切除条件的患者较少[3]。近年来,随着计算机和医学影像学的发展,精确放射治疗在肝癌的总和治疗中取得了一定的作用。肝脏属于运动器官,上下活动的范围大约为2 cm,常规放射治疗会导致肿瘤“脱靶”现象,导致正常肝脏组织受到不必要的照射,容易引起肝损伤,而且肿瘤组织出现欠量[4],造成肿瘤复发。CyberKnife(CK)可以通过金标植入,采用红光同步呼吸追踪系统、实时影像引导等功能改善治疗范围,并且最大限度的避开了毗邻的放射敏感器官肠道、胃、十二指肠等,提高了肿瘤局控率、生存率,降低了毒副反应。
CK系统作为新型的立体定向放射外科治疗设备,代表着肿瘤立体定向放射治疗的进步[5-7]。CK治疗计划系统(MultiPlan®)配置有射线追踪(Ray-Tracing,RT)和蒙特卡罗(Monte Carlo,MC)两种算法,二者剂量计算的结果存在一定的差异[8-9];通常认为MC算法作为剂量沉积计算的金标准,其剂量计算准确性更高。但是由于计算效率、硬件等因素的影响,目前国内外CK系统的临床应用中用户普遍更多采用RT算法,并未普遍采用MC算法,且对于不同临床需求中采用何种算法缺乏明确的界定和数据支持。本研究回顾性分析33例肝癌患者两种算法剂量计算及计划验证的差异,分析和评估其准确性、可靠性,从而为不同算法在临床应用中的选择提供一定的参考依据。
1 资料与方法
1.1 临床资料
本研究选取2018年1月至2019年12月在本院就诊的肝癌患者33例,其中男性26例,女性7例。年龄33~86岁,中位年龄64岁。患者基本情况如表1所示。

表1 33例肝癌患者资料
1.2 仪器设备
采用德国SIEMENS放疗专用大孔径模拟定位CT和GE定位MRI;图像融合和轮廓勾画工作站(MIM MaestroR,6.9.5版本);德国PTW公司UNIDOS webline型静电计、PTW 31010(0.125cc)型电离室和固体水;美国ISP公司EBT3胶片。CK数据管理系统(CyberKnife Data Management System,CDMS)和治疗计划系统MultiPlan®(4.0.2)。
1.3 患者体位固定及靶区和危及器官勾画
在CK治疗定位前约一周在CT引导下经皮肝脏于肿瘤内部或肿瘤附近植入3~6枚金标,作为肿瘤定位及治疗追踪的参考系统。待金标的位置相对稳定后,采用真空垫固定并行CT、MRI定位扫描,扫描范围从膈顶上10 cm至右肾下界,层厚1 mm,扫描完成后将图像经过网络传输至MIM工作站,由临床医师勾画GTV,并勾画重要危及器官包括正常肝组织、心脏、脊髓、胃和十二指肠、小肠、结肠肝区、胰腺、肺、肾脏等。
1.4 计划设计
采用非等中心、非共面照射模式,按照靶区2/3最大径尺寸选择相应大小限光筒,同时选择一个比其小1~2档的另一个较小尺寸限光筒[10]。所有患者都采用Sequentia模块进行计划优化,在计划优化过程中,为提高治疗计划实施效率,设置好每例计划最大单野MU值,计划的总跳数等参数。优化完成后,将计算框覆盖范围拉大,使之包括所有CT扫描体素。为了方便比较两种算法的剂量学差异,首先采用高精度计算网格的RT算法进行精算,记录肿瘤靶区和危及器官的各项剂量指标,然后保持所有计划参数不变,采用MC进行重新精算,不确定度设置成1%。处方剂量统一设定为50/5F,处方剂量线设为70%。
1.5 计划评估
治疗计划设计完成后,通过等剂量曲线分布对各组计划进行评估,通过剂量体积直方图(Dose Volume Histogram,DVH)获取靶区及各危及器官相关剂量学参数,其中靶区剂量评估包括靶区剂量体积参数D98、D95、D90、D50、D10、D5,剂量分布的均匀性指数(Homogeneity Index,HI)、适形度指数(Conformal Index,CI)、新适形指数(New Conformal Index,nCI)、靶区外正常组织剂量跌落梯度参数(Gradient Index,GI),GI意义在于反映靶区外的剂量跌落情况,较小的GI表示靶区外剂量扩散较少,剂量跌落急剧[11]。对于危及器官的评价主要参考AAPM 101号报告的剂量限值[12]。
1.6 验证计划的设计与实施
选取10例已完成计划移植到PTW固体水模体,首先采用RT算法的高精度计算网格行精算。考虑到免冲洗EBT3胶片只能采集0.1~1000 cGy剂量范围的限制,计算时将Scale值设为0.7,对剂量进行比例缩放的降低,保证胶片中计算的剂量小于1000 cGy,排除因剂量过高引起的测量误差。计算完成保存后采用MC算法,将不确定度设为1%重新精算,精确计算完成后对QA计划进行保存。
执行验证计划,记录剂量仪读数,从模体中取出胶片并记录好患者姓名和照射完成时间,在照射完成24 h扫描胶片得到测量的平面剂量分布。将电离室测量的点剂量分别与RT和MC两种算法计算的点剂量进行比对,得到相应的误差值。将胶片采集到的实测剂量图像导入到FilmQA Pro 2016胶片分析软件中,采用2%/2 mm、3%/2 mm两种评价标准组合分别与两种算法得到计划剂量分布进行Gamma分析,定量评价两种算法的计算差异。
1.7 统计学方法
所有计划完成后通过DICOM协议传输至MIM工作站进行数据读取。采用SPSS 19.0软件对计划进行数据分析,首先检验样本数据是否服从正态分布,若满足正态分布对两种算法计算结果的参数比较采用配对t检验分析。数据结果用均值±标准差(±s)表示,P<0.05代表差异具有统计学意义。
2 结果
2.1 肝癌剂量分布比较
如图1所示的剂量分布可以看出两种算法处方剂量均能实现较好的靶区覆盖,且靶区外剂量跌落均能满足临床治疗的要求。
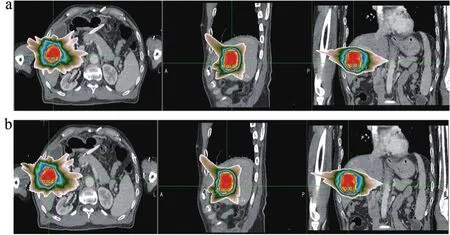
图1 肝癌部位两种算法同一病例计划等剂量曲线分布图
2.2 肝癌病例DVH结果的比较
图2是33例肝癌病例靶区平均DVH比较结果的显示。从图中可以看出使用MC算法计算对比后RT算法略微低估靶区剂量,但差异不大。比较图3左叶肝癌平均DVH和图4右叶肝癌平均DVH可以看出,左叶肝癌两种算法靶区覆盖率差异相对较小,但右叶肝癌靶区覆盖率差异相对较大。对于平均剂量,经计算,左叶肝癌靶区RT算法的平均值为58.21 Gy,MC算法的平均值为57.76,两者相差0.45 Gy(0.78%);右叶肝癌RT算法的平均值为55.82 Gy,MC算法的平均值为54.60 Gy,两者相差1.22 Gy(2.23%)。

图2 肝癌病例靶区平均DVH

图3 左叶肝癌靶区平均DVH

图4 右叶肝癌靶区平均DVH
2.3 肝癌靶区剂量学结果的比较
肝癌病例RT和MC两种算法靶区剂量学比较的结果,见表2。其中,两种算法计算结果对于靶区较大体积剂量参数D98、D95、D90,以及靶区小体积剂量参数D5、D10和50%体积剂量参数D50,MC较RT算法都降低,且差异具有统计学意义;以MC算法计算结果为基准,肿瘤靶区最大剂量和处方剂量的平均值,RT算法低0.71 Gy(0.98%),差异具有统计学意义(P<0.05);靶区平均剂量RT算法高0.62 Gy (1.09%),差异有统计学意义(P<0.05);靶区覆盖率RT算法高1.90%(2.59%),差异具有统计学意义(P<0.05);适形指数CI的平均值,RT算法高0.03(2.54%),具有统计学差异(P<0.05);均匀性指数RT算法降低,差异有统计学意义(P<0.05);梯度指数GI平均值RT算法低0.09(2.59%),差异具有统计学意义,新适形指数nCI无明显差异。
表2 肝癌两种算法靶区剂量学比较的结果(±s)

表2 肝癌两种算法靶区剂量学比较的结果(±s)
参数 RT计划 MC计划 t值 P值Dmax/Gy 71.43±0.00 72.14±1.38 -2.97 0.010 Dmin/Gy 23.42±7.26 22.77±7.29 6.29 <0.001 Dmean/Gy 57.71±2.98 57.09±3.12 4.38 <0.001 Coverage 84.10±8.01 82.53±8.88 4.57 <0.001 D98/Gy 36.72±6.74 36.29±6.81 3.89 <0.001 D95/Gy 41.85±5.93 41.40±5.94 3.81 <0.001 D90/Gy 46.52±4.97 46.03±4.96 3.85 <0.001 D50/Gy 59.30±3.13 58.64±3.32 4.80 <0.001 D10/Gy 66.30±2.44 65.66±2.64 3.77 <0.001 D5/Gy 67.49±2.02 66.91±2.29 3.28 <0.001 CI 1.21±0.16 1.18±0.15 6.83 <0.001 nCI 1.45±0.23 1.46±0.23 -0.47 0.640 HI 1.43±0.00 1.44±0.03 -2.97 0.010 GI 3.38±0.60 3.47±0.69 -3.92 <0.001
2.4 肝癌危及器官剂量学结果的比较
肝癌病例RT和MC两种算法危及器官剂量学比较的结果,见表3。从表中可以看出,采用MC算法重新精算后,食管、胃、脊髓、肠道、十二指肠及肝脏的平均剂量均有所降低,差异有统计学意义(P<0.05);食管、胃、脊髓、肠道、十二指肠和肝脏0.35 cm3和5 cm3体积的剂量均降低,差异有统计学意义(P<0.05)。
表3 肝癌病例危及器官剂量学比较的结果(±s)

表3 肝癌病例危及器官剂量学比较的结果(±s)
器官 参数 RT计划/Gy MC计划/Gy t值 P值食管Dmax 15.48±9.02 15.26±8.73 1.16 0.28 Dmin 3.37±2.91 2.81±2.81 4.71 <0.001 Dmean 7.77±4.93 7.33±4.61 2.93 0.02 D0.35cc 12.72±6.97 12.25±6.63 2.96 0.02 D5cc 7.17±5.99 6.77±5.61 2.49 0.04胃Dmax 21.25±6.99 21.29±6.89 -0.31 0.76 Dmin 1.07±0.81 0.53±0.47 5.67 <0.001 Dmean 5.69±2.95 5.32±2.73 3.87 <0.001 D0.35cc 18.23±5.95 17.88±5.84 3.34 <0.001 D5cc 14.03±4.69 13.58±4.53 4.52 <0.001肠道Dmax 23.06±7.19 23.14±7.07 -0.80 0.43 Dmin 0.86±0.52 0.30±0.27 6.36 <0.001 Dmean 5.02±2.47 4.69±2.40 4.64 <0.001 D0.35cc 19.32±5.44 19.08±5.48 2.61 0.02 D5cc 14.15±3.54 13.84±3.46 5.33 <0.001十二指肠Dmax 17.32±8.22 17.12±8.26 1.05 0.31 Dmin 1.52±0.96 0.95±0.63 3.84 <0.001 Dmean 6.19±3.13 5.84±3.06 2.73 0.01 D0.35cc 13.72±6.59 13.34±6.49 2.51 0.02 D5cc 8.18±5.36 7.85±5.19 2.57 0.02脊髓Dmax 9.16±4.91 9.01±4.55 1.60 0.12 Dmin 1.12±1.12 0.48±0.66 5.30 <0.001 Dmean 3.59±2.81 3.15±2.45 5.17 <0.001 D0.35cc 7.95±4.50 7.59±4.17 4.20 <0.001 D5cc 5.72±3.97 5.35±3.62 4.61 <0.001 Dmax 65.71±13.03 68.05±7.57 -1.29 0.21 Dmin 0.94±0.71 0.34±0.26 6.42 <0.001 Dmean 11.62±5.59 11.28±5.53 4.22 <0.001 D0.35cc 0.57±0.25 0.55±0.23 2.72 0.01 D10cc 0.36±0.19 0.35±0.19 2.24 0.03肝脏
2.5 肝癌计划验证结果的比较
10例肝癌患者在固体水测量结果的平均值,见表4。将RT和MC剂量计算结果分别与电离室测量值进行比较。可以看出,两种算法剂量计算值与电离室测量值之间的平均差异在3%以内。对于平面剂量,MC算法采用2%/2 mm和3%/2 mm标准的平均γ通过率分别为95.38%和97.24%,RT算法通过率分别为91.26%和93.77%。

表4 肝癌计划验证测试结果
3 讨论
自CK问世以来,治疗计划的计算方法得到了实质性的发展。最初,RT算法是CK治疗计划系统唯一配置的算法,该算法模型相对简单,仅对单一路径长度上的光子校正来计算剂量沉积的特性,中心轴有效深度计算考虑了组织的异质性,并对预期的剂量分布作了进一步的调整,整个模拟计算过程需要复杂的近似和必要的简化。虽然这些方法对于处理相对均匀的组织结构和较大的辐射野是足够的,但在精度上确实存在局限性。特别是在对高异质性组织区域的剂量分布进行建模时,RT算法无法考虑自由电子的横向分布、散射和最终剂量沉积的变化,从而导致对沉积剂量的高估[13-15]。此外,由于CK治疗采用小照射野聚焦照射的方式,精确的模拟射野边界的电子不平衡对于预测剂量沉积就显得尤为必要[16-18]。
由于RT和MC算法计算的准确性主要与人体器官组织的密度差异相关,查阅国内外相关文献资料,大都是针对人体组织密度差别最明显的胸部肿瘤进行比较研究[19-20],而对于腹部肿瘤肝癌却鲜有报道。
本研究入组了33例肝癌患者的临床资料,回顾性地分析比较了RT和MC算法在靶区和危及器官方面的剂量学差异性。实验结果表明,靶区PTV无论大体积的剂量还是小体积的剂量都没有统计学意义。危及器官的比较显示,所有感兴趣器官的平均剂量和体积剂量都有所下降,所有差异都具有统计学意义。虽然肝癌病灶常常为实质性的软组织密度结构,但射线在到达靶区之前通常会穿过肺组织和胃肠道等密度不均匀的空腔组织,从而导致MC计算后靶区剂量的降低[21]。对MC算法计算得到的结果分析发现,光子在低密度机构组织中实际能量的沉积低于RT算法得出的计算结果,所以危及器官食管、胃、十二指肠、空回肠等包含空气的部分,经过MC计算得到的剂量结果低于RT算法计算的剂量分布。
CK治疗方式为非共面小野集束照射,小野照射过程中射束容易出现电子不平衡现象[22],测量时极易受到探测器介质和其体积的干扰,带来临床剂量计算及评估的困难。另外,CK患者验证还需要成熟的胶片分析软件及大量的胶片,花费较为昂贵。长期以来,大多单位都没有建立统一的CK患者计划验证规范。
本研究选择10例肝癌经典病例采用固体水对两种算法的治疗计划进行验证,将RT和MC剂量计算结果分别与测量值进行比较。研究表明两种算法在肝癌患者中计算的剂量具有较好的一致性。
综上所述,本研究通过肝癌典型病例计划设计,分别采用两种算法进行剂量的计算,并对两组剂量计算的结果进行对比及测量验证,分析比较两种算法的剂量学差异,评估其准确性、可靠性。结果表明RT算法在肝癌患者的计算精度是足够且适当的。
