细菌素-纳米金壳核结构的形成和特性表征
2021-04-22图尔荪阿依图尔贡葛达娥努尔古丽热合曼刘小莉
图尔荪阿依·图尔贡,王 帆,葛达娥,努尔古丽·热合曼,刘小莉*
(1 江苏省农业科学院农产品加工研究所 南京210014 2 新疆师范大学 乌鲁木齐830054)
纳米金 (Gold nanoparticles,AuNPs)是直径在0.5~250 nm 范围的金超微粒子,具有独特的量子效应、小尺寸效应和极大的比表面积,与各种配体有相对较高的相容性,可以实现对生物大分子的精确定位,而且对生物系统没有毒害作用,因而作为药物传递载体在生物、医学等领域有广泛应用[1-3]。
金纳米颗粒的化学合成方法很多,最为简单和经典的是Turkevitch 等[4]在1951年发表的使用柠檬酸钠作还原剂,巯基丙酸钠作稳定化配体的方法,然而,在Turkevitch 法制备纳米金过程中,容易出现AuNP 稳定性不好,发生聚集沉淀的现象[5]。许多学者普遍认为在纳米粒子合成过程中,添加蛋白质或肽类成分包裹在纳米粒子表面,生物蛋白分子作为“帽子”试剂与纳米颗粒形成核-壳结构,可以保护纳米颗粒,防止团聚,提高稳定性。目前很多研究者发现采用微生物代谢产物、植物提取物等作为还原剂和稳定剂制备纳米金[6-8],然而,培养微生物、准备植物浸提物过程比较繁琐、费时。
食品工业中微生物污染所引起的腐败变质非常普遍,解决这个问题最为简便有效的方法就是使用食品保鲜剂。化学合成防腐剂因潜在的毒性和致癌作用而受到广泛质疑,乳酸菌产生的细菌素一直被人们认为是化学合成防腐剂的理想替代品[9],如目前市场上广泛使用的乳酸链球菌素(Nisin)[10]。不论是乳酸链球菌素还是其它细菌素,虽对大多数革兰氏阳性菌(G+)有良好的抑制作用,但不能有效抑制革兰氏阴性菌(G-),而且有部分研究报道发现了抗性的G+菌株,其主要原因是保鲜剂不能穿透细胞壁或细胞膜进入细胞内部发挥抑菌作用。
纳米金具有很好的生物相容性[11],可渗透进入细胞内部[12]。如果将纳米金和细菌素结合,细菌素作为稳定剂帽子(capping agent)与纳米金形成壳核结构,纳米金携带细菌素协助其破坏细胞壁和细胞膜屏障,为细菌素进入细胞内部打开通道,发挥抑菌作用,则将是解决食品工业防腐问题的有效途径。本研究在柠檬酸还原法合成AuNPs 的基础上,在反应体系中加入前期研究获得的一种新型细菌素[13],通过单因素试验优化AuNPs 制备条件,通过测定反应体系紫外-可见光谱、表面电势、粒径大小、形状等分析制备条件对AuNPs-细菌素壳核结构合成的影响。采用透射电镜观察壳核结构产物与金黄色葡萄球菌、志贺氏菌混合后对细菌细胞膜的穿透能力,评估AuNPs 作为载体协助细菌素对食品腐败菌的抑制作用。
1 材料和方法
1.1 试验材料
1.1.1 材料与试剂 金黄色葡萄球菌(Staphylococcus aureus ATCC25923)、志贺氏菌(Shigella flexneri CMCC51606);LB 液体培养基;氯金酸(分析纯),上海麦克林生化科技有限公司;二水合柠檬酸三钠(分析纯),西陇化工股份有限公司。
1.1.2 仪器与设备 JG-05 型UV-vis 光谱仪,美国BioTeK 公司;ZS90 型Zeta 电位仪,英国Malvern 公司;100CXⅡ型透射电镜,日本日立公司。
1.2 试验方法
1.2.1 纳米金的制备 采用改良的Turkevitch 法制备AuNPs[4]。配制氯金酸储备液(0.34 g 氯金酸,于100 mL 纯水中溶解,浓度10 mol/L)以及二水合柠檬酸三钠储备液(4.05 g,溶解于100 mL 纯水中,浓度40 mol/L)。取玻璃试管,各取1 mL 氯金酸储备液和二水合柠檬酸三钠储备液,加8 mL 纯水,使氯金酸和二水合柠檬酸三钠终浓度分别为1 mol/L 和4 mol/L,加入10 mg/mL 新型细菌素。避光条件下在一定温度下水浴,直至溶液颜色变为紫红色。
1.2.2 纳米金制备条件的优化 设计单因素试验,分别在不同反应温度(30~100 ℃)、不同反应pH (4~10)、不同反应时间(10~60 min)下制备AuNPs-细菌素壳核结构产物,根据反应速率及肉眼观察纳米金溶液颜色变化初步判断纳米金最佳制备条件。
1.2.3 紫外-可见光谱分析 紫外-可见光谱被认为是检测金属纳米颗粒特征性表面等离子体共振(SPR)带的重要技术。将不同条件下制备的AuNPs-细菌素壳核结构产物分别进行紫外-可见光谱扫描,根据表面等离子体共振吸收峰值大小及其移动位置进一步确定最佳制备条件。设定扫描参数为波长200~800 nm,夹缝宽度1 nm,分析速度200 nm/min。
1.2.4 表面电势测定 将不同条件下制备的AuNP-细菌素复合物溶胶注入样品池,采用Zeta电位分析仪测定溶胶的表面电势、粒度分布和分散性指数。每样品测3 组表面电势,求平均值。
1.3 透射电镜表征
1.3.1 纳米金的透射电镜表征 吸取制备所得的AuNP-细菌素壳核结构产物滴到碳膜覆盖的铜网上,室温条件下自然晾干,采用透射电镜观察纳米金粒子的大小和形貌。
1.3.2 纳米金与细菌共培养的透射电镜观察 以金黄色葡萄球菌、志贺氏菌为指示菌,利用LB 液体培养基活化菌体,150 r/min、37 ℃条件下培养24 h,备用。取已活化的菌液2 mL 至离心管中,10 000 r/min 离心3 min,用PBS 缓冲溶液洗涤2~3 次收集菌体,加入1 mL AuNPs-细菌素复合物溶液,于200 r/min、37 ℃ 条件下放置6~8 h,5 000 r/min 离心收集菌体后加入2.5%戊二醛固定12 h,样品脱水后包埋,切片,经柠檬酸铅溶液和醋酸双氧铀溶液染色后,采用透射电镜观察。
1.4 数据分析
试验结果以重复性条件下获得的3 次独立测定结果的算术平均值表示,试验数据用Origin 8.5软件处理。
2 结果与分析
2.1 纳米金制备条件优化
紫外-可见光谱对高分散和缔合态存在的金属颗粒有完全不同的响应,通过分析其谱图,可以得到有关颗粒粒度和结构等重要信息[14]。研究发现,金属离子溶液在特定体系中被还原成纳米粒子后会产生不同颜色的纳米粒子溶胶,在特定波长范围内产生特征性等离子吸收峰,利用这一特性可快速检测纳米粒子的产生。而且吸收峰位置的蓝移或红移也能在一定程度上反映纳米粒径和形貌的变化。AuNPs 颗粒的等离子体共振分为横向伸缩振动与纵向伸缩振动,当AuNPs 为球形时,表现出横向伸缩振动,随着粒径的增大,最大吸收峰蓝移,AuNPs 溶液的颜色发生由深黄色-粉红色-酒红色-紫红色-蓝色-黑色沉淀的变化[15]。另外,Zeta 电位在确定纳米粒子在溶液中的稳定性和分散性方面被认为是一个重要的参数。在20世纪40年代,杨志等[16]提出了描述胶体稳定的理论,认为胶体体系的稳定性是当颗粒相互接近时它们之间的双电层互斥力与范德瓦尔互吸力的净结果。此理论提出当颗粒接近时颗粒之间的能量障碍来自于互斥力,当颗粒有足够的能量克服此障碍时,互吸力将使颗粒进一步接近并不可逆地黏在一起。Zeta 电位对分散体系的凝结稳定性和其流变性,以及界面和分散体系的相互作用有密切关系。Zeta 电位可作为胶体体系稳定性的指示。如果颗粒带有很多负的或正的电荷,也就是说很高的Zeta 电位,它们会相互排斥,从而达到整个体系的稳定性;如果颗粒带有很少负的或正的电荷,也就是说它的Zeta 电位很低,它们会相互吸引,从而达到整个体系的不稳定性。根据研究表明,当反应体系的分散性指数(PDI)越低时,体系稳定性越强[17-18]。
2.1.1 反应时间对纳米金合成的影响 Haiss等[19]的研究表明,金纳米颗粒在520~540 nm 可见光区域的吸收峰与纳米颗粒大小存在对应关系。从图1可以看出本研究中不同时间条件下纳米金溶液在520~525 nm 范围内具有最大吸收峰,反应体系的紫外-可见光谱没有发生明显的蓝移或者红移,说明反应时间的变化对纳米金的粒径影响不大。50 min 纳米金产量最大,60 min 产量反而下降。通过观察溶液颜色发现由深红色逐渐变成紫红色,50 min 开始出现聚集现象。随着反应时间的延长,Zeta 电位先增大后变小,反应时间到达30 min 时Zeta 电位到达最高绝对值45.3±4.36,平均粒径最小为38.86±0.52,平均多分散性指数最低为0.33±0.02(表1),其稳定性强,因此优选反应时间为30 min。
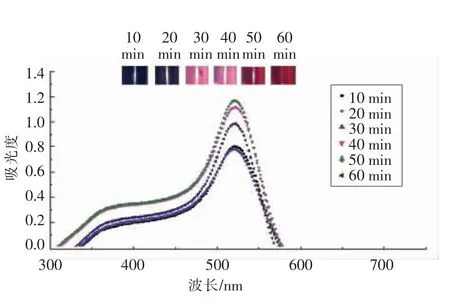
图1 不同反应时间对纳米金合成的影响Fig.1 Effect of different reaction times on the synthesis of AuNPs
2.1.2 pH 值对纳米金合成的影响 由图2可知,pH 5 条件下,吸光值达到峰值,且与其它pH 条件相比发生明显蓝移,可能得到的纳米金粒径较小。随着pH 的变大,纳米金发生聚焦,颜色依次由浅紫红色变深再变浅红色,在偏碱情况下反应体系中黑色沉淀增加,颜色透明。研究表明AuNPs 表面吸附的柠檬酸根负离子之间的静电斥力能够克服颗粒之间的范德华力而稳定存在于溶液中,此时AuNPs 在溶液中呈分散状态。当提高溶液碱性时,AuNPs 表面柠檬酸根离子所带负电荷将被中和,且随着pH 值上升,AuNPs 发生聚集的程度增加[20],试验结果与此理论相符。据表2所知,Zeta电位随pH 值增加呈现减小的趋势,同时纳米金平均粒径变大,吸收光谱值变大,出现聚集现象,合成的纳米金不稳定。在微酸性条件下金纳米颗粒平均粒径小,紫外-可见吸收光谱大,稳定性强。该结果表明微酸性系统中金纳米颗粒含量多,粒径小,反应体系较稳定。
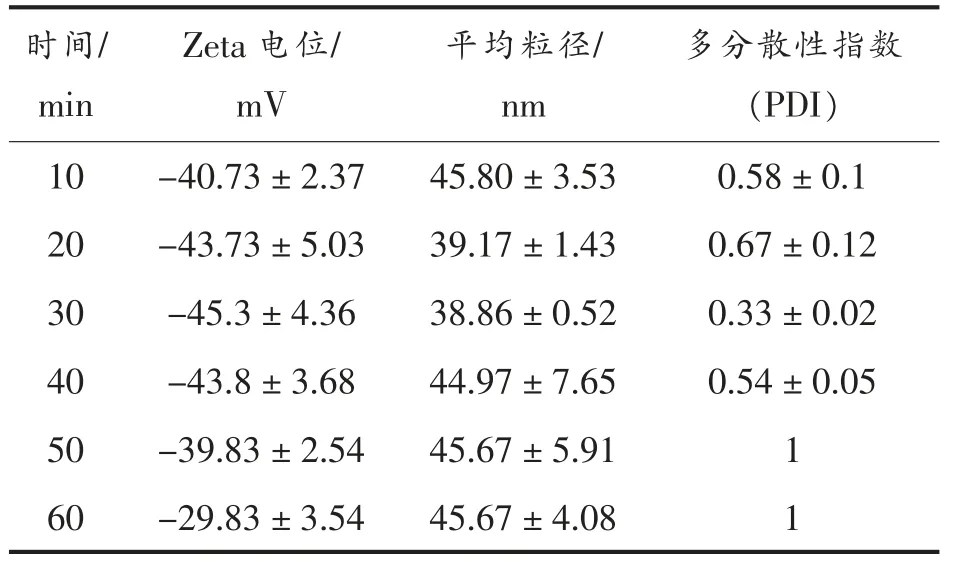
表1 不同反应时间对纳米金Zeta 电位的影响Table 1 Effect of different reaction time on the AuNPs Zeta point
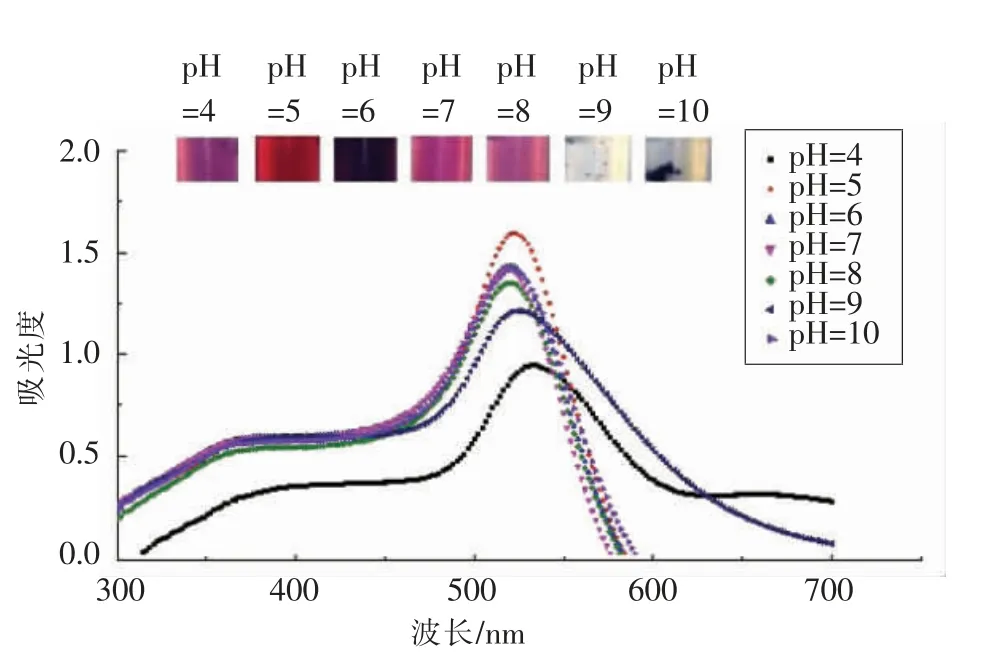
图2 不同反应pH 值对纳米金合成的影响Fig.2 Effect of different reaction pH on AuNPs synthesis
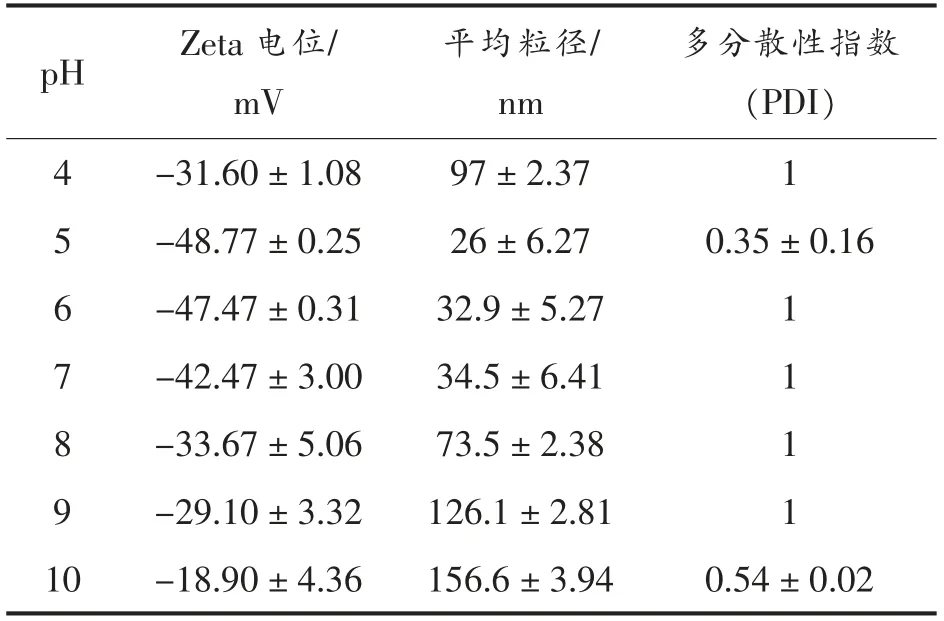
表2 不同反应pH 值对纳米金Zeta 电位分析的影响Table 2 Effect of different reaction pH on the AuNPs Zeta analysis
2.1.3 反应温度对纳米金合成的影响 反应温度对纳米金的合成影响较大。当温度范围在50~60 ℃时,纳米金产量差异不大,当温度上升到70 ℃,产量出现一个小的峰值,溶液颜色较深,出现黑色沉淀,纳米金聚集,之后随着温度进一步升高,产量下降,但当温度达到100 ℃时出现最大吸收峰,纳米金含量最多,而且曲线出现轻的蓝移,纳米金粒径减小。Zeta 电位也随温度升高呈现上升趋势,当温度达到100 ℃时,Zeta 电位值到达最高绝对值,平均粒径最小,多分散性指数低,表明纳米金稳定性最强,是最佳反应温度。
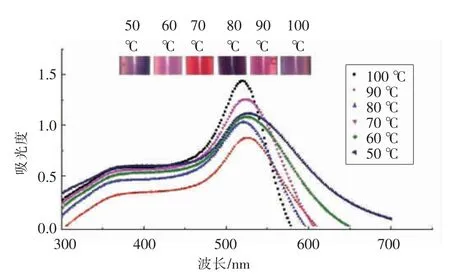
图3 不同反应温度对纳米金合成的影响Fig.3 Effect of different reaction temperatures on AuNPs synthesis
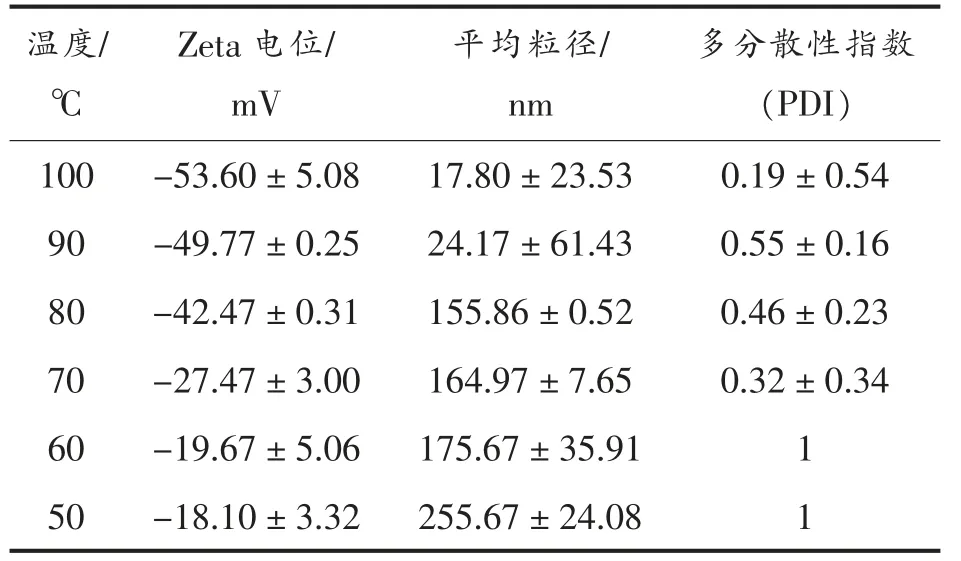
表3 不同反应温度对纳米金Zeta 电位的影响Table 3 Effect of different reaction temperatures on the AuNPs Zeta point
2.2 透射电镜表征
由于纳米金属粒子直径极微小,具有独特的量子效应、小尺寸效应和极大的比表面积,与各种不同的配体有相对较高的相容性[21],很容易进入细胞内[22]。图4为最佳制备条件下(温度100 ℃,pH 5,时间30 min)的纳米金TEM 照片,可看出纳米金均为球形,粒子粒径分布均匀,粒径范围为15~20 nm,溶液呈现酒红色。图5是AuNPs-细菌素复合物与两种食品腐败菌混合后的透射电镜图,如图所示,细胞壁结构发生紊乱,细胞膜被破坏,纳米金颗粒能够穿过细胞膜进入细胞内部,从而协助细菌素进入细胞。
3 结论
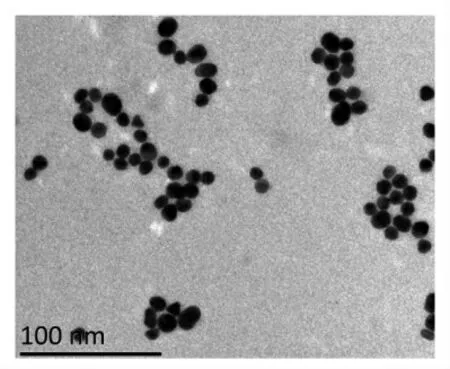
图4 纳米金透射电镜图Fig.4 TEM images of AuNPs

图5 纳米金与菌体混合的透射电镜图Fig.5 TEM image of AuNPs distribution in bacterial cells
本文在改良经典Turkevitch 法制备纳米金的基础上,在反应体系中加入细菌素作为纳米金的帽子试剂,增强纳米金粒子的稳定性,同时借助纳米金穿透细胞膜的特点协助细菌素进入腐败菌内部发挥抑菌作用。通过测定表面等离子共振吸收峰、表面电势、粒径等最后确定纳米金最佳制备条件为:反应体系pH 5,100 ℃反应30 min。在此条件下制备的纳米金经透射电镜检测粒径范围为15~20 nm,以革兰氏阳性菌金黄色葡萄球菌和革兰氏阴性菌志贺氏菌为指示菌,与AuNPs-细菌素复合物混合,透射电镜显示纳米金能渗透进入细菌细胞内部,为下一步利用纳米金协助食品防腐剂进入细胞内部发挥抑菌作用提供依据。
