广州地区老年失眠症患者的健康状况研究
2021-04-17方燕龄徐米清龚梅恩肖新怀宾灶华江幸钻姚建玲
方燕龄,徐米清,龚梅恩,肖新怀,宾灶华,江幸钻,姚建玲*
(广州医科大学附属第二医院 1老年科, 2心理科,广东 广州 510260)
近年来,我国老年人口不断增多,截止到2018年末60岁及以上老年人口已达2.5亿,约占全国人口的17.9%[1],预计到2040年该构成比将上升至28%[2],社会人口老龄化趋势日益显著。老年人的心身健康已成为全社会的关注焦点,其中睡眠障碍是常见问题之一。有研究显示约有47.2%的中国老年人存在睡眠障碍,睡眠障碍会增加老年人慢性疾病的发生风险,严重影响老年人的心理健康、生理功能和生存质量[3]。国内有研究指出在中国老年人中,睡眠质量差的老年人容易发生跌倒风险,有睡眠障碍的老年人需要成为防跌倒的重点关注对象[4]。有横断面研究报道了中国社区老人的睡眠质量与身体素质密切相关,身体素质越差,睡眠质量越差[5]。荷兰有队列研究显示,老人睡眠时间过短与每晚6-7 h睡眠者相比,有更高的焦虑发生风险[6]。美国抗癌协会的调查表明,老年人睡眠障碍患病率高,阻塞性睡眠呼吸暂停症、不宁腿综合征和周期性肢体运动障碍等疾病扰乱睡眠,使老年人患心血管疾病、免疫紊乱和焦虑抑郁的风险显著增加[7]。综上,国内外已有许多关于老年人失眠的文献报道,睡眠时间不足、睡眠质量低下、睡眠效率下降、睡眠潜伏期延长和日间功能差与健康水平具有一定相关性[8-9]。但目前尚无明确结论,而且相关证据不足,对指导临床工作的参考价值比较有限。本研究有鉴于此,拟借助logistics回归方程和ROC曲线模型,分析睡眠障碍对老年人健康状况的影响研究如下:
1 对象与方法
1.1 研究对象
选取2017年7月至2020年6月在广州市某三甲医院的年龄≥60岁的广州地区老年人为研究对象,主诉为睡眠不佳,且PSQI总分>7,排除有严重原发性疾病或心、肝、肾等器官受损的患者,以及有意识障碍或精神障碍的患者。最终本研究共纳入168例受试者,其中男性79例,女性89例,年龄介于60~85岁之间,平均年龄为(67.47±6.21)岁。
1.2 调查方法
采用匹兹堡睡眠质量指数量表(Pittsburgh Sleep Quality Index, PSQI)和症状自评量表(Symptom Checklist 90, SCL-90)对受试者的睡眠和健康状况进行调查:
(1)匹兹堡睡眠质量指数量表:该量表是1989年由Buysse创建,目前已被翻译成多种语言并广泛应用于临床和心理研究,有19个自评和5个他评条目构成,分为主观睡眠质量、入睡时间、睡眠时间、睡眠效率、睡眠障碍、催眠药物和日间功能7个维度。每个维度按0-3计分,累积各维度得分总分为PSQI总分,总分范围为0-21分,得分越高说明睡眠越差。信效度方面,Buysse本人对PSQI做的信效度检验,结果显示该量表有较好的内在一致性(Cronbach’sα=0.83)及重测信度(r=0.85),当总分临界点为5分时,可正确选出88.5%有睡眠困扰的患者(敏感度89.5%,特异度为86.5%)[10]。国内中文版的信效度研究同样显示PSQI有较好的信效度,重测信度为0.994,分半信度系数为0.824,总体Cronbach’sα系数为0.845;当临界点为7分时,敏感度为98.3%,特异性为90.3%,其敏感度和特异度均较高,适合对国内失眠患者睡眠质量进行评估[11]。
(2)症状自评量表:该量表是1975年由Derogatis LR编制,包括90个项目,包括10个因子,躯体化、强迫症状、人际关系敏感、焦虑、敌对、恐怖、偏执、精神病和睡眠饮食状态,评定方法通过计算总分(90个项目所得分之和)、总均分(又称总症状指数,=总分÷90)、阳性项目数(评分为1~4分的项目数)、阳性症状痛苦水平(=总分÷阳性项目数)以及各个因子分(=因子项目总分÷因子项目数),当得到因子分以后,通过绘制轮廓图了解各因子的分布趋势和评定结果的特征。SCL-90评分为5级,无症状为1分、轻度为2分、中度为3分、重度为4分,严重为5分[12]。国内有研究显示,该量表的同质性信度在0.679 6-0.879 2之间,分半信度在0.702 9-0.853 2之间,各分量表与总量表的内容相关效度为0.732 2-0.900 9之间,各量表结构效度为0.546-0.814 1之间,说明有较好的信效度。根据全国2018年版本12160人常模的结果,把总分超过160分,或阳性项目数超过43项的受试者考虑筛选为阳性[13]。
1.3 统计学方法

2 结果
2.1 受试者的睡眠情况
168名调查对象中,平均年龄为(67.47±6.21)岁,PSQI总分为15.05±3.21;其中,男性的PSQI总分为14.54±2.99,女性的PSQI总分为15.21±3.27。经正态分布检验,年龄和PSQI总分均不符合正态分布(P<0.05),故不同性别的睡眠质量对比采用秩和检验,结果显示Z=-0.618,P=0.214;年龄与睡眠质量之间的关联性采用Spearman相关分析,结果显示R=-0.01,P=0.901;说明年龄性别与睡眠质量之间的关联无统计学意义。睡眠情况方面,有86.91%的受试者认为自己睡眠质量差或很差,绝大部分受试者睡眠时间不足,有超过60%的受试者需要依靠药物才能入睡,其余信息详见表1。

表1 受试者的睡眠情况调查表
2.2 受试者的健康状况
168名调查对象的SCL-90总分为180.39±53.33,总均分为2.01±0.58,阳性症状项目数为44.61±20.03,10项因子的得分详见表2。有109名受试者的总分超过160分,或阳性项目数超过43项,相当于有64.88%的受试者存在健康问题。经正态分布检验,SCL-90总分符合近似正态分布(P>0.05),受试者的各项因子得分与2018年全国常模进行比较,采用单样本t检验进行比较,结果显示各项因得分均明显高于全国常模水平(P<0.01),其中睡眠饮食状态的t值最大(t=18.71,P<0.001),与常模的平均差异达到0.69;此外,焦虑、抑郁和躯体化等问题也比较明显(t=11.97、10.84、11.02,P<0.01)。

表2 受试者的SCL-90各因子得分与常模比较情况
2.3 受试者睡眠情况与健康状况的相关性分析
PSQI总分与健康状况之间的关联性采用Spearman相关分析,结果显示R=0.238,P=0.002,说明受试者的健康状况与睡眠质量的关联性有统计学意义,而且两者的得分关系成明显正相关,可以得出结论:睡眠质量越差,老年人的健康问题越严重。把PSQI量表中的7个睡眠成分与健康状况分别进行Spearman相关分析,见表3,发现主观睡眠质量、睡眠障碍和日间功能3个成分与健康状况成明显正相关,而其余4个维度的相关性并不明显。
2.4 受试者健康状况的影响因素分析
为进一步探索影响受试者健康状况的睡眠因素,把健康状况作为因变量,其中SCL-90阳性结果设置为“1”,阴性结果设置为“0”,把与健康状况明显相关的主观睡眠质量、睡眠障碍和日间功能作为输入自变量,构建二元logistics回归模型,见表4。在第一次建立的模型中,主观睡眠质量的P=0.243,无统计学意义,从自变量中取出,再做一次logistics回归,其结果如表5所示,去掉主观睡眠质量后,睡眠障碍和日间功能的Wald值增大,P值变小,说明新方程模型的解释力度更有意义。回归方程显示,睡眠障碍和日间功能的回归系数(B=1.044、0.539)为正数,说明当睡眠障碍和日间功能障碍得分增加,SCL-90越接近1,也就说阳性率可能性变大。因此,睡眠障碍(OR=2.84,P=0.001)与日间功能(OR=1.715,P=0.003)是影响受试者心身健康状况的危险因素。
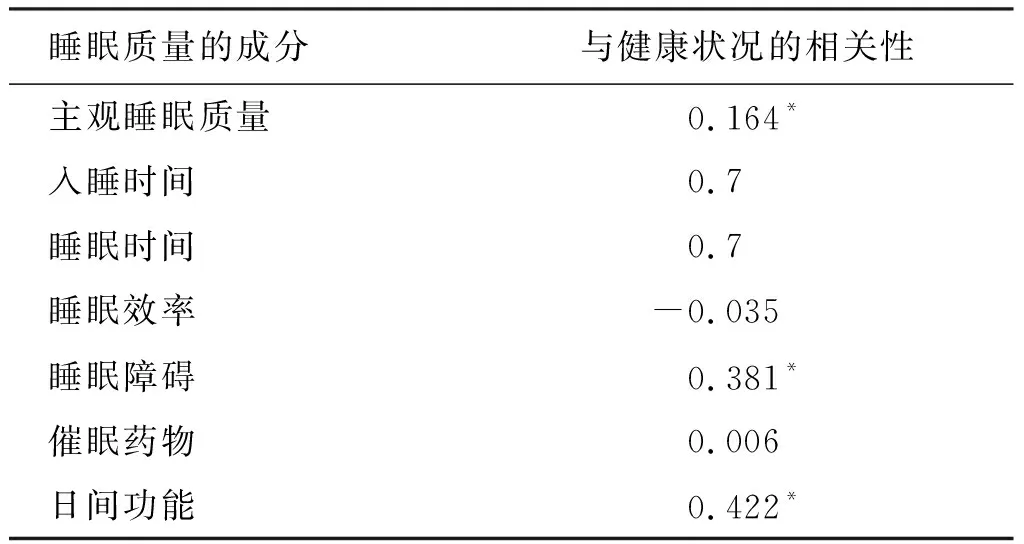
表3 受试者睡眠质量与健康状况的相关性分析结果表

表4 受试者的健康状况与睡眠质量成分的初次logistic回归分析
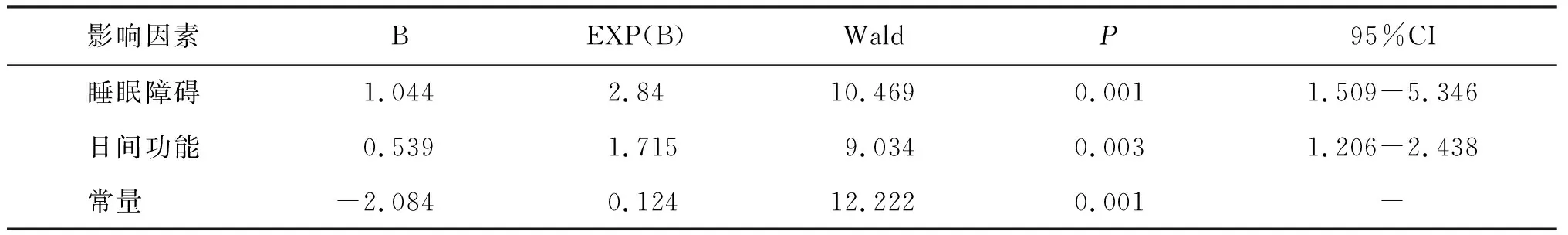
表5 受试者的健康状况与睡眠质量成分的最终logistic回归分析
2.5 受试者健康状况的ROC分析结果
Logistics回归模型证明了在PSQI量表中,睡眠障碍和日间功能障碍这两个睡眠成分对老年人健康状况造成了较大的影响,但不能提供相应的参考临界值。因此下一步把PSQI总分、睡眠障碍以及日间功能得分作为预测失眠患者健康状况的指标,分别构建ROC曲线。图中的横轴为1-特异度,纵轴为敏感度,通过计算正确诊断指数(又叫约登指数),可以获取灵敏度和特异度最高的点,也就是最大正确诊断指数对应的最佳临界点。由图1可见,PSQI总分、睡眠障碍以及日间功能得分代表的曲线均在对角参考线的左上方,而且日间功能代表的曲线相比较睡眠障碍和PSQI总分曲线,更靠近左上角,通过计算曲线下面积分别为0.626、0.66和0.67,与0.5相比差异均有统计学意义(P<0.05),说明分别利用这三个指标预测受试者健康状况的准确性只能接近中等水平(AUC<0.7),而且日间功能对于受试者健康状况的诊断水平高于睡眠障碍和PSQI总分。
使用睡眠障碍和日间功能的联合预测因子作为检测变量,作出来的ROC曲线见图2,结果显示联合因子预测的曲线下面积(AUC:0.71, 95%CI:0.632-0.791)不但优于以上3个指标的单一预测的AUC,而且准确性达到中等水平(AUC>0.7)。因为睡眠障碍和日间功能所对应的ROC曲线最佳临界点分别为1.5和2.5,所以当睡眠障碍得分高于1.5和日间功能得分高于2.5的阈值时,受试者有较大可能出现心身不健康的状况。

表6 受试者健康状况的ROC曲线下面积及其假设检验

图1 受试者健康状况的ROC曲线图(单独预测因子)
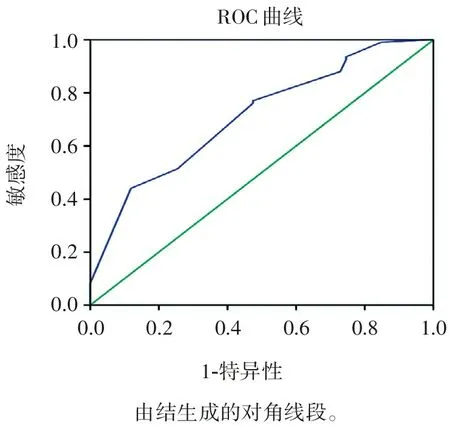
图2 受试者健康状况的ROC曲线图(联合预测因子)
3 讨论
本研究结论与已有研究结果比较一致。首先,本研究发现年龄与睡眠质量之间并不相关,以往研究认为睡眠质量大多与年龄的关系为非线性相关,高龄老年人(>80岁)与低龄老年人(<70岁)的睡眠质量会优于70-80岁之间的老年人[14],这可能与老年人对自身睡眠质量的接受程度高有关,对多年睡眠障碍的习惯和接受,在主观评价时会表示睡眠质量好转[15],因此老年人睡眠障碍与年龄的关联性仍有待深入研究。其次,已有大型研究和Meta分析结果证实了性别差异对睡眠障碍有影响,老年女性睡眠障碍发生率高于老年男性,而且老年女性的睡眠质量更低[3、16],国外研究认为这可能与老年女性的激素水平有关,围绝经期失眠是老年女性常见的失眠类型,由于更年期卵巢功能衰退,导致雌激素和垂体促性腺激素水平紊乱,造成神经神经内分泌一时性失调,从而影响自主神经功能和睡眠质量[17];也有研究认为是女性的行为习惯和对睡眠问题的过分关注[18]。在本研究中,老年女性的睡眠质量和健康状况都低于老年男性,但差异并不明显,这可能与样本量较小有关。
本调查发现老年人的健康状况与睡眠质量有着明显的正相关关系,这与大部分研究观点相同。截至目前为止,影响老年人健康状况的睡眠质量成分暂无定论,例如新加坡有一项针对老年人的横断面研究指出,主观睡眠质量差与睡眠障碍对老年人心理健康有较大的不良影响[9];国内有调查显示主观睡眠质量、睡眠障碍、入睡时间以及睡眠时间都是老年病人患心理疾病的危险因素[19]。而本调查则发现老年人心身健康更容易受睡眠障碍和日间功能受损的影响。笔者通过临床调研,认为原因如下:(1)有睡眠障碍的老年人大多伴有呼吸、泌尿和心脑循环系统等躯体疾病,这类疾病夜晚容易出现阻塞性呼吸窘迫不畅、夜尿次数频、不宁腿综合征以及躯体疼痛等症状,直接导致老年人入睡和睡眠困难[20],给老年人造成了心理和躯体较大的痛苦不适;(2)日间功能差与催眠药物的使用有关,在本研究中有63.5%的老年人需要服用药物才能入睡,有研究报道催眠药物表面上提高了睡眠时间和效率,但对快眼动睡眠有明显抑制作用,不利于脑力和精神的恢复[21]。这类睡眠模式以浅睡眠为主,快眼动睡眠持续时间缩短和梦境减少,实际上患者的睡眠没有得到真正补充,加上老年人对药物的体内消除速度慢,药物聚集作用导致老年人觉醒后精神不振、容易疲乏,日间警觉性以及社会功能下降,对老年人心身健康造成了较大的负面影响。
因此,我们认为改善失眠老年人的心身健康,除了需要宣传教育、心理疏导等常规手段外,对患有慢性疾病的老年人,还需积极治疗引发睡眠障碍的病因,指导其及时就医和科学用药;对于日间功能障碍的老年患者,医护人员必须给予更多关注,一方面是要有防跌倒意识,由于日间功能受损,老年人发生跌倒的风险明显增加;另一方面,对于依靠药物才能入睡的患者,假如日间功能明显受损,则提示临床医生要对药物进行调整,考虑使用其它药物或治疗方法进行代替。
睡眠不佳的老年人普遍存在心身健康问题,主要表现为睡眠质量差、不良心理应激和躯体化症状,睡眠障碍和日间功能得分超过临界点的老年人是患心身健康风险较大的人群,需要引起临床医护人员的重点关注和护理。
