多组分重金属复合体系在高岭土中的吸附差异
2021-04-13梁艳卢燕南唐艳葵贠金虎黄碧艺于淑琪
梁艳,卢燕南,唐艳葵,贠金虎,黄碧艺,于淑琪
(广西大学 资源环境与材料学院, 广西 南宁 530004)
0 引言
重金属环境污染问题日趋严重,通过利用吸附材料对重金属离子从环境介质中去除或使其稳定化而降低生物可利用性是环境修复领域的热点之一[1-4]。重金属污染环境修复可通过物理、化学和生物作用将重金属从土壤或水体中移除,或通过沉淀、络合、螯合等作用使重金属固定在土壤介质中,减少植物对重金属的摄入和吸收[5-7],其中包括使用吸附剂吸附土壤中的重金属,使其固定化而减少重金属的迁移。黏土矿物由于具有极大的比表面积和多种表面官能团,对包括重金属在内的多种污染物有较强的吸附能力,并因物美价廉和稳定性高等特点而在环境修复领域得到广泛关注[8]。
黏土矿物修复重金属污染土壤,主要是通过吸附作用[9]、共沉淀作用以及配合作用[10]进行,从而降低重金属的可移动性及生物有效性。黏土矿物吸附重金属受诸多因素影响,包括黏土的类型、接触时间、pH、重金属的浓度和类型、有机质类型、离子强度、腐殖酸、氧化还原电位以及多种重金属之间的竞争作用[11-14]。高岭土是黏土矿物的一种,具有多种优良的理化性质,如质软、吸水性强、易分散悬浮于水中、良好的可塑性、较高的黏结性和较强的抗酸碱性等,在水环境中具有较大吸附容量,因此是一种良好的吸附剂[15]。近几年关于高岭土吸附污染物的研究主要涉及天然或者改性高岭土对重金属的吸附行为[16-24],其中重金属离子包括Hg2+、Cu2+、Cr(Ⅵ)、Pb2+、Ce2+等。张永利等[22]采用煅烧、酸浸的方法对高岭土进行改性,结果表明高温煅烧增强其活性,而酸浸改性方法使高岭土孔隙通畅,吸附性能增强,在废水中对Cr(Ⅵ)的去除率可达91.4 %。此外,氢氧化物和溶解有机物对铜、镍和锌在黏土矿物表面的竞争性吸附有一定的影响[21]。然而,对于多组分重金属共存于各理化条件下的竞争吸附行为研究还是有所欠缺。已报道的研究通常关注单、双重金属离子及部分环境因素对吸附效率的影响,对三种及以上重金属离子之间的竞争吸附行为研究较少[17-23]。受重金属污染的环境中常存在多种重金属复合污染的情况,因此,研究多组分重金属复合体系在黏土矿物如高岭土中的吸附差异十分必要。
笔者研究了重金属离子Cu2+、Pb2+和Cd2+在高岭土表面于不同理化条件下的竞争吸附行为。采用批量实验的方法,考虑自然环境和受污染环境的理化特点,探讨吸附时间、pH值、离子强度和重金属离子初始浓度对吸附行为的影响。实验拟进行单一金属离子的吸附过程研究、两相(Cu2++Pb2+、Cu2++Cd2+、Pb2++Cd2+)以及三相(Cd2++Cu2++Pb2+)的复合吸附研究,对比不同体系内高岭土对于各重金属的吸附性能,并采用Langmuir方程对结果进行拟合,探讨吸附的机理以及影响因素,以期获得竞争吸附的规律。研究结果有助于进一步探讨黏土矿物用于治理重金属环境污染提供理论依据及数据支持,具有一定的现实意义。
1 实验
1.1 实验材料
Cu2+、Pb2+和Cd2+的储备溶液(1 g/L)分别由Cu(NO3)2·3H2O、Pb(NO3)2和Cd(NO3)2配制;NaNO3、NaOH、 HNO3溶液和重金属溶液均使用分析纯试剂或溶液并用去离子水稀释定容获得;NaNO3溶液作为背景溶液,HNO3和NaOH用于调节溶液pH。
1.2 实验方法
1.2.1 吸附平衡时间的确定和吸附动力学实验
称取0.500 g黏土矿物于50 mL聚乙烯塑料瓶中,加入一定浓度重金属溶液20 mL,调节混合液pH值。用往复式水浴恒温振荡机(SHY-2A型,金坛市天竟实验仪器厂)在(30±1)℃和150 r/min下进行振荡,在振荡10、15、20、30、40、60、90、120、180、240 min后分别取样,然后放置高速离心机(H1850型,湖南湘仪实验室仪器开发有限公司)以5 000 r/min离心5 min ,经0.45 μm滤膜进行固液分离,用火焰原子分光光度计(AA-7000型,日本岛津)测定上清液的重金属离子含量。确定吸附平衡时间后,在特定振荡时间下,进行吸附动力学实验。
1.2.2 单相吸附动力学实验
为探讨在较大的理化环境条件变化情况下,高岭土对重金属离子吸附行为,如受酸碱、共存盐离子、多种重金属复合污染影响等,充分考虑不同pH,离子强度和重金属初始浓度和组成的影响实施吸附实验。
① pH的影响
环境pH值是影响高岭土吸附性能的重要因素。本研究采用与实际环境较相关的pH条件,同时避免过高pH造成重金属离子形成氢氧化物沉淀而影响材料吸附特性分析,通过称取0.500 g黏土矿物于20 mL重金属离子溶液中,pH分别设置为3.0、3.5、4.0、4.5、5.0、5.5、6.0、6.5、7.0、7.5和8.0,金属离子含量均为10 mg/L。在往复式水浴恒温振荡机上以(30±1)℃和150 r/min[25]条件下反应至吸附平衡,用5 000 r/min离心5 min,过滤后取上清液测定金属离子含量。
② 离子强度的影响
分别以离子强度为0、0.001、0.005、0.010、0.100 mol/L的NaNO3作为介质背景溶液配制各重金属离子浓度为10 mg/L的溶液,并用1 % HNO3和0.1 mol/L NaOH调节溶液pH为6.0。吸附平衡后以5 000 r/min离心5 min,过滤后取上清液测定金属离子含量。
1.2.3 多组分金属离子复合体系的吸附试验
设置两相和三相的重金属复合体系,分别为Cu+Cd、Cu+Pb、Cd+Pb以及Cu+Cd+Pb。配制不同浓度的重金属复合溶液:
① 配制浓度分别为10、20、40、60、90、120、150 mg/L的单一重金属溶液。
② 分别配制各重金属离子含量均为10、20、40、60、90、120、150 mg/L的复合重金属溶液。
反应溶液体积均为20 mL,各背景溶液离子强度均为0.01 mol/L,pH为6.0,在振荡机中振荡吸附1 h,振速为150 r/min,恒温(30±1)℃,吸附平衡后在5 000 r/min离心5 min,过滤后取上清液测定金属离子含量。
1.2.4 吸附量、去除率计算方法
重金属离子在高岭土表面的整个吸附过程在恒温振荡中进行,吸附结束后,经离心过滤测定上清液重金属含量,不同时间吸附量、平衡吸附量和去除率分别按式(1)~(3)计算:
(1)
(2)
(3)
其中,qt为t时刻下的吸附量,mg/g;qe为平衡吸附量,mg/g;c0为重金属离子的初始浓度值,mg/L;ct为t时刻上清液中重金属离子的浓度,mg/L;ce为吸附平衡时重金属离子的浓度,mg/L;m为所加高岭土的质量,g。
1.2.5 Langmuir吸附等温式
本研究采用Langmuir吸附等温式对吸附实验结果进行拟合。主要计算式为:
(4)
其线性形式为
(5)
其中,qmax为最大吸附量,mg/g;b是一个常数,代表吸附剂的吸附能力。
2 结果与讨论
2.1 高岭土对单相重金属离子体系的吸附研究
2.1.1 吸附平衡时间
三种金属离子的吸附率与吸附时间的关系如图1所示。
从图1可看出高岭土对三种重金属离子的吸附平衡时间均在10~15 min。为保证能达到较彻底的吸附平衡和高岭土对重金属的吸附稳定性,实验统一将吸附时间设置为1 h。
2.1.2 pH值对吸附的影响
不同pH条件下高岭土对各单一重金属的吸附实验结果如图2所示。

图1 时间对高岭土吸附重金属的影响
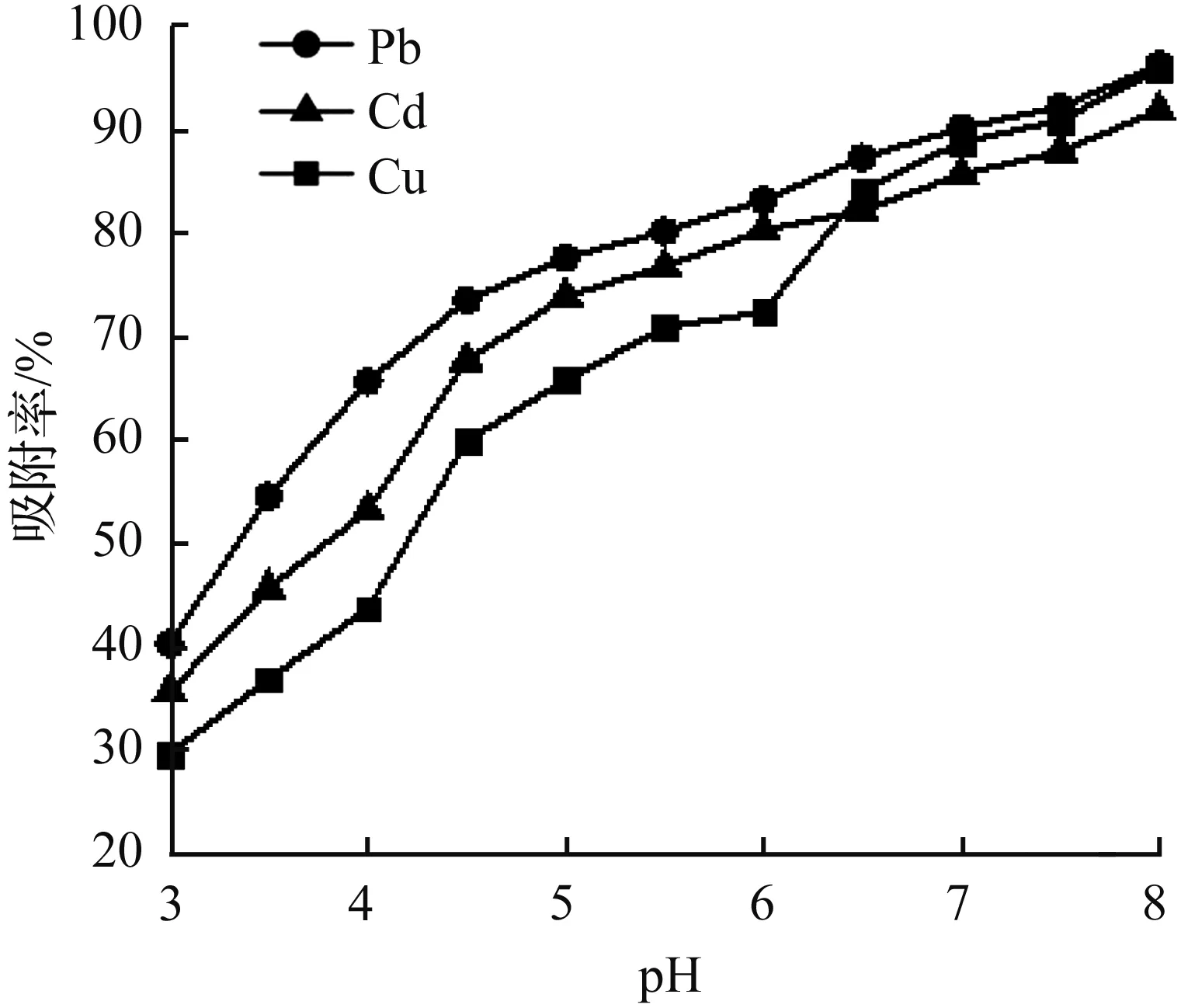
图2 pH对高岭土吸附重金属的影响
从图2可看出高岭土对这三种重金属离子的吸附量都随着pH值的升高而升高。当pH值为3.0时,高岭土对Pb2+、 Cd2+和Cu2+三种重金属离子的吸附率分别为40.3 %、35.7 %、29.7 %;当pH值为5.5时,吸附率上升至分别为80.2 %、76.8 %、70.9 %;当pH值为8.0时,吸附率分别为96.3 %、91.9 %、95.9 %。在相同的pH值条件下,高岭土对Pb2+的吸附量最大,始终大于Cd2+和Cu2+,其中对Cu2+的吸附量受pH值变化的影响较大。
pH对高岭土吸附重金属离子的影响机理主要是通过离子交换、表面络合、静电作用。在pH较低时,主要表现为离子交换吸附,pH较高时会发生离子交换和配位吸附共存,并且在强碱性条件下会生成氢氧化物沉淀[26]。
随着pH升高,高岭土对重金属吸附量增加主要由于高岭土表面的活性位点增多[27]。在pH较低时,大量的H+与重金属发生竞争吸附,吸附量较低。当pH较高时,H+与重金属离子竞争作用减小,高岭土表面的活性位点的负电性随之增强,此时由于静电引力的作用而增强了高岭土对重金属的吸附能力。此外,重金属离子可与OH-形成沉淀,如Cu(OH)2和Pb(OH)2沉淀,从而在一定程度上增加了重金属离子去除率。刘娟娟[28]在对铜和铬的竞争吸附中也有相似的发现,随着溶液pH值的增大,高岭土表面成收缩状态的带负电的基团极大地增加了Cu2+的吸附位点,从而增大了高岭土的吸附能力;而在低pH的环境中,高岭土表面会溶出大量的铝(Al3+),从而使Al3+与Cu2+之间发生竞争吸附,导致高岭土对Cu2+的吸附量降低。
2.1.3 离子强度的影响
不同离子强度下各单一金属的吸附量如图3所示。
图3反映了不同离子强度下高岭土对各重金属吸附量的影响。当离子强度大于0.01 mol/L时,随着溶液离子强度的增加,高岭土对各重金属离子的吸附率降低。溶液离子强度为0.01 mol/L时,高岭土对Pb2+、 Cd2+和Cu2+三种重金属离子的吸附能力最强,其吸附率分别为83.7 %,80.9 %,73.8 %。溶液中无机盐离子会在一定程度促进高岭土的吸附效果,主要是由于无机盐离子促进高岭土表面官能团的吸附能力。当继续增大无机盐离子的浓度时,这些离子与重金属离子存在竞争吸附,导致高岭土对重金属离子的吸附量减少。这一结果与文献[29]在研究水环境中磁性水凝胶吸附Pb2+、Cd2+和Cu2+的结果一致。
离子强度对高岭土吸附重金属离子的影响机理主要是电荷作用为吸附力的离子交换作用[30]。Na+浓度增加时,与溶液中的正电荷的重金属离子存在竞争,从而降低高岭土对重金属离子的吸附能力。溶液中离子强度增加,高岭土表面所带的负电性对重金属的吸附具有选择性,导致高岭土对重金属离子的吸附能力下降。
2.1.4 不同初始浓度的重金属离子的吸附研究
重金属初始溶液的浓度和吸附量的关系如图4。
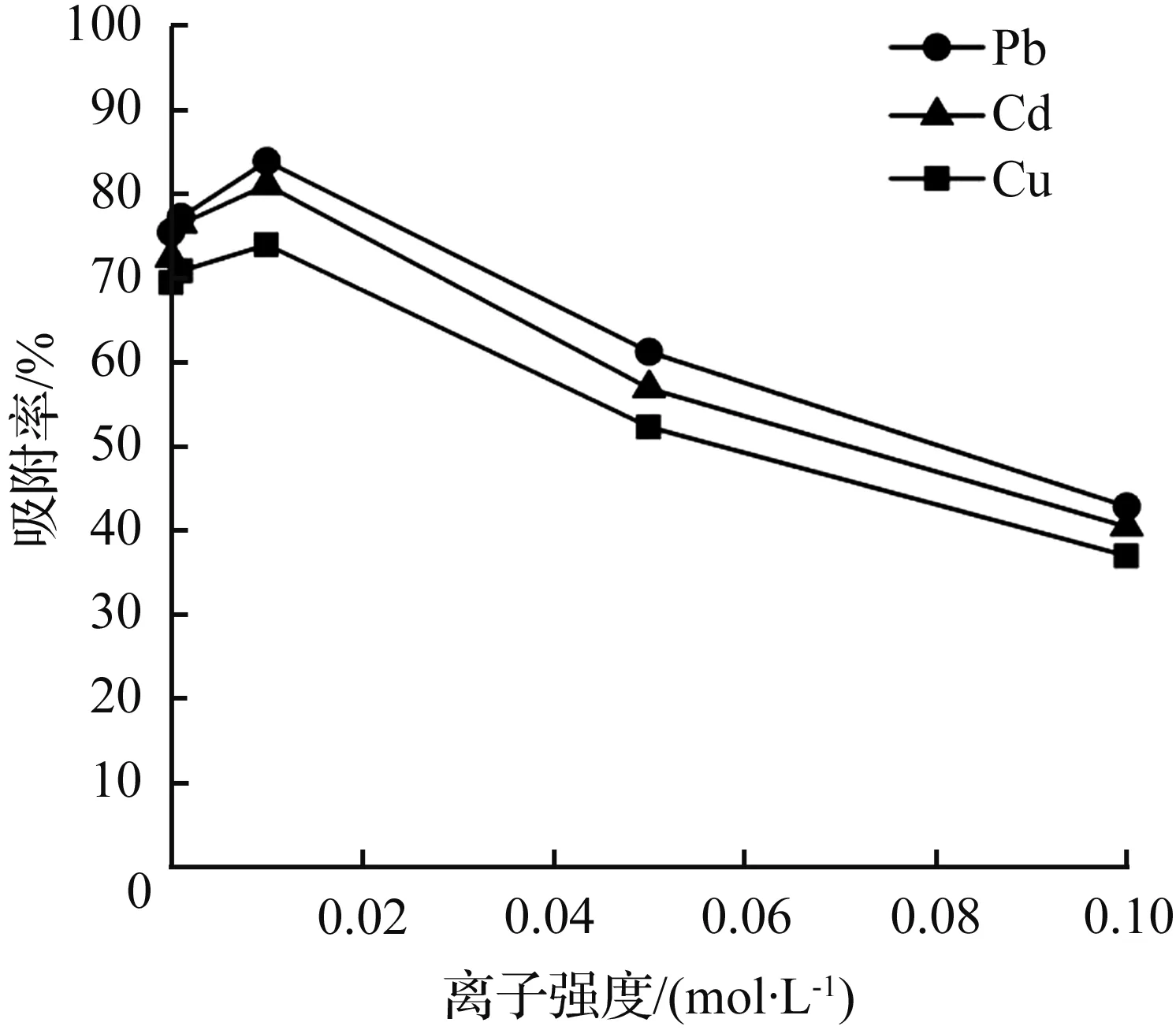
图3 离子强度对高岭土吸附重金属的影响

图4 重金属初始浓度对高岭土吸附重金属的影响
图4通过对比不同初始浓度的重金属离子在高岭土表面吸附作用,表明随着重金属离子的初始浓度增加,高岭土对重金属的吸附率降低。高岭土主要通过其表面的有效位点吸附重金属离子,因此存在吸附饱和容量。当高岭土达到接近其吸附饱和容量时,随着重金属离子浓度增加,高岭土对重金属的吸附率降低。
2.2 高岭土对多组分重金属复合体系的吸附研究
各复合金属的浓度与吸附量的关系如图5所示。
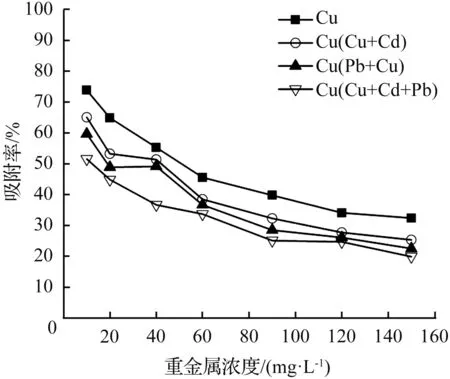
(a) Cu2+在单一和多组分重金属体系的吸附率
溶液体积:20 mL;高岭土质量:0.5 g;振荡速度:150 r/min;温度:30 ℃;离子强度:0.01 mol/L;吸附时间:1 h;pH=6.0
由图5可知,在多种重金属离子体系中,各离子间存在竞争吸附,高岭土对每一种重金属离子的吸附能力均有不同程度的下降。当重金属离子浓度均为20 mg/L时,如图5(b)、(c)所示,在Cd+Pb复合体系中,高岭土对Cd2+和Pb2+的吸附率分别为64.9 %和76.1 %,表明两相重金属离子复合体系中,高岭土对两种金属离子的吸附能力都较单一体系时的吸附能力有所下降,但高岭土对Pb2+的吸附能力始终高于Cd2+;同样的,如图5(a)、(b)所示,在Cu2++Cd2+复合体系中,高岭土对Cd2+和Cu2+的吸附率分别是68.4 %和53.3 %,在两相重金属离子复合体系中高岭土对Cd2+的吸附能力大于其对Cu2+的吸附能力。在三相重金属离子复合体系中,如图5(d)所示,高岭土对Pb2+、 Cd2+和Cu2+三种重金属离子的吸附率的大小顺序为Pb2+>Cd2+> Cu2+,但与单一体系和两相复合体系相比均有较明显的下降,说明反应体系中存在的离子种类越多,浓度越大,重金属离子之间存在的竞争作用就越明显,高岭土对其的吸附能力越低。
此外,相较于单一体系,高岭土在复合体系中对重金属离子的吸附总量增加。王艳[31]在红壤对铜、锌和镉的吸附动力学研究中也有类似的结论,指出重金属元素之间的协同作用是造成这一现象的主要原因,即吸附剂表面的电势电位以及pH会因为某一种重金属离子的存在而发生改变,从而引起吸附剂对另一种重金属离子的吸附行为。JIANG等[32]在研究高岭土对四种重金属离子的吸附过程中发现高岭土对多组分复合体系中单个重金属离子的吸附远远低于单一组分中的吸附,并且指出,在多组分复合体系中,随着各重金属离子浓度的增加,高岭土对重金属离子的吸附能力大大减弱,随着溶液中重金属离子浓度的增加,高岭土表面活性位点的数量随之减少,从而导致高岭土对重金属离子的吸附能力降低。
3 热力学拟合结果
根据公式(5),以1/qe对1/ce作图,比较不同重金属离子组分在不同浓度下的拟合结果(图6)。

(a) Cu2+在单一和多组分重金属体系的拟合
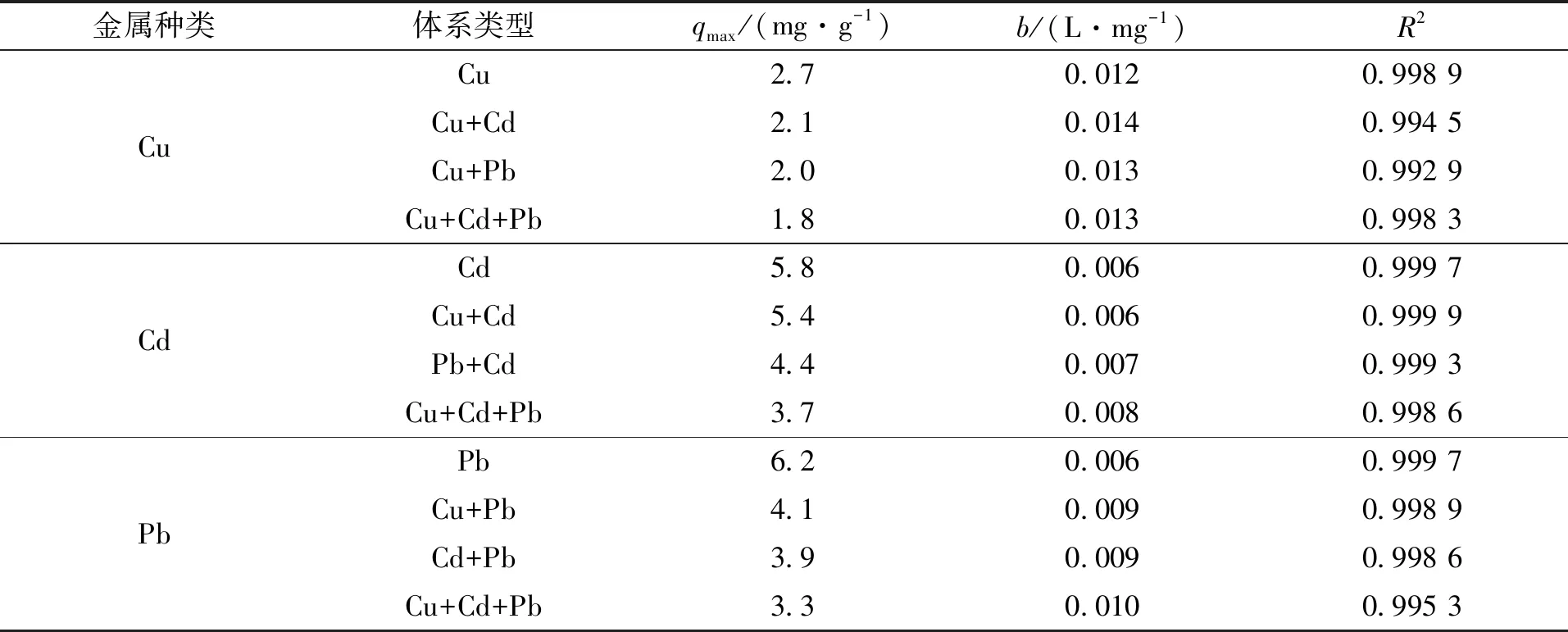
表1 Langmuir等温式参数:单一和三相体系
由图6和表1可知,高岭土对Cu2+的吸附能力最弱,对Cd2+和Pb2+的吸附能力相似,在三相复合重金属离子体系中,高岭土对各重金属离子的吸附能力都有较明显的下滑。上述Langmuir等温式的相关系数R2均大于0.99,说明高岭土吸附Pb2+、 Cd2+和Cu2+的过程符合Langmuir等温式。
4 结论与展望
4.1 结论
本文研究了高岭土对重金属离子Pb2+、Cd2+和Cu2+在单一体系以及多相复合体系吸附行为特性,并采用Langmuir等温式对实测值进行线性拟合,拟合结果较好。
① 反应体系中离子强度的降低、反应体系pH的增加、重金属初始浓度的减少都会造成高岭土对重金属离子吸附能力或吸附率的增强。
② 高岭土对单一的Pb2+、Cd2+和Cu2+三种重金属离子均有较强的吸附能力。当离子强度为0.01 mol/L, pH为8.0时,高岭土对Pb2+、Cd2+和Cu2+三种重金属离子的吸附率分别达到96.3 %、91.9 %、95.9 %。
③ 在多组分重金属离子复合体系中,离子间的竞争吸附使得高岭土对每一种重金属离子的吸附率有所下降。在Cd2++Pb2+复合体系中,高岭土对Cd2+和Pb2+的吸附率分别为64.9 %和76.1 %。在Cu2++Cd2+复合体系中,高岭土对Cd2+和Cu2+的吸附率分别是68.4 %和53.3 %。离子种类越多,浓度越大,重金属离子之间存在的竞争作用就越明显,高岭土对其的吸附能力越低。重金属离子在高岭土表面的竞争吸附能力依次为Cu2+ 本文主要研究了高岭土对Pb2+、Cd2+和Cu2+单一和多相复合体系在不同浓度、pH值、离子强度的吸附行为,为研究重金属污染水体和土壤的修复提供了一定的理论依据和数据参考。然而,自然水体和土壤是一个复杂的环境系统,例如,在受多种重金属复合污染的土壤中,各组分(如多种黏土矿物、有机质等)和理化特性(pH、盐浓度、质地等)将对重金属在土壤中的环境行为产生重要的和综合的影响,进而影响污染修复过程和效能。本研究仅选用了分析纯高岭土,与自然土壤中的黏土成分存在一定的差异;此外,影响土壤颗粒表面对重金属离子吸附行为的因素还有很多,为更深入地探讨其吸附行为和了解吸附机理,应更全面地考虑其他水环境因素和土壤组分及理化因素的影响,例如水环境温度、腐殖酸、其他矿物黏土(如蒙脱石、伊利石)对重金属的吸附等方面的影响。另外,还可通过实施动态迁移实验如填充柱实验研究,结合微观结构和元素分析技术(如电镜、能谱分析仪等)检测重金属与吸附材料表面的结合特性和重金属的化学形态等,以进一步探讨在自然环境条件下矿物黏土吸附重金属的环境效能和关键机制。4.2 展望
