新型冠状病毒肺炎心肌酶学改变及其临床意义的研究
2021-04-01郝建清
李 玲 郝建清
(庆阳市人民医院呼吸内科,甘肃 庆阳745000)
2019年12月底,新型冠状病毒肺炎(2019 novel coronavirus diseases,COVID-19)在武汉爆发,引起了全世界的广泛关注[1]。新型冠状病毒肺炎是SARS-CoV-2 感染引起的严重呼吸道传染性疾病,目前该病在中国已得到基本控制,但仍在世界多个国家爆发。SARS-CoV-2 主要通过S 蛋白与ACE2 受体结合进入细胞,并可以引起“细胞因子风暴”或“细胞因子级联”损伤靶器官[2]。ACE2 广泛表达于人体各个器官,包括肺、口腔、鼻腔及心脏[3],所以COVID-19 除可以损害呼吸系统外,可还累及多个系统。笔者在支援武汉期间于临床上观察到部分患者出现了心肌酶学异常,本文旨在对COVID-19 患者心肌酶学改变进行相关研究,以期对COVID-19 诊治提供参考。
1 资料与方法
1.1 一般资料 收集100例COVID-19 确诊病例,诊断标准参考《新型冠状病毒肺炎诊疗方案(试行第七版)》[4],所有患者均有武汉居留史。男56例,女44例,男女比例约1.27:1,年龄26~90 岁,其中年龄<29岁男0 人,女2 人,年龄在30~39 之间男4人,女4 人,年龄在40~49 之间男10 人,女6 人,年龄在50~59之间男8 人,女10 人,年龄在60~69 之间男18 人,女10 人,年龄大于70 岁男16 人,女12 人。其中40例患者有基础疾病,高血压25例,糖尿病10例,冠心病4例,尿毒症3例,恶性肿瘤术后4例,脑梗死2例。入院后患者常规检测心肌酶,包括肌酸激酶(CK)、肌酸激酶-MB 同工酶(CK-MB)、乳酸脱氢酶(LDH)、天门冬氨酸氨基转移酶(AST)。见表1

表1 COVID-19 患者年龄分布
1.2 实验方法COVID-19 确诊病例入院时静脉取血10mL 以加EDTA 抗凝管中,3500r/min 离心15 分钟后分离血清,由泽成生物技术有限公司提供的检测试剂盒在德赛ResPons920 全自动生化分析检测。心肌酶谱正常参考值:CK:25-129U/L,CK-MB:0-25U/L;LDH:100-198U/L,AST:15-40U/L。
1.3 统计学方法 采用SPSS19.0 统计软件对相关资料进行统计学分析,将研究对象分存活组和死亡组,用χ2对两组数据进行分析,P<0.05 则其差异具有统计学意义。
2 结果
100 例患者中,治愈出院的患者92例,死亡患者8例。8例死亡患者年龄53~90 岁,中位年龄72.5 岁,死亡原因主要是呼吸衰竭,另有2例合并急性心力衰竭,1例合并急性肾功能衰竭。心肌酶谱检查CK 升高34例(34%),其中存活组29例,死亡组5例。CKMB 升高34例(34%),其中存活组29例,死亡组5例。LDH 升高40例(40%),其中存活组32例,死亡组8例。AST 升高27例(27%),其中存活组23例,死亡组4例。除死亡患者外,其余大部分患者在治疗过程中心肌酶学异常逐步恢复正常。死亡组和存活组用χ2检验发现,LDH 组的P<0.01,提示两组差异具有统计学意义。而其余心肌酶两组之间的差异不具统计学意义。见表2
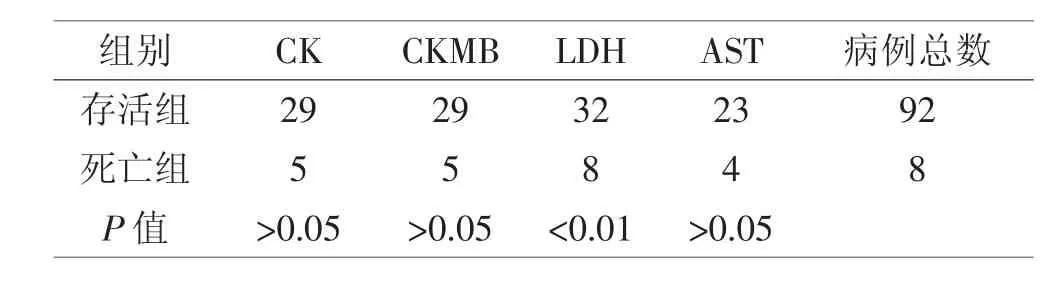
表2 心肌酶升高病例及比例
3 讨论
新型冠状病毒肺炎(COVID-19)是由冠状病毒SARS-CoV-2 感染引起的严重呼吸道传染性疾病。典型的症状包括发热、干咳、呼吸困难、肌肉疼痛、头痛、咽痛、流鼻涕、胸痛、腹泻、恶心、呕吐、结膜充血等。多数感染患者为轻症或可治愈,13.8%为重症患者,6.1%为危重症患者,危重症患者表现为呼吸衰竭、脓毒性休克或者多器官功能衰竭[2]。
冠状病毒广泛存在于人类和其他几种脊椎动物中,并引起呼吸道、胃肠道、肝和神经疾病[1]。2003年严重急性呼吸综合征冠状病毒(SARS-COV)和2012年中东呼吸综合征冠状病毒(MERS-COV)分别引起了两次严重的人类流行病。相比之下SARS-COV 和MERS-COV 的病死率都要高得多(分别为40%和10%),而但它似乎更具传染性,虽然SARS-CoV-2 与sSARS-COV 的基因组有79%相同,但SARS-CoV-2具有更强的传染性[5]。
心肌细胞中含有很多种酶类,如CK、LDH、AST和CK-MB、α-HBDH,称为心肌酶[10]。当心肌细胞受到炎症和缺氧等因素的损伤后,细胞膜通透性会迅速增加,上述酶类会产生增多进释放入血液,从而使血液内的心肌酶增高。在临床实践中,这些生物标志物可被用来识别心肌损伤。CK、AST 和LDH 不仅在心肌细胞中存在,还广泛存在于人体多种脏器中,所以单靠一个指标诊断心肌损伤的特异性不足[11]。本研究中部分COVID-19 确诊病例CK、CK-MB、LDH、AST有不同程度的升高,其中CK 升高34例(34%),CKMB 升高34例,LDH 升高40例,AST 升高27例,显著高于正常人群。提示部分CODID-19 患者存在心肌受损的情况。同时我们分析了存活病例和死亡病例心肌酶水平之间的差异,结果显示LDH 两组之间的差异具有统计学意义(P<0.01),表明LDH 水平升高提示COVID-19 具有不良预后。SARS-CoV-2 主要通过S 蛋白与ACE2 受体结合进入组织细胞,并可以引起“细胞因子风暴”或“细胞因子级联”损伤靶器官[2]。ACE2 广泛表达于人体各个器官,包括肺、口腔及鼻腔及心脏[3],所以COVID-19 除可以损害呼吸系统外,可还累及多个系统,这可能是COVI-19 造成损伤的主要机制。
心血管事件(CVEs)是肺炎最重要和最常见的并发症之一,高达30%的肺炎可以发生,并与显著死亡率有关[6]。常见的心脏并发症包括急性心肌梗死、心律失常(其中房颤最常见)以及心力衰竭。虽然CVEs一般发生于老年人、合并基础疾病的患者,但同样也可以发生于年轻人和没有基础疾病的患者[7]。心肌损伤可以使病情变得复杂化,特别是重症肺炎患者[8]。肺部感染后可以导致大量致炎因子、毒素、酶类释放入血,引起心肌损伤。心肌细胞对缺氧非常敏感,肺炎引起的低氧血症可以导致心肌细胞受损。病毒通过血液循环可以直接攻击心肌细胞或者介导自身的免疫反应损伤心肌细胞。在众多原因引起的肺炎中,病毒性肺炎是最容易引起心肌损伤的[9]。
“新冠”疫情爆发,部分学者对COVID-19 进行了尸检或者死亡后微创病理学检查。Sufang Tian 等[12]对死亡患者进行心脏微创病理检查后发现,心脏部分区域可见局灶性水肿、间质纤维化和心肌肥大,心内膜和心肌未见炎性细胞浸润。这给我们进一步认识COVID-19 引起心肌酶学异常提供了病理学基础。
综上所述,COVID-19 患者在疾病发展过程中会出现心肌酶异常,单独一种心肌酶异常往往不具特异性,联合多种心肌酶改变并结合临床及多种辅助检查能较准确判断COVID-19 是否合并严重的心血管事件,从而采取有效的应对措施,提高患者生存率。目前,中国的“新冠”疫情已经基本控制,但部分国家的情况仍不容乐观,对于COVID-19 临床及基础领域的研究需要进一步深入。
