白藜芦醇/富勒烯纳米组装体的制备
——在胆管支架抗炎涂层中的应用评估
2021-03-23刘永佳戚晓亮徐汪节乔中东
高 建,刘永佳,戚晓亮,徐汪节,乔中东
(1.上海交通大学a.生命科学技术学院;b.分析测试中心,上海 200240;2.上海交通大学医学院附属第九人民医院,上海 200011)
0 引言
胆管狭窄是胆道疾病患者高发病率和高死亡率的重要原因[1]。外科手术中的胆管受损、增生性胆管炎以及恶性肿瘤是导致胆道狭窄的主要原因,狭窄形成与成纤维细胞增殖、胶原蛋白沉积、纤维化和肿瘤生长有关。处置不当会引发胰腺炎,梗阻性黄疸等高风险疾病[2-3]。目前外科手术治疗可以通过植入胆管支架直接改善胆道狭窄[4]。据统计,有30%的患者在第1次手术后出现了良性胆道狭窄,需要再次手术治疗[5]。因此,降低术后增生性胆管炎的发生率和随后的纤维化是一个具有挑战性的问题。
白藜芦醇(Resveratrol,Res)是一种天然多酚类黄酮,在不同的组织和器官中均表现出抗纤维化作用[6]。Res参与巨噬细胞的活化,抑制促炎基因的表达。Res具有激活Sirt1 和抑制炎症的能力,Sirt1 会破坏TLR4/NF-kB/STAT 信号,从而降低巨噬细胞衍生的促炎因子产生[7]。胆管狭窄可通过Res洗脱球囊或支架来实现扩张[8],但Res 直接作用于胆道狭窄部位的药量有限,且胆汁会降低药物作用浓度,但如果使用高浓度的Res又会带来副作用。因此,研究能在胆管狭窄部位局部用药并能持续缓慢释放Res的药物洗脱支架十分重要。
富勒烯(Fullerene,C60)作为一种强大的抗氧化剂,其中空分子结构可负载药物,是一种潜在的药物递送载体。C60 可通过抑制肥大细胞和外周血嗜碱性粒细胞抑制促炎介质的释放,达到抗炎作用[9]。
本文运用分子自组装技术将具有抗炎功能的Res和C60 组装成纳米结构,并选取聚氨酯(Polyurethane,PU)这一力学强度、生物相容性良好的高分子材料做载体,并将该纳米组装体负载PU中,研究其用于胆管支架抗炎涂层领域的可能性。
1 材料与方法
1.1 试 剂
主要试剂:Res和C60 购于SIGMA公司,异丙醇、间二甲苯、PU、购于常熟市杨园化工有限公司。细胞培养基(RPMI1640)固体粉末购买于Gibco 公司,胎牛血清(FBS)购于四季青公司。人脐静脉内皮细胞系(HUVECs)购于中科院上海细胞所。
1.2 试验方法
1.2.1 Res/C60 纳米组装体的制备
配制2 mg/mL的Res异丙醇溶液和6 mg/mL C60间二甲苯溶液。Res 溶液与C60 溶液以不同体积比(2∶1,3∶1,5∶1,10∶1)混合,立即将混合液置于超声仪(KQ-500DE,昆山市超声仪器有限公司)中,室温超声20 min,4 ℃冰箱静置过夜,留存待用。混合溶液于5 000 r/min离心后,取沉淀风干后获得Res/C60 组装体粉末。
1.2.2 载Res/C60 的PU(PU-Res/C60)涂层制备
称取3 g PU,溶于20 mL 四氢呋喃,室温超声20 min,制成15%的PU 溶液。将不同体积(1,2,3 mL)的选定纳米组装体溶液加入相应体积(9,8,7 mL)的15%PU溶液中,涡旋30 min,制成含有纳米组装体溶液体积比10%、20%、30%的载纳米组装体的PU混合溶液。打开自动涂膜机(AFA-II,魅宇仪器),预热至70 ℃,将12 mL混合溶液倾倒在无尘玻璃板一端,用200 nm的金属滚动涂膜器将溶液缓慢滚动成20 cm×10 cm薄膜,将玻璃板放置在通风橱风干,待溶剂完全挥发,揭下薄膜涂层待用。
1.3 Res/C60 纳米组装体理化性能表征
(1)不同投料比例的Res/C60 纳米组装体表面形貌和直径分布。将Res/C60 纳米组装体溶液分别滴在洁净硅片上,保持表面洁净,置于通风橱中过夜让溶剂挥发。样品表面做喷金处理,使用扫描电子显微镜(SEM,Sirion 200,FEI)观察形貌。Nano Measurer 软件随机选择100 个组装体来计算组装体平均直径分布。
(2)Res、C60 和Res/C60 纳米组装体的表面形貌。将6 mg/mL的C60 间二甲苯溶液与2 mg/mL 的Res异丙醇溶液以体积比1∶3混合;纯Res溶液加入相同比例的间二甲苯,纯C60 溶液加入相同比例的异丙醇。将上述3 种溶液分别混合,室温超声20 min,4 ℃冰箱静置过夜。同样条件下经扫SEM 观察纳米组装体的表面形貌。
(3)拉曼光谱分析。将纯Res、C60 和Res/C60组装体粉末分别用镊子挑取少量置于干净的硅片上,用玻璃片压平,用色散型共聚焦拉曼光谱仪(Senterra R200-L,Bruker Optics)进行测试。
(4)X-射线衍射图分析。分别取Res、C60 和Res/C60 粉末用多功能X 射线衍射仪(D8 ADVANCE Da Vinci,Bruker)进行测试。测试条件为40 kV、40 mA和扫描范围2θ=3°~50°。
1.4 PU-Res/C60 涂层的机械性能评价
载药纳米组装体PU涂层的机械性能通过拉伸测试仪(H5K-S,Hounsfield,UK)进行测定。将样品膜裁成50 mm×10 mm 的平行样品,两夹具之间间距为30 mm,以10 mm/min 的速度进行拉伸。每个样条平行测试5 次。
1.5 PU-Res/C60 涂层的药物缓释实验
药物缓释过程采用动态透析法进行研究,具体过程为:取PU-Res/C60 涂层20 mg 置于透析袋中(截留相对分子质量为3.5 kD)。将透析袋浸没在10 mL PBS(0.2 mol/L,pH 7.4)中,放置在摇床中震荡(设定温度为37°C,速度为120 r/min)。一定时间间隔后,将透析袋外液体全部移除,重新加入10 mL PBS(0.2 mol/L,pH 7.4)。收集不同时间点的透析液并离心(5 000 r/min)保管上清,取2 mL上清用2 mL无水乙醇稀释,用紫外分光光度计测定305 nm处药物的特征紫外吸收值。用PBS与无水乙醇体积比为1∶1为溶剂,测定一系列已知浓度的Res溶液紫外吸收值,获得Res标准曲(Y=0.013 03+0.129 63X,R2=0.999 8)。透析液中Res的浓度通过标准曲线计算得出。将组装体溶液离心取上清,通过测得上清液中残留的Res浓度,计算得组装体溶液载药量为8.35%,包封率为20.75%。
1.6 MTT法测定细胞活性
选用HUVECs 进行Res/C60 纳米组装体的MTT(methyl-thiotetrazole)法细胞毒性评价。96 孔板中铺入1 ×104个细胞/孔,用含10%胎牛血清RPMI1640培养基在含5%CO2和37℃培养12 h。加入Res、C60和组装体药物保持其终浓度为10 μg/mL,继续培养48 h。按MTT 试剂盒进行后续操作,用酶标仪(Multiskan MK3;Thermo Labsystems)在492 nm 下测量吸光度。取6 个平行样品的平均值。
1.7 白藜芦醇清除DPPH自由基能力的评价
取0.1 mL 不同浓度(10,20,30,40,50,80,100 μg/mL)梯度的Res、C60 和Res/C60 纳米组装体溶液分别同1.0 mL 1,1-二苯基-2-三硝基苯肼(DPPH)乙醇溶液混匀,DPPH 乙醇溶液为空白样液,于37 ℃反应60 min 后在波长517 nm比色,DPPH 自由基清除率D采用如下公式计算。

1.8 Res/C60 纳米组装体的抗炎效果评价
(1)原代树突状细胞的提取。选取6~8 周龄的C57BL/6 小鼠,颈椎脱臼处死,用注射器反复吸取无菌的PBS缓冲液冲洗出骨髓腔中细胞,1 000 r/min离心10 min后,取细胞沉淀,接种于培养皿中,加入终浓度为100 ng/mL 脂多糖(LPS)刺激骨髓造血细胞成熟,培养的第3 天半量换液,第5 天全量换液,第7 天得成熟的树突状细胞。
(2)Res/C60 纳米组装体对炎症因子抑制效果评价。将树突状细胞以1 ×104个细胞/孔的密度接种于24 孔板中,培养12 h 待细胞完全贴壁后,设定实验分组为空白对照(培养基)、LPS 阳性对照和Res/C60 纳米组装体,阳性组和组装体组分别加入50 μL LPS 溶液,保持其终浓度为100 ng/mL,组装体组加入50 μL组装体原液,其余组用相同体积培养基补齐,培养12 h后通过检测细胞中白细胞介素1(IL-1),白细胞介素6(IL-6)和肿瘤坏死因子α(TNF-α)的mRNA的表达水平来评价纳米组装体的抗炎效果。数据统计P <0.05。
1.9 数据统计
以上所有实验都至少做3 次平行,通过使用单向方差分析比较数据获得统计学上的显著性差异。数据表示为平均值±SD,统计学显著性标准为P <0.05。
2 结果与讨论
2.1 Res、C60 和不同比例纳米组装体的表面形貌及直径分布
观察Res、C60 和Res/C60 纳米组装体的表面形态。纯Res呈花瓣样片状,纯C60 呈细长的棒状,截面为规整的六边形,两者通过分子自组装技术组装后,为短棒状,且棱柱的棱角更圆润。
Res溶液与C60 溶液以体积比3∶1混合后得到的组装体(Res/C60-3∶1),直径分布在250~450 nm,标准差值最小,说明这种比例下的组装体尺寸分布均匀,为最佳的Res/C60 组装体的投料比,文中提到Res/C60 组装体均采用此种制备条件。

图1 Res(a)和C60(b)和组装体(c)Res/C60-2∶1,(d)Res/C60-3∶1,(e)Res/C60-5∶1,(f)Res/C60-10∶1的表面形貌和直径分布
2.2 拉曼光谱及X-射线衍射图
拉曼光谱反映分子的振动频率信息,可用于分析物质的组分和结构。图2(a)拉曼光谱图谱中有较强的C60 信号峰,同样可以说明组装体中存在C60,组装体中新生成的峰可能由于两者组装形成。
图2(b)X-射线衍射图谱显示,纯Res 高度结晶,并在2θ 的范围观察到以16.31°、19.14°、22.39°、23.56°、25.16°、28.26°的尖锐的衍射峰,说明了Res是晶体性质。此外,在Res/C60 的组装体上也出现了部分Res和C60 叠加的特征峰。说明Res与C60 组装成功,且大部分是包括在C60 分子内部,因此未显示出强烈特征性的尖峰。
2.3 PU-Res/C60 涂层表面形貌分析
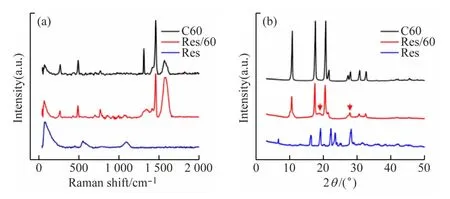
图2 Res、C60和Res/C60纳米组装体的拉曼光谱图和X-射线衍射图谱

图3 (a)裸支架、覆膜支架和扩张后的覆膜支架,(b)覆膜支架SEM图,(c)、(d)分别为裸支架SEM图和EDS能谱,(e)、(f)分别为覆膜支架的SEM图和EDS能谱图
从图3(a)、(b)可观察出,该覆膜弹性良好,扩张后有足够的柔韧性和强度来支持临床使用。比较图3(c)~(f)可知,覆膜的金属支架对应的能谱图中(c)、(d)含量升高,验证了PU-Res/C60 涂层的成功涂覆。
2.4 PU-Res/C60 涂层薄膜的力学性能评价
载药纳米涂层薄膜的机械性能是其在生物医学工程领域应用的重要因素。图4(a)中所有样品均呈现较好的弹性,随着载药量的增加,PU-Res/C60 涂层薄膜的最大断裂强度逐渐增加。如图4(b)所示,PURes/C60 涂层薄膜的弹性模量较纯PU膜大,且随着载药量的增加与增大的趋势。机械性能的结果表明,在PU中载入Res/C60 纳米组装体后形成的涂层薄膜,弹模量增加,弹性稍有降低,但总体满足其应用需求。

图4 载有不同药量的纳米组装体涂层薄膜的机械性能
2.5 PU-Res/C60 涂层薄膜的药物缓释实验和Res/C60 纳米组装体的自由基清除能力
从图5(a)可看出,PU-Res/C60-10%纳涂层在30天后释放出约63%的Res药物,相比较,PU-Res/C60-20%和PU-Res/C60-30%纳米组装体涂层仅释放出约45%和39%,比PU-Res/C60-10%纳米组装体涂层药物释放得更加缓慢,能够持续发挥药效。
通常,聚合物载药体系在药物缓释初始阶段易形成药物突释现象,随后药物以相对稳定的缓释速度持续释放[10]。PU-Res/C60 涂层在第1 天的药物缓释实验中药物累积释放量最高达20%左右,在30 天的长周期内PU-Res/C60-10%涂层能够持续累积释放60%左右的药量。由于白藜芦醇不溶于水,故其在血液中的半衰期较短,生物利用度低,不能长时间对免疫细胞产生抗炎作用[11],所以需要设计Res 药物缓释系统,达到药物持续释放和在较长时间内发挥抗炎效果。本研究设计的PU-Res/C60 纳米组装体涂层,可以通过添加不用含量的Res/C60 纳米组装体来实现不同载药量的需求,Res 与C60 形成的自组装结构,再与PU形成涂层,两者都有助于控制其药物释放速度,使其在长时间内可达到药物持续释放的目的。
羟自由基作用于体内蛋白质、核酸、脂类等生物分子,造成细胞结构和功能损伤,易引发炎症反应,羟自由基清除能力是样品抗氧化能力的重要指标。据图5(b)可知,Res、C60 和Res/C60 纳米组装体这3 种物质的羟自由基清除能力随浓度增大逐渐成上升趋势。组装体浓度达100 μg/mL时,有50%以上的自由基清除率。

图5 (a)PU-Res/C60 涂层在PBS 缓冲液(pH 7.4)中的体外药物释放曲线;(b)Res、C60和Res/C60纳米组装体的自由基清除能力
2.6 Res、C60 和Res/C60 纳米组装体对体外细胞存活率的影响及其抗炎效果评估
如图6(a)所示,各实验组在培养48 h 后,HUVECs存活率均在90%以上,说明Res、C60 和Res/C60 纳米组装对正常细胞毒性较低,有较好的生物相容性。
通过对与组装体共培养12 h 后的炎症因子的表达水平进行研究,发现LPS 炎症因子出现明显下降,如图6(b)所示,IL-1,IL-6,TNF-α 3 个代表性的炎症因子,在LPS诱导下表达量显著上升,在持续的Res释放条件下,3 种炎症因子的mRNA 表达水平受到明显抑制。
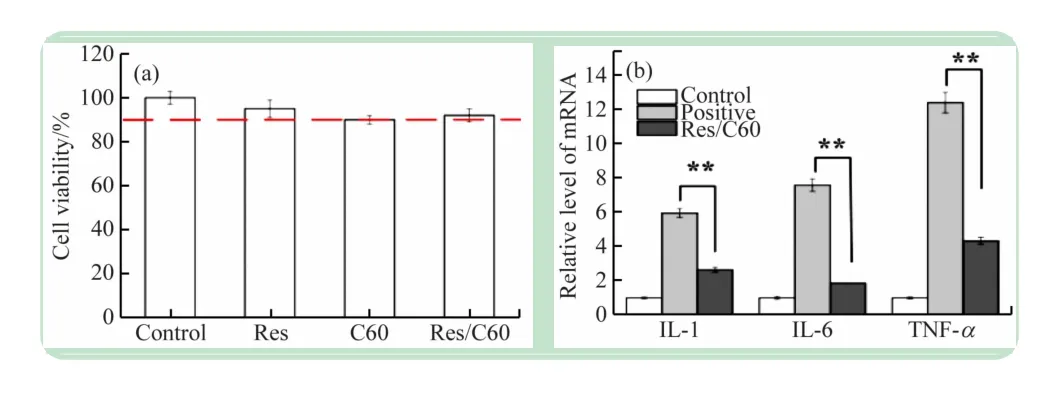
图6 MTT法测定Res/C60 纳米组装体48 h 后HUVECs 的存活率;Res/C60纳米组装体孵育12 h后各炎症相关基因的mRNA表达水平
有研究发现Res可以减少巨噬细胞中IL-1 和IL-6的表达[12],而IL-1 和IL-6 表达量增加说明细胞处在促炎状态[13]。在慢性胆道梗阻所致大鼠肝损伤动物模型实验中[14],Res 具有显著性保护作用,可抑制导管增生和淋巴细胞炎症,能很好抑制组织中慢性疾病有关的低度炎症状态[15]。同时,Res 可用作胆道梗阻的保护剂,治疗胆管结扎后的肝功能受损,减少凋亡细胞数量[16]。本实验中Res 表现出与上文一致的抗炎效果,说明纳米组装体对炎症因子的释放有明显的抑制作用。
3 结语
本文基于分子自组装技术得到Res/C60 纳米组装体,在此基础上研究了该组装体的理化性能与其应用于药物洗脱支架的可能性。更进一步运用PU作为组装体载体,制备得到PU-Res/C60 涂层,验证了其在胆管支架抗炎涂层领域的应用。Res/C60 纳米组装体具有良好的药物缓释性能、低毒性和抗炎功能,且在胆管支架抗炎涂层领域有一定的应用前景,未来有希望用于临床改善胆管炎性狭窄。
