携带乙型肝炎病毒孕妇血清标志物模式、病毒载量和肝功能在母婴传播中的风险评估
2021-03-18王玥琦潘禹辰陶雪蓉杨娜赵天业王崇吴燕华姜晶吉林大学第一医院临床研究部长春300吉林大学第一医院肝胆胰内科长春300
王玥琦 潘禹辰 陶雪蓉 杨娜 赵天业 王崇 吴燕华 姜晶吉林大学第一医院临床研究部,长春300; 吉林大学第一医院肝胆胰内科,长春300
目前我国约有7000 万HBV 感染者,2000 万~3000 万慢性乙型肝炎患者,HBV 感染依旧是我国严重的公共卫生问题之一[1]。 母婴传播是造成HBV感染的主要原因之一,目前我国新发HBV 感染者约50%来自于母婴传播[2]。 我国自1992年开始实施乙型肝炎疫苗免疫策略后, 儿童和一般人群血清HBsAg 阳性率明显下降,但是育龄女性的感染率维持在6%~8%, 这增加了HBV 母婴传播的风险, 并且HBV 慢性感染状态还可能对孕产妇健康构成威胁[3]。
目前乙型肝炎的诊断及治疗方案确定主要依靠实验室检测, 包括HBV 标志物、HBV DNA 载量及与肝细胞损伤相关的AST 和ALT 等。 相关研究主要关注慢性HBV 感染人群, 对具有高传播风险性的HBsAg 阳性妊娠期妇女缺乏关注[4-5]。本研究重点关注HBsAg 阳性的妊娠期妇女, 探讨其HBV 标志物模式与HBV DNA 载量及ALT、AST 的关系,为HBsAg 阳性孕妇的妊娠期管理和调整母婴传播阻断方案提供理论参考。
对象与方法
一、研究对象
本研究纳入标准:(1) 于2012年7 月至2015年6 月参加吉林大学第一医院乙型肝炎母婴传播阻断项目的HBsAg 阳性母亲及其分娩的新生儿;(2)经知情同意说明,自愿参加本研究。 排除标准:(1)孕妇因慢性乙型肝炎治疗需要,服用抗病毒药物或接受其他免疫调节治疗;(2) 合并其他病毒感染;(3)有免疫缺陷者;(4)母亲或新生儿信息不全者。 本研究经吉林大学第一医院伦理委员会批准(伦理审批号:2012-098)。
二、研究方法
1.数据收集
在乙型肝炎母婴传播阻断门诊,由经过统一培训的专业人员对所有研究对象进行问卷调查,收集孕妇的年龄、孕产情况、既往抗病毒治疗情况等信息, 在分娩后1 周、1 个月、7 个月时随访收集新生儿出生及疫苗接种信息。
2.母婴传播阻断
新生儿出生后均接受了主被动联合免疫,对于母亲为HBsAg 及HBeAg 双阳性的新生儿采用20 μg乙型肝炎疫苗(Hep B) +100 IU 乙型肝炎免疫球蛋白(HBIG)方案,对HBsAg 阳性、HBeAg 阴性母亲分娩的新生儿采用10 μg Hep B + 100 IU HBIG 方案。 第1 针Hep B 注射要求在新生儿出生2 h 内给予,同时肌肉注射HBIG 100 IU。第2、3 针分别在新生儿1 月龄及6 月龄时接种10 或20 μg Hep B。HBV 母婴阻断方案详见本课题组已发表的研究[6]。
3.实验室检测
采集孕妇孕晚期(孕28~32 周)静脉血,婴儿7月龄静脉血。利用化学发光法检测孕妇及婴儿HBV血清学标志物(仪器为美国雅培Architect i2000;试剂为美国Abbott Axsym 雅培检测试剂盒),结果分别以HBsAg<0.05 IU/mL、 抗-HBs<10.00 mIU/mL、HBeAg及抗-HBc S/CO <1 、抗-HBe S/CO>1 为阴性。 HBV DNA 病毒定量扩增仪为ABI7500 自动提取仪,以<500 IU/mL 判定为阴性 (试剂购自上海浩源公司)。应用LXH20 同步自动分析仪(购自美国克曼库尔特公司)检测孕妇ALT 及AST 水平,以超过正常值上限,即ALT >40 U/L 视为ATL 异常升高,AST >35 U/L 视为AST 异常升高。
三、统计学分析
采用SPSS 21.0 统计软件进行统计学分析。 对于服从正态分布的计量资料,应用x±s 进行描述,两组间比较采用两独立样本t 检验, 三组间比较采用方差分析; 非正态分布计量资料以M (Q25,Q75) 表示,采用非参数(Mann-Whitney U 检验) 检验进行两组间比较;计数资料以例数和构成比(%)表示,应用χ2检验及趋势性χ2检验进行组间比较。P<0.05 表示差异具有统计学意义。
结 果
一、一般资料
本研究共纳入657 例孕妇及662 例新生儿(含5 对双胞胎),孕妇年龄为(28.19±3.96)岁,范围20~40岁。 以HBsAg 和HBeAg 双阳性孕妇为主(367例,55.8%),且364 例(55.4%)孕妇的HBV DNA 载量高于2×105IU/mL。 全部孕妇中67 例 (10.2%)ALT 异常,79 例(12.0%) AST 异常。 按照阻断方案,全程实施主、被动免疫后,仅16 例新生儿经HBV标志物和HBV DNA 定量检测,最后确定为HBV 母婴传播阻断失败,研究对象的部分实验室检查情况详见表1。
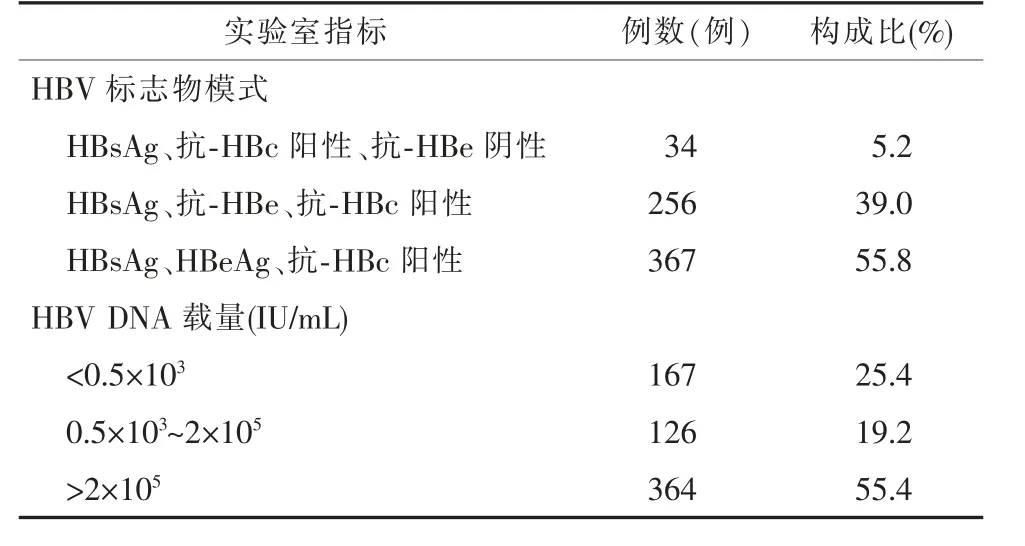
表1 HBsAg 阳性孕妇的部分实验室检查结果(n=657)
二、不同HBV 标志物模式孕妇HBV DNA 载量及肝功能的比较
HBeAg 阳性患者HBV DNA 载量的中位数为1×108IU/mL,ALT 和AST异常升高比例分别为13.1%和17.2%,均高于HBeAg 阴性患者,且差异均具有统计学意义(Z=-21.554, χ2=7.536,20.780,P 均<0.01); 抗-HBe 阴性患者HBV DNA 载量的中位数为1745 IU/mL,高于抗-HBe 阳性患者(Z=-2.313,P<0.05),且抗-HBe 阴性孕妇中病毒载量>2×105IU/mL 的比例为14.7%, 显著高于抗-HBe 阳性孕妇的2.7%,差异有统计学意义(χ2=10.844,P<0.01);ALT和AST 异常比例在两组间的差异没有统计学意义(χ2=2.700,2.249,P均>0.05)。 具体结果详见表2。
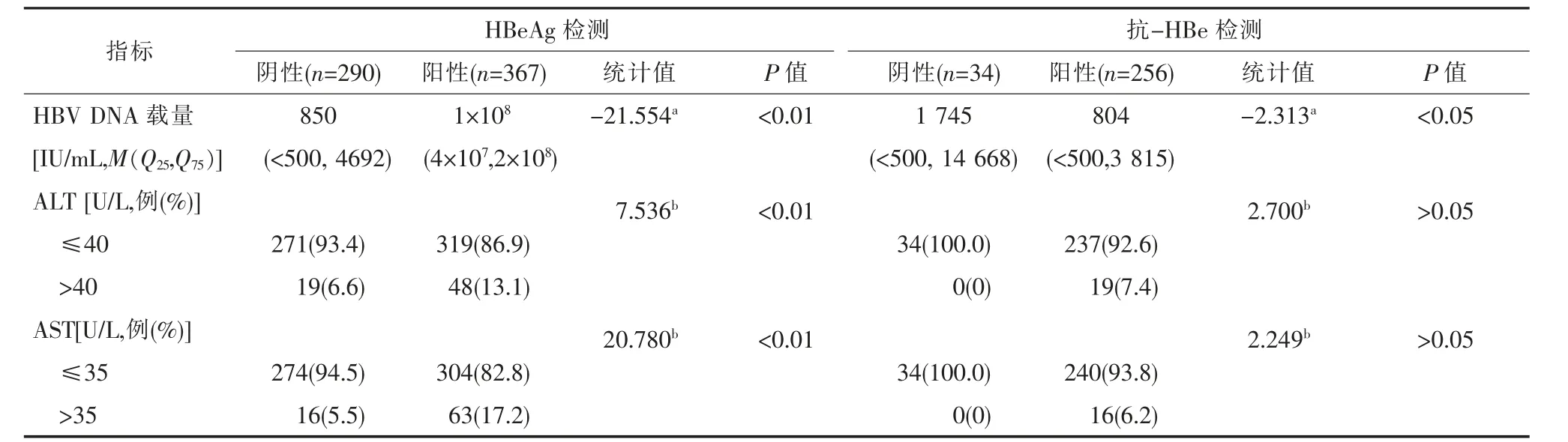
表2 不同HBV 标志物模式HBsAg 阳性孕妇的HBV DNA 载量与肝功能情况
三、孕妇HBV DNA 水平与肝功能的关系
在HBV DNA 阴性孕妇中,ALT 及AST 异常升高者均占1.8%;在HBV DNA 载量<2×105IU/mL 的孕妇中,ALT 异常者占9.5%,AST 异常者占7.1%;在HBV DNA 载量>2×105IU/mL 的孕妇中,ALT 升高者占14.3%,AST 升高者占18.4%,随着病毒载量的升高,ALT 及AST 异常率呈现逐步上升的趋势(χ2趋势=19.309 和32.502,P 均<0.01),具体结果详见表3。
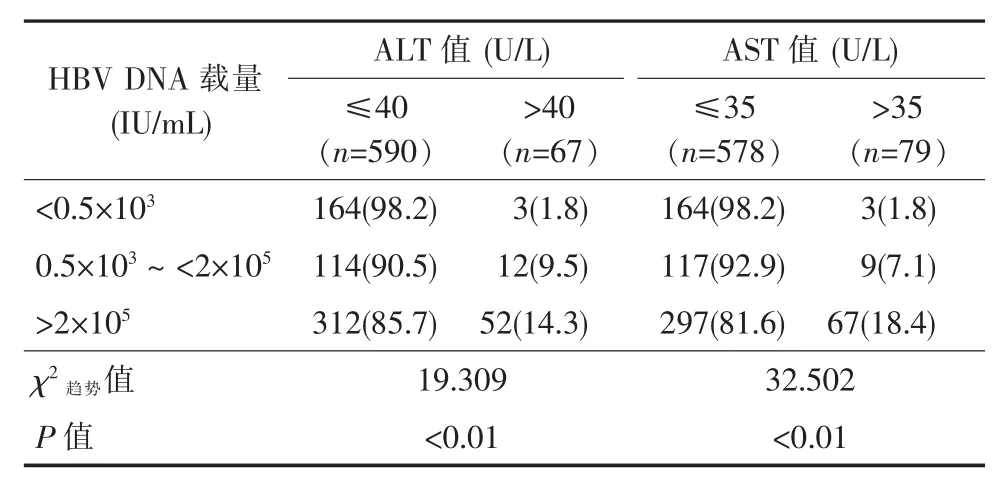
表3 HBsAg 阳性孕妇HBV DNA 载量分布与肝功能的关系[例(%)]
四、 新生儿HBV 感染情况与母亲HBV 标志物模式、HBV DNA 载量及肝功能的关系
依据方案进行主被动联合免疫后,7 月龄检查后发现16 例新生儿感染HBV, 其母亲均为HBeAg阳性,且HBV DNA 病毒载量均>2×105IU/mL,其余亚组孕妇分娩的新生儿均未感染 (不同孕妇HBV标志物模式:χ2=14.056,P<0.01; 不同HBV DNA 载量:χ2=13.446,P<0.01); 孕晚期不同肝功能水平的孕妇,其分娩新生儿的感染率差异没有统计学意义(χ2=2.326,P>0.05),结果详见表4。
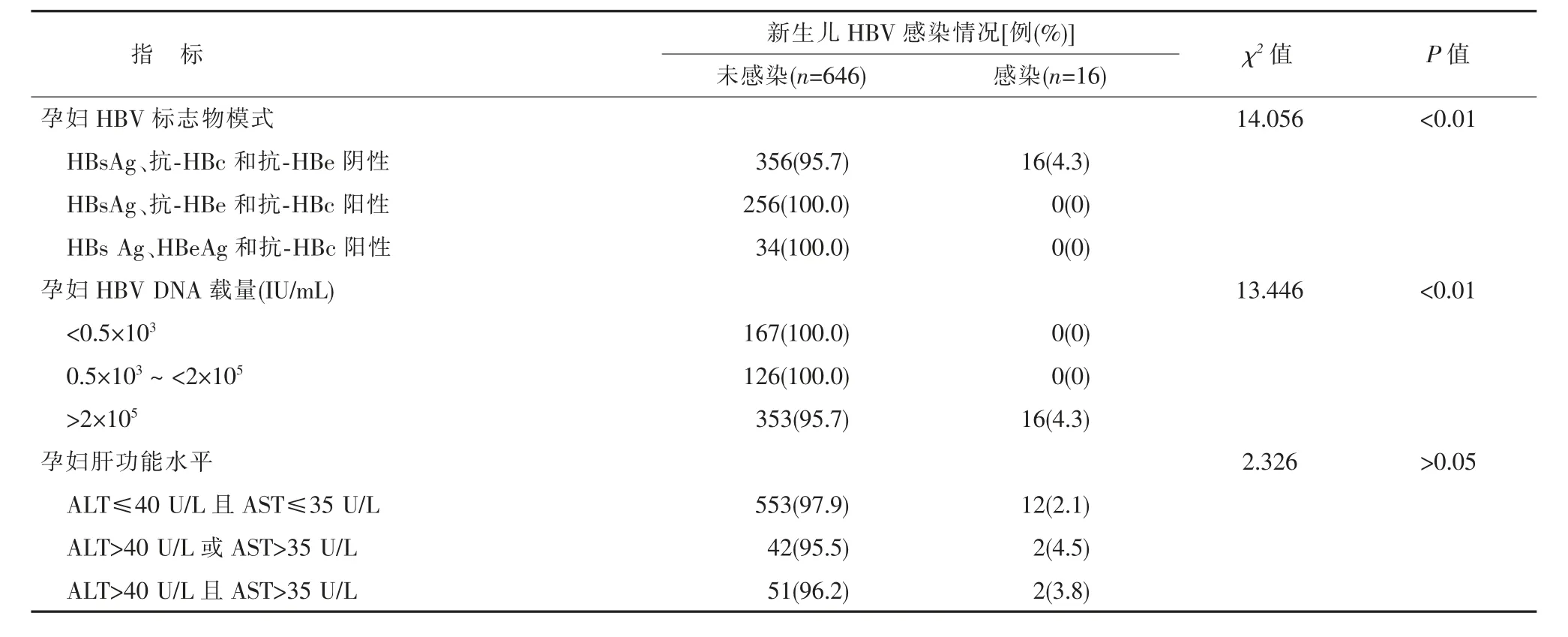
表4 新生儿HBV 感染情况与母亲HBV 标志物模式、HBV DNA 载量及肝功能的关系
讨 论
胎盘组织内的HBV 可能导致孕妇出现高应激状态,造成体内炎性细胞因子水平上升,可诱发自发性早产等妊娠期并发症的发生[7]。此外,慢性HBV感染孕妇的胎儿在宫内发生缺血缺氧及产妇发生产后出血的风险也明显升高[8-10],因此,孕产妇携带HBV 对母婴健康均有较严重的影响。 对于HBsAg阳性孕妇这一特殊人群,应在孕期密切监测病毒复制水平及肝脏损伤程度的变化,充分掌握疾病的转归,给予个性化的妊娠期管理,保证母婴的安全。
HBeAg 常被用作判断HBV 复制程度的间接指标[11]。有研究表明,在慢性HBV 感染的一般人群中,HBeAg 与HBV DNA 水平呈正相关[12]。由于HBV DNA可以直接反映HBV 复制状态, 因此孕妇血清中的HBV DNA 水平可能与HBV 母婴传播风险密切相关[13]。 本研究以HBsAg 阳性的孕妇为研究对象,结果显示其中HBeAg 阳性孕妇的HBV DNA 载量远高于HBeAg 阴性孕妇, 提示HBeAg 阳性孕妇病毒复制活跃,母婴传播风险高,这部分孕妇在孕期需特别关注HBV DNA 水平, 对于高病毒载量孕妇在孕晚期可考虑进行抗病毒治疗, 以降低HBV 母婴传播率。 特别值得注意的是,本研究发现, 在抗-HBe阴性孕妇中高病毒载量 (>2×105IU/mL) 比例显著高于抗-HBe 阳性孕妇(14.7% vs 2.7%)。一般认为,HBsAg 和抗-HBc 双阳性表明患者正处于感染恢复期及血清学转换期, 或提示HBV 前C 区可能发生了突变[14]。 HBV 前C 区是HBV 病毒中的高变区,参与编码HBcAg 和HBeAg[15]。 当前C 区发生突变后,血清中HBeAg 可由阳性转为阴性,还会对IFN 的治疗效果产生影响,也易诱发慢性化[16],因此具有更高的传播风险。 本研究结果提示在临床中应加强对抗-HBe 阴性乙型肝炎携带孕妇的关注,重视监测这部分孕妇的病毒定量与疾病进展情况。
ALT 和AST 能够在一定程度上反映肝细胞的损伤程度[17]。受患者基线特征、对肝功能异常界定不同等影响,孕妇在孕期出现肝功能异常的比例也有所差别。 本研究结果显示,慢性HBV 感染的孕妇在孕期ALT 及AST 的异常率分别为10.2%和12.0%,ALT 异常率高于部分研究[18-19],其中HBeAg 阳性孕妇出现ALT 及AST 异常的发生率显著高于HBeAg阴性孕妇, 且随孕妇病毒载量的升高, 孕妇出现ALT 及AST 异常比例呈现逐步升高的趋势。 目前妊娠合并慢性HBV 感染的孕妇, 孕期出现肝功能异常的原因尚不十分明确,有研究指出妊娠期机体处于免疫耐受状态,在孕早期和孕中期Th1-Th2 型细胞因子平衡偏向Th2 型, 而孕晚期则偏向Th1 型,激活抗感染免疫,导致肝细胞受到损害造成肝功能异常[20]。结合本研究结果,对于偏远地区的乙型肝炎孕妇,若无法检测病毒定量,应定期监测肝功能指标,如果出现ALT 或AST 异常,应进一步检查病毒载量,对于高病毒载量的孕妇可考虑孕晚期给予抗病毒治疗以降低母体病毒载量,降低乙型肝炎母婴传播的发生风险。
本研究还对新生儿HBV 感染情况与母亲感染情况、病毒载量和肝功能的关系进行了探讨。 16 例感染HBV 的新生儿,其母亲均为HBeAg 阳性,并且HBV DNA>2×105IU/mL。 虽然在肝功能异常组分娩的新生儿感染率高于肝功能正常组分娩新生儿的感染率,但尚未发现统计学差异,可以考虑HBV 携带母亲传染性的高低主要取决于HBV DNA 水平,与血清ALT 和AST 水平无关。 新生儿实施标准化母婴阻断方案后, 即使在高病毒载量组,HBV 母婴传播的发生率也降至4.3%, 取得了较好的阻断效果。 由于所有病毒载量低于2×105IU/mL 母亲分娩的新生儿都未感染, 因此为进一步达到HBV 母婴零传播,可以考虑在分娩前通过短期抗病毒治疗进一步降低分娩时孕妇的HBV DNA 水平或增加Hep B剂量。
综上所述,HBV 携带的孕妇中,HBeAg 阳性或HBsAg 阳性和抗-HBc 阳性孕妇病毒复制活跃,应对这部分高危人群加强孕期病毒监测,必要时孕晚期进行抗病毒干预,减少乙型肝炎母婴垂直传播的发生; 对于孕晚期肝功异常的孕妇, 应进一步检测HBV DNA 水平, 如果病毒载量较高应考虑在孕晚期给予抗病毒治疗以降低乙型肝炎母婴传播的发生风险和减轻肝细胞炎症坏死及肝脏纤维组织增生。
利益冲突所有作者均声明不存在利益冲突
